Отличие вирусной инфекции от бактериальной у детей
Болезнь ребенка волнует каждого родителя. И тут главное, определиться что это — легкая простуда, инфекционное заболевание или аллергия.
Они бывают 2-х видов – вирусные и бактериальные. И если, с первыми организм борется сам, то вторые должен лечить специалист. Каждый родитель должен знать и понимать их основные различия.
Острые респираторные вирусные инфекции –самые распространенные, ими болеют все –дети и взрослые во всех странах мира. Практически каждый взрослый несколько раз в год переносит ОРВИ, а у детей они составляют до 75% от всех детских болезней. Часто у ребенка с ослабленным иммунитетом к вирусной, как новая волна, присоединяется бактериальная инфекция дыхательных путей.
Что такое вирусы?
Это самая примитивная форма жизни. Микроорганизм-паразит, который не может размножаться вне живой клетки. Внедряясь внутрь, он вынуждает её производить тысячи своих копий. При этом, она погибает, или прекращает выполнять свои функции, а у человека возникают болезненные симптомы.
Что такое бактерии?
Это одноклеточные организмы, размножающиеся делением клетки, способны жить самостоятельно вокруг и внутри нас.
Вирусы способны поражать бактерии, используя их для размножения.
Вирусы и бактерии – микроскопические организмы, вызывающие заболевания у людей, животных и растений, живут в любой, вплоть до агрессивной, среде.
Как распространяются:
- воздушно-капельным путем — чихание, кашель,
- через грязную посуду, руки, пищу, воду,
- от матери к ребенку при беременности,
- через нестерильный медицинский инструмент,
- через поврежденную кожу, слизистые оболочки.
Попадая в организм человека они начинают размножаться. Инкубационный период может быть от нескольких часов до года и больше. Действие их проявляется характерными симптомами, опираясь на которые опытный врач отличает вид инфекции.
Интенсивность симптомов – самый первый критерий. У бактериальных инфекций они проявляются сильнее и в более тяжелой форме.
У бактериальных инфекций они проявляются сильнее и в более тяжелой форме.
Особенности вирусной инфекции
ОРВИ – это целая группа болезней, возникающих при заражении разнообразными вирусами. Отличить один от другого можно по анализам, необходимость проведения которых определяет врач.
Заражение проявляется во всем теле, так как вирус редко поражает только одну область.
- Для вируса характерно бурное начало.
- Температура поднимается вплоть до 40 градусов.
- Обильные прозрачные выделения из носа часто сопровождаются слезотечением.
- В горле — першение и боль, сиплый голос, появляется сухой кашель.
- Возникают симптомы общей интоксикации: озноб, мышечная и суставная боль, головная боль и отсутствие аппетита.
Особенности бактериальной инфекции
Она чаще всего присоединяется к вирусной, когда иммунитет уже ослаблен, при этом всегда имеет четкую локализацию – нос, уши или легкие.
- Начало болезни медленное (бактерии развиваются медленнее)
- Температура поднимается постепенно и несильно.
- Общее состояние меняется незаметно – от начала заболевания до первых проявлений до 2 недель.
- Появляются характерные (гнойные) выделения из носа.
- Кашель чаще всего влажный, но мокрота отходит с трудом.
- На миндалинах и на языке – налет.
- Появляются признаки бронхита, отита, гайморита или пневмонии.
Различить инфекции можно по анализу крови. Для лечения бактериальной требуются антибиотики и помощь врача.
Квалифицированную консультацию педиатра можно получить в медицинском центре «Таврия».
Здесь же можно сдать все необходимые анализы:
- клинические — крови, мочи, мокроты;
- бактериологические;
- серологические;
- биохимический анализ крови;
- рентгенологические.
Анализы необходимы для определения типа возбудителя инфекции и постановки точного диагноза. Назначенные физиопроцедуры можно сделать здесь же.
Назначенные физиопроцедуры можно сделать здесь же.
Поделитесь статьёй в соцсетях:
Бактериальная инфекция: как распознать и предотвратить?
Время сезонных простуд, гриппа и ОРВИ не заставило себя ждать, и, к сожалению, неокрепшему организму ребёнка еще трудно противостоять этим болезням. Если у ребенка появился жар, насморк и болит горло, возникает вопрос: что является причиной заболевания – бактерия или вирус? Про признаки вирусной инфекции мы рассказывали здесь, сегодня же поговорим о бактериальных инфекциях.
Признаки бактериальной инфекции и ее лечение
В отличие от вирусов, нуждающихся в носителе, бактерии – это полноценные одноклеточные микроорганизмы, способные существовать самостоятельно. Они есть везде – в земле, воде, воздухе, на нашей коже и внутри нас, при этом большинство бактерий для человека безвредны, а некоторые даже полезны, например микрофлора кишечника.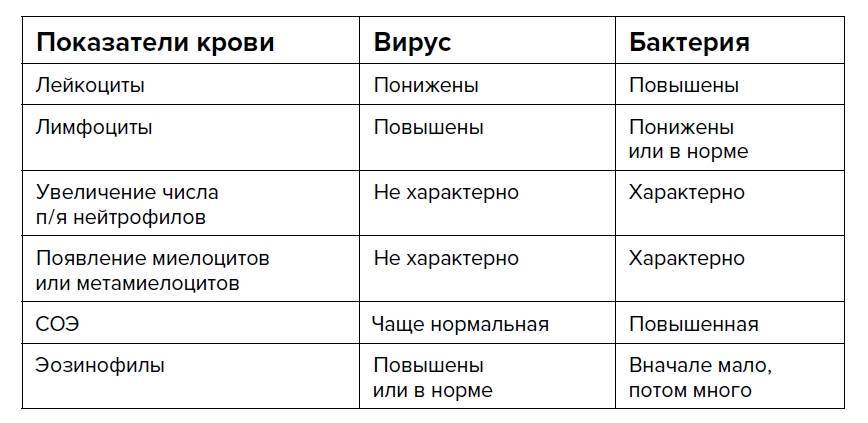
Однако существуют и опасные для нас бактерии. Симптомы, которыми проявляется бактериальная инфекция, распространяются только на какую-то конкретную часть тела, а не на весь организм. Обратите внимание, не болит ли у ребенка только в каком-то одном месте. Например, инфекции, поражающие уши, будут проявляться острой и постоянной болью в пораженном ухе. Проверьте, не отекли ли лимфоузлы (они расположены на шее, ниже ушей, в подмышечных впадинах, в районе локтя, в паху и за коленом)? Когда организм борется с бактериальной инфекцией, у лимфоузлов начинается непростое время, что дает о себе знать их отеком. Также признаком такого рода инфекции служит высокая температура (выше 38 градусов по Цельсию).
Общий признак бактериальных инфекций: состояние здоровья без лечения ухудшается. Вылечить бактериальную инфекцию можно только медикаментозно.
В зависимости от типа инфекции, ее локализации, иммунитета больного, состояния его здоровья, а также используемых лекарств, заболевание может длиться от 5 до 14 дней. Общим признаком бактериальных инфекций является то, что с течением времени состояние здоровья без лечения ухудшается. Вылечить бактериальную инфекцию можно только медикаментозно – антибиотиками.
Общим признаком бактериальных инфекций является то, что с течением времени состояние здоровья без лечения ухудшается. Вылечить бактериальную инфекцию можно только медикаментозно – антибиотиками.
При первых симптомах подозрения на бактериальную инфекцию необходимо показать ребенка врачу. Только он сможет назначить необходимые антибиотики для лечения выявленной им бактериальной инфекции. Строго следуйте указаниям врача: принимайте лекарства по графику, не пропуская ни дня. Пропить нужно полный курс, чтобы избежать рецидива. Когда ребенок начнет прием антибиотиков, он перестанет быть заразным – это, кстати, еще одна причина скорее начать лечение.
Виды бактериальной инфекции
Среди бактериальных инфекций выделим опасные для детей пневмококковую и менингококковую. Пневмококковая инфекция – это тяжелое заболевание, в основном, у детей до двух лет, протекает в виде менингитов, пневмоний, отитов и др. Пневмококк часто присутствует на слизистых оболочках, где он может затаиться и выжидать удобного момента для атаки на организм.
Пневмококк часто присутствует на слизистых оболочках, где он может затаиться и выжидать удобного момента для атаки на организм.
Дети до пяти лет могут болеть пневмококковыми инфекциями многократно.
В настоящее время ученым известно примерно 80 разных типов пневмококковой инфекции, некоторые из которых являются представителями микрофлоры дыхательных путей человека. Основная особенность пневмококка – это специфическая оболочка, защищающая микроорганизм и препятствующая выработке иммунитета к заболеваниям, которые он вызывает. Именно поэтому дети до пяти лет могут болеть пневмококковыми инфекциями многократно.
Кроме того, бактерия передается при чихании и кашле ее носителя и может проникать в спинномозговую жидкость, кровь и другие среды, вызывая самые разные заболевания. Особенно подвержены таким недугам маленькие дети, иммунитет которых недостаточно силен для борьбы с пневмококком, а также пожилые люди старше 60 лет.
Менингококковая инфекция – это острое инфекционное заболевание, причиной которого является бактерия Neisseria meningitidis. Коварство этой инфекции в том, что начальные клинические проявления заболевания напоминают простуду или грипп. Тяжесть менингококковой инфекции колеблется от назофарингита до молниеносного сепсиса, приводящего к смерти за несколько часов. Немногие инфекции имеют столь катастрофическое течение. Около 10% заболевших менингококковой инфекцией умирают, а у 20% возникают инвалидизирующие осложнения.
Коварство этой инфекции в том, что начальные клинические проявления заболевания напоминают простуду или грипп. Тяжесть менингококковой инфекции колеблется от назофарингита до молниеносного сепсиса, приводящего к смерти за несколько часов. Немногие инфекции имеют столь катастрофическое течение. Около 10% заболевших менингококковой инфекцией умирают, а у 20% возникают инвалидизирующие осложнения.
В настоящее время основным методом профилактики является активная иммунизация – вакцинация.
Основой эффективного лечения является ранняя диагностика заболевания, которая позволяет начать лечебные мероприятия максимально быстро, чтобы спасти жизнь и здоровье человека. Возбудитель менингококковой инфекции постоянно циркулирует среди различных возрастных групп населения, но наибольшую эпидемическую опасность для окружающих представляют бактерионосители. Считается, что на одного больного приходится 1200 бактерионосителей. Чаще носителями являются взрослые, даже не подозревая об этом, а болеют преимущественно дети.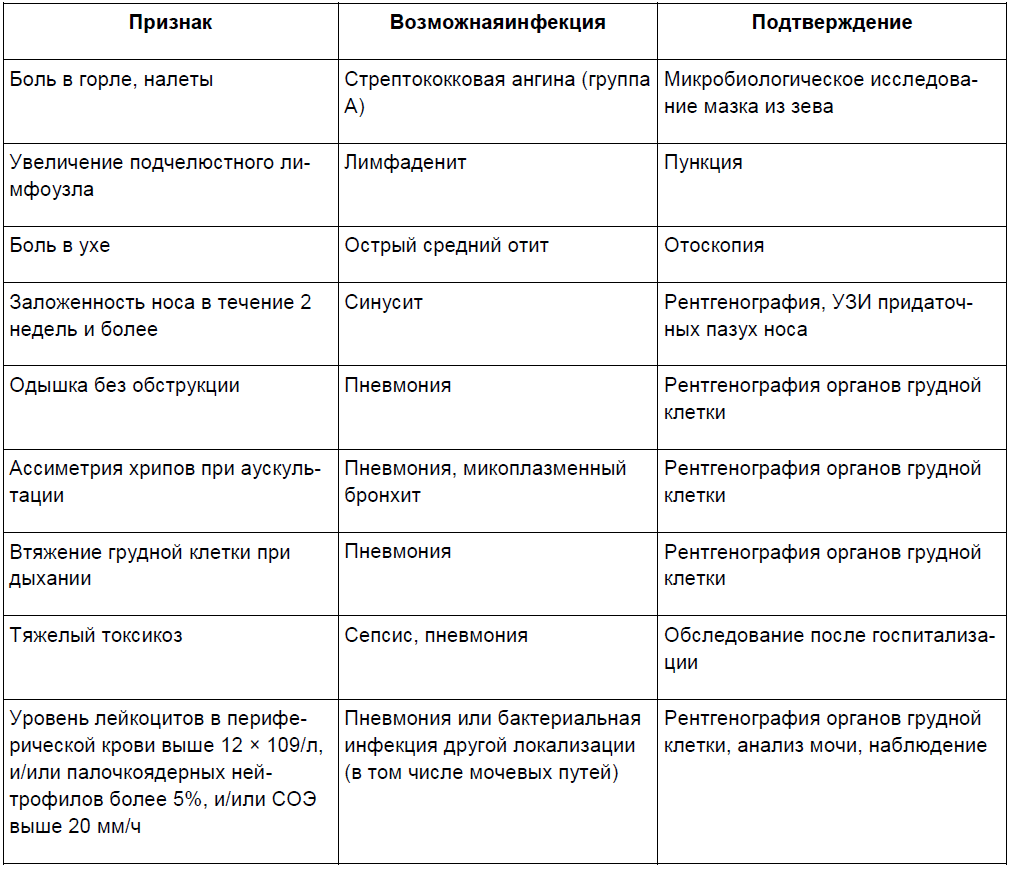
Профилактика бактериальных инфекций
В настоящее время основным методом профилактики является активная иммунизация – вакцинация. Несколько лет назад пневмококковая прививка в России не была обязательной профилактической мерой и проводилась только в отдельных случаях: например, детям, страдающим различными хроническими заболеваниями (бронхитами, заболеваниями сердца и т.д.), сахарным диабетом, ВИЧ-инфицированным и т.д. Однако на фоне роста количества заболеваний, вызванных пневмококком, а также ухудшения эпидемиологической ситуации в стране, было принято решение внести пневмококковую прививку в Национальный календарь прививок, начиная с 2014 года.
Промывайте солевым раствором нос ребенку после прихода с улицы или из общественных мест, чтобы удалить вирусы и бактерии с поверхности слизистой оболочки.
Дети дошкольного возраста чаще всего заражаются бактериальной инфекцией в детских садах, торговых и развлекательных центрах, а иногда и дома от простуженных родителей. Ведь бактерии, как и вирусы, передаются достаточно легко: по воздуху, если вы оказались поблизости с чихающим или кашляющим человеком, после совместной игры, при соприкосновении с предметами личной гигиены носителя вируса.
Ведь бактерии, как и вирусы, передаются достаточно легко: по воздуху, если вы оказались поблизости с чихающим или кашляющим человеком, после совместной игры, при соприкосновении с предметами личной гигиены носителя вируса.
Поэтому промывайте солевым раствором нос ребенку после прихода с улицы или из общественных мест, чтобы удалить вирусы и бактерии с поверхности слизистой оболочки. Также приучите его мыть руки после прогулки, перед едой и соблюдать правила гигиены (например, при пользовании кулером не пить из одного стаканчика воду с кем-то, даже если это лучший друг).
***
Бактериальная инфекция по анализу крови
27.11.2019
Общий анализ крови (ОАК) — это лабораторный метод, позволяющий объективно оценить качественный и количественный состав клеток крови для диагностики различных заболеваний. Подсчет количества лейкоцитов (WBC), процентное соотношение лейкоцитов (лейкоцитарная формула) и СОЭ (скорость оседания эритроцитов) — основные параметры, отражающие активность вирусных и бактериальных инфекций.
Лейкоциты WBC – «белые рыцари» иммунной системы. Лейкопоэз (образование лейкоцитов) происходит в красном костном мозге. В зависимости от морфологических особенностей (размер клетки, форма ядра, наличие специфических гранул) и функции, которую они выполняют, лейкоциты разделяют на две группы: гранулоциты (нейтрофильные, базофильные и эозинофильные лейкоциты), агранулоциты (моноциты, лимфоциты).
· Нейтрофилы (NE) В сосудистом русле в норме циркулируют два типа NE: палочкоядерные (молодые) и сегментоядерные (зрелые). Более юные элементы гранулоцитарного ряда выходят в кровь из красного костного мозга только при патологии. Основная функция NE- уничтожение микроорганизмов, путем распознавания, активного захвата, и переваривания микробного агента (фагоцитоз). Нейтрофилы участвуют во всех этапах воспалительного процесса.
· Эозинофилы (EO)- ведущие форменные элементы в борьбе с паразитами (простейшие, гельминты), принимают участие в аллергических реакциях.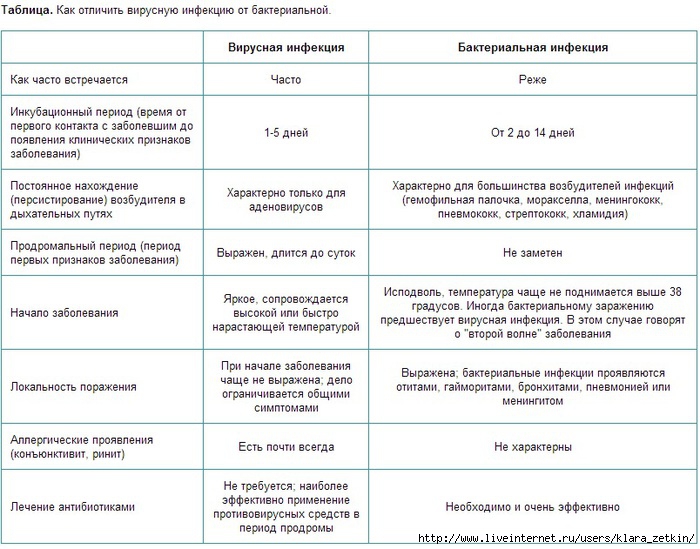
· Базофилы (BA)- принимают участие в аллергических реакциях, а также в регуляции кровообращения посредством секреции гормоноподобных веществ: гистамин, серотонин и гепарин.
· Лимфоциты (LYM)- играют центральную роль во всех иммунологических реакциях организма. Благодаря рецепторам на поверхности клеток, они способны различать «свое» и «чужое». Основная функция LYM- синтез защитных антител и обеспечение иммунной памяти.
· Моноциты (MON)- агранулоцитарные клетки, которые находятся в крови несколько суток, затем покидают кровоток перемещаясь в ткани, где выполняют свою функцию как макрофаги, фагоцитируя частицы более крупных размеров, чем нейтрофилы, а иногда и целые микробные агенты.
· Плазматические клетки (Плазмоциты)- клетки лимфоидной ткани, развивающиеся из клеток – предшественниц В-лимфоцитов, ответственные за выработку антител, в ответ на стимуляцию чужеродными антигенами. В норме в крови плазмоциты не циркулируют.
В норме в крови плазмоциты не циркулируют.
· СОЭ- определяется интенсивностью и скоростью склеивания эритроцитов в кровеносном русле. Этот параметр косвенно указывает на наличие патологического процесса, например, воспаления, в организме.
Для расшифровки анализа все перечисленные показатели важно оценивать в комплексе, а не по-одному. К тому же, для правильной интерпретации изменений в ОАК необходимо учитывать возрастные особенности лейкоцитарной формулы.
Рис.1
При рождении ребенка количество нейтрофилов(NE) преобладает над содержанием лимфоцитов (LYM). На 4-5 дни величина NE и LYM находится приблизительно на одном уровне (Первый перекрест). Далее, начиная со 2-го месяца жизни ребенка, число NE снова уменьшается, а LYM — возрастает, следом показатель NE нарастает, а LYM снижается. Затем, в 4 года количество клеток примерно одинаково (Второй перекрест). Наконец, к четырнадцатилетнему возрасту, процентное соотношении лейкоцитов (WBC) соответствует показателям взрослого человека.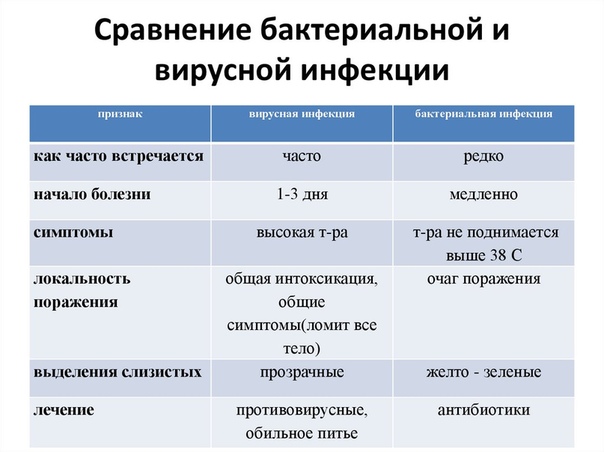
В таблице представлены показатели процентного соотношения WBC.
|
|
|
|
|
|
| ||
|
|
|
| |||||
|
|
|
|
|
|
|
|
|
Признаки бактериальной инфекции по анализу крови.
Человеческий организм постоянно сталкивается с внешними угрозами в виде патогенных микроорганизмов. При подготовке к возможному повреждению в крови быстро образуется мобильный пул циркулирующих нейтрофилов, в результате ускоренного выхода гранулоцитов из красного костного мозга, прекращения выхода нейтрофилов в ткани и мобилизацией пристеночного пула элементов.
При острых бактериальных инфекциях количество этих элементов в крови резко увеличивается, могут появляться менее зрелые клетки. (Сдвиг влево). Интенсивное разрушение зрелых нейтрофилов в тканях приводит к активной продукции костным мозгом более юных клеток. В крови увеличивается количество как самих лейкоцитов, так и отдельной фракции – нейтрофилов.
Чем выше количество этих клеток, тем более активен воспалительный процесс в организме. Нередко эти изменения помогают выявить признаки бактериальной инфекции по анализу крови у взрослых. При воспалительном процессе бактериальной этиологии, характерно повышение в плазме крови некоторых воспалительных белков (фибриногена, церулоплазмина, иммуноглобулинов). Некоторые из этих белков присоединяются к эритроцитам, следовательно, СОЭ увеличивается в разы.
Анализ крови при вирусной инфекции.
Вирусу для репликации необходима полноценная клетка организма, которую он использует как полигон для производства собственного генома, поэтому вирус находит и поражает определенные клетки, содержащие на своей поверхности специфические рецепторы. Для того, чтобы клетки иммунной системы могли отличать инфицированную клетку от здоровой и уничтожить ее, в качестве «метки зараженности» выступают белки главного комплекса гистосовместимости класса I (MHC I). Так активируются Т-лимфоциты, имеющие на своей поверхности определенные рецепторы, с помощью которых они распознают меченные, а значит инфицированные клетки.
Для того, чтобы клетки иммунной системы могли отличать инфицированную клетку от здоровой и уничтожить ее, в качестве «метки зараженности» выступают белки главного комплекса гистосовместимости класса I (MHC I). Так активируются Т-лимфоциты, имеющие на своей поверхности определенные рецепторы, с помощью которых они распознают меченные, а значит инфицированные клетки.
В связи с этим, при острых вирусных заболеваниях в ОАК увеличиваться количество лимфоцитов и/или моноцитов. Общее количество лейкоцитов обычно снижено или в пределах возрастной нормы.
Однако при патологическом процессе вирусной этиологии анализ крови может соответствовать и нормальным показателям здорового человека, а при течении бактериального процесса количество лейкоцитов и абсолютное число нейтрофилов не всегда являются надежным маркером. Именно поэтому для назначения эффективного и адекватного лечения каждый случай должен оцениваться врачом индивидуально.
Кроме того, в настоящее время можно защитить себя и своих родных от многих вирусных и бактериальных инфекций с помощью эффективной и безопасной вакцинации.
Автор: врач-ординатор Университетской клиники H-Clinic Пушик Елена Павловна
Медицинский редактор: руководитель Университетской клиники, к.м.н., врач-инфекционист Коннов Данила Сергеевич
Возврат к списку
Бактериальные инфекции верхних дыхательных путей – как лечить? | Полякова
1. Adoga AA, Okwori ET, Yaro JP, Iduh AA. Pediatric otorhinolaryngology emergencies at the Jos University Teaching Hospital: Study of frequency, management, and outcomes. Ann Afr Med, 2017 Apr-Jun, 16(2):81-84. doi: 10.4103/aam.aam_21_16.
2. Heikkinen T, Jarvinen A. The common cold. Lancet, 2003, 361: 51.
3. Баранов А.А., Таточенко В.К., Бакрадзе М.Д. Лихорадящий ребенок. Протоколы диагностики и лечения. 3-е издание. М.: Педиатр. 2017. 304 с.
Баранов А.А., Таточенко В.К., Бакрадзе М.Д. Лихорадящий ребенок. Протоколы диагностики и лечения. 3-е издание. М.: Педиатр. 2017. 304 с.
4. Ababneh MA, Al-Azzam SI, Ababneh R, Rababa’h AM, Demour SA. Antibiotic prescribing for acute respiratory infections in children in Jordan. Int Health, 2017 Mar 1, 9(2): 124-130. doi: 10.1093/inthealth/ihx003.
5. O’Brien K, Bellis TW, Kelson M, Hood K, Butler CC, Edwards A. Clinical predictors of antibiotic prescribing for acutely ill children in primary care: an observational study. Br J Gen Pract, 2015 Sep, 65(638): e585-92. doi: 10.3399/bjgp15X686497.
6. Croche Santander B, Campos Alonso E, Sanchez Carrion A, Marcos Fuentes L, Diaz Flores I, Vargas JC, Fernandez Dominguez B, Toro Ibanez C. Appropriateness of antibiotic prescribing in paediatric patients in a hospital emergency department. An Pediatr (Barc), 2017 Jul 12. pii: S1695-4033(17)30220-5. doi: 10.1016/j.anpedi.2017.06.001. [Epub ahead of print].
An Pediatr (Barc), 2017 Jul 12. pii: S1695-4033(17)30220-5. doi: 10.1016/j.anpedi.2017.06.001. [Epub ahead of print].
7. Жукова О.В., Кононова С.В., Конышкина Т.М. Распределение затрат на фармакотерапию острого обструктивного бронхита у детей в условиях реальной клинической практики и с учетом фармакоэкономических исследований. Фарматека, 2011, 18: 63-67.
8. Таточенко В.К. Антибиотикои химиотерапия инфекций у детей. М.: ИПК Континент пресс, 2008. С. 253. /Tatochenko VK. Antibiotic and chemotherapy of infections in children. M.: IPK Continent Press, 2008. P. 253.
9. Bozic B, Bajcetic M. Use of antibiotics in paediatric primary care settings in Serbia. Arch Dis Child, 2015 Oct, 100(10): 966-9. doi: 10.1136/archdischild-2015-308274.
10. Kanji K, Saatci D, Rao GG, Khanna P, Bassett P, Williams B, Khan M. Antibiotics for tonsillitis: should the emergency department emulate general practice? J Clin Pathol, 2016 Sep, 69(9): 834-6. doi: 10.1136/jclinpath-2016-203808. Epub2016 Jun 29.
Kanji K, Saatci D, Rao GG, Khanna P, Bassett P, Williams B, Khan M. Antibiotics for tonsillitis: should the emergency department emulate general practice? J Clin Pathol, 2016 Sep, 69(9): 834-6. doi: 10.1136/jclinpath-2016-203808. Epub2016 Jun 29.
11. Ong S, Nakase J, Moran GJ, Karras DJ, Kuehnert MJ, Talan DA, EMERGEncy ID NET Study Group. Antibiotic use for emergency department patients with upper respiratory infections: prescribing practices, patient expectations, and patient satisfaction. Ann Emerg Med, 2007 Sep, 50(3): 213-20. Epub 2007 Apr 30.
12. Esposito S, Rosazza C, Sciarrabba CS, Principi N. Inhaled Antibiotic Therapy for the Treatment of Upper Respiratory Tract Infections. J Aerosol Med Pulm Drug Deliv, 2017 Feb, 30(1): 14-19. doi: 10.1089/jamp.2016.1300.
13. M Thompson, HD Cohen, TA Vodicka, PS Blair, DI Buckley, C Heneghan, AD Hay. Duration of symptoms of respiratory tract infections in children: systematic review. BMJ, 2013, 347. doi: https: //doi.org/10.1136/bmj.f7027.
M Thompson, HD Cohen, TA Vodicka, PS Blair, DI Buckley, C Heneghan, AD Hay. Duration of symptoms of respiratory tract infections in children: systematic review. BMJ, 2013, 347. doi: https: //doi.org/10.1136/bmj.f7027.
14. Fokkens WJ, Lund VJ, Mullol J et al. European Position Paper on Nasal Polyps 2012. Rhinology, 2012, 50(Suppl. 23): 1–298.
15. Chow AW, Benninger MS, Brook I et al. IDSA Clinical Practice Guideline for Acute Bacterial Rhinosinusitis in Children and Adults. Clinical Infectious Dis, 2012, 54(8): e72–e112.
16. Hansen JG, Lund E. The association between paranasal computer ized tomography scans and symptoms and signs in a general practice population with acute maxillary sinusitis. Apmis, 2011, 119(1): 44–8.
17. Anon JB, Jacobs MR, Poole MD et al. Antimicrobial treatment guidelines for acute bacterial rhinosinusitis. Otolaryngology head and neck surgery, 2004, 130(Suppl. 1): 1–45.
Anon JB, Jacobs MR, Poole MD et al. Antimicrobial treatment guidelines for acute bacterial rhinosinusitis. Otolaryngology head and neck surgery, 2004, 130(Suppl. 1): 1–45.
18. Лопатин А.С. Назальные деконгестанты: старые препараты и новые формы. Доктор.Ру. 2011, 6 (65): 17–23
19. Рязанцев С.В., Гаращенко Т.А., Гуров А.В., Карнеева О.В., Карпова Е.П., Свистушкин В.М., Абдулкеримов Х.Т., Кошель В.И., Лопатин А.С., Поляков Д.П., Косяков С.Я., Кириченко И.М. Принципы этиопатогенетической терапии острых синуситов. Клинические рекомендации. Москва – Санкт-Петербург. 2014.
20. Cervera J, Villafruela MA, del Castillo F et al. National Consensus on Acute Otitis Media. Acta Otorrinolaringol Esp, 2007, 58(6): 225–31.
21. Янов Ю.К., Рязанцев С.В. Этиопатогенетическая терапия острых средних отитов. Consilium Medicum, 2005, 7(7): 290–97.
Янов Ю.К., Рязанцев С.В. Этиопатогенетическая терапия острых средних отитов. Consilium Medicum, 2005, 7(7): 290–97.
22. Lieberthal AS, Carroll A, EChonmaitree T et al. The Diagnosis and Management of Acute Otitis Media. Pediatrics, 2013, 131(3): 1–38.
23. Casey JR, Pichichero ME. Changes in frequency and pathogens causing acute otitis media in 1995–2003. Pediatr Infect Dis J, 2004, 23(9): 824–828.
24. Карнеева О.В., Поляков Д.П. Современный подход к лечению заболеваний верхних дыхательных путей и среднего уха как мера профилактики тугоухости. Педиатрическая фармакология, 2012, 9(1): 30-34.
25. Поляков Д.П. Терапия острого среднего отита у детей: эволюция международных клинических рекомендаций. Фарматека, 2014, 6: 64-67.
Фарматека, 2014, 6: 64-67.
26. Takahashi H et al. Clinical practice guidelines for the diagnosis and management of acute otitis media (AOM) in children in Japan. Auris Nasus Larynx, 2012, 39: 1–8.
27. Forgie S, Zhanel G, Robinson J. Canadian Paediatric Society Infectious Diseases and Immunization Committee, Management of acute otitis media. Abridged version: Paediatr Child Health, 2009, 14(7): 457–60.
28. Поляков Д.П. Принципы антибактериальной терапии стрептококкового тонзиллофарингита. Вопросы современной педиатрии, 2014, 13(2): 83-88.
29. Chazan B, Raz R, Edelstein H, Kennes Y, Gal V, Colodner R. Susceptibility of Group A Streptococcus to Antimicrobial Agents in Northern Israel: A Surveillance Study. Microb Drug Resist, 2015 Oct, 21(5): 551-555. doi: 10.1089/mdr.2015.0040. Epub 2015.
Microb Drug Resist, 2015 Oct, 21(5): 551-555. doi: 10.1089/mdr.2015.0040. Epub 2015.
30. Shulman ST, Bisno AL, Clegg HW, Gerber MA, Kaplan EL, Lee G, Martin JM, Van Beneden C. IDSA Guideline for GAS Pharyngitis, Clinical Practice Guideline for the Diagnosis and Management of Group A Streptococcal Pharyngitis: 2012 Update by the Infectious Diseases Society of America. Clinical Infectious Diseases, 2012, 3: 1-17.
31. Regoli M, Chiappini E, Bonsignori F, Galli L, de Martino M. Update on the management of acute pharyngitis in children Regoli et al. Italian Journal of Pediatrics, 2011, 37: 10.
32. Espadas Macia D, Flor Macian EM, Borras R, Poujois Gisbert S, Munoz Bonet JI. Streptococcus pyogenes infection in paediatrics: from pharyngotonsillitis to invasive infections. An Pediatr (Barc), 2017 Mar 31. pii: S16954033(17)30056-5. doi: 10.1016/j.anpedi.2017.02.011. [Epub ahead of print].
An Pediatr (Barc), 2017 Mar 31. pii: S16954033(17)30056-5. doi: 10.1016/j.anpedi.2017.02.011. [Epub ahead of print].
33. Дарманян А.С. Совершенствование методов диагностики и лечения острых тонзиллитов у детей. Дисс. канд. мед. наук. 2010
34. Christensen AM, Thomsen MK, Ovesen T, Klug TE. Are procalcitonin or other infection markers useful in the detection of group A streptococcal acute tonsillitis? Scand J Infect Dis, 2014 May, 46(5): 376−383.
35. Skovbjerg S, Roos K, Olofsson S, Lindh M, Ljung A, Hynsjo L, Holm SE, Adlerberth I, Wold AE. High Cytokine Levels in Tonsillitis Secretions Regardless of Presence of Beta-Hemolytic Streptococci. J Interferon Cytokine Res, 2015 Sep, 35(9): 682-689. doi: 10.1089/jir.2014.0123. Epub
36. Fontes MJ, Bottrel FB, Fonseca MT, Lasmar LB et al. Early diagnosis of streptococcal pharyngotonsillitis: assessment by latex particle agglutination test. J Pediatr (Rio J), 2007, 83(5): 465-470.
Fontes MJ, Bottrel FB, Fonseca MT, Lasmar LB et al. Early diagnosis of streptococcal pharyngotonsillitis: assessment by latex particle agglutination test. J Pediatr (Rio J), 2007, 83(5): 465-470.
37. Баранов А.А. (ред.). Руководство по амбулаторно-клинической педиатрии. 2-е изд. М.: ГЭОТАР-Медиа. 2009
38. Маянский Н.А., Алябьева Н.М., Иваненко А.М. с соавт. Бактериальная этиология острого среднего отита у детей до 5 лет: роль Streptococcus pneumoniаe. Вопросы диагностики в педиатрии, 2013, 3: 5-13.
39. Pichichero ME, Doern GV, Kuti JL, Nicolau DP. Probability of achieving requisite pharmacodynamic exposure for oral beta-lactam regimens against Haemophilus influenzae in children. Paediatr Drugs, 2008, 10(6): 391–397.
40. Brook I, Gober AE. Failure to eradicate streptococci and beta-lactamase producing bacteria. Acta Paediatr, 2008 Feb, 97(2): 193-195. doi: 10.1111/j.1651-2227.2007.00610.x.
Brook I, Gober AE. Failure to eradicate streptococci and beta-lactamase producing bacteria. Acta Paediatr, 2008 Feb, 97(2): 193-195. doi: 10.1111/j.1651-2227.2007.00610.x.
41. Brook I, Gober AE. Frequency of recovery of pathogens from the nasopharynx of children with acute maxillary sinusitis before and after the introduction of vaccination with the 7-valent pneumococcal vaccine. Int J Pediatr Otorhinolaryngol, 2007 Apr, 71(4): 575-579. Epub 2007 Jan 30.
42. Dagan R. Impact of pneumococcal conjugate vaccine on infections caused by antibioticresistant Streptococcus pneumoniae. Clin Microbiol Infect, 2009 Apr, 15(Suppl 3): 16-20. doi: 10.1111/j.1469-0691.2009.02726.x.
43. Picazo JJ. Management of antibiotic-resistant Streptococcus pneumoniae infections and the use of pneumococcal conjugate vaccines. Clin Microbiol Infect, 2009 Apr, 15(Suppl 3): 4-6. doi: 10.1111/j.1469-0691.2009.02723.x.
Clin Microbiol Infect, 2009 Apr, 15(Suppl 3): 4-6. doi: 10.1111/j.1469-0691.2009.02723.x.
44. Сидоренко С.В., Грудинина С.А., Филимонова О.Ю. Резистентность к макролидам и линкозамидам среди Streptococcus pneumoniae и Streptococcus pyogenes в Российской Федерации. Клинич. фармакология и терапия, 2008, 17(2): 1–4.
45. King LM, Sanchez GV, Bartoces M, Hicks LA, Fleming-Dutra KE. Antibiotic Therapy Duration in US Adults With Sinusitis. JAMA Intern Med, 2018 Mar 26. doi: 10.1001/jamainternmed.2018.0407. [Epub ahead of print].
46. Бакрадзе М.Д., Таточенко В.К., Полякова А.С., Чащина И.Л., Хохлова Т.А., Гадлия Д.Д., Рогова О.А. Низкая эффективность антибиотиков, назначаемых амбулаторно детям с пневмонией и острым средним отитом, как следствие несоблюдения клинических рекомендаций..gif) Педиатрическая фармакология, 2016, 13(5): 425-430. doi: 10.15690/pf.v13i5.1636.
Педиатрическая фармакология, 2016, 13(5): 425-430. doi: 10.15690/pf.v13i5.1636.
Лечение бактериальных инфекций в ЕМС
Рассказывает дерматовенеролог, врач высшей категории Иванов Артур
Инфекции, передаваемые половым путем (ИППП), вызываемые бактериями.
К ИППП, вызванными бактериями, относят сифилис, гонорею, хламидиоз, уреамикоплазмоз, гарднереллез и др.
Урогенитальный хламидиоз
Инфекционное заболевание, вызываемое Chlamydia trachomatis. У женщин после заражения может протекать бессимптомно, часто переходит в хроническую форму, рецидивирует и сопровождается различными осложнениями, которые нередко являются причиной бесплодия, прерывания беременности.
К особенностям течения данной инфекции у мужчин относятся: многоочаговость (одномоментно поражаются разные органы мочеполового тракта) поражения способствует возникновению уретропростатитов (воспаление уретры и предстательной железы), везикулитов, эпидидимитов, орхитов (воспаление яичек, придатков яичек и семенных пузырьков).
Длительное течение с минимальным проявлением симптомов ведет к репродуктивным и иммунологическим нарушениям за счет воспаления и развития аутоиммунных процессов (агрессия иммунной системы).
Поражение глаз и суставов при определенной наследственной предрасположенности может привести к системному хроническому заболеванию – болезни Рейтера, которая включает три симптома – уретрит, конъюнктивит и артрит).
Инфекция, активная на протяжении длительного периода времени, приводит к снижению эффективности лечения различными антибиотиками.
Инкубационный период хламидиоза составляет 21-30 дней.
Первые клинические симптомы – это жжение, резь при мочеиспускании, учащение мочеиспусканий, слизистые выделения из уретры. Через 1-2 недели данные симптомы стихают и процесс переходит в вялотекущую форму.
В случае отсутствия терапии заболевание переходит в хроническую форму и приводит к поражению верхних отделов генитального тракта (матки, труб, яичников, простаты, яичек) с формированием воспалительного процесса.
Даже после полноценного лечения может возникнуть синдром хронической тазовой боли и бесплодие.
Таким образом, очень важна своевременная диагностика и адекватная терапия хламидиоза. Диагностика осуществляется с использованием различных методов выявления хламидий в ПЦР, ПИФ, при посеве на специфические среды (полимеразная цепная реакция, прямая реакция иммунофлюоресценции, посев отделяемого на среду, для определения наличия роста микроорганизмов).
В комплексной диагностике также используют методику определения специфических антител в крови пациента.
Лечение осуществляют курсами антибактериальных препаратов. Длительность терапии зависит от стадии и активности процесса.
Уреамикоплазма
Поражения урогенитального тракта этим возбудителем во многом схожи с хламидией. Инкубационный период составляет до 3 недель, заболевание характеризуется вялотекущим течением. Среди клинических проявлений нарушение мочеиспускания и появление слизистых выделений, возможно жжение.
Уреамикоплазменные поражения приводят к тяжелым осложнениям. Исключение составляют инфекции, вызванные бактерией «Mycoplasma genitalium». Проявляется в форме хронического воспаления мочеиспускательного канала.
Все пациенты Европейского медицинского центра пользуются такими преимуществами лечения ИППП как:
-
Быстрая и удобная диагностика: возможность использования медикаментозной стимуляции иммунной системы при лечении ИППП, возможность выполнения лабораторных исследований в срочном порядке.
-
Возможность проведения диагностики по моче, сперме, без взятия уретральных мазков.
-
Лечение согласно европейским медицинским протоколам.
-
Вакцинации при вирусных ИППП для профилактики и терапии. Снижение риска инфицирования и частоты возникновения рецидивов в 2 и более раза.
-
В своей работе врачи-венерологи ЕМС используют самое современное оснащение и медикаменты.

Инвитро. Бактериальные инфекции, узнать цены на анализы и сдать в г. Бор
Сифилис иммуноблот IgM (anti-Treponema pallidum IgM immunoblot)
Исследование IgM-антител к антигенам возбудителя сифилиса Treponema pallidum методом иммуноблота используют в качестве дополнительного специфического трепонемного теста при необходимости углубленного исследования при сомнительных результатах скрининговых и подтверждающих тестов диагностики сифилиса.
Сифилис иммуноблот IgG (anti-Treponema pallidum IgG immunoblot)
Исследование IgG-антител к антигенам возбудителя сифилиса Treponema pallidum методом иммуноблота используют в качестве дополнительного специфического трепонемного теста при необходимости углубленного исследования при сомнительных результатах скрининговых и подтверждающих тестов диагностики сифилиса.
Антитела класса IgG к Borrelia burgdorferi
Специфические антитела к возбудителю боррелиоза (болезни Лайма, Lyme Disease), свидетельствующие о текущей или перенесённой в прошлом инфекции.
Антитела класса IgM к Borrelia burgdorferi
Выявление антител класса IgM к Borrelia burgdorferi, как серологического показателя ранних стадий инфекции спирохетами Borrelia, служит лабораторным подтверждением клинического диагноза Лайм-боррелиоза. Тест также можно использовать в диагностике ассоциированных с Borrelia заболеваний: хронической мигрирующей эритемы, доброкачественной лимфоцитомы кожи, атрофического акродерматита, артритов, миокардитов, перикардитов, лимфоцитарного менингорадикулоневрита, нейроборрелиоза.
Боррелии, антитела класса IgM методом Вестерн-блота (anti-Borrelia IgM, Western blot)
Развернутое исследование IgM-антител к антигенам боррелий методом Вестерн-блота. Тест используют как дополнительный для подтверждения результатов ИФА методов серологической диагностики боррелиоза, при подозрении на иксодовый клещевой боррелиоз, болезнь Лайма и ассоциированные патологические состояния: хроническую мигрирующую эритему, доброкачественный кожный лимфаденоз, атрофический хронический акродерматит, артрит, кардит, нейроборрелиоз.
Гонококк, определение ДНК (Neisseria gonorrhoeae, DNA) в моче
Выявление ДНК Neisseria gonorrhoeae в моче используется для подтверждения инфицированности при наличии клинических проявлений воспаления урогенитального тракта (в основном у мужчин), для дифференциации гоноккового и негонококкового уретрита, для контроля эффективности антибактериальной терапии.
Гонококк (Neisseria gonorrhoeae), антигенный тест, различные локализации
Иммунохроматографический тест позволяет визуально и быстро определить присутствие гонорейного антигена в пробах пациента. Применяется в скрининговых исследованиях для постановки предварительного диагноза, а также для оценки эффективности ранее применяемой терапии.
Гарднерелла, определение ДНК (Gardnerella vaginalis, DNA) в моче
Выявление ДНК Gardnerella vaginalis в моче используется для подтверждения инфицированности при наличии признаков воспаления у мужчин или при проявлениях бактериального вагиноза (гарднереллеза) у женщин репродуктивного возраста.
Микобактерии туберкулеза, определение ДНК (Mycobacterium tuberculosis, DNA) в секрете простаты, эякуляте
Определение ДНК возбудителей туберкулеза методом ПЦР позволяет дифференцировать ограниченные и диссеминированные формы туберкулеза даже при отрицательных результатах микробиологических исследований. Исследование также целесообразно использовать при возникновении лихорадки, сопровождаемой ежедневным двойным повышением и понижением температуры тела, на фоне туберкулиновой гиперчувствительности или туберкулиновой анергии.
Helicobacter Pylori IgA (антитела класса IgА к Helicobacter pylori)
Обнаружение IgA-антител к Helicobacter pylori указывает на местное воспаление. Анализ выполняют для диагностики хеликобактериоза у пациентов с гастритом, язвенной болезнью желудка и 12-перстной кишки, а также для мониторинга эрадикации Helicobacter pylori после проведения антибактериальной терапии.
Helicobacter Pylori IgM (антитела класса IgM к Helicobacter pylori)
Антитела класса IgM служат индикатором ранней инфекции Helicobacter pylori. Анализ выполняют с целью выявления причин хронического гастрита, язвенной болезни желудка и 12-перстной кишки, а также для определения степени остроты текущей инфекции.
Anti-H.pylori IgG (антитела класса IgG к Helicobacter pylori)
Антитела класса IgG к Helicobacter pylori – маркер, подтверждающий инфицированность бактерией Хеликобактер пилори. Тест используют для оценки эффективности эрадикационной терапии.
Антитела к Helicobacter pyl. IgG (блот)
Высокоспецифичный тест, выявляющий факт инфицирования Helicobacter pylori. Метод Вестерн-блота для определения антител к хеликобактеру пилори, в отличие от обычного ИФА, дает дифференцированные сведения о наличии антител к спектру антигенов возбудителя.
Антитела к Helicobacter pyl. IgА (блот)
Высокоспецифичный тест диагностики и мониторинга инфекции Helicobacter pylori – основной причины ассоциированного гастрита и язвенной болезни желудка и 12-перстной кишки. Метод Вестерн-блота для определения антител к Helicobacter pylori, в отличие от обычного ИФА, дает дифференцированные сведения о наличии антител к спектру антигенов возбудителя.
Метод Вестерн-блота для определения антител к Helicobacter pylori, в отличие от обычного ИФА, дает дифференцированные сведения о наличии антител к спектру антигенов возбудителя.
ИНБИОФЛОР. Условно-патогенные микоплазмы, мониторинг эффективности лечения (Ureaplasma parvum, ДНК человека (КВМ)).
ИНБИОФЛОР – комплексное исследование микрофлоры урогенитального тракта. Предлагаемый комплекс состоит из нескольких отдельных профилей для скрининговой оценки состава микрофлоры слизистых оболочек мочеполовой системы и мониторинга эффективности проводимой терапии. Профиль может быть использован для контроля эффективности терапии воспалительных заболеваний урогенитального тракта после установления возбудителя.
Микоплазма, определение ДНК (Mycoplasma pneumoniae, DNA) в слюне
Определение ДНК Mycoplasma pneumoniae в биоматериале методом полимеразной цепной реакции (ПЦР) с детекцией в режиме «реального времени» применяют для диагностики атипичной пневмонии и для оценки эффективности проводимой антибактериальной терапии.
Anti-Mycoplasma hominis-IgM/G (антитела класса IgM и класса IgG к Mycoplasma)
Выявление антител класса IgM к возбудителю урогенитального микоплазмоза применяют для диагностики острой и текущей инфекции. Антитела класса IgG вырабатываются в организме человека в период выраженных клинических проявлений заболевания.
Anti-Mycoplasma pneumoniae-IgM/G (антитела класса IgM и класса IgG к Mycoplasma pneumoniae)
Антитела класса IgM и класса IgG служат индикатором текущей или имевшей место в прошлом инфекции Mycoplasma pneumoniae. Антитела класса IgM, специфичные к Mycoplasma pneumonia, появляются вскоре после начала заболевания. Достоверный прирост уровня IgG антител может указывать на текущую инфекцию или реинфекцию.
Антитела класса IgA к Mycoplasma hominis
Тест применяют для диагностики патологических состояний, ассоциируемых с Mycoplasma hominis. Концентрация IgA в крови коррелирует с выраженностью патологического процесса на уровне слизистых оболочек.
Микоплазма, определение ДНК (Mycoplasma hominis, DNA ) в моче
Выявление ДНК Mycoplasma hominis в моче используется для подтверждения инфицированности при наличии клинических проявлений в нижних отделах мочеполового тракта (цистит, уретрит). Может выявляться у клинически здоровых лиц.
Микоплазма, определение ДНК (Mycoplasma pneumoniae, DNA) в плазме крови
Определение ДНК Mycoplasma pneumoniae в плазме крови методом полимеразной цепной реакции (ПЦР) с детекцией в режиме «реального времени» применяют для дифференциальной диагностики микоплазменной пневмонии и других инфекционных заболеваний дыхательных путей, а также для оценки эффективности антибактериальной терапии.
Уреаплазма, определение ДНК (Ureaplasma urealyticum+parvum, DNA) в моче
Выявление ДНК Ureaplasma urealyticum + parvum в моче используется для подтверждения инфицированности при наличии характерных признаков воспаления мочеполовой системы, при стертой картине воспаления, при планировании беременности, бесплодии. Может выявляться у клинически здоровых лиц.
Может выявляться у клинически здоровых лиц.
Уреаплазма, определение ДНК (Ureaplasma parvum, DNA) в моче
Выявление ДНК Ureaplasma parvum в моче используется для подтверждения инфицированности при наличии характерных признаков воспаления мочеполовой системы, при стертой картине воспаления, при планировании беременности, бесплодии. Может выявляться у клинически здоровых лиц.
Уреаплазма , определение ДНК (Ureaplasma urealyticum, DNA) в моче
Выявление ДНК Ureaplasma urealyticum в моче используется для подтверждения инфицированности при наличии клинических проявлений в нижних отделах мочеполового тракта (цистит, уретрит), при стертой картине воспаления. Может выявляться у клинически здоровых лиц.
Антитела класса IgA к Ureaplasma urealyticum
Обнаружение в сыворотке крови антител класса IgА к Ureaplasma urealyticum указывает на первичное инфицирование. Также их появление возможно при реинфицировании или обострении инфекции.
Антитела класса IgG к Ureaplasma urealyticum
Антитела класса IgG – маркер текущей или перенесенной инфекции Ureaplasma urealyticum. Тест выполняют при подозрении на уреаплазмоз, в комплексе с исследованиями, направленными на выявление других патогенов при негонококковых уретритах, воспалительных заболеваниях матки и придатков, сальпингитах, бесплодии и других патологических состояниях, ассоциируемых с Ureaplasma urealyticum.
Аnti- Chlamydia tr. IgA + anti- Chlamydia tr. IgG
Антихламидийные антитела в крови – серологический маркер урогенитального хламидиоза. Антитела класса IgA к возбудителю вырабатываются в организме человека в период выраженных клинических проявлений заболевания. Антитела класса IgG являются маркером перенесенной в недавнем прошлом инфекции.
Anti-Сhlamydia tr.-IgM (Антитела класса IgМ к Chlamydia trachomatis)
Антитела класса IgM появляются первыми в ходе иммунного ответа организма на проникновение инфекционного агента. Присутствие в крови IgM-антител к Chlamydia trachomatis наблюдается в раннем периоде заболевания или в начале обострения хронического процесса.
Присутствие в крови IgM-антител к Chlamydia trachomatis наблюдается в раннем периоде заболевания или в начале обострения хронического процесса.
Хламидии, определение ДНК (Chlamydia trachomatis, DNA) в моче
Выявление ДНК хламидий в моче используется для подтверждения инфицированности (в основном у мужчин) при наличии клинических проявлений воспаления урогенитального тракта, для контроля эффективности антибактериальной терапии.
Anti-Chlamydophila pneumoniae IgA
Анализ на выявление антител класса IgA к Chlamydophila pneumoniae выполняют при подозрении на инфекцию Chlamydia pneumoniae при длительном кашле, фарингитах, синуситах, отитах, острых и хронических бронхитах, пневмонии, поскольку данные антитела являются маркером первичной инфекции.
Anti-Chlamydophila pneumonia-IgM (антитела класса IgM к Chlamydophila pneumonia)
Обнаружение IgM-антител в сыворотке крови указывает на текущую или недавнюю инфекцию Chlamydophila pneumonia. Исследование также целесообразно провести при длительном кашле, фарингитах, синуситах, отитах, острых и хронических бронхитах, пневмонии.
Исследование также целесообразно провести при длительном кашле, фарингитах, синуситах, отитах, острых и хронических бронхитах, пневмонии.
Хламидия, определение ДНК (Chlamydophila pneumoniae, DNA) в плазме крови
Специфичный тест, направленный на определение ДНК Chlamydоphila pneumoniae в плазме крови высокочувствительным методом полимеразной цепной реакции (ПЦР) с детекцией в режиме «реального времени», предназначен для диагностики респираторного хламидиоза.
Хламидия, определение ДНК (Chlamydophila pneumoniae, DNA) в слюне
Определение ДНК Chlamydophila pneumoniae методом полимеразной цепной реакции (ПЦР) с детекцией в режиме «реального времени» используют в диагностике персистирующих (хронических) инфекций верхних дыхательных путей, атипичного воспаления легких, пневмонии, устойчивой к антибиотикотерапии.
Anti-Chlamydophila pneumonia-IgG (антитела класса IgG к Chlamydophila pneumonia)
Обнаружение IgG-антител в сыворотке крови указывает на текущую или имевшую место в прошлом инфекцию Chlamydia pneumoniae. Исследование также целесообразно провести при длительном кашле, фарингитах, синуситах, отитах, острых и хронических бронхитах, пневмонии.
Исследование также целесообразно провести при длительном кашле, фарингитах, синуситах, отитах, острых и хронических бронхитах, пневмонии.
Листерия (Listeria monocytogenes), антигенный тест, кал
Тест предназначен для качественного выявления антигена Listeria monocytogenes в фекалиях человека с целью ранней диагностики листериозa; дифференциальной диагностики заболеваний, сопровождаемых увеличением печени и селезенки, судорогами, абдоминальными болями, лихорадкой, тошнотой, рвотой, диареей на фоне повышения температуры тела до 38-39° С с поражением лимфоидной ткани и нервной системы; для оценки эффективности терапии.
Пневмококк (Streptococcus pneumoniae), антигенный тест, моча
Тест предназначен для выявления пневмонии и менингита, вызванных пневмококком (Streptococcus pneumoniae), на ранних стадиях заболевания. Особенно эффективен при невозможности собрать мокроту. Результаты теста не зависят от предыдущей антибиотикотерапии.
Особенно эффективен при невозможности собрать мокроту. Результаты теста не зависят от предыдущей антибиотикотерапии.
Посев на метициллинрезистентный золотистый стафилококк, МРЗС (Staphylococcus aureus, MRSA)
Посев на Staphylococcus aureus – микробиологическое исследование, позволяющее выявить инфицированность золотистым стафилококком и подобрать рациональную антибиотикотерапию. При обнаружении патогенных и/или условно-патогенных микроорганизмов определяется их чувствительность к антимикробным препаратам (антибиотикам и бактериофагам).
Посев на золотистый стафилококк (Staphylococcus aureus)
Микробиологический метод с использованием специальных питательных сред позволяет выделить золотистый стафилококк, тем самым доказав его наличие в организме и возможную роль в развитии патологии либо скрытое бактерионосительство.
Антитела класса IgG Bordetella pertussis
Тест направлен на выявление антител класса IgG к антигенам и к токсину Bordetella pertussis – возбудителю коклюша. Положительный результат теста может определяться при текущей или имевшей место в прошлом инфекции Bordetella pertussis, а также после вакцинации против коклюша.
Положительный результат теста может определяться при текущей или имевшей место в прошлом инфекции Bordetella pertussis, а также после вакцинации против коклюша.
Антитела класса IgM к Bordetella pertussis
Антитела класса IgM являются маркером первичной инфекции Bordetella pertussis или обнаруживаются после недавней вакцинации против коклюша.
Посев на патогенную кишечную флору
Посев на патогенную кишечную флору используют для определения этиологии острого кишечного инфекционного заболевания и выбора рациональной антибиотикотерапии. Тест целесообразно проводить при заболеваниях желудочно-кишечного тракта, сопровождаемых поносами (основная цель исследования – выявление дизентерии и сальмонеллеза у детей и взрослых).
РПГА с Shigella flexneri 1-5 (Shigella flexneri 1-5, IHA)
Серологическая диагностика дизентерии — исследование антител к Shigella flexneri подтипов 1-5 методом РПГА (реакция пассивной гемагглютинации).
РПГА с Shigella flexneri 6 (Shigella flexneri 6, IHA)
Серологическая диагностика дизентерии — исследование антител к Shigella flexneri подтипа 6 методом РПГА (реакция пассивной гемагглютинации).
РПГА с Shigella sonnei (Shigella sonnei, IHA)
Серологическая диагностика дизентерии – исследование антител к Shigella sonnei методом РПГА (реакция пассивной гемагглютинации). Тест выполняют с целью диагностики острых кишечных инфекций.
РПГА с Yersinia Enterocolitica серотипа О3 (Y. enterocolitica O3, IHA)
Исследование антител к Yersinia enterocolitica серотипа О:3 методом РПГА (реакция непрямой гемагглютинации) снижает потенциально возможные перекрестные реакции с другими микроорганизмами (Brucella abortus, Rickettsia spp., Salmonella spp., Morganella morganii) и используется в комплексе тестов при подозрении на иерсиниоз.
РПГА с Yersinia pseudotuberculosis (Y. pseudotuberculosis IHA)
Выявление специфических антител к возбудителю псевдотуберкулеза методом РПГА (реакция пассивной, или непрямой гемагглютинации) применяется в комплексе тестов при подозрении на иерсиниоз.
РПГА с Salmonella O-комплекс (Salmonella O-antigens, IHA)
Выявление в сыворотке крови антител к O-антигену сальмонелл применяют в качестве вспомогательного теста при диагностике острых кишечных инфекций (после первой недели заболевания и далее в динамике через неделю) для подтверждения клинического диагноза при получении отрицательного результата бактериологического обследования; в целях ретроспективного подтверждения диагноза; при затяжном течении заболевания.
РПГА с Salmonella gr.A (Salmonella gr.A, IHA)
Выявление антител к O-антигену сальмонелл серогруппы A применяют в качестве вспомогательного теста при диагностике острых кишечных инфекций (после первой недели заболевания и далее в динамике через неделю).
РПГА с Salmonella gr.D (Salmonella gr.D, IHA)
Выявление антител к O-антигену сальмонелл серогруппы D применяют в качестве вспомогательного теста при диагностике острых кишечных инфекций (после первой недели заболевания и далее в динамике через неделю)..jpg)
Антитела к Salmonella gr.E, РПГА (Salmonella gr.E antibodies, IHA)
Выявление антител к O-антигену сальмонелл серогруппы E применяют в качестве вспомогательного теста при диагностике острых кишечных инфекций (после первой недели заболевания и далее в динамике через неделю).
Кампилобактер (Campylobacter spp.), антигенный тест, кал
Антигенный тест в образцах кала применяют при проведении скрининговых исследований для постановки предварительного диагноза кампилобактериоза; для дифференциальной диагностики заболеваний, сопровождаемых диареей (иногда с примесью крови), судорогами, абдоминальными болями, лихорадкой, тошнотой, рвотой, поражением лимфоидной ткани и нервной системы; для оценки эффективности ранее применяемой терапии.
Посев на клостридии диффициле (Clostridium difficile)
Clostridium difficile является основной причиной антибиотико-ассоциированной диареи и псевдомембранозного колита. Посев на клостридии проводят для дифференциальной диагностики со стафилококковым энтероколитом, имеющим схожие проявления.
Посев на клостридии проводят для дифференциальной диагностики со стафилококковым энтероколитом, имеющим схожие проявления.
Антитела класса IgA к антигенам Yersinia Enterocolitica (Аnti-Yersinia Enterocolitica IgA)
Антитела класса IgA к антигенам Yersinia enterocolitica служат серологическим маркером текущей инфекции. Yersinia enterocolitica может длительно персистировать в слизистой кишечника и лимфатической ткани. Персистенция возбудителя может ассоциироваться с персистенцией специфических IgA-антител.
Антитела к столбнячному анатоксину, IgG Tetanus Toxoid IgG Antibody
Антитела класса IgG к возбудителю столбняка появляются в организме в ответ на инфицирование возбудителем столбняка или вакцинацию столбнячным анатоксином. В большинстве случаев тест используют для оценки уровня антитоксических антител после вакцинации против столбняка.
Подходы к терапии бактериальных инфекций дыхательных путей с учетом современных данных о микробиоме | Колосова
1. Bosch A., Biesbroek G., Trzcinski K., Sanders E.M., Bogaert D. Viral and Bacterial Interactions in the Upper Respiratory Tract. PLoS Pathog 2013; 9(1): e1003057. DOI: 10.1371/journal.ppat.1003057
Bosch A., Biesbroek G., Trzcinski K., Sanders E.M., Bogaert D. Viral and Bacterial Interactions in the Upper Respiratory Tract. PLoS Pathog 2013; 9(1): e1003057. DOI: 10.1371/journal.ppat.1003057
2. Murphy T., Bakaletz L., Smeesters P. Microbial interactions in the respiratory tract. Pediatr Infect Dis J 2009; 28(10): S121–S126. DOI: 10.1097/INF.0b013e3181b6d7ec
3. De Steenhuijsen P.W.A., Sanders E.A., Bogaert D. The role of the local microbial ecosystem in respiratory health and disease. Phil Trans R Soc 2015; B370: 20140294. DOI: 10.1098/rstb.2014.0294
4. Tracy M., Cogen J., Hoffman L.R. The Pediatric Microbiome and the Lung. Curr Opin Pediatr 2015; 27(3): 348–355. DOI: 10.1097/MOP.0000000000000212
5. McCullers J.A. Insights into the interaction between influenza virus and pneumococcus. Clin Microbiol Rev 2006; 19: 571–582. DOI: 10.1128/CMR.00058-05
McCullers J.A. Insights into the interaction between influenza virus and pneumococcus. Clin Microbiol Rev 2006; 19: 571–582. DOI: 10.1128/CMR.00058-05
6. Wang J.H., Kwon H.J., Jang Y.J. Rhinovirus enhances various bacterial adhesions to nasal epithelial cells simultaneously. Laryngoscope 2009; 119(7): 1406–1411. DOI: 10.1002/lary.20498
7. Verkaik N.J., Nguyen D.T., de Vogel C.P., Moll H.A., Verbrugh H.A., Jaddoe V.W. et al. Streptococcus pneumoniae exposure is associated with human metapneumovirus seroconversion and increased susceptibility to in vitro HMPV infection. Clin Microbiol Infect 2011; 17(12): 1840–1844. DOI: 10.1111/j.1469-0691.2011.03480.x
8. Sajjan U.S., Jia Y., Newcomb D.C., Bentley J.K., Lukacs N.W., LiPuma J.J. et al. H. influenzae potentiates airway epithelial cell responses to rhinovirus by increasing ICAM-1 and TLR3 expression. FASEB J 2006; 20(12): 2121–2123. DOI: 10.1096/fj.06-5806fje
FASEB J 2006; 20(12): 2121–2123. DOI: 10.1096/fj.06-5806fje
9. Yokota S., Okabayashi T., Yoto Y., Hori T., Tsutsumi H., Fujii N. Fosfomycin suppresses RS-virus-induced streptococcus pneumoniae and haemophilus influenzae adhesion to respiratory epithelial cells via the platelet-activating factor receptor. FEMS Microbiol Lett 2010; 310(1): 84–90. DOI: 10.1111/j.1574-6968.2010.02049.x
10. Goulding J., Godlee A., Vekaria S., Hilty M., Snelgrove R., Hussell T. Lowering the threshold of lung innate immune cell activation alters susceptibility to secondary bacterial superinfection. J Infect Dis 2011; 204(7): 1086–1094. DOI: 10.1093/infdis/jir467
11. Teo S.M., Mok D., Pham K., Kusel M., Serralha M., Troy N. et al. The infant nasopharyngeal microbiome impacts severity of lower respiratory infection and risk of asthma development. Cell Host Microbe 2015; 17: 704–715. DOI: 10.1016/j.chom.2015.03.008
Cell Host Microbe 2015; 17: 704–715. DOI: 10.1016/j.chom.2015.03.008
12. Учайкин В.Ф., Харламова Ф.С., Шамшева О.В., Полеско И.В. Инфекционные болезни. Атлас руководство. М.: ГЭОТАР Медиа, 2010; 384.
13. Manual of Childhood Infections. The Blue Book. Fourth Edition Oxford, 2016; 1032.
14. Белевский А.С., Княжеская Н.П. Тиамфеникола глицинат ацетилцистеинат: некоторые аспекты применения при острых и хронических легочных заболеваниях. Практическая пульмонология 2017; 3: 122–126.
15. Инструкция по медицинскому применению препарата Флуимуцил-антибиотик ИТ, регистрационный номер: П N012977/01-090609. https://grls.rosminzdrav.ru/Grls_View_v2.aspx?routingGuid=cb2ce15f-58e5-4f22-b534-8bfcfd27a0b9&t=74d849bf-34e4-4fb5-9953-25fd328f0fb5. Ссылка активна на 15.12.2017.
Ссылка активна на 15.12.2017.
16. Чучалин А.Г., Соодаева С.К., Авдеев С.Н. Флуимуцил: механизмы действия и значение в терапии заболеваний органов дыхания. М.: Изд-во Zambon Group S.P.A, 2004; 53.
17. Drago L., De Vecchi E., Fassina M.C. Comparative in vitro activity of thiamphenicol-glycinate and thiamphenicol-glycinate-acetylcysteinate and other antimicrobials against respiratory pathogens. Arzneimittelforschung 2001; 51(4): 315–324.
18. Геппе Н.А., Малявина У.С., Дронов И.А., Титова Е.Л. Новая технология в лечении риносинуситов у детей. Доктор.Ру 2010; 1: 7–10.
19. Карпова Е.П., Тулупов Д.А. О возможностях небулайзерной терапии в лечении острых риносинуситов у детей. Российская оториноларингология 2013; 4: 7–10.
20. Grassi C., De Benedetto F. Recent clinical evidence of the efficacy and safety of thiamphenicol glycinate acetylcysteinate and thiamphenicol glycinate. J Chemother 2002; 14(3): 279–284.
21. Овчаренко С.И., Капустина В.А., Сон Е.А. Успешное применение ингаляционной формы флуимуцил-антибиотика ИТ в комплексной терапии инфекционно-воспалительных заболеваний органов дыхания. Фарматека 2010; 11: 42–45.
22. Todisco T., Eslami A., Baglioni S., Todisco C. An open, comparative pilot study of thiamphenicol glycinate hydrochloride vs clarithromycin in the treatment of acute lower respiratory tract infections due to Chlamydia pneumonia. J Chemother 2002; 14(3): 265–271.
23. Геппе Н. А., Колосова Н.Г., Дронов И.А. Опыт применения тиамфеникола глицинат ацетилцистеината при остром бронхите у детей. Пульмонология 2017; 27(4): 496–501.
А., Колосова Н.Г., Дронов И.А. Опыт применения тиамфеникола глицинат ацетилцистеината при остром бронхите у детей. Пульмонология 2017; 27(4): 496–501.
24. Serra A. Schito G.C., Nicoletti G., Fadda G. A therapeutic approach in the treatment of infections of the upper airways: thiamphenicol glycinate acetylcysteinate in sequential treatment (systemic-inhalatory route). Int J Immunopathol Pharmacol 2007; 20(3): 607–617. DOI: 10.1177/039463200702000319
Это бактериальная инфекция или вирус?
В некоторых случаях нас больше беспокоит то, что инфекция может быть вызвана бактериальной инфекцией. Бактериальные инфекции могут быть результатом «вторичной инфекции» (это означает, что вирус инициировал процесс, а бактерии последовали), когда:
- Симптомы сохраняются дольше ожидаемых 10-14 дней, в течение которых вирус имеет тенденцию длиться
- Температура выше, чем обычно можно ожидать от вируса
- Повышение температуры тела через несколько дней после начала болезни, а не улучшение
Синусит, ушные инфекции и пневмония — частые примеры вторичных инфекций. Например, насморк, который сохраняется более 10-14 дней, может быть инфекцией носовых пазух, которую лучше всего лечить антибиотиками. Боль в ушах и новое начало лихорадки после нескольких дней насморка, вероятно, являются инфекцией уха. В зависимости от возраста вашего ребенка при этих инфекциях может потребоваться или не потребоваться антибиотик.
Например, насморк, который сохраняется более 10-14 дней, может быть инфекцией носовых пазух, которую лучше всего лечить антибиотиками. Боль в ушах и новое начало лихорадки после нескольких дней насморка, вероятно, являются инфекцией уха. В зависимости от возраста вашего ребенка при этих инфекциях может потребоваться или не потребоваться антибиотик.
Пневмонию можно определить по постоянному кашлю, боли в животе или затрудненному дыханию. Ваш врач может диагностировать пневмонию при физическом осмотре или может запросить рентген грудной клетки.
Другие бактериальные заболевания, которые вызывают у нас беспокойство, включают инфекции мочевыводящих путей (ИМП), которые трудно обнаружить и которые могут вызвать повреждение почек, если их не лечить.Если у вашего ребенка высокая температура без серьезного источника инфекции, ваш врач, скорее всего, захочет проверить мочу. ИМП чаще встречаются у маленьких девочек и мальчиков в возрасте до одного года, которые не подвергались обрезанию.
Более серьезные опасения вызывают бактериальные заболевания, такие как сепсис (бактерии в крови) и бактериальный менингит (бактериальная инфекция слизистой оболочки головного и спинного мозга). Нас беспокоит менингит у детей старшего возраста с ригидностью шеи или изменениями психического статуса.Младенцы с меньшей вероятностью смогут показать нам эти симптомы, и мы с большей вероятностью проведем с ними больше тестов, чтобы убедиться, что эти инфекции не являются частью болезни.
Помните, что многие вакцины, которые ваш ребенок получает в первые годы жизни, предназначены для предотвращения этих серьезных бактериальных инфекций.
Антибиотиков для лечения инфекций уха у детей
Когда они вам нужны, а когда нет
Многие дети заболевают ушными инфекциями.Инфекции обычно находятся в среднем ухе за барабанной перепонкой. Они могут быть вызваны бактериями или вирусом. Врачи часто лечат бактериальные инфекции антибиотиками. Антибиотики — сильные лекарства, убивающие бактерии.
Врачи часто лечат бактериальные инфекции антибиотиками. Антибиотики — сильные лекарства, убивающие бактерии.
Младенцы и некоторые младенцы и дети нуждаются в антибиотиках.
Но слишком частое употребление антибиотиков может нанести вред. Вот почему:
В большинстве случаев антибиотики не нужны.
- Они не работают при ушных инфекциях, вызванных вирусами.
- Они не помогают боли.
- Обычно вирусные и многие бактериальные инфекции проходят сами по себе в течение двух-трех дней, особенно у детей старше двух лет.
Сначала вызовите врача и снимите боль.
Если вы подозреваете, что у вашего ребенка ушная инфекция, вам следует позвонить в кабинет врача и описать симптомы. Обычно врач просит вас подождать несколько дней, прежде чем привести ребенка.
Главный признак ушной инфекции — боль, особенно в первые сутки.Или у ребенка может подняться температура.
Начните с того, что дайте ребенку безрецептурное обезболивающее, например:
- ацетаминофен (детский или детский тайленол и дженерики).

- ибупрофен (детский мотрин и дженерик).
Антибиотики не снимают боль в первые 24 часа. После этого они лишь незначительно влияют на боль. Таким образом, обезболивающие — важное лечение, и обычно они единственное необходимое лечение.
Дайте большинству детей два или три дня, чтобы поправиться.
Спросите врача, необходимы ли антибиотики или может ли подождать и посмотреть. Дети с ушными инфекциями выздоравливают так же хорошо, как и дети, которые сразу же получают антибиотики. Однако вашему ребенку следует обратиться к врачу, если симптомы не улучшатся в течение двух-трех дней или если они ухудшатся в любое время.
Антибиотики могут иметь побочные эффекты .
Когда дети принимают антибиотики при первых признаках ушной инфекции, из-за лекарств у них чаще возникают рвота, диарея и аллергические реакции.Кроме того, антибиотики могут убить «дружественные» микробы в организме и вызвать другие проблемы, такие как диарея.
Чрезмерное употребление антибиотиков — проблема.
Антибиотики могут способствовать росту устойчивых к лекарствам бактерий. Эти бактерии труднее убить. Они могут вызывать болезни, которые труднее вылечить и которые обходятся дороже. Это увеличивает риск осложнений и побочных эффектов. Устойчивые бактерии также могут заразить других людей.
Антибиотики — пустая трата денег.
Антибиотики, отпускаемые по рецепту, могут стоить до 50 долларов для лечения легкой ушной инфекции у среднего двухлетнего ребенка.Инфекции, устойчивые к лекарствам, могут привести к увеличению количества посещений врачей и увеличению стоимости лекарств.
Когда необходимо лечение антибиотиками?
Если инфекция очень болезненна и длится более нескольких дней, скорее всего, это бактериальная инфекция.
Иногда важно немедленное лечение. Этим детям антибиотики часто нужны сразу:
- Младенцы в возрасте шести месяцев и младше.

- Младенцы в возрасте от шести месяцев до двух лет с умеренной или сильной болью в ушах.
- Дети в возрасте двух лет и старше, у которых температура 102,2 по Фаренгейту или выше.
- Дети с другим заболеванием, которое может затруднить выздоровление, в том числе дети с:
- Расщелина неба
- Синдром Дауна
- Иммунное расстройство
- А кохлеарный имплант
Этот отчет предназначен для использования при разговоре со своим врачом. Это не заменяет медицинские консультации и лечение. Вы используете этот отчет на свой страх и риск.
Разработано в сотрудничестве с Американской академией семейных врачей.
02/2021
Сепсис у детей: узнайте признаки
Когда у ребенка или взрослого есть инфекция, иммунная система организма срабатывает, чтобы бороться с ней. Столкнувшись с вирусной инфекцией (например, простудой или гриппом) или бактериальной инфекцией (например, стрептококком), ребенок может испытывать такие симптомы, как жар, боль в горле, ломота в теле и головная боль. Эти симптомы обычно поддаются лечению, и здоровый иммунный ответ гарантирует, что ребенок полностью выздоровеет в течение нескольких дней.
Эти симптомы обычно поддаются лечению, и здоровый иммунный ответ гарантирует, что ребенок полностью выздоровеет в течение нескольких дней.
Иногда, когда иммунная система выпускает химические вещества в кровоток для борьбы с инфекцией, эти химические вещества могут атаковать нормальные органы и ткани. Эта чрезмерная иммунная реакция называется сепсисом и может вызвать воспаление, проблемы с кровотоком, низкое кровяное давление, проблемы с дыханием и отказ жизненно важных органов. Сепсис у детей и взрослых может быть опасным для жизни.
Кто подвержен риску развития сепсиса?
Сепсис встречается редко, но может развиться у детей или взрослых любого возраста.Чаще всего встречается в:
- Новорожденные и младенцы в возрасте до 3 месяцев , незрелая иммунная система которых не может бороться с подавляющими инфекциями
- Дети, не вакцинированные против двух бактерий, которые чаще всего вызывают сепсис, Streptococcus pneumoniae (также называемого пневмококком) и Haemophilus influenzae
- Дети или взрослые с хроническими заболеваниями
- Дети или взрослые с ВИЧ, раком или другими состояниями, ослабляющими иммунную систему
- Пожилые люди
Примечание о сепсисе у младенцев:
Сепсис, поражающий новорожденных, почти всегда вызывается бактериями в крови. Общие виновники включают стрептококки группы B (GBS), Escherichia coli (E. coli), Listeria monocytogenes , Neisseria meningitis, Streptococcus pneumoniae , Haemophilus influenzae типа B и сальмонеллы.
Общие виновники включают стрептококки группы B (GBS), Escherichia coli (E. coli), Listeria monocytogenes , Neisseria meningitis, Streptococcus pneumoniae , Haemophilus influenzae типа B и сальмонеллы.
Недоношенные дети, особенно те, которые вынуждены проводить время в отделении интенсивной терапии, наиболее подвержены риску сепсиса, поскольку у них недостаточно развитая иммунная система и они могут подвергаться воздействию бактерий в результате процедур, включающих длительные внутривенные (IV) линии, катетеры или трубки и дыхание трубки, прикрепленные к вентилятору.
Иногда инфекции, передаваемые от матери ребенку, могут вызывать сепсис. Следующие факторы могут повысить риск заражения новорожденного:
- Инфекция матери / лихорадка во время родов
- Инфекция матки или плаценты
- Разрыв амниотического мешка до 37 недель
- Разрыв амниотического мешка за 18+ часов до родов
До 30 процентов беременных женщин являются носителями стрептококка группы B (GBS), который может передаваться ребенку во время родов. Женщин проверяют на наличие этой бактерии на поздних сроках беременности с помощью простого мазка, и, если он присутствует, матери вводят антибиотики внутривенно во время родов, чтобы предотвратить передачу. Стрептококк группы B безвреден для матери.
Женщин проверяют на наличие этой бактерии на поздних сроках беременности с помощью простого мазка, и, если он присутствует, матери вводят антибиотики внутривенно во время родов, чтобы предотвратить передачу. Стрептококк группы B безвреден для матери.
Какие симптомы сепсиса у ребенка?
У новорожденных или младенцев с сепсисом могут проявляться следующие симптомы:
- Вздутие мягкого пятна
- Изменения частоты пульса
- Уменьшение мочеиспускания
- Затруднения при пробуждении от сна
- Отсутствие интереса к кормлению или трудности с кормлением
- Лихорадка (ректальная температура) 100.4 градуса или больше
- Неспособность или нежелание смотреть в глаза
- Раздражительность или безутешный плач
- Желтуха (желтоватая кожа и / или глаза)
- Летаргия
- Пауза в дыхании более 10 секунд (апноэ)
- Сыпь
- Болезненный вид
- Изменение цвета кожи (бледное, пятнистое, голубоватое)
- Проблемы с дыханием или учащенное дыхание
Симптомы сепсиса у младенцев старше 3 месяцев и детей могут включать:
- Путаница
- Затрудненное дыхание
- Затруднения при пробуждении от сна
- Существующая инфекция (например, пневмония) с ухудшением симптомов вместо улучшения
- Температура 102 градуса и выше
- Неспособность или нежелание смотреть в глаза
- Раздражительность
- Летаргия
- Гоночное сердце
- Сыпь
- Изменение цвета кожи
- Проблемы с дыханием
Если вы заметили какой-либо из этих симптомов, немедленно обратитесь к врачу вашего ребенка. Младенцам с высокой температурой или любому ребенку с тяжелыми симптомами может потребоваться неотложная медицинская помощь.
Младенцам с высокой температурой или любому ребенку с тяжелыми симптомами может потребоваться неотложная медицинская помощь.
Что такое септический шок?
Сепсис считается тяжелым, если у кого-то проявляется хотя бы один из следующих симптомов, которые могут указывать на органную недостаточность:
- Боль в животе
- Нарушение сердечной деятельности
- Изменение психического статуса
- Снижение тромбоцитов
- Затрудненное дыхание
- Значительно уменьшился диурез
Септический шок характеризуется серьезными симптомами и очень низким кровяным давлением, которое не поддается лечению.
Как диагностируют сепсис у детей?
Если врач вашего ребенка подозревает сепсис или хочет исключить серьезную инфекцию, он может заказать:
- Кровь анализов. Изучив образец крови, врач вашего ребенка может выявить инфекцию, нарушение функции печени или почек или низкий уровень кислорода, которые могут указывать на сепсис.

- Анализы мочи. Изучив образец мочи, врач вашего ребенка может найти бактерии, которые могут указывать на сепсис.
- Люмбальная пункция. Изучив образец спинномозговой жидкости, врач вашего ребенка может проверить наличие инфекции, в том числе менингита.
- Рентгеновские снимки. Рентген может показать пневмонию или другие состояния, которые могут вызвать сепсис.
Врач может сразу же назначить вашему ребенку антибиотики, даже до того, как эти анализы вернутся. Если у вашего ребенка сепсис, ему или ей нужно будет лечить в больнице антибиотиками и внутривенными вливаниями, а в некоторых случаях — лекарствами от кровяного давления и оборудованием, которое поможет ребенку дышать. Раннее лечение имеет решающее значение для предотвращения повреждения органов.
Как уберечь ребенка от сепсиса.
Невозможно предотвратить все случаи сепсиса. Но есть способы защитить своего ребенка от многих инфекций, которые могут привести к сепсису:
Но есть способы защитить своего ребенка от многих инфекций, которые могут привести к сепсису:
- Убедитесь, что ваш ребенок вакцинирован против Streptococcus pneumoniae (также называемого пневмококком) и Haemophilus influenzae в возрасте и в дозах, рекомендованных Центрами по контролю и профилактике заболеваний .
- Если вы беременны, убедитесь, что вы прошли тест на СГБ между 35 и 37 неделями, и проверьте свои результаты, чтобы знать, нужны ли вам антибиотики во время родов. Если у вас возникли преждевременные роды, спросите своего врача, следует ли вам принимать антибиотики. Если вы знаете, что вы инфицированы СГБ, отправляйтесь в больницу вскоре после появления симптомов родов или при отхождении воды.
- Убедитесь, что вы и другие люди, контактирующие с вашими детьми, прошли вакцинацию и часто мойте руки, чтобы предотвратить заражение.Не позволяйте больным посетителям находиться рядом с младенцами и детьми.
- Если вашему ребенку нужны медицинские устройства, такие как катетеры или долгосрочные внутривенные инъекции, следуйте указаниям врача по очистке и доступу к устройству.

- Немедленно обратитесь к врачу вашего ребенка, если вы заметили какие-либо из вышеперечисленных симптомов или другие симптомы или поведение, которые вас беспокоят.
Зарегистрироваться
Следите за новостями о здоровье, которые важны для ваших детей. Подпишитесь на рассылку новостей здоровья детей и получайте больше советов прямо на ваш почтовый ящик.
Заболеваемость, клинический профиль и факторы риска серьезных бактериальных инфекций у детей, госпитализированных с лихорадкой в Удджайне, Индия | BMC Infectious Diseases
NICE: Лихорадочное заболевание у детей: оценка и начальное лечение у детей младше 5 лет. Клинические рекомендации Национального института здравоохранения и качества обслуживания № 160. NICE, Лондон, 2013 г. [Доступно по адресу: https://www.nice.org.uk/CG047].
Детское глобальное бремя болезней, Здоровье подростков, Райнер Р.С. мл., Олсен Х.Э., Икеда К.Т., Эчко М.М. , Баллестрерос К.Э., Мангуэрра Х., Мартопулло И., Миллеар А. и др.Болезни, травмы и факторы риска в здоровье детей и подростков, 1990-2017 гг .: результаты исследования глобального бремени болезней, травм и факторов риска, 2017 г. JAMA Pediatr. 2019; 173 (6): e1
, Баллестрерос К.Э., Мангуэрра Х., Мартопулло И., Миллеар А. и др.Болезни, травмы и факторы риска в здоровье детей и подростков, 1990-2017 гг .: результаты исследования глобального бремени болезней, травм и факторов риска, 2017 г. JAMA Pediatr. 2019; 173 (6): e1
.
Артикул
Google Scholar
Клигман Р., Джем III Дж. Стрит, Блюм Н., Шах С., Уилсон К., Бехерман Р. (ред.). Учебник педиатрии Нельсона, 21-е издание. Филадельфия: Elsevier Inc; 2020.
Kanchanachitra C, Lindelow M, Johnston T, Hanvoravongchai P, Lorenzo FM, Huong NL.Wilopo SA, dela Rosa JF: Кадровые ресурсы здравоохранения в Юго-Восточной Азии: дефицит, проблемы распределения и международная торговля услугами здравоохранения. Ланцет. 2011. 377 (9767): 769–81.
PubMed
Статья
Google Scholar
Патхак A: Уроки, полученные в результате назначения диагнозов и надзора за устойчивостью к антибиотикам в Удджайне, Индия: затишье перед бурей. Швеция Институт Каролоски, Стокгольм, Швеция; 2012. [Доступно по адресу: https: // openarchive.ki.se/xmlui/handle/10616/40948].
Швеция Институт Каролоски, Стокгольм, Швеция; 2012. [Доступно по адресу: https: // openarchive.ki.se/xmlui/handle/10616/40948].
NHFS-4: Национальное обследование здоровья семьи-4-Министерство здравоохранения и благополучия семьи, правительство Индии, Международный институт демографических наук, Мумбаи. В.; 2015–16 гг. [Доступно по адресу: http://rchiips.org/nfhs/NFHS-4Reports/India.pdf/].
Бхарти Б., Бхарти С., Верма В. Тяжелая пневмония в отдаленной холмистой местности: комплексное лечение детских болезней. Индийский J Pediatr. 2006. 73 (1): 33–7.
PubMed
Статья
PubMed Central
Google Scholar
Заки С.А., Каранде С. Брюшной тиф с множественной лекарственной устойчивостью: обзор. J Infect Dev Ctries. 2011; 5 (5): 324–37.
PubMed
Статья
Google Scholar
Goel S, Mukherjee SB. Инфекция мочевыводящих путей, сказка 50 лет. Indian Pediatr. 2016; 53 (1): 57–8.
Indian Pediatr. 2016; 53 (1): 57–8.
PubMed
Статья
PubMed Central
Google Scholar
Dharmapalan D, Shet A, Yewale V, Sharland M.Сообщается о высоких показателях устойчивости к противомикробным препаратам при инфекциях кровотока у новорожденных и детей в Индии. J Pediatric Infect Dis Soc. 2017; 6 (3): e62–8.
PubMed
Статья
Google Scholar
Батра П., Гупта С., Гомбер С., Саха А. Предикторы менингита у детей с первыми фебрильными припадками. Pediatr Neurol. 2011; 44 (1): 35–9.
PubMed
Статья
Google Scholar
Leroy S, Bressan S, Lacroix L, Andreola B, Zamora S, Bailey B, Da Dalt L, Manzano S, Gervaix A, Galetto-Lacour A. Уточненная лабораторная оценка, оценка риска, позволяющая прогнозировать серьезную бактериальную инфекцию у детей с лихорадкой, реже возраст старше 3 лет. Pediatr Infect Dis J. 2018; 37 (5): 387–93.
Pediatr Infect Dis J. 2018; 37 (5): 387–93.
PubMed
Статья
Google Scholar
Nijman RG, Vergouwe Y, Moll HA, Smit FJ, Weerkamp F, Steyerberg EW, van der Lei J, de Rijke YB, Oostenbrink R.Валидация стула для лихорадки и прокальцитонина для выявления серьезных бактериальных инфекций у детей с лихорадкой. Pediatr Res. 2018; 83 (2): 466–76.
CAS
PubMed
Статья
Google Scholar
Falk G, Fahey T. C-реактивный белок и внебольничная пневмония в амбулаторной помощи: систематический обзор исследований диагностической точности. Fam Pract. 2009. 26 (1): 10–21.
PubMed
Статья
Google Scholar
Институт клинических и лабораторных стандартов. Стандарты эффективности тестирования на чувствительность к противомикробным препаратам; 24-е информационное приложение. CLSI M100-S24. Клинические и лабораторные стандарты. Уэйн: CLSI; 2015.
Уэйн: CLSI; 2015.
Google Scholar
Ярлье В., Николас М.Х., Фурнье Г., Филиппон А. Бета-лактамазы с расширенным спектром действия, обеспечивающие переносимую резистентность к новым бета-лактамным агентам у Enterobacteriaceae: характер распространенности и восприимчивости в больницах.Rev Infect Dis. 1988. 10 (4): 867–78.
CAS
PubMed
Статья
Google Scholar
Магиоракос А.П., Сринивасан А., Кэри Р.Б., Кармели Ю., Фалагас М.Э., Гиске К.Г., Харбарт С., Хиндлер Дж. Ф., Калметер Г., Олссон-Лильеквист Б. и др. Бактерии с множественной лекарственной устойчивостью, широкой лекарственной устойчивостью и устойчивостью к пандемиям: предложение международного эксперта по временным стандартным определениям приобретенной устойчивости. Clin Microbiol Infect. 2012. 18 (3): 268–81.
CAS
Статья
Google Scholar

Де С., Уильямс Г.Дж., Хайен А., Макаскилл П., Маккаскилл М., Айзекс Д., Крейг Дж. Точность правила клинического решения «светофора» для серьезных бактериальных инфекций у маленьких детей с лихорадкой: ретроспективное когортное исследование. BMJ. 2013; 346: f866.
PubMed
PubMed Central
Статья
Google Scholar
Chipwaza B, Mhamphi GG, Ngatunga SD, Selemani M, Amuri M, Mugasa JP, Gwakisa PS.Распространенность бактериальных лихорадочных заболеваний у детей в районе Килоса, Танзания. PLoS Negl Trop Dis. 2015; 9 (5): e0003750.
PubMed
PubMed Central
Статья
CAS
Google Scholar
Benigno Miguel ME. Herrera Labarca Patricio дети до 3 месяцев, госпитализированные по поводу острого фебрильного синдрома: клинический стаж 5 лет. Преподобный Чил Педиатр. 2015; 86 (4): 270–8.
Артикул
Google Scholar

Чоффреди Л.А., Джавери Р. Оценка и лечение лихорадочных детей: обзор. JAMA Pediatr. 2016; 170 (8): 794–800.
PubMed
Статья
PubMed Central
Google Scholar
Надеми З., Кларк Дж., Ричардс К.Г., Уолшоу Д., Кант А.Дж. Причины повышения температуры у детей, обращающихся в больницу на севере Англии. J Inf Secur. 2001. 43 (4): 221–5.
CAS
Google Scholar
Sunguya BF, Koola JI, Atkinson S. Инфекции, связанные с тяжелым недоеданием среди госпитализированных детей в Восточной Африке. Tanzan Health Res Bull. 2006; 8 (3): 189–92.
CAS
PubMed
PubMed Central
Google Scholar
Кумар Р., Сингх Дж., Джоши К., Сингх Х.П., Биджеш С. Сопутствующие заболевания у госпитализированных детей с тяжелой острой недостаточностью питания. Indian Pediatr. 2014. 51 (2): 125–7.
PubMed
Статья
PubMed Central
Google Scholar

Ирена А.Х., Мвамбази М., Муленга В. Диарея — главная причина смерти детей с тяжелой острой недостаточностью питания, госпитализированных в стационар в Лусаке, Замбия. Нутр Дж. 2011; 10: 110.
PubMed
PubMed Central
Статья
Google Scholar
Фонсека В., Кирквуд Б. Р., Виктора К. Г., Фукс С. Р., Флорес Дж. А., Мисаго С. Факторы риска детской пневмонии среди городской бедноты в Форталезе, Бразилия: исследование случай — контроль. Bull World Health Organ.1996. 74 (2): 199–208.
CAS
PubMed
PubMed Central
Google Scholar
Schaible UE, Kaufmann SH. Недоедание и инфекция: сложные механизмы и глобальные последствия. PLoS Med. 2007; 4 (5): e115.
PubMed
PubMed Central
Статья
CAS
Google Scholar
Кумар П., Кумар Р. Кишечная лихорадка. Индийский J Pediatr. 2017; 84 (3): 227–30.
PubMed
Статья
PubMed Central
Google Scholar
Lindsjo C, Sharma M, Mahadik VK, Sharma S, Stalsby Lundborg C, Pathak A. Инфекции в области хирургического вмешательства, их возникновение и факторы риска до и после процедуры антисептической антисептики рук в общем хирургическом отделении сельской больницы в Удджайне , Индия. Am J Infect Control. 2015; 43 (11): 1184–9.
PubMed
Статья
PubMed Central
Google Scholar
Nguyen DK, Friedlander S, Fleischman RJ, Zangwill KM. Продолжительность пребывания и осложнения, связанные с младенцами с лихорадкой <90 дней, госпитализированными в США, 2000-2012 гг.Hosp Pediatr. 2018; 8 (12): 746–52.
PubMed
Статья
Google Scholar
Moorlag S, Arts RJW, van Crevel R, Netea MG. Неспецифические эффекты вакцины БЦЖ при вирусных инфекциях.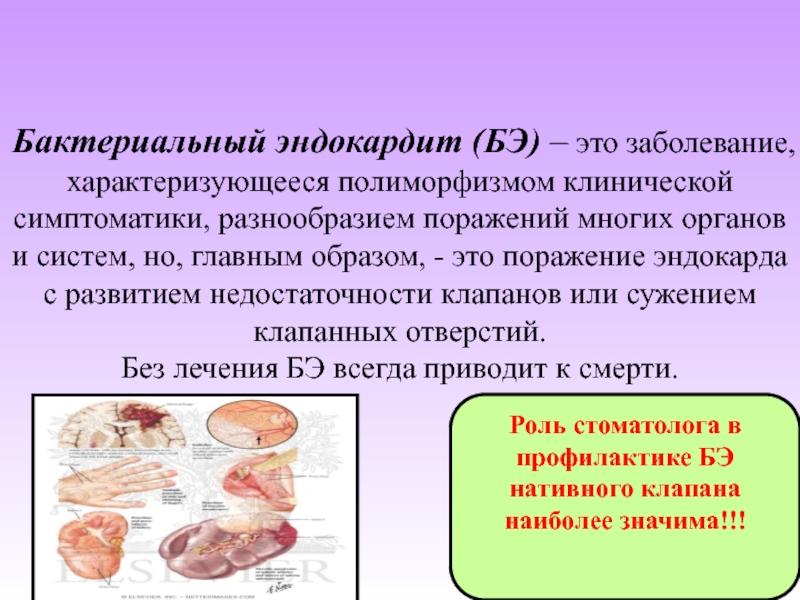 Clin Microbiol Infect. 2019; 25 (12): 1473–8.
Clin Microbiol Infect. 2019; 25 (12): 1473–8.
CAS
PubMed
Статья
Google Scholar
Утаякумар Д., Пэрис С., Чапат Л., Фрейбургер Л., Пуле Х., Де Лука К. Неспецифические эффекты вакцин, проиллюстрированные на примере БЦЖ: от наблюдений к демонстрациям.Фронт Иммунол. 2018; 9: 2869.
CAS
PubMed
PubMed Central
Статья
Google Scholar
Брент А.Дж., Лакханпол М., Томпсон М., Коллиер Дж., Рэй С., Нинис Н., Левин М., Макфол Р. Оценка риска для стратификации детей с подозрением на серьезную бактериальную инфекцию: наблюдательное когортное исследование. Arch Dis Child. 2011; 96 (4): 361–7.
PubMed
PubMed Central
Статья
Google Scholar
Craig JC, Williams GJ, Jones M, Codarini M, Macaskill P, Hayen A, Irwig L, Fitzgerald DA, Isaacs D, McCaskill M. Точность клинических симптомов и признаков для диагностики серьезной бактериальной инфекции у маленьких детей с лихорадкой: проспективное когортное исследование 15 781 фебрильных заболеваний. BMJ. 2010; 340: c1594.
BMJ. 2010; 340: c1594.
PubMed
PubMed Central
Статья
Google Scholar
Sedlacek M, Schoolwerth AC, Remillard BD. Электролитные нарушения в реанимации.Semin Dial. 2006. 19 (6): 496–501.
PubMed
Статья
Google Scholar
Гонсалес К.Ф., Финберг Л., Блюстейн Д.Д. Концентрация электролита при острых инфекциях. Наблюдения у младенцев и детей. Am J Dis Child. 1964; 107: 476–82.
CAS
PubMed
Статья
Google Scholar
Де С., Уильямс Дж. Дж., Хайен А., Макаскилл П., Маккаскилл М., Айзекс Д., Крейг Дж. С..Значение количества лейкоцитов в прогнозировании серьезной бактериальной инфекции у детей в возрасте до 5 лет с лихорадкой. Arch Dis Child. 2014; 99 (6): 493–9.
PubMed
Статья
Google Scholar
Ларру Б. , Гонг В., Вендетти Н., Салливан К.В., Локалио Р., Заутис Т.Э., Гербер Дж. С.. Инфекции кровотока у госпитализированных детей: эпидемиология и чувствительность к противомикробным препаратам. Pediatr Infect Dis J. 2016; 35 (5): 507–10.
, Гонг В., Вендетти Н., Салливан К.В., Локалио Р., Заутис Т.Э., Гербер Дж. С.. Инфекции кровотока у госпитализированных детей: эпидемиология и чувствительность к противомикробным препаратам. Pediatr Infect Dis J. 2016; 35 (5): 507–10.
PubMed
Статья
Google Scholar
Musicha P, Cornick JE, Bar-Zeev N, French N, Masesa C, Denis B, Kennedy N, Mallewa J, Gordon MA, Msefula CL, et al. Тенденции устойчивости к противомикробным препаратам у изолятов инфекций кровотока в крупной городской больнице в Малави (1998–2016 гг.): Эпиднадзорное исследование. Lancet Infect Dis. 2017; 17 (10): 1042–52.
PubMed
PubMed Central
Статья
Google Scholar
Патхак А., Мароти Й, Кекре В., Махадик К., Макаден Р., Лундборг К.С.Высокая распространенность возбудителей бета-лактамаз расширенного спектра действия: результаты эпиднадзора в двух больницах в Удджайне, Индия. Устойчивость к заражению лекарствами. 2012; 5: 65–73.
Устойчивость к заражению лекарствами. 2012; 5: 65–73.
CAS
PubMed
PubMed Central
Статья
Google Scholar
Рудинский С.Л., Карстэйрс К.Л., Рирдон Дж.М., Саймон Л.В., Риффенбург Р.Х., Танен Д.А. Серьезные бактериальные инфекции у детей с лихорадкой в эпоху постпневмококковой конъюгированной вакцины. Acad Emerg Med.2009. 16 (7): 585–90.
PubMed
Статья
PubMed Central
Google Scholar
Thacker N, Pereira N, Banavali SD, Narula G, Vora T., Chinnaswamy G, Prasad M, Kelkar R, Biswas S., Arora B. Эпидемиология инфекций кровотока у педиатрических пациентов в онкологическом центре третичного уровня . Индийский рак J. 2014. 51 (4): 438–41.
CAS
PubMed
Статья
PubMed Central
Google Scholar
Патхак А., Чандран С.П., Махадик К., Макаден Р., Лундборг К.С. Частота и факторы, связанные с носительством комменсальной кишечной палочки с множественной лекарственной устойчивостью, среди женщин, посещающих женские консультации в Центральной Индии. BMC Infect Dis. 2013; 13: 199.
BMC Infect Dis. 2013; 13: 199.
PubMed
PubMed Central
Статья
Google Scholar
Шарма Р., Сайни Н.К. Критическая оценка шкалы социально-экономического статуса Куппусвами в настоящем сценарии. J Family Med Prim Care.2014; 3 (1): 3–4.
PubMed
PubMed Central
Статья
Google Scholar
Индийская академия П., Далвай С., Чоудхури П., Бавдекар С.Б., Далал Р., Капил Ю., Дубей А.П., Югра Д., Агнани М., Сачдев Х.П. и др. Заявление о консенсусе Индийской академии педиатрии по интегрированному ведению тяжелой острой недостаточности питания. Indian Pediatr. 2013. 50 (4): 399–404.
Артикул
Google Scholar
Продолжительность лихорадки и серьезных бактериальных инфекций у детей: систематический обзор | BMC Family Practice
Bruijnzeels MA, Foets M, van der Wouden JC, van den Heuvel WJ, Prins A: Повседневные симптомы в детстве: частота встречаемости и частота консультаций с терапевтом. Br J Gen Pract. 1998, 48: 880-884.
Br J Gen Pract. 1998, 48: 880-884.
CAS
PubMed
PubMed Central
Google Scholar
Berger RM, Berger MY, van Steensel-Moll HA, Dzoljic-Danilovic G, Derksen-Lubsen G: прогностическая модель для оценки риска серьезных бактериальных инфекций у младенцев с лихорадкой.Eur J Pediatr. 1996, 155: 468-473. 10.1007 / BF01955183.
CAS
Статья
PubMed
Google Scholar
Bleeker SE, Derksen-Lubsen G, Grobbee DE, Donders AR, Moons KG, Moll HA: Проверка и обновление правила прогнозирования серьезной бактериальной инфекции у пациентов с лихорадкой без источника. Acta Paediatr. 2007, 96: 100-104.
CAS
Статья
PubMed
Google Scholar
Goh PL, Lee SW, Wong EH: Предикторы серьезной бактериальной инфекции у детей в возрасте от 3 до 36 месяцев с лихорадкой без источника. Singapore Med J. 2006, 47: 276-280.
2006, 47: 276-280.
CAS
PubMed
Google Scholar
Горелик М.Х., Шоу К.Н.: Правило клинического решения для выявления молодых девушек с лихорадкой, подверженных риску инфекции мочевыводящих путей. Arch Pediatr Adolesc Med. 2000, 154: 386-390.
CAS
Статья
PubMed
Google Scholar
Мерфи К.Г., ван де Пол А.С., Харпер М.Б., Бачур Р.Г.: Клинические предикторы скрытой пневмонии у ребенка с лихорадкой. Acad Emerg Med. 2007, 14: 243-249. 10.1111 / j.1553-2712.2007.tb01781.x.
Артикул
PubMed
Google Scholar
Berger MY, Boomsma LJ, Albeda FW, Dijkstra RH, Graafmans TA, Van der Laan JR, Lemmen WH, Oteman N: NHG-Standaard. Киндерен встретил корц (Tweede herziening). Huisarts Wet. 2008, 51 (6): 287-296. 10.1007 / BF03086785. на голландском
Статья
Google Scholar

Ричардсон М., Лакханпаул М., Группа разработки рекомендаций и техническая группа: Оценка и начальное лечение лихорадки у детей младше 5 лет: краткое изложение рекомендаций NICE. BMJ. 2007, 334: 1163-1164. 10.1136 / bmj.39218.495255.AE.
Артикул
PubMed
PubMed Central
Google Scholar
Всемирная организация здравоохранения: позиционный документ ВОЗ по конъюгированным вакцинам против Haemophilus influenzae типа b. Wkly Epidemiol Rec. 2006, 81: 445-452. (Заменяет позиционный документ ВОЗ по вакцинам против Hib, ранее опубликованный в Еженедельном эпидемиологическом журнале)
Google Scholar
Всемирная организация здравоохранения: ВОЗ болезни, предупреждаемые с помощью вакцин: система мониторинга, глобальное резюме за 2005 год. 2006 г., Всемирная организация здравоохранения: международный веб-сайт, [http: // www.who.int/vaccinesdocuments/DocsPDF05/WHO_IVB_2005.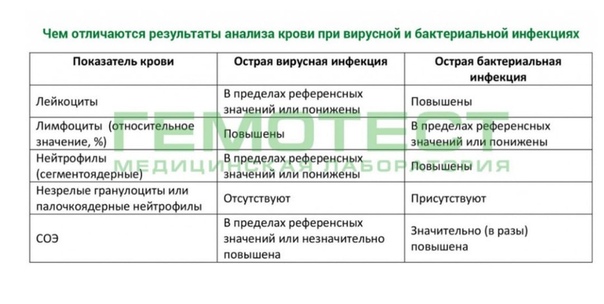 pdf]
pdf]
Google Scholar
Вильчинский Н.Л., Хейнс Р.Б .: Разработка оптимальных стратегий поиска для выявления клинически обоснованных прогностических исследований в MEDLINE: аналитический обзор. BMC Med. 2004, 2: 23-10.1186 / 1741-7015-2-23.
Артикул
PubMed
PubMed Central
Google Scholar
Хайнес Р. Б., Вильчинский Н. Л.: Оптимальные стратегии поиска для получения научно обоснованных исследований диагноза из Medline: аналитический обзор.BMJ. 2004, 328: 1040-10.1136 / bmj.38068.557998.EE.
Артикул
PubMed
PubMed Central
Google Scholar
Робинсон К.А., Дикерсин К. Разработка высокочувствительной стратегии поиска для получения отчетов о контролируемых испытаниях с использованием PubMed. Int J Epidemiol. 2002, 31: 150-153. 10.1093 / ije / 31.1.150.
Артикул
PubMed
Google Scholar
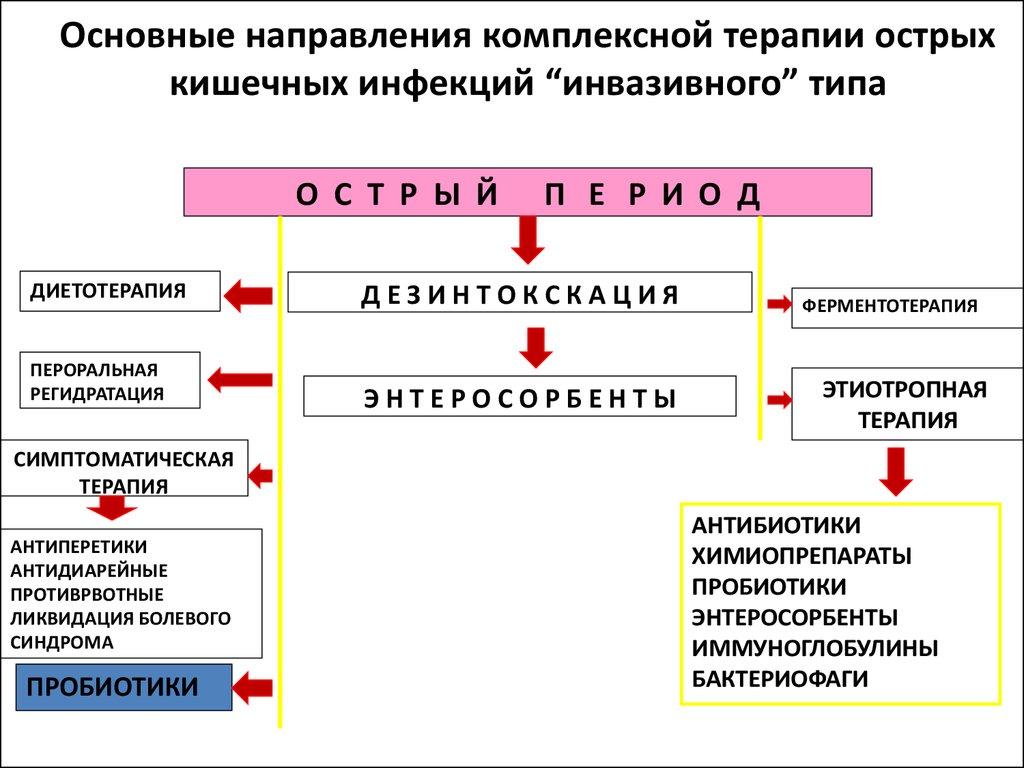
Hayden JA, Cote P, Bombardier C: Оценка качества исследований прогнозов в систематических обзорах. Ann Intern Med. 2006, 144: 427-437.
Артикул
PubMed
Google Scholar
Ландис Дж. Р., Кох Г. Г.: Измерение согласия наблюдателя для категориальных данных. Биометрия. 1977, 33: 159-174. 10.2307 / 2529310.
CAS
Статья
PubMed
Google Scholar
Сакетт Д.Л., Штраус С.Е., Ричардсон В.С., Розенберг В., Хейнс Р. Б.: Доказательная медицина. Как практиковать и преподавать ДМ. 2000, Эдинбург: Черчилль Ливингстон
Google Scholar
Ариенс Г.А., ван Мехелен В., Бонгерс П.М., Боутер Л.М., ван дер Валь Дж .: Физические факторы риска боли в шее. Scand J Work Environ Health. 2000, 26: 7-19.
CAS
Статья
PubMed
Google Scholar
Fernandez Lopez A, Luaces Cubells C, Garcia Garcia JJ, Fernandez Pou J, Испанское общество неотложной медицинской помощи: Прокальцитонин в педиатрических отделениях неотложной помощи для ранней диагностики инвазивных бактериальных инфекций у детей с лихорадкой: результаты многоцентрового исследования и полезность быстрого качественный тест на этот маркер. Pediatr Infect Dis J. 2003, 22: 895-903. 10.1097 / 01.inf.0000091360.11784.21.
Артикул
PubMed
Google Scholar
Hsiao AL, Chen L, Baker MD: Заболеваемость и предикторы серьезных бактериальных инфекций среди младенцев в возрасте от 57 до 180 дней. Педиатрия. 2006, 117: 1695-1701. 10.1542 / peds.2005-1673.
Артикул
PubMed
Google Scholar
Исаакман Д.Д., Берк Б.Л .: Использование сывороточного С-реактивного белка для обнаружения скрытой бактериальной инфекции у детей. Arch Pediatr Adolesc Med. 2002, 156: 905-909.
Артикул
PubMed
Google Scholar
Pulliam PN, Attia MW, Cronan KM: C-реактивный белок у детей с лихорадкой от 1 до 36 месяцев с клинически неопределяемой серьезной бактериальной инфекцией. Педиатрия. 2001, 108: 1275-1279. 10.1542 / peds.108.6.1275.
CAS
Статья
PubMed
Google Scholar
Пратт А., Аттиа М.В.: Продолжительность лихорадки и маркеры серьезной бактериальной инфекции у маленьких детей с лихорадкой. Pediatr Int. 2007, 49: 31-35. 10.1111 / j.1442-200X.2007.02316.x.
CAS
Статья
PubMed
Google Scholar
Trautner BW, Caviness AC, Gerlacher GR, Demmler G, Macias CG: Проспективная оценка риска серьезной бактериальной инфекции у детей, поступающих в отделение неотложной помощи с гиперпирексией (температура 106 градусов по Фаренгейту или выше). Педиатрия. 2006, 118: 34-40. 10.1542 / peds.2005-2823.
Артикул
PubMed
PubMed Central
Google Scholar
Guen CG, Delmas C, Launay E, Caillon J, Loubersac V, Picherot G, Roze JC: Вклад прокальцитонина в обнаружение скрытой бактериемии у детей. Scand J Infect Dis. 2007, 39: 157-159. 10.1080 / 00365540600
3.
Артикул
PubMed
Google Scholar
Van den Bruel A, Haj-Hassan T., Thompson M, Buntinx F, Mant D, Европейская исследовательская сеть по распознаванию серьезных инфекций для исследователей: диагностическая ценность клинических признаков при представлении для выявления серьезной бактериальной инфекции у детей в развитых странах. страны: систематический обзор.Ланцет. 2010, 375: 834-845. 10.1016 / S0140-6736 (09) 62000-6.
Артикул
PubMed
Google Scholar
Андреола Б., Брессан С., Каллегаро С., Ливерани А., Плебани М., Да Дальт Л. Прокальцитонин и С-реактивный белок как диагностические маркеры тяжелых бактериальных инфекций у младенцев с лихорадкой и детей в отделении неотложной помощи. Pediatr Infect Dis J. 2007, 26: 672-677. 10.1097 / INF.0b013e31806215e3.
Артикул
PubMed
Google Scholar
Ван ден Брюэль А., Аэртгертс Б., Брюнинкс Р., Аэртс М., Бантинкс Ф: Признаки и симптомы для диагностики серьезных инфекций у детей: проспективное исследование в первичной медико-санитарной помощи. Br J Gen Pract. 2007, 57: 538-546.
PubMed
PubMed Central
Google Scholar
Хаддон Р.А., Барнетт П.Л., Гримвуд К., Хогг Г.Г.: Бактериемия у детей с лихорадкой, поступающих в педиатрическое отделение неотложной помощи. Med J Aust. 1999, 170: 475-478.
CAS
PubMed
Google Scholar
Teach SJ, Fleisher GR: Продолжительность лихорадки и ее связь с бактериемией у амбулаторных пациентов с лихорадкой от трех до 36 месяцев. Группа изучения оккультной бактериемии. Педиатр Emerg Care. 1997, 13: 317-319. 10.1097 / 00006565-199710000-00004.
CAS
Статья
PubMed
Google Scholar
У детей с лихорадкой исследователи отличают бактериальные инфекции от вирусных
?
ИЗОБРАЖЕНИЕ: Используя технологию микроматриц, исследователи могут различать вирусные и бактериальные инфекции у детей с лихорадкой, анализируя активность генов в образце крови.Хотя необходимы дополнительные исследования, …
посмотреть еще
Кредит: Роберт Бостон, Вашингтонский университет в Сент-Луисе
У детей с лихорадкой, но без других симптомов болезни, трудно определить, есть ли у ребенка вирусная инфекция, которая разрешится сама по себе, или потенциально серьезная бактериальная инфекция, требующая антибиотиков.
Теперь исследователи из Медицинской школы Вашингтонского университета в Сент-Луисе сообщают, что они могут различать вирусные и бактериальные инфекции у детей с лихорадкой, анализируя активность генов в образце крови.В небольшом исследовании анализ генов лейкоцитов был точен более чем на 90 процентов, что намного лучше, чем стандартный диагностический тест, который верен только примерно в 70 процентах случаев.
Исследование опубликовано 15 июля в Proceedings of the National Academy of Sciences Online Early Edition.
Хотя требуется дополнительная работа, результаты исследования подтверждают идею о том, что анализ активности генов организма в ответ на детские инфекции может помочь выявить причину болезни и гарантировать, что дети получат правильное лечение.
«Это обычная проблема, когда у детей развивается лихорадка без какой-либо очевидной причины», — говорит старший автор Грегори Сторч, доктор медицины, профессор педиатрии Рут Л. Ситман и руководитель отделения детских инфекционных заболеваний Медицинской школы Вашингтонского университета и Св. Детская больница Луи. «У некоторых из этих детей серьезные бактериальные инфекции, которые могут быть опасными для жизни, но у большинства из них есть вирусные инфекции. Проблема в том, что с практической точки зрения трудно понять, что есть что.«
В качестве меры предосторожности многие дети, у которых лихорадка без видимой причины, получают лечение антибиотиками, даже если лекарства не действуют против вирусов, а их чрезмерное назначение способствует устойчивости к антибиотикам.
В новом исследовании приняли участие 30 детей в возрасте от двух месяцев до трех лет, у которых была температура выше 100,4 ° F, но не было явных признаков болезни, таких как кашель или диарея. На основании предыдущего обширного геномного тестирования, которое еще не практично для использования в клинических условиях, было известно, что у 22 детей вирусные инфекции, а у восьми других детей были бактериальные инфекции.
Но Сторч и его коллеги из Института генома университета и Центра доступа к геномным технологиям хотели знать, может ли тест, называемый микрочипом экспрессии генов, выявить паттерны активности генов в лейкоцитах, которые могут отличить детей с вирусными инфекциями от детей с бактериальными инфекциями. . Лейкоциты — первая линия защиты иммунной системы от чужеродных захватчиков, и ученые предположили, что они будут иначе реагировать на вирусы, чем на бактерии.
Исследователи также имели доступ к результатам стандартного диагностического теста, проведенного, когда у детей изначально была диагностирована лихорадка в Детской больнице Сент-Луиса. Этот тест включает в себя анализ количества лейкоцитов в образце крови. Как правило, количество повышенных показателей для бактериальных инфекций и низкого или нормального для вирусных инфекций.
«Мы знаем, что есть много исключений из этого правила, и мы, безусловно, увидели это в этом исследовании», — сказал Сторч. «У многих пациентов с вирусными инфекциями было повышенное количество лейкоцитов, поэтому врачи думали, что у них бактериальные инфекции, и прописывали антибиотики, в которых на самом деле не было необходимости.«
Используя технологию микрочипов, исследователи могли легко отличить бактериальные инфекции от вирусных, основываясь на характерных паттернах экспрессии генов. «Это действительно важно для клиницистов, потому что, если они увидят образец экспрессии генов, указывающий на вирусную инфекцию, они могут чувствовать себя комфортно, не прописывая антибиотики», — добавил Сторч.
Для сравнения, исследовательская группа провела микроматричный анализ образцов крови 35 детей без лихорадки в возрасте от 2 месяцев до 3 лет, перенесших амбулаторную операцию.Предыдущее геномное тестирование показало, что у восьми из этих детей были вирусы, хотя они не вызывали никаких симптомов.
«У детей с вирусом и лихорадкой многие гены были очень активны по сравнению с детьми, у которых не было вирусов, но без лихорадки, чьи гены были тихими», — объяснил Сторч. «Микроматрица в основном сообщает нам, как пациент считывает инфекцию. Очень активные гены говорят нам, что инфекция вызывает у пациента заболевание, в то время как тихие гены говорят нам, что либо нет инфекции, либо, возможно, есть бактерия или вирус, но это не так. вызывая лихорадку или болезнь.«
Это различие важно, потому что, когда стандартные тесты предполагают, что у ребенка есть вирус, врачи не знают, вызывает ли этот вирус болезнь ребенка или это невинный прохожий. По словам Сторча, «опасность приписать симптомы вирусу, который на самом деле является невинным свидетелем, заключается в том, что ребенок может не получить необходимые антибиотики».
Это указывает на потенциальную пользу использования тестов, которые измеряют реакцию генов, чтобы получить более убедительные ответы на болезнь.Это поможет обеспечить, чтобы антибиотики были нацелены на тех детей, которые действительно в них нуждаются, добавил он.
Затем Сторч надеется усовершенствовать технологию микрочипов, которая одновременно анализирует все 25 000 генов в организме. Это делает тест слишком затратным по времени и дорогим для использования в условиях клиники. Но он и его коллеги хотят идентифицировать меньшее количество критических генов, которые можно было бы использовать для различения вирусных и бактериальных инфекций, и оценить тест второго поколения у детей в рамках нового исследования.
###
Исследование финансируется за счет грантов NIAID, UL1 RR024992 Национального центра исследовательских ресурсов NIH, Института клинических и трансляционных наук Вашингтонского университета и гранта на обучение T32HD049338 от NICHD. Центр доступа к геномным технологиям Медицинской школы Вашингтонского университета оказал помощь в проведении геномного анализа. Центр частично поддерживается грантом поддержки онкологического центра NCI № P30 CA91842 для онкологического центра Siteman и грантом ICTS / CTSA № UL1RR024992 Национального центра исследовательских ресурсов (NCRR), составляющим часть NIH, и дорожной карты NIH для медицинских исследований. .
Сторч Г.А., Кросби С.Д., Ю. Дж., Ху X. Профили экспрессии генов у детей с лихорадкой и определенной вирусной и бактериальной инфекцией. Труды Национальной академии наук . Онлайн 15 июля 2013 г.
Медицинский факультет Вашингтонского университета 2 100 штатных и добровольных врачей-преподавателей также входят в медицинский персонал больниц Барнс-Еврей и Детских больниц Сент-Луиса. Медицинский факультет — одно из ведущих медицинских научно-исследовательских, учебных и лечебных учреждений в стране, которое в настоящее время занимает шестое место в стране по мнению У.S. News & World Report. Медицинская школа связана с BJC HealthCare через свои связи с больницами Barnes-Jewish и St. Louis Children’s.
Заявление об отказе от ответственности: AAAS и EurekAlert! не несут ответственности за точность выпусков новостей, размещенных на EurekAlert! участвующими учреждениями или для использования любой информации через систему EurekAlert.
Симптомы, Диагностика и лечение> Информационные бюллетени> Йельская медицина
Как и у взрослых, когда у младенцев и детей развивается инфекция, их иммунная система борется с вторгшимся виновником, будь то бактерии, вирус или грибок.Но иногда реакция иммунной системы на инфекцию выходит из-под контроля, что приводит к опасному для жизни состоянию, называемому сепсисом. Сепсис возникает, когда реакция организма на уже имеющуюся инфекцию выходит из-под контроля, что приводит к серьезному воспалению по всему телу, которое, в свою очередь, может вызвать повреждение тканей и отказ органа. Когда органы начинают перестать функционировать, тело может перейти в стадию сепсиса, называемую «септический шок», и угроза смерти неминуема.
Хотя сепсис является серьезным заболеванием в любом возрасте, он особенно опасен для детей, поскольку его симптомы бывает труднее обнаружить.«Самая большая разница между взрослым и детским сепсисом — это признание», — говорит доктор детской интенсивной терапии Йельской медицины Сара Кандил. «Многие симптомы, которые мы ищем при сепсисе, например, лихорадка, похожи на другие болезни у детей».
Хотя детский сепсис — явление необычное, но и не такое уж редкое. По оценкам исследований, в США
ежегодно проходят лечение от тяжелого сепсиса более 75000 детей3.
Сепсис может развиться в результате такой простой травмы, как инфицированная царапина на руке, или он может возникать на фоне уже опасного для жизни состояния, такого как острый аппендицит.«Те, у кого ослабленная иммунная система, например дети, проходящие химиотерапию, могут быть особенно восприимчивыми», — говорит доктор Кандил.

 0-9.0
0-9.0