инструкция по применению, аналоги, состав, показания
Повышенная чувствительность к действующему веществу или растениям семейства сложноцветных (ромашка, арника, календула, тысячелистник) или к любому из вспомогательных веществ.
В связи с возможным иммуностимулирующим действием не принимать в случаях прогрессирующих системных заболеваний, в т.ч. туберкулез, саркоидоз, системные заболевания соединительной ткани (коллагенозы), рассеянный склероз, ВИЧ-инфекция или СПИД, злокачественные заболевания, патология системы лейкоцитов (гемобластозы, агранулоцитоз и др.), состояния иммунодефицита или иммуносупрессии, прием иммунодепрессантов, склонность к аллергическим реакциям (атопический дерматит, бронхиальная астма и др.).
Не рекомендуется беременным и кормящим женщинам, детям до 12 лет.
Частота неизвестна. В отдельных случаях могут отмечаться следующие побочные эффекты:
Могут отмечаться реакции гиперчувствительности (сыпь, крапивница, отек лица, синдром Стивенса-Джонсона, ангиоотек кожи, отек Квинке, анафилактический шок, реакция бронхоспазма с обструкцией и приступ астмы).
Эхинацея может вызвать развитие аллергических реакций у пациентов с атопическими заболеваниями.
Связь с аутоиммунными заболеваниями (рассеянный склероз, диссеминированный энцефалит, узловатая эритема, иммунотромбоцитопения, синдром Эванса, синдром Шегрена с тубулярной почечной дисфункцией) не исключена.
В случае возникновения нежелательных реакций, в том числе не указанных в данной инструкции, следует прекратить прием лекарственного средства и обратиться к врачу.
Иммунал — справочник лекарств — ЗдоровьеИнфо
Состав и форма выпуска. Основное действующее вещество препарата — экстракт эхинацеи. Выпускают: 1) таблетки по 80, 100 мг — 20, 50 шт. в упаковке; 2) капли для приема внутрь — во флаконах по 50 мл; 3) раствор для приема внутрь — по 50, 100 и 150 мл во флаконе.
Лечебные свойства. Оказывает иммуномодулирующее и противовоспалительное действие, стимулирует костномозговое кроветворение.
Показания к применению. Грипп, ОРВИ, инфекционно-воспалительные заболевания носоглотки и полости рта. Профилактика этих заболеваний.
Правила применения. Иммунал. Суточная доза для взрослых и детей старше 12 лет — 20 капель 3 раза в день или по 1 таблетке 3–4 раза в день. При острой стадии заболевания начальная доза — 40 капель, затем первые 2 дня принимают по 20 капель через каждые 2 ч, далее продолжают лечение дозами по 20 капель 3 раза в день. Детям от 1 года до 6 лет — по 5–10 капель 3 раза в день, от 4 до 6 лет — по 1 таблетке 1–2 раза в день, от 6 до 12 лет — 10–15 капель 3 раза в день или по 1 таблетке 1–3 раза в день. Капли и таблетки следует запивать небольшим количеством жидкости, маленьким детям можно растолочь таблетку и смешать с небольшим количеством воды, чая или сока. Для достижения терапевтического эффекта препарат следует принимать не менее 1 недели. Продолжительность 1 курса лечения не должна превышать 8 недель.
Для достижения терапевтического эффекта препарат следует принимать не менее 1 недели. Продолжительность 1 курса лечения не должна превышать 8 недель.
Иммунорм. Взрослым и детям старше 12 лет — по 2.5 мл раствора для приема внутрь в достаточном количестве воды 3 раза в день или по 1 таблетке 3–4 раза в день. Длительность лечения — не более 8 недель. Таблетки можно рассасывать, жевать, запивать водой, время приема таблеток не зависит от времени приема пищи.
Эхинацея Гексал. Взрослым и детям старше 12 лет — по 3 мл (1/2 мерного стаканчика) 3–4 раза в день (с первых признаков заболевания до их исчезновения), курс лечения — не более 2 недель.
Побочные явления. При применении в рекомендуемых дозах побочные явления не выявлены.
Противопоказания. Туберкулез, лейкозы, коллагенозы, рассеянный склероз.
Беременность и лактация. Вопрос о целесообразности применения препарата должен решать врач. Следует избегать приема больших доз препарата.
Взаимодействие с алкоголем. Препарат содержит спирт.
Особые указания. Больным сахарным диабетом следует учитывать, что в 30 каплях препарата содержится 0,02 ХЕ. Помутнение или появление хлопьевидного осадка не оказывает влияния на эффективность препарата.
Условия хранения. Хранить при комнатной температуре. Срок годности — 3 года.
‘
20 отзывов, инструкция по применению
Иммунал — иммуностимулятор на основе эхинацеи пурпурной. Содержит биологически активные вещества, способствующие усилению неспецифического (видового) иммунитета. Увеличивая количество лейкоцитов и стимулируя фагоцитоз, тормозит рост и развитие патогенных микроорганизмов. Помимо этого, препарат обладает противовирусным действием и может использоваться при вирусных и бактериальных респираторных инфекциях, в т.ч. в педиатрической практике. К достоинствам иммуностимуляторов растительного происхождения относится их эффективность, благоприятный профиль безопасности, безрецептурный статус, обусловливающий доступность для населения.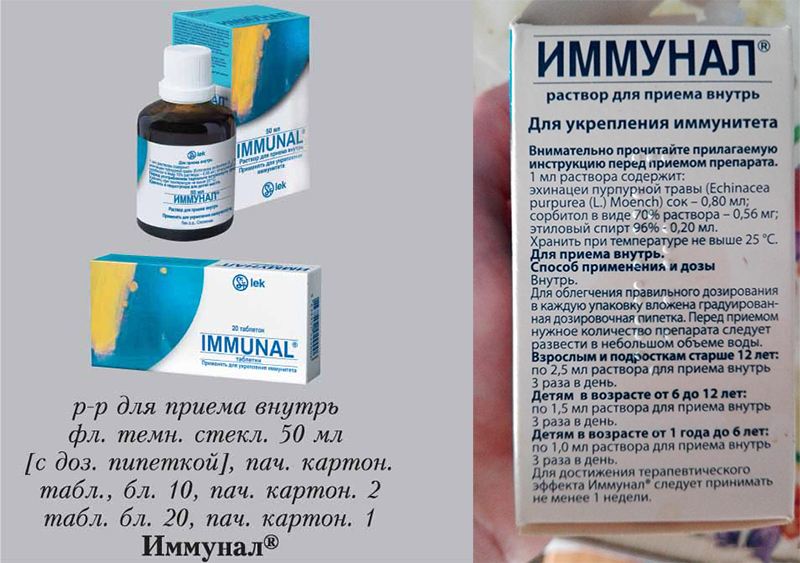 Все вышеперечисленное можно сказать и о препаратах на основе травы эхинацеи, включая иммунал. Активными компонентами эхинацеи являются фенольные кислоты — кофейная и феруловая, а также их производные (гликозид эхинакозид и цикориевая кислота). Полисахарид эхинацин оказывает противомикробное и антимикотическое действие, повышая устойчивость организма (а точнее — его иммунный статус) к бактериальным и вирусным агентам, подавляет очаг воспаления. Сесквитерпеновые эфиры также вносят свой вклад в общую иммуностимулирующую «копилку» препарата. Входящий в состав иммунала полисахарид инулин активирует так называемую систему комплемента — комплекс протеолитических ферментов, являющихся инструментом системы гуморального иммунитета и призванных защищать организм от проникновения чужеродных агентов. Помимо этого, в наземной части эхинацеи содержатся: макро- и микроэлементы, бетаин, флавоноидные гликозиды, фитостерин, насыщенные и омега-3-полиненасыщенные жирные кислоты. Помимо иммуностимулирующего, препарат обладает антиоксидантным действием, подавляя перекисное окисления жиров и защищая клеточные мембраны от повреждений. В различных источниках отмечалось наличие у препаратов эхинацеи сахароснижающего, противоаллергического, гипохолестеринемического, спазмолитического и даже цитостатического действия. Иммунал — наиболее популярный и изученный препарат эхинацеи.
Все вышеперечисленное можно сказать и о препаратах на основе травы эхинацеи, включая иммунал. Активными компонентами эхинацеи являются фенольные кислоты — кофейная и феруловая, а также их производные (гликозид эхинакозид и цикориевая кислота). Полисахарид эхинацин оказывает противомикробное и антимикотическое действие, повышая устойчивость организма (а точнее — его иммунный статус) к бактериальным и вирусным агентам, подавляет очаг воспаления. Сесквитерпеновые эфиры также вносят свой вклад в общую иммуностимулирующую «копилку» препарата. Входящий в состав иммунала полисахарид инулин активирует так называемую систему комплемента — комплекс протеолитических ферментов, являющихся инструментом системы гуморального иммунитета и призванных защищать организм от проникновения чужеродных агентов. Помимо этого, в наземной части эхинацеи содержатся: макро- и микроэлементы, бетаин, флавоноидные гликозиды, фитостерин, насыщенные и омега-3-полиненасыщенные жирные кислоты. Помимо иммуностимулирующего, препарат обладает антиоксидантным действием, подавляя перекисное окисления жиров и защищая клеточные мембраны от повреждений. В различных источниках отмечалось наличие у препаратов эхинацеи сахароснижающего, противоаллергического, гипохолестеринемического, спазмолитического и даже цитостатического действия. Иммунал — наиболее популярный и изученный препарат эхинацеи.
Важно, что в его основе лежит сок именно наземной части этого растения, т.к. терапевтическая эффективность в отношении ОРЗ/ОРВИ была доказана только для таких препаратов. Иммунал можно использовать при длительной терапии антибактериальными и противовирусными лекарственными средствами. Препарат проявляет адаптогенные свойства, что наделяет его максимально соответствующим физиологическому комплексным действием на все иммунологические механизмы. Иммунал хорош как в качестве лечебного средства, так и профилактанта. Клинические исследования наглядно продемонстрировали эффективность использования препарата в острой фазе ОРВИ (но не позднее первых суток заболевания). При этом у больных смягчались клинические проявления инфекции, быстрее происходило исцеление. Прием иммунала способствует снижению вероятности развития бактериальных осложнений ОРВИ. Препарат хорошо переносится при длительном приеме в течение 2-3 месяцев.
При этом у больных смягчались клинические проявления инфекции, быстрее происходило исцеление. Прием иммунала способствует снижению вероятности развития бактериальных осложнений ОРВИ. Препарат хорошо переносится при длительном приеме в течение 2-3 месяцев.
Иммунал выпускается в виде раствора для приема внутрь и таблеток. Рекомендованные разовые дозы препарата в виде раствора составляют: 2,5 мл (для взрослых и детей от 12 лет), 1,5 мл (для детей от 6 до 12 лет), 1 мл (для детей от 1 года до 6 лет). Кратность приема — 3 раза в сутки. Разовая доза иммунала в виде таблеток едина для всех возрастов и составляет 1 таблетку, различается лишь кратность приема: 3-4 раза в день (взрослые и дети старше 12 лет), 1-3 раза в день (дети 6-12 лет), 1 раз в день (дети 4-6 лет). Минимальная длительность лечения — 1 неделя. Таблетки глотаются целиком, либо измельчаются и смешиваются с водой или соком. Для увеличения точности дозирования в упаковку с раствором вкладывается специальная откалиброванная пипетка. При отсутствии терапевтического ответа на прием иммунала в течение 10 дней настоятельно рекомендуется обратиться к врачу. При хранении препарата не следует паниковать при обнаружении хлопьевидного осадка: в таких случаях перед употреблением требуется всего лишь встряхнуть флакон.
Иммунал — Лекарства — Справочники — Медицинский портал «МЕД-инфо»
ИММУНАЛ
Фармакологическое действие
Иммуностимулирующий препарат. Эхинацея пурпурная содержит активные вещества, усиливающие неспецифический иммунитет. Повышая число лейкоцитов (гранулоцитов) и активизируя фагоцитоз, препарат подавляет рост и размножение микроорганизмов. Кроме того, установлено противовирусное действие травы эхинацеи пурпурной в отношении вирусов гриппа и герпеса.
Фармакокинетика
Данные о фармакокинетике препарата Иммунал® не предоставлены.
Показания к применению препарата ИММУНАЛ
®
— для стимуляции иммунитета при неосложненных острых инфекционных заболеваниях и при предрасположенности к частым простудным заболеваниям;
— профилактика ОРВИ и гриппа;
— в качестве вспомогательного средства при продолжительной антибиотикотерапии хронических инфекционных заболеваний, сопровождающихся снижением иммунитета.
Режим дозирования
Препарат в форме раствора для приема внутрь назначают взрослым и подросткам старше 12 лет по 2.5 мл 3сут.сут.; детям в возрасте от 6 до 12 лет — по 1.5 мл 3сут.сут.; детям в возрасте от 1 года до 6 лет — по 1 мл 3сут.сут.
Препарат в форме таблеток назначают взрослым и подросткам старше 12 лет по 1 таблетки 3-4сут.сут.; детям в возрасте от 6 до 12 лет — по 1 таблетки 1-3сут.сут.; детям в возрасте от 4 до 6 лет — по 1 таблетки 1-2сут.сут.
Для достижения клинического эффекта Иммунал® следует принимать не менее 1 недели.
Продолжительность непрерывного приема — не более 8 недель.
Таблетки следует запивать водой. Для маленьких детей рекомендуется растолочь таблетку и смешать с небольшим количеством воды, чая или сока.
Для облегчения правильного дозирования раствора для приема внутрь в каждую упаковку вложена градуированная дозировочная пипетка. Перед приемом необходимое количество капель следует развести в небольшом объеме воды.
Побочное действие
Аллергические реакции: редко — сыпь, гиперемия кожных покровов.
Противопоказания к применению препарата ИММУНАЛ
®
— туберкулез;
— лейкозы;
— коллагенозы;
— рассеянный склероз;
— ВИЧ-инфекция, СПИД;
— повышенная чувствительность к компонентам препарата и растениям семейства сложноцветных.
Применение препарата ИММУНАЛ
® при беременности и кормлении грудью
Пациентка должна быть предупреждена о том, что не рекомендуется применять Иммунал® при беременности и в период лактации (грудного вскармливания) без предварительной консультации с врачом.
Применение у детей в возрасте до 12 лет
Возможно применение по показаниям в дозах, учитывающих возраст пациента.
Особые указания
При хранении раствора для приема внутрь возможно помутнение раствора или выпадение хлопьевидного осадка, состоящего из активных полисахаридов. Перед употреблением следует тщательно встряхнуть флакон.
Передозировка
В настоящее время о случаях передозировки препарата Иммунал® не сообщалось.
Лекарственное взаимодействие
Раствор для приема внутрь содержит этанол, в связи с чем препарат может усиливать или изменять эффект других лекарственных препаратов.
Клинически значимое лекарственное взаимодействие отмечено при применении антибиотиков группы цефалоспоринов (цефамандол, цефотетан, цефменоксим, цефоперазон, моксалактам) и одновременном приеме этанола (даже в небольших количествах). Реакция пациента характеризовалась покраснением лица, тошнотой, повышенным потоотделением, головной болью, учащенным сердцебиением. В связи с этим Иммунал® не следует применять одновременно с вышеперечисленными антибиотиками. Прием Иммунала возможен только через 3 дня после окончания курса лечения указанными цефалоспоринами.
Условия отпуска из аптек
Препарат разрешен к применению в качестве средства безрецептурного отпуска.
Условия и сроки хранения
Препарат следует хранить в недоступном для детей месте при температуре не выше 25°С. Срок годности раствора для приема внутрь – 2 года, таблеток — 3 года.
Профилактика и лечение респираторных заболеваний у детей препаратами эхинацеи пурпурной (препаратом Иммунал®) | Савенкова М.С.
Для лечения и профилактики острых респираторных вирусных инфекций (ОРВИ) в последние годы применяется большое количество противовирусных препаратов и иммуномодуляторов. Практикующий врач нередко испытывает затруднение при выборе и назначении каких-либо иммуномодулирующих препаратов. Как поступить в том случае, если ребенок уже получал разные иммуномодуляторы? Однозначного ответа на этот вопрос нет. Однако, как показывает практика, их назначение необходимо детям с частыми острыми респираторными заболеваниями (ОРЗ).
Как поступить в том случае, если ребенок уже получал разные иммуномодуляторы? Однозначного ответа на этот вопрос нет. Однако, как показывает практика, их назначение необходимо детям с частыми острыми респираторными заболеваниями (ОРЗ).
Клинические особенности
ОРВИ и ОРЗ
ОРВИ являются едва ли не самыми частыми респираторными заболеваниями у детей. Во многом начальные клинические симптомы схожи при разных респираторных заболеваниях – это кашель, ринит, головная боль, увеличение лимфатических узлов, гипертермия, нередко артралгия, боли в животе и др.
У специалистов имеются различные мнения относительно пользы и вреда перенесенных заболеваний детьми разного возраста с позиции стимуляции иммунных ответов. С одной стороны, перенесенные респираторные заболевания способствуют формированию иммунитета. С другой стороны, рецидивирующие заболевания нижних дыхательных путей, особенно у детей первых 3-х лет жизни, способствуют развитию бронхоспазма к 7 годам. Известно, что частые респираторные заболевания приводят к повышению сенсибилизации организма и развитию хронической патологии (бронхиальной астмы (БА), аденоидитов, тонзиллитов, синуситов, обструктивных бронхитов, рецидивирующего синдрома крупа), которые, в свою очередь, способствуют формированию функциональных нарушений со стороны сердечно-сосудистой и бронхолегочной систем [1–3].
Несмотря на схожую клиническую картину, имеются и определенные различия между респираторными заболеваниями как по симптомам, так и по продолжительности инкубационного периода. Грипп является острым инфекционным заболеванием с коротким (от 2–5 ч до 7 сут), внезапным началом, выраженной интоксикацией. Инкубационный период риновирусной инфекции –10–12 ч. При аденовирусной инфекции и заболеваниях внутриклеточной этиологии инкубационный период может быть более продолжительным – от 2 до 14 дней. В последние годы уделяется внимание группе герпесвирусов, которые также могут вызывать респираторные симптомы и протекать под маской различных заболеваний респираторного тракта (чаще как ОРЗ и бронхит). Для герпесвирусных инфекций инкубационный период может быть различным по продолжительности – от 1–2 сут до 3 нед.
Для герпесвирусных инфекций инкубационный период может быть различным по продолжительности – от 1–2 сут до 3 нед.
В целом для острых респираторных инфекций можно выделить наиболее значимые клинические синдромы, представленные в таблице 1.
Бронхообструктивный синдром (БОС) возникает при следующих вирусных инфекциях: респираторно-синтициальной вирусной инфекции (РСВИ), риновирусной, метапневмовирусной, аденовирусной. Поражения желудочно-кишечного тракта и боли в животе могут быть обусловлены разными причинами, такими как нарушение микроциркуляции (при гриппе), увеличение лимфоузлов – мезаденит (при аденовирусной инфекции), а также гастроэнтерит (при коронавирусной, бокавирусной, энтеровирусной инфекциях) из-за разных путей передачи возбудителя: воздушно-капельного и фекально-орального. Поражение центральной нервной системы встречается реже, чем другие клинические симптомы (при гриппе, энтеровирусной инфекции). Что касается катаральных симптомов, то при всех респираторных инфекциях они обязательно присутствуют, но могут быть выражены в большей или меньшей степени.
Известно, что возбудители проявляют определенный тропизм к отдельным участкам слизистой респираторного тракта, тем самым определяя основную симптоматику заболевания.
За последние годы значительно возрос интерес к РСВИ, особенностью течения которой является прежде всего поражение нижних отделов дыхательных путей, нередко с ателектазами легких. Перенесенная РСВИ значительно повышает риск развития БА у детей.
Лихорадочный период при ОРВИ также различный: при гриппе гипертермия достигает 38–40°С и сохраняется 1–2 дня, при парагриппе – 37,5–38°С (до 5 сут), при аденовирусной инфекции лихорадочный период с температурой до 38–39° может сохраняться в течение 2 нед. При риновирусной инфекции температурная реакция незначительно выражена, чаще температура субфебрильная.
Известно, что группа часто болеющих детей (ЧБД) – это «проблемные» дети с часто возникающими респираторными заболеваниями, заболеваниями ЛОР-органов, требующие определенного обследования, лечения и профилактики с учетом локализации инфекционного процесса, его этиологии, особенностей дисфункции иммунной системы, формирования функциональных расстройств со стороны органов дыхания и сердечно-сосудистой системы [4]. На практике каждого пятого ребенка можно отнести к группе ЧБД.
На практике каждого пятого ребенка можно отнести к группе ЧБД.
Одной из принципиальных задач лечения ЧБД следует считать рациональный выбор антибактериальной терапии. Лечение детей основывается на результатах комплексного обследования, включающего микробиологические и серологические данные, а также других вспомогательных методов: УЗИ органов брюшной полости, ЭХО-КГ, мониторирования ЭГК и АД, на показателях ФВД, которые позволяют определить степень выраженности функциональных расстройств и решить вопрос о необходимости их коррекции.
По результатам комплексного обследования (микробиологического и серологического) на сегодняшний день у ЧБД могут определяться несколько возбудителей, в т.ч., помимо банальных грамположительных кокков, и внутриклеточные возбудители (хламидии и микоплазмы), а также герпесвирусы – преимущественно вирус Эпштейна–Барр и цитомегаловирус. В таких случаях требуется назначение этиотропных антибактериальных и противовирусных препаратов. Из антибиотиков предпочтительны группы аминопенициллинов, цефалоспоринов и макролидов.
Особую роль при лечении ЧБД играют иммуномодуляторы, которые могут применяться как в остром периоде (для лечения), так и для профилактики, однако у отдельных препаратов имеются возрастные противопоказания, отсутствует доказательная база. Поэтому наряду со вышеуказанными препаратами возможно применение иммуномодуляторов растительного происхождения, к которым относится Иммунал® – препарат, созданный на основе эхинацеи.
История изучения
препаратов эхинацеи
Впервые это растение описал в 1753 г. Карл Линней под названием «рудбекия пурпурная» (Rudbeckia purpurea). Это название он дал в честь своего наставника и учителя, шведского ботаника Олафа Рудбека (1630–1702), профессора Упсальского университета, прапрадеда Альфреда Нобеля.
Эхинацея пурпурная произрастает в Северной Америке: США и Мексике. Американские индейцы, зная о лечебной силе эхинацеи, столетия назад использовали ее при разных заболеваниях. В Европу эхинацея была завезена вскоре после открытия Американского континента. С тех пор это растение культивируется во многих странах мира – Германии, Франции, Молдове, России (в европейской части).
В Европу эхинацея была завезена вскоре после открытия Американского континента. С тех пор это растение культивируется во многих странах мира – Германии, Франции, Молдове, России (в европейской части).
Род эхинацеи включает 9 ботанических видов: эхинацея пурпурная, эхинацея бледная, эхинацея узколистная, эхинацея парадоксальная, эхинацея теннессийская, эхинацея кровавая, эхинацея стимулирующая, эхинацея неглегта, эхинацея темно-красная. В медицине в качестве лекарственного сырья используют разные части растений: цветки, стебли, листья, корневища с корнями.
Состав эхинацеи
Корни и трава эхинацеи содержат эфирное масло, смолы, фитостерины, углеводы, изобутиламиды, жирное масло. В растении обнаружено 7 групп биологически активных веществ: полисахариды, флавоноиды, производные кофеиновой кислоты, эссенциальные липиды, алкиламиды, витамины и микроэлементы.
Основные действующие вещества, обладающие иммуностимулирующей активностью, – полисахариды, которые содержатся во всех частях растения. Эхиназиды, хлорогеновая кислота, синарин – производные кофеиновой кислоты – повышают сопротивляемость организма к инфекционным и вирусным заболеваниям, ускоряя процесс выздоровления. Эхинацин, который содержится в корнях растений, обладает кортизоноподобной активностью, ускоряет заживление ран. У эхинацеи богатейший минеральный состав: калий, кальций, серебро, литий, сера, молибден, никель, барий, бериллий, ванадий, марганец, а также важные для иммунной системы цинк, селен, кобальт.
В этой связи лекарства на основе эхинацеи издавна применялись в медицине для лечения инфекций респираторного тракта, мочевыводящих путей, уха, местно – для лечения ран, ожогов, при абсцессах, фурункулезе, укусах насекомых, крапивнице, герпесе, экземе. Препараты эхинацеи применяют при заболеваниях, вызванных воздействием ионизирующей радиации, ультрафиолетовых лучей, пестицидов, фунгицидов, солей тяжелых металлов, инсектицидов, а также при продолжительном лечении антибиотиками, хронических воспалительных процессах, сахарном диабете, заболеваниях печени. Эхинацея вызывает гибель некоторых бактерий, вирусов, грибов. Экстракты эхинацеи угнетают рост стафилококков, стрептококков, кишечной палочки.
Эхинацея вызывает гибель некоторых бактерий, вирусов, грибов. Экстракты эхинацеи угнетают рост стафилококков, стрептококков, кишечной палочки.
Применение препарата Иммунал®
в современной медицине
По классификации иммуномодуляторов по происхождению Иммунал® относится к I группе иммуномодулирующих препаратов экзогенного (растительного) происхождения (табл. 2) [4].
Иммунал® применяется как в остром периоде болезни, так и для профилактики респираторных заболеваний [5–7]. Эффективность, целесообразность и безопасность его применения были подтверждены при метаанализе ряда научных исследований [8]. Авторами показана терапевтическая эффективность только наземных частей растений и в раннем периоде ОРВИ. R. Schoope (2006) было доказано, что при профилактическом применении эхинацеи пурпурной у добровольцев с индуцированной риновирусной инфекцией по сравнению с плацебо на 55% снижалась частота клинических проявлений болезни [9].
Основные работы по изучению эффективности препарата Иммунал® были проведены в конце XX в. и начале XXI в. В двойном слепом рандомизированном плацебо-контролируемом исследовании было показано, что применение эхинацеи пурпурной способствует более быстрому выздоровлению при респираторной инфекции. В исследование было включено 120 больных (60 в группе получавших препараты эхинацеи и 60 – в контрольной группе) [10].
Врачу особенно важно быть уверенным в том, что применяемые препараты не вызывают аллергических реакций у детей с БА. В исследовании, проведенном М.К. Ерофеевой и соавт. (2004), применение препарата Иммунал® у детей с аллергическими заболеваниями способствовало сокращению сроков заболевания, не вызывая аллергических реакций [11].
Эффективность применения препарата Иммунал® была доказана в экспериментах и клинических исследованиях, показавших положительное влияние препарата на следующие звенья иммуногенеза [12–18]:
• стабилизацию эпителиальных барьеров;
• усиление фагоцитарной активности;
• стимуляцию синтеза интерферона;
• повышение активности киллерных клеток;
• усиление синтеза антител;
• антиоксидантный эффект.
Повышая число лейкоцитов (гранулоцитов) и активизируя фагоцитоз, действующие вещества препарата подавляют размножение микроорганизмов в организме человека и способствуют уничтожению болезнетворных бактерий. Кроме того, установлено противовирусное действие травы эхинацеи пурпурной в отношении возбудителей гриппа и герпеса.
При назначении препарата Иммунал® в группе ЧБД отмечалась быстрая нормализация показателей неспецифического звена иммунитета [19].
В ряде работ доказано, что при включении в терапию препаратов эхинацеи с первых дней развития ОРЗ отмечались облегчение течения заболевания [20] и более быстрое выздоровление [21].
Профилактическое назначение препарата Иммунал® допустимо курсами от 7 дней, максимальная продолжительность непрерывного курса не должна превышать 8 нед.
Показания к назначению Иммунала®
Иммунал® особенно показан взрослым и детям с вторичными иммунодефицитами на фоне частых ОРВИ и при хронических заболеваниях. Препарат может назначаться реконвалесцентам, детям в период адаптации в детских дошкольных учреждениях, в период формирования коллективов (школьных, воинских), в стационарах общесоматического профиля для предупреждения вспышек заболевания, а также в качестве вспомогательного лекарственного средства при продолжительной антибиотикотерапии хронических инфекционных заболеваний, сопровождающихся снижением иммунитета.
Противопоказаниями являются:
– повышенная чувствительность к компонентам препарата и растениям семейства сложноцветных;
– прогрессирующие системные и аутоиммунные заболевания, такие как туберкулез, лейкозы, коллагенозы, рассеянный склероз, СПИД или ВИЧ-инфекция;
– возраст до 1 года.
Способ применения и дозы
Препарат представлен в следующих формах и дозировках для применения в педиатрической практике: таблетки (эхинацеи пурпурной травы (Echinacea purpurea (L.) Moench) сок высушенный – 80 мг в 1 таблетке) и раствор для приема внутрь (эхинацеи пурпурной травы (Echinacea purpurea (L. ) Moench) сок – 0,80 мл в 1 мл раствора).
) Moench) сок – 0,80 мл в 1 мл раствора).
Для маленьких детей рекомендуется растолочь таблетку и смешать с небольшим количеством жидкости или использовать раствор для приема внутрь. Для облегчения правильного дозирования в каждую упаковку с раствором вложена градуированная дозировочная пипетка. Перед приемом нужное количество препарата следует развести в небольшом объеме воды.
Препарат назначают:
– взрослым и подросткам старше 12 лет: по 2,5 мл раствора для приема внутрь 3 р./сут или по 1 таблетке 3–4 р./сут;
– детям в возрасте от 6 до 12 лет: по 1,5 мл раствора для приема внутрь 3 р./сут или по 1 таблетке 1–3 р./сут;
– детям в возрасте от 4 до 6 лет: по 1 таблетке 1–2 р./сут;
– детям в возрасте от 1 до 6 лет: по 1,0 мл раствора для приема внутрь 3 р./сут.
Для достижения терапевтического эффекта Иммунал® следует принимать не менее 1 нед.
В последние годы на российском рынке появился комбинированный препарат Иммунал® плюс С в форме раствора (содержит сок свежесобранной эхинацеи и витамин С (аскорбиновую кислоту)). Витамин С является мощным антиоксидантом и защищает клетки от повреждения свободными радикалами, образующимися при инфекционно-воспалительных заболеваниях. Аскорбиновая кислота усиливает иммунный ответ организма, способствуя повышению сывороточной концентрации интерферона и защитных антител. Применяется в виде раствора [22]. Издавна было известно положительное влияние аскорбиновой кислоты на процессы кроветворения, регенерации, на стабилизацию структуры эндотелия сосудистой стенки, в стрессовых ситуациях. В систематическом Кокрановском обзоре был проведен анализ 15 исследований с участием 7045 пациентов. Применение витамина С в терапии респираторных инфекций способствовало снижению степени тяжести простудного заболевания, уменьшению числа дней нетрудоспособности [23].
Способ применения и дозы
препарата Иммунал® плюс С
Применяется внутрь независимо от приема пищи:
– дети старше 12 лет и взрослые: по 2–3 мл 3 р. /сут;
/сут;
– дети в возрасте от 4 до 12 лет: по 1–2 мл 3 р./сут;
– дети в возрасте от 1 до 4 лет: по 1 мл 3 р./сут.
Для достижения терапевтического эффекта Иммунал® плюс С следует принимать в течение 7–10 дней. Повторные курсы возможны после 14-дневного перерыва. Эффективность препарата повышается при его применении при ОРВИ и гриппе с первых дней заболевания.
Таким образом, препараты эхинацеи широко применяются как во взрослой, так и в детской практике для коррекции вторичной иммунной недостаточности в остром периоде болезни и для профилактики респираторных заболеваний (острых и хронических).
Литература
1. Иванова Н.А. Часто болеющие дети // Русский медицинский журнал. 2008. Т. 16. № 4. С. 183–185.
2. Самсыгина Г.А., Коваль Г.С. Часто болеющие дети. Проблемы диагностики, патогенеза и терапии // Детский врач. 2008. № 6. С. 5–10.
3. Булгакова В.А., Балаболкин И.И., Ушакова В.В. Современное состояние проблемы часто болеющих детей // Педиатрическая фармакология. 2007. Т. 4. № 2. С. 48–52.
4. Федеральное руководство по использованию лекарственных средств (формулярная система). Выпуск XIV. 2013. 995 с.
5. Сенцова Т.Б., Ревякина В.А., Ворожко И.В., Кириллова О.О., Моносова О.Ю. Современные аспекты применения иммуномодуляторов в лечении и профилактике респираторных вирусных инфекциях у детей // Вопросы практической педиатрии. 2011. Т. 6. № 5. С. 110–113.
6. Ушкалова Е. Препараты эхинацеи в профилактике и лечении респираторных инфекций: в фокусе – иммунал // Врач. 2007. № 8. С. 35–37.
7. Дронов, И.А., Эрдес С.И. применение лекарственных средств на основе эхинацеи для профилактики и лечения острых респираторных инфекций у детей // Вопросы практической педиатрии. 2011. Т. 6. С. 51–54.
8. Linde K., Barrett B., Wolkart K. et al. Echinacea for preventing and treating the common cold // Cochran Database syst Rev. 2006. Jan 25 (1). СD000530.
9. Schoop R., Klein P. , Suter A., Johnston S.L. Echinacea in the Prevention of Induced Rhinovirus Cold: A Meta-Analys // Сlinical Therapeutics. 2006. Vol. 28. № 2. С. 174–183.
, Suter A., Johnston S.L. Echinacea in the Prevention of Induced Rhinovirus Cold: A Meta-Analys // Сlinical Therapeutics. 2006. Vol. 28. № 2. С. 174–183.
10. Hoheisel O. et al. Echinagard treatment shortens the course of the common cold: double blind, placebo controlled clinical trial // European Journal Clinical Research. 1997. Vol. 9. Р. 261–268.
11. Ерофеева М.К., Шадрин А.С., Максакова В.Л. и др. Обоснование показаний к применению эхинацеи для профилактики гриппоподобных заболеваний у взрослых и детей // Русский медицинский журнал. 2004. № 12 (21). С. 1213–1215.
12. Groom S.N., Johns T., Oldfield P.R. The potency of immunomodulatory herbs may be primarily dependent upon macrophage activation // J Med. Food. 2007. Vol. 10 (1). 73–9.
13. Sullivan A.M., Laba J.G., Moore J.A., Lee T.D. Echinacea-induced macrophage activation // Immunopharmacol. Immunotoxicol. 2008. Vol. 30 (3). Р. 553–574.
14. Mishima S., Saito K., Maruyama H. et al. Antioxidant and immuno-enhancing effects of Echinacea purpurea // Biol. Pharm. Bull. 2004. Vol. 27 (7). Р. 1004–1009.
15. Zhai Z., Liu Y., Wu L. et al. Enhancement of innate and adaptive immune functions by multiple Echinacea species // J Med. Food. 2007. Vol. 10 (3). Р. 423–434.
16. Freier D.O., Wright K., Klein K. et al. Enhancement of the humoral immune response by Echinacea purpurea in female Swiss mice // Immunopharmacol. Immunotoxicol. 2003. Vol. 25 (4). Р. 551–560.
17. Hall H., Fahlman M.M., Engels H.J. Echinacea purpurea and mucosal immunity // Int. J Sports Med. 2007. Vol. 28 (9). Р. 792–797.
18. Gan X.H., Zhang L., Heber D., Bonavida B. Mechanism of activation of human peripheral blood NK cells at the single cell level by Echinacea water soluble extracts: recruitment of lymphocyte-target conjugates and killer cells and activation of programming for lysis // Int. Immunopharmacol. 2003. Vol. 3 (6). Р. 811–824.
19. Харитонова Л., Исрафаилова О. Коррекция иммунного статуса у часто болеющих детей // Врач. 2011. Т. 10. № 10. С. 53–56.
Коррекция иммунного статуса у часто болеющих детей // Врач. 2011. Т. 10. № 10. С. 53–56.
20. GoelV. Efficacy of a standardized echinacea preparation (EchinilinTM) for the treatment of the common cold: a randomized, double-blind, placebo-controlled trial // Journal of Clinical Pharmacy and Therapeutics. 2004. Vol. 29. Р. 75–83.
21. Schulten B., Bulitta M., Brigitta B., Koster U., Schafer M. Efficacy of Echinacea purpurea in patients with a common cold: a placebo-controlled, randomised, double-blind clinical trial // Arzneimittelforschung. 2001. Vol. 51. P. 563–568.
22. Maggini S. Essential Role of Vitamin C and Zinc in Child Immunity and Health // The Journal of International Medical Research. 2010. Vol. 38. Р. 386–414.
23. Douglas R.M., Hemila H., D’Souza R., Chalker E. B., Treacy B. Vitamin C for preventing and treating the common cold. Cochrane Database Systematic Reviews. 2004. Vol. 18 (4). CD000980.
RU1309129068
.
Иммунал таблетки (раствор) — инструкция по применению, описание, аналоги препарата
Качественный и количественный состав
В 1 таблетке содержится 80 мг высушенного сока, полученного из свежесобранной цветущей эхинацеи пурпурной (Echinacea purpurea L., succus), свежее растение: высушенный сок = 30-60 : 1.
Полный перечень вспомогательных веществ смотри в разделе «Перечень вспомогательных веществ».
Описание
Круглые, плоские с обеих сторон таблетки светло-коричневого цвета, с вкраплениями.
Фармакотерапевтическая группа, код АТС:
Код АТС: R05X. Прочие средства, применяемые при простудных заболеваниях.
Показания к применению
Кратковременная профилактика и лечение в составе комплексной терапии острых респираторных заболеваний.
Дозировка и способ применения
Лечение следует начинать при выявлении первых признаков заболевания.
Взрослые и подростки старше 12 лет, а также пациенты пожилого возраста: по 1 таблетке 3-4 раза в день.
Лекарственное средство не рекомендовано для детей до 12 лет.
Перед применением препарата детьми необходима консультация врача (см. раздел «Особые предостережения и предосторожности при применении»).
Продолжительность приема
Курс лечения не должен превышать 10 дней.
Если симптомы сохраняются больше 10 дней, необходимо проконсультироваться с врачом или фармацевтом.
Способ назначения
Таблетки следует запивать достаточным количеством воды. Принимать независимо от приема пищи.
Противопоказания
Повышенная чувствительность к действующему веществу или растениям семейства сложноцветных (ромашка, арника, календула, тысячелистник) или к любому из вспомогательных веществ.
В связи с возможным иммуностимулирующим действием не принимать в случаях прогрессирующих системных заболеваний, в т.ч. туберкулез, саркоидоз, системные заболевания соединительной ткани (коллагенозы), рассеянный склероз, ВИЧ-инфекция или СПИД, злокачественные заболевания, патология системы лейкоцитов (гемобластозы, агранулоцитоз и др.), состояния иммунодефицита или иммуносупрессии, прием иммунодепрессантов, склонность к аллергическим реакциям (атопический дерматит, бронхиальная астма и др.).
Не рекомендуется беременным и кормящим женщинам, детям до 12 лет.
Особые предостережения и предосторожности при применении
Не превышать указанную дозу.
Если во время приема лекарственного средства симптомы не улучшаются или происходит ухудшение состояния, поднимается температура, необходимо обратиться к врачу.
У пациентов с атопией имеется риск развития анафилактических реакций. Таким пациентам перед приемом Эхинацеи следует проконсультироваться со своим врачом.
Таким пациентам перед приемом Эхинацеи следует проконсультироваться со своим врачом.
Применение лекарственного средства у детей до 12 лет не рекомендуется в связи с отсутствием достаточных данных.
Если симптомы не проходят в течение 10 дней, пациент должен обратиться к врачу.
Особые предупреждения, касающиеся вспомогательных веществ
Таблетки Иммунал содержат лактозу. Пациентам с непереносимостью галактозы, дефицитом лактазы или нарушением всасывания глюкозы-галактозы не следует принимать данное лекарственное средство.
Взаимодействия с другими лекарственными средствами
Исследования по взаимодействию эхинацеи пурпурной с другими лекарственными препаратами не проводились. Однако не рекомендуется применять таблетки Иммунал в период приема иммуносупрессивных лекарств, таких как циклоспорин и метотрексат.
Перед совместным приемом с другими лекарственными препаратами пациент должен проконсультироваться с врачом.
Беременность и лактация
В связи с отсутствием достаточных данных применение лекарственного средства в период беременности и лактации не рекомендуется. Данные о влиянии лекарственного средства на фертильность отсутствуют.
Влияние на способность к вождению автомобиля и управлению механизмами
Исследования по оценке влияния эхинацеи на способность управлять автомобилем и работать с механизмами не проводились.
Нежелательные эффекты
Частота неизвестна. В отдельных случаях могут отмечаться следующие побочные эффекты:
Могут отмечаться реакции гиперчувствительности (сыпь, крапивница, отек лица, синдром Стивенса-Джонсона, ангиоотек кожи, отек Квинке, анафилактический шок, реакция бронхоспазма с обструкцией и приступ астмы).
Эхинацея может вызвать развитие аллергических реакций у пациентов с атопическими заболеваниями.
Связь с аутоиммунными заболеваниями (рассеянный склероз, диссеминированный энцефалит, узловатая эритема, иммунотромбоцитопения, синдром Эванса, синдром Шегрена с тубулярной почечной дисфункцией) не исключена.
В случае возникновения нежелательных реакций, в том числе не указанных в данной инструкции, следует прекратить прием лекарственного средства и обратиться к врачу.
Передозировка
Случаи передозировки не описаны.
Фармакологические свойства
Фармакодинамические свойства
Таблетки Иммунал содержат сок эхинацеи пурпурной (Echinacea purpurea (L. )). В доклинических экспериментальных исследованиях обнаружено влияние эхинацеи пурпурной на неспецифическую иммунную систему (фагоцитоз макрофагов и активность естественных клеток-киллеров). Механизм действия не установлен.
)). В доклинических экспериментальных исследованиях обнаружено влияние эхинацеи пурпурной на неспецифическую иммунную систему (фагоцитоз макрофагов и активность естественных клеток-киллеров). Механизм действия не установлен.
Фармакокинетические свойства
Данные отсутствуют.
Доклинические данные по безопасности
Эхинацея пурпурная не показала токсичности в исследованиях по изучению токсичности разовой дозы (грызуны), повторных доз (грызуны) и генотоксичности in vitro и in vivo. Тесты на репродуктивную токсичность и канцерогенность не выполнялись.
Перечень вспомогательных веществ
магния стеарат, лактозы моногидрат, кремния диоксид коллоидный безводный, сахарин натрия Е954, ванилин, вишневая отдушка.
Срок годности
3 года.
Срок годности указан на упаковке.
Особые предосторожности при хранении
Хранить при температуре не выше 25°С.
Не использовать по истечении даты срока годности, указанной на упаковке.
Хранить в защищенном от детей месте.
Упаковка
По 10 таблеток в блистере из ПВХ/ПВДХ и алюминиевой фольги.
2 или 4 блистера вместе с листком-вкладышем в картонной коробке.
Условия отпуска из аптек
Без рецепта.
Владелец регистрационного удостоверения и производитель
Лек д.д., Веровшкова 57, Любляна, Словения
Иммунал, таблетки, 20 шт.
Действующее вещество
Эхинацеи пурпурной травы сок
Лекарственная форма
таблетки
Производитель
Сандоз, Швейцария
Состав
Действующее вещество: эхинацеи пурпурной травы (Echinacea purpurea (L.) Moench) сок высушенный 80 мг;
Вспомогательные вещества: кремния диоксид коллоидный; лактоза; магния стеарат; натрия сахаринат; ванилин; ароматизатор вишневый
Фармакологическое действие
Иммунал® является иммуностимулирующим препаратом, изготовленным из лекарственного растительного сырья.
Эхинацея пурпурная (Echinacea purpurea (L.) Moench) содержит активные вещества, усиливающие естественные защитные силы организма и действующие в качестве стимуляторов иммунитета.
Повышая число лейкоцитов (гранулоцитов) и активизируя фагоцитоз, действующие вещества препарата подавляют размножение микроорганизмов в организме человека и способствуют уничтожению болезнетворных бактерий. Кроме того, установлено противовирусное действие травы эхинацеи пурпурной в отношении возбудителей гриппа и герпеса.
Показания
Иммунал® рекомендуется применять:
- для укрепления иммунитета у пациентов с неосложненными острыми инфекционными заболеваниями, предрасположенностью к частым простудам;
- для профилактики простудных заболеваний и гриппа;
- в качестве вспомогательного лекарственного средства при продолжительной антибиотикотерапии хронических инфекционных заболеваний, сопровождающихся снижением иммунитета.

Применение при беременности и кормлении грудью
Данные о негативном воздействии препарата Иммунал® отсутствуют. Перед применением препарата при беременности и в период грудного вскармливания необходимо проконсультироваться с лечащим врачом.
Противопоказания
- повышенная чувствительность к компонентам препарата и растениям семейства сложноцветных;
- прогрессирующие системные и аутоиммунные заболевания, такие как туберкулез, лейкозы, коллагенозы, рассеянный склероз, СПИД или ВИЧ-инфекция;
- детский возраст до 1 года (для раствора для приема внутрь) или до 4 лет (для таблеток).
Побочные действия
В отдельных случаях возможно развитие реакций повышенной чувствительности: кожная сыпь, зуд, головокружение, бронхоспазм, ангионевротический отек, синдром Стивенса-Джонсона, анафилактический шок.
Прочие: лейкопения (при непрерывном применении более 8 нед).
Взаимодействие
При одновременном приеме с иммунодепрессантами — взаимное ослабление действия.
Сообщения о каком-либо клинически значимом взаимодействии с другими лекарственными средствами отсутствуют.
Как принимать, курс приема и дозировка
Для маленьких детей рекомендуется растолочь таблетку и смешать с небольшим количеством жидкости. Взрослым и подросткам старше 12 лет: по 1 таблетке 3–4 раза в день; детям в возрасте от 6 до 12 лет: по 1 таблетке 1–3 раза в день; детям в возрасте от 4 до 6 лет: по 1 таблетке 1–2 раза в день.
Для достижения терапевтического эффекта Иммунал® следует принимать не менее 1 недели. Продолжительность непрерывного курса лечения не должна превышать 8 недель.
Специальные указания
Перед применением препарата Иммунал® у детей до 12 лет и пациентам с аллергическими заболеваниями и бронхиальной астмой в анамнезе необходимо проконсультироваться с лечащим врачом.
В случае возникновения побочных эффектов следует прекратить прием препарата Иммунал® и обратиться к врачу.
Если симптомы заболевания сохраняются более 10 дней необходимо проконсультироваться с лечащим врачом.
Иммунал® раствор для приема внутрь содержит 20% этанола (т.е. содержание спирта в максимальной разовой дозе эквивалентно 1 ч.ложке сухого вина). При хранении допустимо выпадение хлопьевидного осадка, состоящего из активных полисахаридов. Перед употреблением тщательно встряхнуть флакон.
Форма выпуска
Условия хранения
При температуре не выше 25 °C
Срок годности
3 года
Бренд
ИММУНАЛ
Условия отпуска из аптек
Без рецепта
Штрих-код и вес
Штрих-код: 3838957029006
Вес: 0.020 кг;
Сохраните у себя
Возьми с собой Иммунал, таблетки, 20 шт.. Нормальная цена за Иммунал, таблетки, 20 шт.. Почем купить Иммунал, таблетки, 20 шт.? Иммунал, таблетки, 20 шт. найти на сайте. Постоянное использование Иммунал, таблетки, 20 шт.. Лечение Иммунал, таблетки, 20 шт.. Срок годности Иммунал, таблетки, 20 шт.. Асортимент Иммунал, таблетки, 20 шт..
препарата, приема, вещество, принимать, действия, Условия, таблетке, вещества, травы, врачом, иммунитета, лечащим, Перед, беременности, необходимо, проконсультироваться, детей, применением, facebook, Moench, гриппа, лекарственного, заболевания, возрасте, purpurea, детям, качестве, внутрь, Echinacea, дозировка, Форма, выпуска, хранения, Противопоказания, грудью
Иммунный глобулин (человеческий) (IgG) Внутривенно: использование, побочные эффекты, взаимодействия, изображения, предупреждения и дозировка
См. Также раздел «Предупреждение».
Могут возникнуть приливы, головная боль, головокружение, озноб, мышечные спазмы, боль в спине / суставах, лихорадка, тошнота или рвота. Немедленно сообщите своему врачу или другому специалисту в области здравоохранения, если какие-либо из этих эффектов возникают, сохраняются или ухудшаются. Также могут возникнуть боль, покраснение и отек в месте инъекции. Если эти эффекты продолжаются или становятся надоедливыми, сообщите об этом своему врачу.
Помните, что ваш врач прописал это лекарство, потому что он или она посчитали, что польза для вас больше, чем риск побочных эффектов. Многие люди, принимающие это лекарство, не имеют серьезных побочных эффектов.
Это лекарство может повысить ваше кровяное давление. Регулярно проверяйте свое кровяное давление и сообщайте врачу, если результаты будут высокими.
Немедленно сообщите своему врачу, если у вас есть какие-либо серьезные побочные эффекты, в том числе: легкое кровотечение / синяк, обморок, быстрое / нерегулярное сердцебиение, необычная усталость.
В редких случаях этот продукт может содержать вещества, которые могут вызвать инфекции, поскольку он сделан из крови человека. Хотя риск очень низок из-за тщательного скрининга доноров крови, обсудите риски и преимущества со своим врачом. Немедленно сообщите своему врачу, если у вас появятся какие-либо признаки инфекции, такие как постоянная боль в горле / лихорадка, пожелтение глаз / кожи или темная моча.
Лечение этим препаратом в редких случаях может вызвать серьезное воспаление головного мозга (синдром асептического менингита) от нескольких часов до 2 дней после лечения.Немедленно обратитесь за медицинской помощью, если у вас возникнет сильная головная боль, ригидность шеи, сонливость, высокая температура, чувствительность к свету, боль в глазах или сильная тошнота / рвота.
Проблемы с легкими могут редко возникать через 1–6 часов после лечения. После лечения за вами будут внимательно наблюдать на предмет любых проблем с легкими.
Очень серьезные аллергические реакции на этот препарат возникают редко. Однако немедленно обратитесь за медицинской помощью, если вы заметили какие-либо симптомы серьезной аллергической реакции, в том числе: сыпь, зуд / отек (особенно лица / языка / горла), сильное головокружение, затрудненное дыхание.
Это не полный список возможных побочных эффектов. Если вы заметили другие эффекты, не указанные выше, обратитесь к врачу или фармацевту.
В США —
Обратитесь к врачу за медицинской консультацией по поводу побочных эффектов. Вы можете сообщить о побочных эффектах в FDA по телефону 1-800-FDA-1088 или на сайте www.fda.gov/medwatch.
В Канаде — Обратитесь к врачу за медицинской консультацией по поводу побочных эффектов. Вы можете сообщить о побочных эффектах в Министерство здравоохранения Канады по телефону 1-866-234-2345.
Иммуносупрессивные препараты для лечения аутоиммунных заболеваний
Болезни в области аллергии, иммунологии и ревматологии часто возникают из-за проблем с иммунной системой.Препараты для лечения аутоиммунных и аллергических заболеваний нацелены на различные компоненты иммунной системы. Лечение может ослабить всю иммунную систему или только некоторые ее части. То, как каждый из этих препаратов воздействует на определенные части иммунной системы, может повысить вероятность заражения пациента определенными инфекциями. Здесь мы обсудим широкий спектр лекарств, используемых для лечения аутоиммунных заболеваний, компоненты иммунной системы, на которые нацелены эти лекарства, и виды инфекций (если таковые имеются), которые могут чаще встречаться у людей, принимающих эти иммуносупрессивные препараты.
Иммунная система состоит из двух частей: врожденной и адаптивной. Врожденная иммунная система — это первая линия защиты от бактерий и вирусов. Эта защита включает клетки и молекулы, расположенные в местах проникновения инородных захватчиков (нос, легкие, кишечник и кожа). Иммунные клетки вырабатывают молекулы, называемые цитокинами, для связи между различными частями тела. Эти цитокины, такие как фактор некроза опухоли (TNF), интерлейкин-1 (IL-1) и интерлейкин-6 (IL-6), могут быть нацелены на лечение аутоиммунного заболевания, когда иммунная система атакует собственные клетки организма.
Адаптивная иммунная система со временем развивается. Два типа лейкоцитов, называемые Т-клетками и В-клетками, являются важными составляющими адаптивного иммунитета. Когда организм видит новые бактерии или вирус, он создает Т-клетки и В-клетки, которые распознают захватчика и помогают организму избавиться от инфекции. Если иммунная система работает хорошо, организм запоминает эти бактерии или вирус после борьбы с первой инфекцией. Части адаптивной иммунной системы также являются мишенями для лечения аутоиммунных заболеваний.У нас есть лекарства для удаления В-клеток и замедления В-клеток и Т-клеток. Некоторые цитокины, такие как интерлейкин-17 (IL-17), интерлейкин-12 (IL-12) и интерлейкин-23 (IL-23), также важны для адаптивного иммунитета.
Есть разные способы попасть в организм этих лекарств. Некоторые лекарства, такие как стероиды, азатиоприн и метотрексат, можно принимать внутрь. Другие лекарства, называемые биологическими препаратами, необходимо вводить либо в кровь через вену, либо подкожно в подкожный жир.
Также имейте в виду, что исследования аутоиммунных заболеваний и их лечения очень активны, а лекарства и показания для лечения часто меняются. Это обсуждение не включает полный список показаний или побочных эффектов для этих лекарств. Например, при приеме многих из этих лекарств следует избегать беременности (будь то будущий отец или мать). Если у вас есть конкретные вопросы относительно следующих лекарств или состояний, обязательно поговорите со своим личным врачом, иммунологом или ревматологом.
Общие иммунодепрессанты
Стероиды
Примеры: Преднизон, метилпреднизолон, дексаметазон
Показания к применению: Многочисленное использование при многих аутоиммунных заболеваниях, астме, крапивнице.
Цель лечения: Стероиды обладают широким действием, блокируя воспаление.
Как это работает: Стероиды не позволяют организму вырабатывать цитокины, вызывающие воспаление, истощают определенные иммунные клетки, называемые Т- и В-клетки и эозинофилы, а также затрудняют проникновение иммунных клеток к местам инфекции или травм через тело.Они отличаются от «анаболических стероидов», которыми иногда злоупотребляют спортсмены.
На что обращать внимание: Продолжительное употребление стероидов подвергает вас риску многих проблем, связанных со здоровьем костей, высоким кровяным давлением, контролем уровня сахара в крови, катарактой и инфекциями. В зависимости от того, сколько стероидов вы принимаете и как долго вы будете их принимать, вы будете находиться под наблюдением на предмет определенных типов инфекций, включая редкие виды пневмонии. Возможно, вам придется использовать антибиотики, чтобы предотвратить некоторые типы инфекций.Эти меры обычно не нужны, если вы принимаете стероиды в течение короткого времени. Тем, кто длительно принимает стероиды, следует поговорить с врачом перед вакцинацией.
Колхицин
Показания к применению: Обострения подагры, семейная средиземноморская лихорадка (FMF), другие аутовоспалительные заболевания
Цель лекарства: Подавляет функцию нейтрофилов (тип лейкоцитов)
Как это работает: By уменьшая функцию нейтрофилов, он работает за счет уменьшения воспаления при определенных заболеваниях.
На что обращать внимание: Колхицин обычно может вызывать диарею, тошноту и рвоту. Это также может вызвать повреждение печени, почек или мышц и привести к снижению количества клеток крови. Это лекарство может вызывать опасные взаимодействия с другими лекарствами, поэтому необходима полная проверка лекарств. Не следует запивать грейпфрутовым соком.
Гидроксихлорохин (Плаквенил)
Показания к применению: Волчанка, ревматоидный артрит, малярия, хронические крапивницы и другие аутоиммунные состояния
Цель лечения: Передача сигналов иммунных клеток
Как это работает: Путем снижения передачи сигналов в иммунной системе системы, снижает воспалительную реакцию.Это может предотвратить активацию определенных иммунных клеток, называемых дендритными клетками.
На что обращать внимание: Гидроксихлорохин может вызвать диарею, тошноту, рвоту и боль в животе. Это также может вызвать сыпь, изменения зрения и снижение количества клеток крови. Это не связано с повышенным риском заражения. При приеме этого лекарства пациенты должны регулярно проходить обследование глаз. Он имеет множество лекарственных взаимодействий.
Сульфасалазин
Показания к применению: Ревматоидный артрит, ювенильный ревматоидный артрит, псориатический артрит, язвенный колит и другие аутовоспалительные состояния
Цель лечения: Подавляет образование химических веществ, называемых простагландинами
Компонент сульфасалазина, 5-аминосалицилат, помогает постепенно уменьшить воспаление.
На что обращать внимание: Это лекарство может вызвать тошноту, головную боль, чувствительность к солнцу и сыпь. Его следует избегать у пациентов с аллергией на сульфамидные антибиотики или салицилаты и с осторожностью применять у пациентов с дефицитом G6PD. Пациентам следует использовать солнцезащитные средства при приеме этого лекарства. Это может временно уменьшить количество сперматозоидов и вызвать оранжевую мочу. Поскольку это редко может приводить к снижению показателей крови и риску заражения, при приеме этого лекарства вы можете сдать анализы крови.
Дапсон
Показания к применению: Проказа и другие инфекции, герпетиформный дерматит, другие аутоиммунные заболевания
Цель лекарства: Препятствует синтезу бактериального фолата
Принцип действия: Он также предотвращает повреждение клеток свободными радикалами, и подавляет химические вещества, называемые лейкотриенами или простагландинами, обеспечивая противовоспалительный эффект.
На что обращать внимание: Это лекарство может вызвать расстройство желудочно-кишечного тракта, сыпь и головную боль.Реже это может вызвать изменение настроения, снижение количества клеток крови, повреждение почек и печени и мужское бесплодие. Его следует использовать с осторожностью у пациентов с дефицитом G6PD и избегать у пациентов с сульфамидной аллергией. Он может иметь много лекарственных взаимодействий.
Метотрексат
Показания к применению: Ревматоидный артрит, многие другие аутоиммунные заболевания и некоторые виды рака
Цель лекарства: Блокирует использование клетками фолиевой кислоты, определенного питательного вещества.Это ключевая часть создания ДНК и РНК, которые важны для роста, деления и выживания Т-клеток и В-клеток.
Как это работает: Т-клетки и В-клетки должны производить ДНК и РНК, чтобы жить и расти. Замедление этого процесса помогает контролировать воспаление при аутоиммунных заболеваниях.
На что обращать внимание: Метотрексат — это лекарство, подавляющее иммунитет. Он используется в низких дозах для лечения аутоиммунных заболеваний. Когда вы принимаете метотрексат, у вас больше шансов получить бактериальные и вирусные инфекции, потому что он снижает способность вашего организма вырабатывать Т- и В-клетки.Перед началом приема этого препарата вас следует проверить на наличие вирусных инфекций, таких как гепатиты B и C, а также на состояние почек и печени. Пока вы принимаете это лекарство, вам будут проверять анализы почек и печени. Пациентам часто назначают фолиевую кислоту, чтобы уменьшить побочные эффекты этого лекарства, такие как язвы во рту, диарея или тошнота.
Mycophenolate Mofetil (Cellcept, Myfortic)
Показания к применению: Используется при многих других аутоиммунных заболеваниях и предотвращении отторжения при трансплантации твердых органов
Цель лечения: Фермент инозин-5′-монофосфатдегидрогеназа (IMPDH)
Как это работает: Фермент IMPDH важен для создания ДНК и РНК.Т-клетки и В-клетки нуждаются в этом ферменте для роста и деления, а его блокирование помогает контролировать иммунные реакции при аутоиммунных состояниях.
На что обращать внимание: При приеме микофенолата повышается риск заражения бактериями или вирусами, поскольку он снижает способность вашего организма вырабатывать Т- и В-клетки. Перед началом приема этого лекарства вас следует проверить на наличие вирусных инфекций, таких как гепатиты B и C. Пока вы принимаете этот препарат, вам будут проверяться количество клеток крови, анализы почек и печени.Живых вакцин следует избегать.
Азатиоприн (имуран)
Показания к применению: Используется при многих других аутоиммунных заболеваниях и профилактике отторжения трансплантата
Цель лекарства: Этот препарат расщепляется на молекулу, которая встроена в ДНК по мере ее сборки и мешает правильному созданию ДНК. Это заставляет Т- и В-клетки расти и делиться медленнее.
Как это работает: Т-клетки и В-клетки должны заставлять ДНК и РНК расти и делиться.Замедление этого процесса помогает контролировать иммунные реакции при аутоиммунных заболеваниях.
На что обращать внимание: При приеме азатиоприна повышается риск заражения бактериями или вирусами, поскольку он снижает способность вашего организма вырабатывать Т- и В-клетки. Перед началом приема этого лекарства вас следует проверить на наличие вирусных инфекций, таких как гепатиты B и C. Ваш врач может проверить, вырабатывает ли ваше тело белок под названием тиопуринметилтрансфераза (TPMT), прежде чем начинать прием этого лекарства, чтобы убедиться, что ваше тело может избавиться от него в обычном режиме.Пока вы принимаете этот препарат, вам будут проверяться количество клеток крови, анализы почек и печени. Это может увеличить риск развития злокачественных новообразований.
Врожденный иммунитет
Anti-IL-1 Biologics
Примеры: Anakinra (Kineret), Canakinumab (Ilaris), Rilonacept (Arcalyst)
Показания к применению: Cryopyrin-Associated Periodic Syndromes (CAPS), включая
Семейный аутовоспалительный синдром от холода и синдром Макл-Уэллса, системный ювенильный идиопатический артрит (канакинумаб), ревматоидный артрит (анакинра)
Цель лечения: Интерлейкин-1 (IL-1)
Как это работает: IL-1 помогает вашему организму немедленно реагировать, когда микробы контактируют с клетками.Это вызывает жар и побуждает другие клетки присоединиться к инфекции и бороться с ней. Блокируя IL-1, мы можем уменьшить жар, воспаление суставов и кожи, а также помочь уменьшить общее воспаление, вызванное этими состояниями.
На что обращать внимание: Поскольку IL-1 важен для защиты от микробов, у вас может быть больше шансов получить инфекции (бактериальные и вирусные), такие как инфекции верхних дыхательных путей и инфекции мочевыводящих путей, при длительном лечении с помощью препарат, блокирующий ИЛ-1.Реактивация такого заболевания, как туберкулез, случается редко, но перед началом приема этого препарата рекомендуется пройти тест на туберкулезную инфекцию. Рекомендуется избегать использования живых вакцин во время приема этих лекарств и сделать все необходимые прививки любого типа перед началом приема лекарств, поскольку неизвестно, насколько хорошо организм реагирует на вакцину, пока вы принимаете этот тип лекарств. При приеме этих лекарств часто контролируют количество лейкоцитов.
Биопрепараты против TNF (ингибиторы TNF)
Примеры: Инфликсимаб (Ремикейд), Адалимумаб (Хумира), Голимумаб (Симпони), Этанерцепт (Энбрел), Цертолизумаб (Цимзия)
Показания к применению: , бляшечный псориаз / артрит, анкилозирующий спондилит, болезнь Крона, язвенный колит
Цель лечения: Фактор некроза опухоли (TNF)
Как это работает: TNF важен для воспаления, которое начинается при контакте организма с микробами.TNF активирует воспаление по всему телу, вызывает лихорадку и привлекает другие лейкоциты к той части тела, где есть инфекция. При воспалительных состояниях, таких как ревматоидный артрит и воспалительное заболевание кишечника, TNF может вызывать повреждение суставов, кожи и пищеварительного тракта. Блокирование TNF может помочь держать эти воспалительные заболевания под контролем.
На что обращать внимание: TNF также является важной частью способности организма избавляться от вторгающихся бактерий, вирусов и грибков.При приеме терапии, блокирующей ФНО, повышается риск серьезных инфекций. Кроме того, вам следует пройти тестирование на туберкулез, гепатиты B и C, ВИЧ и проверить на любой риск грибковой инфекции, потому что, если у вас есть эти инфекции, они могут стать активными, когда мы заблокируем TNF. Вам также следует избегать живых вакцин при приеме лекарств этого семейства. Долгосрочный риск рака, такого как лимфома, также может быть выше у пациентов, принимающих терапию анти-TNF.
Anti-IL-6 Biologics
Примеры: Тоцилизумаб (Актемра), Сарилумаб (Кевзара)
Показания к применению: Ревматоидный артрит, гигантоклеточный артериит, ювенильный идиопатический артрит
Цель лечения:
Интерлейкин-6 Рецептор (ИЛ-6)
Как это работает: ИЛ-6 является важным цитокином, который вызывает активацию Т-клеток и В-клеток.Это также важно при воспалении по всему телу, которое приводит к лихорадке. При аутоиммунном заболевании, таком как ревматоидный артрит, IL-6 вызывает воспаление, которое повреждает суставы и другие части тела.
На что обращать внимание: Поскольку IL-6 является важным цитокином для многих лейкоцитов и воспаления в целом, существует более высокий риск заражения обычными инфекциями, такими как вирусы верхних дыхательных путей, и менее распространенными инфекциями, например туберкулез. Как и в случае терапии, блокирующей TNF, вы должны пройти тест на туберкулез, прежде чем начинать лечение, блокирующее IL-6.
Комплемент
Примеры: Экулизумаб
Показания к применению: Пароксизмальная ночная гемоглобинурия (ПНГ), атипичный гемолитико-уремический синдром (a-HUS)
Цель лечения: Комплемент C5
Как это работает: является частью врожденной иммунной системы, которая связывается с определенными типами бактерий и уничтожает их (например, Neisseria — семейство бактерий, вызывающих гонорею и менингококковый менингит). В нормальных условиях организм контролирует комплемент, имея белки, предотвращающие активацию комплемента.В определенных условиях, таких как PNH и a-HUS, организм не может остановить активацию комплемента, и организм разрушает свои собственные клетки. Экулизумаб помогает предотвратить этот тип спонтанной активации комплемента.
На что обращать внимание: Поскольку комплемент очень важен для защиты организма от Neisseria, люди, принимающие экулизумаб, с большей вероятностью заразятся этой инфекцией. Перед началом приема этого препарата вам следует сделать прививку от менингококка и принимать антибиотики для предотвращения инфекций во время приема этого препарата.
Адаптивный иммунитет — В-клетки
Anti-CD20 Biologics
Примеры: Ритуксимаб (Ритуксан)
Показания к применению: Неходжкинская лимфома, хронический лимфоцитарный лейкоз, ревматоидный артрит, васкулит (например, гранулематоз с полиангиопатией и микроскопическая болезнь кожи)
Цель лекарства: CD20, поверхностный белок на В-клетках
Как это работает: Ритуксимаб связывается с белком CD20 на В-клетках и разрушает В-клетки в кровотоке.Все заболевания, которые лечатся ритуксимабом, требуют, чтобы В-клетки либо росли (например, лимфома), либо вырабатывали антитела, которые связываются с определенными частями нашего тела и вызывают воспаление (например, ревматоидный артрит, васкулит и аутоиммунное заболевание кожи). Когда ритуксимаб удаляет В-клетки, организм избавляется от растущих В-клеток и В-клеток, вырабатывающих антитела, вызывающие заболевание.
На что обращать внимание: При удалении В-клеток из организма повышается риск заболеваний, которые обычно излечиваются антителами.К ним относятся инфекции носовых пазух и легких. Некоторые заболевания, такие как гепатит B, могут повторно активироваться после ритуксимаба, и вам следует пройти тест на гепатит B перед лечением. Также наблюдались другие типы вирусных инфекций, такие как герпес. Ответ на вакцины также ограничен после ритуксимаба, и все указанные вакцинации должны быть сделаны перед его применением. У большинства людей, получающих ритуксимаб, В-клетки возвращаются в течение одного года. Однако у части лиц, получавших ритуксимаб, В-клетки не возвращаются, и у вас могут быть низкие уровни антител в течение многих лет или всей жизни.Это может повысить риск заражения.
Фактор роста В-клеток, нацеленный на биологические препараты
Примеры: Белимумаб (Бенлиста)
Показания к применению: Системная красная волчанка
Цель лечения: BLyS (стимулятор В-лимфоцитов, также называемый BAFF)
Как это работает : Белимумаб нацелен на цитокин BLyS, который является важным белком для выживания и роста В-клеток. Блокируя этот фактор роста у пациентов с волчанкой, вы можете уменьшить количество аутоиммунных антител, вырабатываемых В-клетками.
На что обращать внимание: У пациентов, принимающих белимумаб, наиболее распространенными инфекциями являются кожные инфекции и пневмония. Пациенты, принимающие белимумаб, у которых развивается снижение иммунной функции, также более склонны к развитию пневмонии, вызванной грибами или цитомегаловирусом. При приеме белимумаба следует избегать использования живых вакцин.
Адаптивный иммунитет — Т-клетки
Примеры: Циклоспорин
Показания к применению: Предотвращение отторжения трансплантата, реакции трансплантата против хозяина, ревматоидного артрита, псориаза, хронической крапивницы
Цель лечения: Кальциневрин, который дает сигналы для активации Т-клеток
Как это работает: Циклоспорин — это пероральный препарат, который попадает в Т-клетки, где связывает белок кальциневрин.Когда это происходит, Т-клетки не могут производить цитокины или производить больше Т-клеток.
На что обращать внимание: Наиболее частыми побочными эффектами циклоспорина являются высокое кровяное давление и снижение функции почек, и за ними следует внимательно следить. Поскольку циклоспорин блокирует Т-клетки, это лекарство, подавляющее иммунитет. Это может увеличить риск злокачественного новообразования. Когда вы принимаете это лекарство, вы в целом подвержены более высокому риску инфекций. По этой причине при приеме этого лекарства рекомендуется избегать всех живых вакцин.
Костимуляция и активация Т-клеток
Примеры: Abatacept (Orencia)
Показания к применению: Ревматоидный артрит, ювенильный идиопатический артрит, псориатический артрит
Цель лечения: CTLA-447 / CD28
это работает: Т-клеток активируются двумя сигналами. Первый сигнал — это когда рецептор Т-клеток связывает определенную часть микроба (антигена), доставленную ему иммунной клеткой, называемой антигенпредставляющей клеткой (APC).Второй сигнал возникает, когда Т-клетка и APC связываются вторым набором белков, когда эти клетки взаимодействуют. Примером этого второго сигнала является белок Т-клеток, называемый CD28, который связывается с белками АРС CD80 / 86, активируя как Т-клетки, так и АРС. Чтобы выключиться, Т-клетка внесет CTLA-4, который блокирует связывание CD28 с CD80 / 86. Абатацепт представляет собой лекарственную форму CTLA-4. Используя это лекарство, мы можем отключить иммунный ответ Т-клеток. При воспалительном артрите это помогает успокоить воспаление, вызванное Т-клетками, которое вызывает боль в суставах и отек.
На что обращать внимание: Поскольку абатацепт помогает отключить все ответы Т-лимфоцитов, вы подвергаетесь более высокому риску инфекций при приеме этого лекарства. Вам следует пройти тестирование на туберкулез и гепатиты B и C, потому что, если у вас есть эти инфекции, они могут стать активными, когда мы снизим активность Т-клеток. Живые вакцины не следует вводить одновременно или в течение 3 месяцев после прекращения приема этого лекарства.
Адаптивный иммунитет — Цитокины
Anti-IL-17 Biologics
Примеры: Секукинумаб (Cosentyx), Ixekizumab (Taltz), Brodalumab (Siliq)
Показания к применению: Псориаз, псориатический артрит, анкилозирующий спондилит
Целевое лекарство IL 17 (секукинумаб, иксекизумаб), рецептор IL-17 (бродалумаб)
Как это работает: IL-17 является важным цитокином при аутоиммунных заболеваниях.Это важно при таких заболеваниях, как псориаз и анкилозирующий спондилит. Обычно IL-17 является важной частью нашей защиты от бактериальных и грибковых инфекций, рекрутируя другие типы белых кровяных телец, называемых нейтрофилами, в места инфицирования.
На что обращать внимание: Когда используются препараты, блокирующие ИЛ-17, повышается вероятность инфекций, в основном включая инфекции верхних дыхательных путей. Серьезные инфекции и грибковые инфекции были редкими в исследованиях этих типов лекарств.При использовании терапии, блокирующей ИЛ-17, следует избегать использования живых вакцин.
Anti-IL-23 Biologics
Примеры: Guselkumab (Tremfya)
Показания к применению: Псориаз
Цель лекарства: Цитокин IL-23
Как это работает: IL-23 является цитокином важен для поддержания жизни типа Т-лимфоцитов, называемых Th27-клетками (которые делают IL-17). Поддерживая эти клетки живыми и активными, IL-23 является важной частью защиты организма от бактериальной инфекции и других инфекций кишечника.При аутоиммунных заболеваниях, таких как псориаз, IL-23 может быть частью воспалительной реакции, вызывая воспаление кожи и симптомы.
На что обращать внимание: Блокирование IL-23 не оказывает большого влияния на количество инфекций, перенесенных пациентами во время клинических испытаний.
Биопрепараты против IL-12/23
Примеры: Устекинумаб (Stelara)
Показания к применению: Псориаз, псориатический артрит, болезнь Крона
Цель лечения: Цитокиновые рецепторы IL-12 и IL-23
Как это работает: Устекинумаб связывается с частью общих рецепторов IL-12 и IL-23, называемой IL-12p40.IL-12 является важным цитокином для активации Т-клеток и других белых кровяных телец, называемых естественными клетками-киллерами, которые помогают избавиться от бактериальных и вирусных инфекций. Когда эти цитокины регулируются ненормально при аутоиммунном заболевании, это может вызывать повреждение тканей, как это наблюдается при псориазе и болезни Крона.
На что обращать внимание: Поскольку IL-12 является важной частью иммунной системы для активации Т-клеток, это может подвергнуть пациентов более высокому риску заражения микобактериями, сальмонеллой, туберкулезом или БЦЖ.Это кажется очень редким. Перед началом терапии устекинумабом рекомендуется пройти обследование на туберкулез.
Anti-IL-5 Biologics
Примеры: Меполизумаб (Nucala), Reslizumab (Cinqair), Benralizumab (Fasenra)
Показания к применению: Тяжелая эозинофильная астма, другие эозинофильные расстройства-мишени
ИЛ-5 (меполизумаб и реслизумаб), рецептор ИЛ-5 (бенрализумаб)
Как это работает: ИЛ-5 является важным цитокином для определенного типа белых кровяных телец, называемых эозинофилами.Эозинофилы важны для организма в борьбе с глистными инфекциями и активируются при аллергических состояниях, таких как астма.
На что обращать внимание: Если у вас есть гельминтозная инфекция, ее следует вылечить до начала приема этих лекарств. Если вы получили гельминтозную инфекцию, которая не проходит лечением, пока вы принимаете препараты, нацеленные на IL-5, вам следует прекратить прием этих лекарств.
Anti-IL-4 / IL-13 Biologics
Примеры: Дупилумаб (Dupixent)
Показания к применению: Атопический дерматит, астма, хронический риносинусит с полипами носа
Цель лечения: Рецептор IL-4 альфа (часть рецептора IL-4 и IL-13)
Как это работает: Цитокины IL-4 и IL-13 участвуют в иммунном ответе, который приводит к выработке антител к аллергии (IgE), слизистой оболочки дыхательные пути и активация аллергического иммунного ответа.
На что обращать внимание: При использовании дупилумаба рекомендуется избегать использования живых вакцин (таких как MMR и ветряная оспа). При приеме этого лекарства реакция на убитые или неактивные вакцины (например, вакцину против менингита) является нормальной. Риск заражения кожными инфекциями, гриппом или простудой, скорее всего, отсутствует или очень незначительно повышен. IL-4 и IL-13, вероятно, важны для борьбы с глистными инфекциями. Исследования не измеряли влияние дупилумаба на эти типы инфекций.Если вы живете в районе, где есть гельминты, вам следует периодически наблюдать или проверять, есть ли у вас симптомы.
Биологические препараты, нацеленные на IgE
Примеры: Омализумаб (Xolair)
Показания к применению: Аллергическая астма, хроническая крапивница
Цель лечения: IgE — антитела к аллергии
Как это работает: Часто называют IgE как «антитело против аллергии». Когда IgE связывается с аллергеном, он вызывает высвобождение гистамина и других молекул, вызывающих аллергическую реакцию (зуд, покраснение, крапивница).
На что обращать внимание: Блокирующий IgE не оказывает большого влияния на способность организма бороться с типичными бактериальными и вирусными инфекциями. IgE может иметь важное значение для атаки других типов инфекций, таких как гельминты (также называемые глистами, такими как аскариды, анкилостомы, власоглавы, острицы). Исследования показали немного повышенный риск заражения в тех регионах мира, где живут эти паразиты, если вы принимаете омализумаб. Если вы живете в районе, где есть гельминты, вам следует периодически наблюдать или проверять, есть ли у вас симптомы.
Движение лимфоцитов (белых кровяных телец)
Примеры: Ведолизумаб (Entyvio)
Показания к применению: Воспалительное заболевание кишечника (язвенный колит и болезнь Крона)
Цель лечения: Интегрин α4β7 (белок снаружи лейкоцитов, которые помогают им попасть в кишечник)
Как это работает: Лейкоциты с интегринами α4β7 попадают в кишечник, где они могут оказывать воспалительное действие при воспалительном заболевании кишечника.Ведолизумаб блокирует попадание этих клеток в кишечник, уменьшая воспаление.
На что обращать внимание: частота общих инфекций (включая инфекции носовых пазух и инфекции мочевыводящих путей) несколько выше у пациентов, принимающих ведолизумаб. Что касается инфекций в кишечнике, есть сообщения об абсцессах в нижних отделах пищеварительного тракта и бактериальных инфекциях у пациентов, принимающих это лекарство.
Лекарства для нацеливания на малые молекулы
Ингибиторы JAK
Примеры: Тофацитиниб (Ксельянц), Упадацитиниб (Ринвок), Барицитиниб (Олумиант)
Показания к применению: Ревматоидный артрит, псориатический артрит, язвенный колит
Медикаменты для лечения язвенного колита Ферменты
Как это работает: Ферменты JAK — важные белки внутри клетки, которые передают сигналы извне клетки ядру или механизму внутри клетки.Многие различные цитокиновые сигналы используют JAK для передачи сообщений в клетках. При заболеваниях, при которых наблюдается слишком сильное воспаление, блокирование JAK может помочь снизить степень воспаления за счет уменьшения сигналов, которые говорят клетке производить и высвобождать воспалительные молекулы, такие как цитокины.
На что обращать внимание: Как и в случае с другими лекарствами, подавляющими иммунитет, ингибиторы JAK вызывают повышенное количество инфекций. Одним из вирусов, который чаще всего обнаруживается у пациентов, принимающих ингибиторы JAK, является опоясывающий герпес.Живые вакцины не следует вводить одновременно.
Эта статья была отрецензирована Эндрю Муром, MD, FAAAAI
Рецензия: 28.09.20
Такролимус: информация о лекарствах MedlinePlus
Такролимус выпускается в виде капсулы, гранул для пероральной суспензии (для смешивания с жидкостью), капсулы с пролонгированным высвобождением (длительного действия) и таблетки с пролонгированным высвобождением для приема внутрь. Капсулы с немедленным высвобождением (Prograf) и пероральная суспензия (Prograf) обычно принимают два раза в день (с интервалом 12 часов).Вы можете принимать капсулы с немедленным высвобождением и пероральную суспензию как с едой, так и без нее, но обязательно принимайте их каждый раз одинаково. Капсулы с пролонгированным высвобождением (Astagraf XL) или таблетки с пролонгированным высвобождением (Envarsus XR) обычно принимают каждое утро натощак, по крайней мере, за 1 час до завтрака или как минимум через 2 часа после завтрака. Принимайте такролимус каждый день в одно и то же время. Тщательно следуйте инструкциям на этикетке рецепта и попросите своего врача или фармацевта объяснить любую часть, которую вы не понимаете.Принимайте такролимус точно в соответствии с указаниями. Не принимайте больше или меньше и не принимайте чаще, чем предписано вашим доктором.
Если вы принимаете гранулы для приготовления суспензии для приема внутрь, вам необходимо смешать их с водой комнатной температуры перед использованием. Налейте от 1 до 2 столовых ложек (от 15 до 30 миллилитров) воды в чашку с гранулами. Смешайте содержимое и сразу же возьмите смесь через рот из чашки или с помощью орального шприца; не сохраняйте смесь на более позднее время. Гранулы не растворятся полностью.Если какая-либо часть смеси осталась, добавьте к смеси 1-2 столовые ложки (от 15 до 30 миллилитров) воды и немедленно примите ее.
Проглатывайте капсулы с расширенным выпуском и таблетки с расширенным выпуском целиком, запивая водой; не раскалывайте, не жуйте и не раздавливайте их. Не открывайте капсулы с немедленным высвобождением,
. Ваш врач будет внимательно следить за вами и при необходимости корректировать дозу. Часто говорите со своим врачом о том, как вы себя чувствуете во время лечения. Спросите своего врача, есть ли у вас какие-либо вопросы о том, сколько такролимуса вам следует принимать.
Различные продукты такролимуса выделяют лекарство в организме по-разному, и их нельзя использовать взаимозаменяемо. Принимайте только такролимус, прописанный вашим врачом, и не переходите на другой продукт такролимуса, если ваш врач не скажет, что вы должны.
Такролимус может предотвратить отторжение трансплантата, только если вы принимаете лекарство. Продолжайте прием такролимуса, даже если чувствуете себя хорошо. Не прекращайте прием такролимуса, не посоветовавшись с врачом.
Лечение волчанки иммунодепрессантами: Центр волчанки Джонса Хопкинса
- Азатиоприн (Имуран)
- Микофенолятмофетил (Селлсепт)
- Циклоспорин (Неорал, Сандиммун, Генграф)
- Метотрексат (Ревматрекс)
- Лефлуномид (Циклорапан
- ) Лефлуномид (
Лефлуномид (
Леклорацил) Лефлуномид (
) Леклорацил
(Арава) горчица (Mustargen)
Что такое иммунодепрессанты?
Иммунодепрессанты — это лекарства, которые помогают подавить иммунную систему.Многие из них изначально использовались у пациентов, которым была проведена трансплантация органов, чтобы помочь предотвратить отторжение пересаженного органа их телом. Однако в настоящее время эти препараты также используются для лечения некоторых аутоиммунных заболеваний, таких как волчанка и ревматоидный артрит. У людей с волчанкой иммунная система по ошибке атакует собственные ткани организма. Большинство иммунодепрессантов подавляют (подавляют) эту атаку, препятствуя синтезу ДНК, материала в ваших клетках, который содержит образцы всей вашей генетической информации.При этом эти лекарства предотвращают деление клеток вашей иммунной системы. Когда клетки не могут правильно делиться, они рано или поздно умрут. Чаще всего для лечения волчанки назначаются иммунодепрессанты: азатиоприн (имуран), микофенолат (целлцепт) и циклоспорин (неорал, сандиммун, генграф).
Иммунодепрессанты используются для борьбы с более серьезной волчанкой, поражающей основные органы, включая почки, мозг, сердечно-сосудистую систему и легкие.Прежде чем назначить иммунодепрессанты, ваш врач может выполнить биопсию почки или пораженной системы органов, чтобы оценить наиболее эффективный курс лечения. Иногда иммунодепрессанты назначают в дополнение к стероидной терапии или вместо нее, чтобы снизить необходимую дозу стероидов и, таким образом, избавить от некоторых нежелательных побочных эффектов стероидной терапии. По этой причине эти препараты иногда называют «стероидсберегающими» или «вспомогательными» (вспомогательными) препаратами. Стероидсберегающие препараты обычно имеют двойную пользу, поскольку они часто уменьшают или устраняют потребность в стероидах, а также улучшают симптомы волчанки.
Поскольку иммунодепрессанты подавляют иммунную систему, люди, принимающие их, подвергаются повышенному риску заражения. Старайтесь держаться подальше от людей, страдающих простудой или другими заболеваниями, регулярно мойте руки и соблюдайте правила личной гигиены. Если вы также принимаете стероидные препараты, вы можете не осознавать, что больны, потому что стероид может подавлять симптомы лихорадки. Немедленно обратитесь к врачу при первых признаках инфекции или болезни.
Кроме того, известно, что иммунодепрессанты повышают риск развития рака в более позднем возрасте.Однако известно, что волчанка сама по себе увеличивает риск рака, поэтому, контролируя волчанку сейчас и предотвращая ее дальнейшее повреждение вашему организму, иммуносупрессивная терапия может фактически снизить риск развития рака. В любом случае очень важно контролировать свою волчаночную активность сейчас, чтобы предотвратить другие потенциально опасные для жизни осложнения.
Типы иммунодепрессантов
Азатиоприн (Имуран)
Имуран — это противовоспалительное иммунодепрессивное средство, которое может уменьшить повреждение суставов и инвалидность у людей с волчанкой, ревматоидным артритом и другими заболеваниями.Кроме того, было доказано, что Имуран значительно улучшает волчанку, поражающую печень и почки. Имуран «экономит стероиды», что означает, что он позволяет снизить количество принимаемых стероидов. Поскольку побочные эффекты стероидов обычно усиливаются с дозировкой, это лекарство обычно способствует уменьшению побочных эффектов стероидов.
У людей с волчанкой сверхактивная иммунная система. Имуран работает, предотвращая распространение некоторых клеток, участвующих в этом иммунном ответе (в частности, лейкоцитов [WBC] или лейкоцитов).Имуран — это препарат с «медленным действием», а это означает, что вам может потребоваться 6-12 недель, чтобы заметить его эффекты. Обычно он выпускается в форме таблеток и имеет меньше побочных эффектов, чем многие другие иммунодепрессанты. Наиболее частые и серьезные побочные эффекты связаны с клетками желудка и крови. Могут возникать тошнота и рвота, иногда с болью в животе и диареей. Прием лекарства во время еды может помочь уменьшить эти симптомы. Имуран также может уменьшить количество определенных клеток в крови. По этой причине следует регулярно сдавать анализы крови, чтобы определять количество лейкоцитов, тромбоцитов и эритроцитов.
Менее распространенные побочные эффекты включают аномалии печеночных тестов, гепатит (воспаление печени), панкреатит (воспаление поджелудочной железы, железы позади желудка, которое может вызвать боль в животе) или аллергическую реакцию, которая может походить на грипп. Во время лечения ваш врач может провести тесты на продукты распада (метаболиты) имурана, которые помогут контролировать реакцию вашего организма на препарат.
Несмотря на то, что Имуран эффективен при лечении серьезных симптомов волчанки, длительное использование этого лекарства действительно увеличивает риск развития рака.Ваш врач может поговорить с вами об этом риске и любых других проблемах, которые могут у вас возникнуть. Он / она будет работать с вами, чтобы минимизировать побочные эффекты ваших лекарств, а также максимизировать пользу.
Помимо регулярных анализов крови (CBC), вы должны уведомить своего врача, если вы испытываете какие-либо из следующих симптомов во время приема Imuran: лихорадка, новая сыпь, легкие синяки или кровотечения или признаки инфекции. Обязательно поговорите со своим врачом, прежде чем делать какие-либо вакцины или делать операцию.Кроме того, проконсультируйтесь с врачом, если вы беременны, можете забеременеть или кормите грудью, поскольку Имуран может нанести вред вашему ребенку.
Некоторые лекарства могут влиять на Imuran, поэтому обязательно сообщите своему врачу о любых других лекарствах, которые вы принимаете. Лекарства, которые могут влиять на Imuran, включают лекарства от подагры аллопуринол (Aloprim, Zyloprim), варфарин (Coumadin), некоторые лекарства от артериального давления, включая некоторые ингибиторы ACE (Accupril или Vasotec), олсалазин (Dipentum), месаламин (Asacol, Pentasalazine) и сульфасалазин. * (Азульфидин).
Микофенолятмофетил (Селлсепт)
Селлсепт — это иммунодепрессант, который используется особенно у пациентов с волчанкой с признаками заболевания почек. Он работает, воздействуя на фермент в организме — белок, ответственный за определенные химические реакции, — который важен для образования ДНК в ваших клетках. При этом Cellcept также ухудшает функцию вашей иммунной системы. Обычно Селлсепт назначают два раза в день, общая доза составляет около 2000-3000 миллиграммов (мг) в день, но эта дозировка может быть уменьшена.Как и Imuran, Cellcept экономит стероиды, поэтому он может позволить вам и вашему врачу уменьшить дозировку стероидных препаратов и, таким образом, также уменьшить их побочные эффекты.
Cellcept может вызывать некоторые побочные эффекты. Наиболее частые эффекты включают боль в животе, тошноту, рвоту и / или диарею. Также могут возникать головная боль, головокружение, бессонница и тремор (непроизвольные движения мышц). Кожная сыпь может возникнуть, но встречается реже. Поскольку волчанка также может вызывать кожную сыпь, может быть трудно определить, возникла ли сыпь от лекарств или от волчанки.Вам следует поговорить со своим врачом при обнаружении любых новых высыпаний или симптомов.
Cellcept может также вызвать уменьшение количества определенных клеток в крови. Снижение количества лейкоцитов может увеличить вероятность заражения. Как и в случае с другими иммунодепрессантами, важно избегать заражения и уведомлять врача при первых признаках болезни. Кроме того, снижение количества красных кровяных телец, вызванное Cellcept, может привести к анемии, которая может утомить вас или привести к легким синякам.Cellcept также может снизить количество тромбоцитов в крови, что также может вызвать легкие синяки или желудочно-кишечное кровотечение (кровотечение в любом месте на пути прохождения пищи по организму). Периодические анализы крови во время приема Селлсепта могут помочь вам и вашему врачу обнаружить и исправить эти проблемы. Анализы крови следует проводить часто в течение первых нескольких месяцев приема этого лекарства и реже по мере того, как проходит больше времени.
Людям старше 65 лет и тем, у кого были язвы или другие желудочно-кишечные расстройства, перед приемом Селлсепта следует проконсультироваться со своим врачом.Люди в этих группах могут испытывать повышенный риск побочных эффектов. Кроме того, при приеме иммунодепрессантов, таких как Селлсепт, может возникнуть повышенный риск развития рака, такого как лимфома и рак кожи. Вы должны обсудить это со своим врачом, прежде чем начинать прием этого лекарства. Однако важно понимать, что Cellcept может быть лучшим способом контролировать заболевание почек, связанное с волчанкой, и что волчанка также может вызывать рак. Таким образом, назначение Селлсепта при поражении почек не предназначено для введения новых факторов риска, а скорее для лечения серьезности вашего состояния в данный момент.
Кроме того, обязательно пользуйтесь солнцезащитным кремом, выходя на улицу, и избегайте длительного пребывания на солнце, даже если вы не принимаете иммунодепрессанты, поскольку солнечный свет также может усугубить симптомы волчанки.
Если вы беременны, можете забеременеть или кормите грудью, ваш врач настоятельно рекомендует прекратить прием Селлсепта из-за риска врожденных дефектов. Кроме того, хотя неизвестно, снижает ли Cellcept эффективность оральных контрацептивов, он может снизить их концентрацию в крови, поэтому рекомендуется использовать другие формы контроля над рождаемостью.Антациды также могут препятствовать усвоению организмом Cellcept. Если вам необходимо принять антацид, сделайте это как минимум за час до или как минимум через два часа после приема Селлсепта. Как и в случае с другими иммунодепрессантами, вам следует поговорить со своим врачом, прежде чем делать какие-либо вакцины или делать какую-либо операцию.
Некоторые препараты могут взаимодействовать с Cellcept или снижать его эффективность. Эти лекарства включают: холестерхолестирамин (Questran), ацикловир (Zovirax), ганцикловир (Cytovene), азатиоприн (Imuran), антациды, содержащие гидроксид магния или алюминия (такие как Maalox, Rolaids или Mylanta), пероральные контрацептивы, триметоприм / сульфаметоксазол (сульфаметоприм). , * теофиллин (Theo-Dur), фенитоин (дилантин), пробенецид (Бенемид) или аспирин и другие салицилаты.
Обязательно немедленно сообщите своему врачу, если у вас появятся легкие синяки или кровотечения, постоянная или кровавая диарея, затрудненное дыхание, лихорадка или любые признаки инфекции.
Недавно FDA выпустило предупреждение о возможной связи между Cellcept и серьезным неврологическим заболеванием, называемым мультифокальной лейкоэнцефалопатией (PML). Аналогичное предупреждение было выпущено в отношении препарата ритуксимаб (Ритуксан) в конце 2006 года. ПМЛ — чрезвычайно редкое, но смертельное заболевание, но важно понимать, что Селлсепт и ритуксимаб не уникальны в своей связи с ПМЛ.ПМЛ ассоциируется с состояниями тяжелого иммунодефицита, такими как СПИД, рак, волчанка, а также с иммуносупрессией, которая может быть задействована в лечении этих состояний. Хотя иммунодепрессанты эффективны при лечении волчанки, ваш врач может обсудить с вами риск этой возможной взаимосвязи и использование иммунодепрессивных препаратов, используемых в рекомендованном вами лечении.
Циклоспорин (Неорал, Сандиммун, Генграф)
Циклоспорин — более мощное иммунодепрессивное лекарство, которое действует путем блокирования функции клеток иммунной системы, называемых Т-лимфоцитами или «Т-клетками».«Как и другие иммунодепрессанты, он изначально использовался для предотвращения отторжения трансплантированных органов иммунной системой пациентов с трансплантированными почками. Теперь его также назначают людям, страдающим воспалением почек, вызванным волчанкой, также известным как волчаночный нефрит. Однако циклоспорин может быть токсичным для почек, поэтому использование этого лекарства обычно применяется в случаях, когда волчанка не реагирует на другие иммунодепрессанты, такие как Селлсепт. Циклоспорин также назначают людям с тяжелым псориазом, заболеванием кожи, которое также может вызывать боль и отек суставов, и он может быть полезен для уменьшения боли, отека и жесткости, связанных с волчаночным артритом.
Начальная доза циклоспорина зависит от массы вашего тела (обычно 2,5 миллиграмма [мг] на килограмм [кг] в день). Затем доза увеличивается в зависимости от того, насколько хорошо лекарство подействует на вас и насколько хорошо ваш организм его переносит. Циклоспорин выпускается в таблетках по 25 и 100 мг, и пациенты обычно принимают 75 или 100 мг в день. Вы можете заметить некоторое уменьшение боли и отека примерно через неделю приема лекарства, но его полный эффект обычно не ощущается в течение примерно 3 месяцев.
Циклоспорин может вызывать некоторые побочные эффекты. Около 25% людей, принимающих циклоспорин, заболевают высоким кровяным давлением (гипертонией). Кроме того, поскольку циклоспорин может оказывать сильное воздействие на почки, он может вызывать накопление вещества, называемого мочевой кислотой, в крови (состояние, известное как гиперурикемия). Иногда это накопление мочевой кислоты может вызвать подагру — состояние, которое вызывает сильный отек одного из суставов, часто большого пальца ноги. Если у вас уже есть подагра, ваше состояние может ухудшиться на фоне приема циклоспорина.К счастью, многие из этих побочных эффектов проходят по мере уменьшения или прекращения лечения циклоспорином, поэтому ваш врач может вместе с вами скорректировать дозировку, если вы начнете испытывать эти проблемы.
К другим частым побочным эффектам относятся головные боли, боли в животе (включая диспепсию, грызущую или жгучую боль в подложечной области, сопровождающуюся вздутием живота), рвоту, диарею и отек рук или ног. Менее распространенные побочные эффекты включают тремор (непреднамеренные движения мышц), усиленный рост волос, мышечные судороги, онемение или покалывание в руках и ногах (состояние, известное как невропатия).Некоторые люди могут также испытывать отек десен при приеме циклоспорина. Обязательно регулярно чистите щеткой и пользуйтесь зубной нитью; этот распорядок может частично облегчить отек.
Циклоспорин может увеличить риск развития определенных типов рака, включая рак кожи. По этой причине вам следует согласовывать регулярные осмотры кожи со своим врачом. Кроме того, старайтесь держаться подальше от солнца и обязательно пользуйтесь солнцезащитным кремом, когда выходите на улицу.
Не ешьте грейпфрут и не пейте грейпфрутовый сок во время приема циклоспорина.Грейпфрут увеличивает количество циклоспорина, усваиваемого вашим телом.
Как и другие иммунодепрессанты, циклоспорин увеличивает риск заражения, поэтому обязательно мойте руки и держитесь подальше от людей, которые могут быть больны. Сообщите своему врачу при первых признаках болезни. Кроме того, сообщите своему врачу, если вы планируете сделать какие-либо вакцины или операцию, поскольку и то, и другое может представлять опасность для людей, принимающих иммунодепрессанты.
Циклоспорин может вызвать серьезные осложнения во время беременности, такие как преждевременные роды, высокое кровяное давление и задержка жидкости у вашего ребенка, поэтому вам не следует принимать циклоспорин, если вы беременны или можете забеременеть.Также не принимайте циклоспорин во время кормления грудью, так как он может передаваться вашему ребенку с грудным молоком.
Циклоспорин взаимодействует с некоторыми лекарствами, поэтому обязательно сообщите своему врачу о любых лекарствах, которые вы можете принимать, включая рецептурные и безрецептурные лекарства, добавки и витамины. Лекарства, которые могут влиять на циклоспорин или взаимодействовать с ним, включают:
- Лекарства от сердца и артериального давления: дилтиазем (Cardizem, Tiazac), никардипин (Cardene), верапамил (Calan, Covera-HS, Isoptin, Verelan), «калийсберегающие диуретики» амилорид (Midamor), спиронолактон (Aldactone) и триамтерен (Aldactone) и триамтерен Dyrenium)
- Лекарства, снижающие уровень холестерина: ловастатин (Мевакор) и симвастатин (Зокор)
- Антибиотики и противогрибковые средства: кларитромицин (биаксин), эритромицин, нациллин, флуконазол (дифлюкан), интраконазол (спокран), интраконазол (спокран) Рифадин, Римактан)
- Противосудорожные (противоэпилептические) препараты: карбамазепин (Тегретол), фенобарбитал (Сольфотон) и фенитоин (Дилантин)
- Антидепрессанты: нефазадон (Серзон) и селективные ингибиторы серотонина (такие как SS) парокситин (Паксил), флуоксетин (Прозак) и сертралин (Золофт)
- Ингибиторы протеазы вируса иммунодефицита человека (ВИЧ): индинивир (Криксиван), саквинавир (Фортоваза, Инвираза), ритонавир (N орвир) и нелфинавир (Вирасепт)
- Прочие: аллопуринол (Лопурин, Зилоприм), бромокриптин (Парлодел), андрогены (мужские гормоны), эстрогены (женские гормоны), даназол (данокрин), метоклопрамид (Реглан), метоклопрамид (Реглан), тиклопидин (Ticlid), циметидин (Tagamet), метоксален (Oxsoralen), каменноугольная смола (Balnetar, Zetar), триоксален (Trisoralen)
Обязательно сообщите своему врачу, если вы принимаете какие-либо из этих лекарств.
Противоревматические препараты, изменяющие заболевание (БПВП)
Метотрексат (ревматрекс)
Лефлуномид (Арава)
Модифицирующие заболевание противоревматические препараты, более известные как «DMARD», представляют собой иммунодепрессанты, которые используются для лечения боли и отека при артрите, который может сопровождать волчанку. БПВП не только уменьшают эту боль и отек, но также могут уменьшить долгосрочное повреждение ваших суставов.
Метотрексат (ревматрекс)
Метотрексат — одно из наиболее часто используемых лекарств для лечения ревматоидного артрита, и он используется у пациентов с волчанкой для облегчения боли в суставах и отека при полиартрите (артрите с поражением нескольких суставов).Он лишь умеренно эффективен при более серьезных симптомах волчанки, затрагивающих почки и другие органы, и его следует осторожно применять людям с этими состояниями. Исторически метотрексат использовался для лечения рака и псориаза, состояния кожи, которое также может влиять на суставы. Однако в конце 1980-х это лекарство было одобрено FDA для лечения артрита и с тех пор широко используется для этого. Метотрексат действует, препятствуя выработке фолиевой кислоты, которая является строительным блоком для роста клеток в вашем теле.В результате метотрексат препятствует росту некоторых клеток, в том числе иммунной системы. Это лекарство также сберегает стероиды, то есть его можно использовать в сочетании со стероидами для снижения дозы стероидной терапии и, таким образом, также для снижения связанных побочных эффектов.
Лекарство обычно принимают в виде таблеток в дозах от 7,5 до 25 миллиграммов (мг) в неделю, но его также можно вводить в виде инъекции. Люди, принимающие метотрексат, обычно чувствуют улучшение через 3-6 недель, но может потребоваться до 3 месяцев, чтобы ощутить все преимущества препарата.Обязательно принимайте это лекарство в соответствии с указаниями. Если вы пропустите прием, вы обычно можете принять лекарство через 4 или 5 дней после этого. Однако, если вы пропустите это окно, обратитесь к врачу, чтобы узнать, что делать дальше.
Большинство людей, принимающих метотрексат, не испытывают побочных эффектов, и многие из более незначительных побочных эффектов со временем уменьшатся. Однако вероятность этих побочных эффектов увеличивается с увеличением дозировки. Многие из побочных эффектов метотрексата связаны с тем, что лекарство действует, препятствуя выработке фолиевой кислоты в организме.Поэтому ваш врач, скорее всего, порекомендует вам принимать добавки с фолиевой кислотой, которые предотвратят многие из этих побочных эффектов, включая язвы во рту (стоматит). Другие побочные эффекты могут включать тошноту, рвоту и повышенный риск аномальных функциональных тестов печени. Из-за опасности для печени вы не должны употреблять алкоголь во время приема метотрексата; употребление алкоголя во время приема этого лекарства может вызвать необратимое повреждение печени. Кроме того, важно, чтобы у людей, принимающих метотрексат, были нормальные показатели функции печени.Обязательно сообщите своему врачу, если у вас в анамнезе есть заболевания печени. Кроме того, при приеме этого лекарства могут возникнуть проблемы с легкими, такие как продолжающийся кашель или одышка, но чаще встречаются у людей с уже существующими заболеваниями легких. Если вы испытываете эти симптомы, обратитесь к врачу.
У некоторых пациентов наблюдается постепенное выпадение волос (алопеция), но волосы обычно отрастают снова после прекращения приема метотрексата. Кроме того, метотрексат может повысить вашу чувствительность к солнечному свету.Поскольку многие пациенты с волчанкой уже испытывают чувствительность к солнцу, постарайтесь ограничить пребывание на солнце и обязательно пользуйтесь солнцезащитным кремом, когда выходите на улицу.
Важно помнить, что иногда побочные эффекты этого лекарства могут остаться незамеченными; Иногда у людей могут быть отклонения от нормы в анализах крови при отсутствии побочных эффектов, поэтому важно проводить анализы крови (общий анализ крови или «общий анализ крови») каждые 2-3 месяца во время приема метотрексата.
Если вы беременны, можете забеременеть или кормите грудью, вам не следует принимать этот препарат, поскольку он может вызвать серьезные врожденные дефекты и осложнения во время беременности.Женщины, принимающие это лекарство, должны использовать эффективный метод контроля над рождаемостью. Поговорите со своим врачом о любых планах или проблемах беременности.
Как и в случае с другими лекарствами, которые могут подавлять вашу иммунную систему, поговорите со своим врачом о любых вакцинах или операциях, которые вам могут быть сделаны. Кроме того, не забудьте сообщить ему / ей о любых других лекарствах, как рецептурных, так и внебиржевых, которые вы можете принимать. Метотрексат может взаимодействовать с некоторыми лекарствами, включая антибиотик триметоприм (Бактрим) * и НПВП, такие как ибупрофен (Адвил, Мотрин) и целекоксиб (Целебрекс).Однако помните, что иногда метотрексат может использоваться в сочетании с некоторыми НПВП для лечения волчанки. Ваш врач будет работать с вами, чтобы определить, какие методы лечения лучше всего подойдут для лечения симптомов волчанки с наименьшими побочными эффектами.
Лефлуномид (Арава)
Лефлуномид — еще один DMARD, используемый для лечения отека, боли и скованности, которые испытывают многие пациенты с волчанкой из-за артрита. Его можно назначать отдельно или в сочетании с другими методами лечения, такими как метотрексат; Часто лефлуномид назначают пациентам, которые плохо реагируют на метотрексат.Лефлуномид работает, блокируя образование ДНК в клетках вашего тела, включая клетки иммунной системы. Препятствуя образованию ДНК, лефлуномид препятствует выработке организмом сверхактивных иммунных клеток, ответственных за опухоль, жесткость и боль в суставах.
Лефлуномид обычно принимают в таблетках по 10 или 20 миллиграммов (мг) один раз в день. Может пройти 6–12 недель, прежде чем вы почувствуете все преимущества этого лекарства, хотя боль в суставах и скованность, вероятно, начнут уменьшаться уже через несколько недель.Чтобы лекарство накопилось в организме, требуется некоторое время, поэтому некоторые врачи могут назначить так называемую «нагрузочную дозу», когда вы впервые начинаете принимать лефлуномид. Ударная доза — это большая доза (около 100 мг), которую обычно назначают один раз в неделю в течение трех недель в дополнение к вашей обычной дозе. В качестве альтернативы некоторые врачи могут назначать эту нагрузочную дозу в течение первых трех дней. Однако этот метод обычно увеличивает вероятность развития побочных эффектов, в том числе диареи. Хорошая новость заключается в том, что диарея обычно проходит после прекращения приема ударной дозы.
Лефлуномид действительно имеет несколько побочных эффектов. Наиболее частым побочным эффектом является диарея, от которой страдает примерно 1 из 5 человек, но этот симптом обычно проходит со временем. Кроме того, ваш врач может поговорить с вами о приеме антидиарейного лекарства, чтобы уменьшить этот дискомфорт. Если диарея не проходит, он / она может снизить дозировку.
Другие побочные эффекты включают тошноту, несварение желудка, сыпь или выпадение волос (алопецию), но эти эффекты встречаются реже. Кроме того, примерно у 1 из 10 пациентов, принимающих лефлуномид, наблюдаются аномальные функциональные тесты печени или сниженное количество клеток крови, поэтому людям, принимающим это лекарство, следует регулярно каждые 3-4 месяца делать анализ ферментов печени и анализ крови.Из-за этого риска для вашей печени вам не следует употреблять алкоголь во время приема лефлуномида, и вы должны сообщить своему врачу, если у вас были проблемы с печенью в прошлом.
Беременным, беременным или кормящим женщинам следует поговорить со своим врачом перед приемом лефлуномида, поскольку это лекарство может вызвать серьезные врожденные дефекты и осложнения. Кроме того, женщины должны использовать эффективный метод контроля над рождаемостью во время приема лефлуномида и продолжать делать это до двух лет после отмены лефлуномида, поскольку известно, что лекарство остается в вашем организме и после того, как вы фактически прекратите его принимать.Мужчинам, которые хотят иметь детей, также следует поговорить со своим врачом о прекращении приема лекарств. Любой, кто принимает лекарства и хотел бы иметь детей, должен поговорить со своим врачом о лекарстве под названием холестирамин (квестран), которое может помочь вывести лефлуномид из вашего организма.
Как и в случае с другими лекарствами, подавляющими вашу иммунную систему, поговорите со своим врачом о любых вакцинациях или операциях, которые вы планируете сделать, а также о любых других лекарствах, которые вы можете принимать, включая лекарства, отпускаемые по рецепту, лекарства, отпускаемые без рецепта, витамины и добавки.Лекарства, которые могут взаимодействовать с лефлуномидом, включают холестирамин (Квестран), толбутамид (Ориназа) и рифампицин (Рифадин, Римактан), поэтому обязательно сообщите своему врачу, если вы принимаете эти лекарства.
Цитотоксические препараты
Циклофосфамид (Цитоксан)
Хлорамбуцил (лейкеран)
Азотный горчица (Мустарген)
Цитотоксические препараты — это класс иммунодепрессантов, которые изначально были разработаны (и используются до сих пор) для лечения определенных типов рака.Цитотоксические препараты, обычно назначаемые для лечения симптомов волчанки, классифицируются как алкилирующие агенты и предназначены для пациентов с более серьезными формами волчанки, которые поражают такие органы, как почки, центральная нервная система, легкие и кровеносные сосуды. Цитотоксические препараты действуют против клеток вашей иммунной системы, вырабатывающих антитела (иммуноглобулины). Обычно эти молекулы помогают организму защищаться от инфекций и других захватчиков. Однако при волчанке эти антитела на самом деле работают против вашего собственного тела и вырабатываются очень быстро.Цитоксические препараты борются с быстро делящимися клетками иммунной системы, но при этом они также действуют против других быстро делящихся клеток вашего тела, включая клетки крови, волосковые клетки и половые клетки. В результате цитотоксические препараты могут иметь серьезные долгосрочные побочные эффекты. Несмотря на то, что доказано, что цитотоксики улучшают симптомы заболеваний почек, нервной системы, легких и кровеносных сосудов у пациентов с волчанкой, вам и вашему врачу важно оценить стоимость и преимущества цитотоксической терапии до начала этого лечения.
Цитоксан (циклофосфамид)
Цитоксан — цитотоксический препарат, обычно применяемый для пациентов с волчанкой и серьезными проблемами с почками, которые не реагируют на другие лекарства. Дозировка Cytoxan варьируется от человека к человеку. Его можно принимать в форме таблеток, но чаще его вводят внутривенно (в / в) на приеме у врача. Процедура внутривенного вливания обычно занимает от 15 до 60 минут, и перед ней могут быть назначены лекарства, чтобы уменьшить тошноту, которую вы можете почувствовать. Врачи обычно назначают цитоксан один раз в месяц в течение 6 месяцев, а затем каждые 2–3 месяца в течение двух лет.Цитоксану может потребоваться несколько недель или месяцев, чтобы улучшить симптомы волчанки.
Побочные эффекты Cytoxan варьируются от легких до тяжелых и могут усиливаться, когда лекарство принимается в форме таблеток. Побочные эффекты включают тошноту и рвоту, которые иногда можно предотвратить с помощью лекарства от тошноты, такого как ондансетрон (Зофран). Может произойти выпадение волос (алопеция), но после прекращения приема лекарств волосы обычно отрастают. Также может возникнуть кожная сыпь, которую трудно отличить от симптомов волчанки.Как и другие лекарства, подавляющие вашу иммунную систему, Cytoxan может увеличить риск инфекций, особенно опоясывающего лишая и некоторых «оппортунистических инфекций», инфекций, которые обычно не вызывают заболевания у здоровых людей. Поэтому важно регулярно мыть руки, соблюдать личную гигиену и уведомлять врача при первых признаках инфекции или лихорадки. Также сообщите своему врачу, если вам предстоит вакцинация или операция, поскольку ваша иммунная система будет подавлена цитоксаном.
Более серьезные побочные эффекты включают снижение количества лейкоцитов, которое обычно происходит примерно через 8–12 дней после начала лечения. Ваш врач должен провести анализы крови в это время, чтобы определить, следует ли изменить дозировку. Кроме того, Цитоксан может вызвать бесплодие как у мужчин, так и у женщин при длительном приеме. Однако можно сделать инъекцию под названием лейпролид (лупрон), чтобы защитить ваше тело от этого бесплодия; вы можете обсудить этот вопрос со своим врачом, прежде чем начинать прием лекарства.Кроме того, у женщин могут прекратиться менструации при приеме Цитоксана. Однако вы все равно можете забеременеть, поэтому рекомендуется использовать метод контрацепции, поскольку прием этого препарата может нанести серьезный вред плоду. Обязательно проконсультируйтесь с врачом перед приемом Цитоксана, если вы беременны, можете забеременеть или кормите грудью.
Цитоксан также может вызывать определенные проблемы с мочевым пузырем. Чтобы использовать этот препарат, ваше тело должно расщепить его на несколько побочных продуктов, один из которых может вызвать раздражение мочевого пузыря и вызвать образование рубцов или кровь в моче.Этот побочный эффект является обычным явлением, поэтому вам следует пить много жидкости — не менее 8 стаканов воды — в день. Если вы принимаете цитоксан внутривенно, вам могут дать месну (Mesnex), чтобы предотвратить эти проблемы с мочевым пузырем.
Поскольку Цитоксан нацелен не только на клетки иммунной системы, но и на нормальные клетки вашего тела, он увеличивает риск рака. Чем больше цитоксана вы принимаете и чем дольше вы его принимаете, тем выше риск развития рака даже в более позднем возрасте. Лейкемия и рак мочевого пузыря являются наиболее распространенной формой рака, развивающейся у пациентов, принимающих цитоксан, поэтому ваш врач должен регулярно проводить анализы мочи.
Цитоксан может взаимодействовать с некоторыми лекарствами, поэтому обязательно сообщите своему врачу о любых лекарствах, которые вы принимаете, как по рецепту, так и без рецепта. Также расскажите ему / ей о любых пищевых добавках (включая травяные добавки) и / или витаминах, которые вы, возможно, принимаете. Следующие препараты могут взаимодействовать с Цитоксаном: лекарство от подагры аллопуринол (Алоприм, Зилоприм), фенобарбитал (Сольфотон), варфарин (Кумадин), тиазидные диуретики, такие как гидрохлоротиазид, и некоторые психиатрические препараты.Обязательно сообщите своему врачу, если вы принимаете какие-либо из этих лекарств.
Хлорамбуцил (Leukeran) и азотистый иприт (Mustargen)
Хлорамбуцил (лейкеран) и азотистый иприт (мустарген) являются цитотоксическими препаратами, подобными цитоксану. В прошлом они использовались для лечения симптомов волчанки, но в настоящее время не используются так часто, как цитоксан. Лейкеран обычно принимают внутрь и широко используется в Европе и развивающихся странах. В США его обычно назначают людям, которые не переносят цитоксан или страдают аллергией на это лекарство.Лекарство обычно переносится лучше, чем таблетки Цитоксана. Однако он более опасен, чем цитоксан внутривенно, потому что его нужно принимать в течение более длительного периода времени, что увеличивает риск развития рака. Таким образом, если вы принимаете таблетки лейкеран, вы должны принимать их не более двух лет.
Азотный горчичник на самом деле был первым цитотоксическим препаратом, который оказался эффективным при лечении волчанки. Однако сегодня он редко используется, потому что его сложнее вводить, и его нужно вводить внутривенно в больнице.Ваш врач поговорит с вами более подробно, если этот препарат будет задействован в вашем лечении.
∗ Людям с волчанкой не следует принимать Бактрим, сульфамидные антибиотики (например, Гантризин, Септра) или сульфамидные средства (например, Альдактон), поскольку эти лекарства могут вызывать вспышки волчанки из-за повышения чувствительности к солнцу и иногда снижения показателей крови. Если вам прописали одно из этих лекарств, поговорите со своим врачом о возможных альтернативах.
Подавление иммунной системы | Пациент
Что такое иммунная система?
Нас постоянно окружают миллионы бактерий, вирусов и других микробов (микробов).Некоторые из них активно помогают нам — например, мы не смогли бы переваривать пищу без «дружественных» кишечных бактерий. Большинство из них безвредны, если они не попадают в нашу систему — и задача нашей иммунной системы — остановить это.
Иммунная система — защита организма от болезнетворных микробов (патогенов) — может быть разделена на:
- Линии первой защиты (наша кожа, слюна, слизистая оболочка носа, кислые желудочные соки и т. Д.)
- Специально адаптированные лейкоциты, называемые лимфоцитами
- Другие типы белых кровяных телец
- Ваша лимфатическая система (сеть трубок и желез — лимфатических узлов или желез, которые переносят жидкость, называемую лимфатическими клетками, называемыми лимфоцитами)
См. Также отдельная брошюра под названием «Иммунная система» для получения дополнительной информации.
Что такое подавление иммунитета?
Подавление иммунитета, также известное как иммуносупрессия или ослабление иммунитета, означает, что ваша иммунная система не работает должным образом. Это включает в себя любую или все защитные механизмы, из которых состоит ваша иммунная система, особенно белые клетки в нашем кровотоке, а также селезенка и лимфатические узлы.
Когда эта система заблокирована, т.е. не работает должным образом, мы более уязвимы для заражения.
Что это значит для меня?
Если ваша иммунная система подавлена, вы можете быть более уязвимы для инфекции.Вам с большей вероятностью понадобится обратиться к врачу, вам с большей вероятностью понадобятся антибиотики, и вы с большей вероятностью попадете в больницу для лечения, если у вас разовьется инфекция, чем человеку, у которого нет иммуносупрессии. Вы не можете получать живые вакцины, если у вас подавленный иммунитет, и вам, возможно, придется принимать особые меры предосторожности во время путешествий.
Вы также более уязвимы к определенным видам рака кожи, если у вас подавленный иммунитет.
Что вызывает иммуносупрессию?
Причинами иммуносупрессии могут быть:
- Возраст.Когда мы стареем, наша иммунная система становится менее эффективной.
- Хроническая (хроническая) болезнь. Иммунные системы, как правило, становятся менее эффективными по мере прогрессирования некоторых долгосрочных заболеваний. Примеры включают тяжелое хроническое заболевание почек, хроническое заболевание печени и сахарный диабет.
- Недоедание.
- Лекарства от болезней, вызванных атакой иммунной системы (аутоиммунные состояния). Примеры включают ревматоидный артрит и болезнь Крона.
- Лекарства в виде пероральных стероидов для состояний, которые приводят к воспалению, когда лечение необходимо для уменьшения воспаления.
- Лекарства, принимаемые для предотвращения отторжения у людей, перенесших трансплантацию органов или костного мозга.
- Химиотерапия или лучевая терапия для лечения рака
- Рак. Некоторые виды рака могут вызывать подавление иммунитета, особенно те, которые затрагивают клетки крови, которые так важны для нашей иммунной системы. Лимфомы, лейкемии и миелома — это виды рака, которые могут подавлять иммунную систему.
- Отсутствие селезенки из-за ее удаления. Или наличие неработающей селезенки.Это может произойти из-за определенных состояний, таких как серповидноклеточная анемия, большая талассемия или лимфома, или после лучевой терапии.
- ВИЧ и СПИД. Вирус иммунодефицита человека (ВИЧ) влияет на иммунную систему.
- Редкие генетические состояния, которые приводят к потере иммунной функции — например, синдром тяжелого комбинированного иммунодефицита (ТКИД), синдром ДиДжорджи, синдром Вискотта-Олдрича.
Какие лекарства вызывают подавление иммунитета?
Пероральные стероиды являются частой причиной подавления иммунитета и используются при различных состояниях.Они с большей вероятностью снизят вашу иммунную защиту при длительном применении в высоких дозах. Более низкие дозы обычно не вызывают проблем. Для взрослого доза преднизолона 40 мг в день в течение более недели может вызвать подавление иммунитета, но эта доза варьируется для других стероидов и для детей. См. Дополнительную информацию в отдельной брошюре «Оральные стероиды».
К другим лекарствам, подавляющим иммунную систему, относятся:
Эти лекарства используются для лечения всех видов состояний, в том числе наиболее распространенных из них:
Почему удаляют селезенку?
Ваша селезенка является важной частью вашей иммунной системы, но иногда ее необходимо удалить с помощью операции, называемой спленэктомией.Это может потребоваться, если вы попали в аварию или получили травму в результате разрыва селезенки. Возможно, его потребуется удалить, чтобы предотвратить потерю большого количества крови.
Иногда он становится слишком большим и разрушает слишком много клеток крови. Примеры, когда это происходит и может потребоваться удаление селезенки, включают:
См. Отдельные брошюры «Селезенка и предотвращение инфекции после спленэктомии или если у вас нет рабочей селезенки» для получения дополнительной информации о селезенке.
Каковы симптомы подавления иммунитета
?
В большинстве случаев, если у вас есть подавление иммунитета, вы не знаете, что оно у вас есть. Однако вы можете чаще заражаться инфекциями. Кроме того, инфекции могут быть более серьезными, и у вас повышается вероятность развития серьезных осложнений. Вы также можете получить необычные или необычные инфекции. Например, у здоровых взрослых обычно не бывает молочницы во рту, если для этого нет веской причины, например, при использовании стероидного ингалятора.Однако у людей со СПИДом молочница является обычным явлением и может быть очень широко распространенным или тяжелым заболеванием.
Лекарства, подавляющие вашу иммунную систему, могут вызывать и другие побочные эффекты. Они различаются и будут перечислены в информации, прилагаемой к вашему лекарству.
Каковы осложнения подавления иммунитета?
Инфекции могут развиваться и распространяться особенно быстро у людей с подавленной иммунной системой. Например, боль в горле с большей вероятностью перерастет в инфекцию грудной клетки.У вас больше шансов заразить любую отдельную инфекцию на все ваше тело (сепсис), что может привести к опасному заболеванию.
Люди с подавленным иммунитетом также подвержены более высокому риску определенных типов рака кожи. Это включает плоскоклеточный рак (SCC), меланому и саркому Капоши. Не совсем понятно, почему это так. Это может быть потому, что иммунная система помогает разрушать клетки кожи, поврежденные солнцем. Эти клетки, если их не удалить иммунной системой, могут продолжать размножаться и вызывать рак.Также может быть, что вирусы (например, вирус папилломы человека — ВПЧ или вирусы герпеса), вызывающие некоторые виды рака, с большей вероятностью будут присутствовать, если иммунная система подавлена. Некоторые иммунодепрессанты могут напрямую влиять на клетки кожи, повышая вероятность развития рака кожи.
Если у меня подавление иммунитета, какие симптомы должны побудить меня обратиться к врачу?
Если у вас подавленный иммунитет, правила посещения врача меняются. Иммунная система здоровых людей может бороться с большинством незначительных инфекций в считанные дни без какого-либо медицинского вмешательства.Вот почему при большинстве незначительных инфекций здоровым людям рекомендуется проявлять выжидательность. Это означает лечение симптомов и посещение врача только в том случае, если они очень плохо себя чувствуют или инфекция не проходит сама по себе.
Однако при подавлении иммунитета даже легкая инфекция может очень быстро стать серьезной. Так что лучше обратиться к врачу как можно скорее, чем ждать, чтобы посмотреть, как идут дела. Выявленные на ранней стадии инфекции можно быстро вылечить, предотвратив их распространение и ухудшение здоровья.У вас больше шансов получить антибиотик от легкой инфекции, чем у человека, у которого нет иммуносупрессии, и в крайних случаях это может спасти вашу жизнь.
Так что обратитесь к врачу, если вы подозреваете, что у вас инфекция, например, боль в горле, кашель, симптомы мочевой инфекции, пищевое отравление и т. Д.
Немедленно обратитесь за медицинской помощью, если:
- У вас высокий температура (лихорадка) более 38 ° C.
- Вас озноб или трясет (озноб).
- В целом вы чувствуете себя плохо с головокружением, сонливостью или спутанностью сознания.
- У вас сыпь.
- Свет режет глаза.
- У вас припадки.
Если у вас есть ребенок с ослабленным иммунитетом, применимо все вышеперечисленное. Но вам также следует срочно обратиться за медицинской помощью, если ваш ребенок дышит учащенно или не ест и не пьет как обычно.
Также следите за своей кожей. Если у вас появляются чешуйчатые участки, которые не исчезают быстро с помощью хорошего увлажняющего крема, или если у вас появилась новая или изменившаяся родинка, обратитесь к врачу.Будем надеяться, что это не будет какой-либо рак кожи, но если это так, то чем раньше вылечить, тем лучше будет результат.
Как контролируется прием иммунодепрессантов?
Это зависит от конкретного лекарства. Некоторые лекарства требуют регулярного анализа крови. Они контролируют ваши кровяные тельца (лейкоциты, эритроциты и тромбоциты) и проверяют, не становятся ли их слишком низкими. Также могут быть сданы анализы крови, чтобы проверить, не влияет ли лекарство на вашу печень или функцию почек.
Для других препаратов, подавляющих иммунитет, вы можете регулярно сдавать анализ крови, чтобы узнать, насколько хорошо они действуют. Например, если вы принимаете стероиды от ревматической полимиалгии (PMR), проводится анализ крови, чтобы проверить уровень воспаления в вашем организме. По мере снижения этих уровней дозу можно постепенно снижать. Если анализы крови показывают, что болезнь снова активна, возможно, вам потребуется увеличить дозу. Подобные анализы крови проводятся для контроля некоторых лекарств, используемых для лечения ревматоидного артрита.
Он также может меняться со временем. Например, для некоторых лекарств, таких как метотрексат, вам сначала потребуется частый анализ крови каждые одну или две недели, тогда как после того, как вы принимаете их в течение некоторого времени, если кажется, что все будет стабильно, это будет снижаться до каждые три месяца.
Спросите своего терапевта или специалиста о требованиях к мониторингу ваших лекарств.
Есть ли другие тесты?
Для лечения состояния, от которого вы проходите, могут потребоваться другие анализы.Например, при некоторых формах рака может потребоваться биопсия костного мозга для наблюдения за происходящим. При ВИЧ и СПИДе для отслеживания того, что происходит, можно использовать специальные анализы крови на иммунную функцию.
Ваш специалист может также наблюдать за вами на предмет любых изменений на вашей коже, поскольку подавление иммунитета может сделать вас более восприимчивыми к раку кожи.
Другие тесты и требования к мониторингу будут зависеть от конкретного лекарства. Например, если вы принимаете оральные стероиды, вы можете контролировать свой вес и артериальное давление, поскольку увеличение веса и высокое артериальное давление могут быть побочными эффектами этого типа лекарств.На стероидах также будет контролироваться плотность ваших костей, так как они могут вызвать «истончение» костей (остеопороз), а ваши глаза будут проверяться на предмет катаракты.
Можно ли лечить подавление иммунитета?
Все зависит от причины. В одних случаях это можно вылечить, в других — под контролем. Например:
- ВИЧ-инфекцию и СПИД лечат специальными препаратами против ВИЧ. См. Отдельную брошюру под названием «ВИЧ и СПИД».
- Многие виды рака можно успешно лечить или, по крайней мере, отсрочить их прогрессирование с помощью химиотерапии.
- В некоторых случаях используются трансплантаты стволовых клеток (или костного мозга). Поврежденные клетки заменяют нормальными. Это используется при некоторых формах рака, а также при некоторых состояниях генетической иммуносупрессии.
- Подавление иммунитета, вызванное лекарствами, должно прекратиться, если их прекратить. Если подавление иммунитета причиняет вред, иногда можно использовать альтернативу или снизить дозу. В других случаях инфекция быстро лечится по мере ее возникновения, пока продолжают прием лекарств.Как долго используется лекарство, зависит от состояния, которое лечится.
- Эффект от спленэктомии сохраняется на всю жизнь, но есть способы снизить риск заражения (см. Раздел ниже).
- При некоторых состояниях, таких как генетические иммунные нарушения, можно делать инъекции белков антител (иммуноглобулинов), чтобы помочь организму бороться с инфекцией.
Раннее лечение инфекций имеет решающее значение, если у вас ослаблен иммунитет. Вам назначат лечение от инфекции.Если вы нездоровы или не работаете, вас могут госпитализировать.
Нужно ли мне какое-либо специальное лечение для предотвращения проблем, если у меня подавлен иммунитет?
Если ваша иммунная система подавлена, важно принять меры, чтобы избежать заражения. Это можно сделать несколькими способами:
- Примите общие меры, чтобы избежать заражения. Например, избегайте еды, которая подвергает вас риску пищевого отравления. Обращайтесь с сырым мясом осторожно. Используйте общие меры гигиены, чтобы содержать дом и т. Д. В чистоте и без микробов.
- По возможности избегайте тесного контакта с людьми с инфекционными заболеваниями.
- Обеспечьте своевременность всех плановых прививок. (Конкретные рекомендации даны для детей с ослабленным иммунитетом, которым делают прививки в детстве.)
- Дополнительные прививки для людей с повышенным риском, такие как ежегодная прививка от гриппа и вакцинация против пневмонии и опоясывающего лишая.
- Некоторые живые вакцины (содержащие живые микробы) не делаются некоторым людям с подавленной иммунной системой.
- Некоторым людям, перенесшим спленэктомию и подвергающимся особому риску инфицирования, рекомендуется ежедневно принимать антибиотики, например пенициллин.
Существуют ли какие-либо особые меры предосторожности во время путешествий?
Поскольку вы подвергаетесь особому риску заражения, разумно очень тщательно спланировать поездку. Сообщите всем туристам о вакцинации к месту назначения. (В зависимости от причины подавления иммунитета вам могут быть рекомендованы не принимать определенные живые вакцины.Остерегайтесь путешествовать в страны с высоким риском заболеваний, против которых вы не можете пройти вакцинацию.) Избегайте посещения мест, где у вас не будет доступа к хорошей медицинской помощи, если вы заболеете. Путешествуйте с информацией о вашем состоянии и лекарствах на случай, если вам понадобится помощь медицинского работника, находясь вдали от вашего обычного врача (ов). Убедитесь, что ваша туристическая страховка покрывает вас, если вы заболеете. Обсудите со своим врачом и рассмотрите возможность приема некоторых антибиотиков «на всякий случай» и инструкций о том, когда их принимать, если вы подвержены риску определенных инфекций.Примите обычные меры предосторожности, чтобы избежать пищевого отравления / диареи путешественника, если посещение места может быть опасным.
И, наконец, если вы путешествуете в жаркое место, используйте много солнцезащитного крема с высоким содержанием факторов, чтобы защитить кожу.
Картирование воздействия лекарств на иммунную систему
Abstract
Понимание того, как лекарства влияют на иммунную систему, имеет последствия для лечения заболеваний и минимизации нежелательных побочных эффектов. Здесь мы представляем интегративный вычислительный подход для прогнозирования взаимодействий между лекарствами и иммунными клетками в масштабе всей системы.Этот подход сопоставляет наборы генов между сигнатурами транскрипции, чтобы определить их сходство. Мы применяем этот метод для моделирования взаимодействий между 1309 лекарствами и 221 типом иммунных клеток и прогнозируем 69 995 известных и новых взаимодействий. Полученная в результате карта фармакологии иммунных клеток используется для прогнозирования того, как 5 препаратов влияют на 4 типа иммунных клеток у людей и мышей. Чтобы подтвердить прогнозы, мы проанализировали истории болезни пациентов и изучили изменения клеточной популяции из экспериментов in vivo . Наш метод предлагает инструмент для проверки тысяч взаимодействий с целью выявления взаимосвязей между лекарствами и иммунной системой.
Фармацевтические препараты всех типов и классов влияют на иммунную систему 1–4 , но механизмы этих нарушений часто недостаточно изучены. Некоторые препараты нацелены на иммунные клетки специально для лечения иммунологических заболеваний, таких как В-клеточные лимфомы (например, ритуксимаб 5 ), тогда как другие обладают широким иммунодепрессивным или противовоспалительным действием (например, талидомид 6 , лефлуномид 7 или сиролимус 8 ). Однако многие препараты, которые не были разработаны как иммуномодулирующие, тем не менее связаны с легкими и тяжелыми иммунными фенотипами.Например, считается, что некоторые противоинфекционные, противосудорожные и антидиабетические препараты вызывают реакцию гиперчувствительности кожи крапивница 9–11 , а психоаналептики, такие как респиридон, мемантин и циталопрам, имеют редкий, но опасный для жизни побочный эффект. иммунной комплексной гиперчувствительности, называемой синдромом Стивенса-Джонсона 1 . Наше непонимание глобальных взаимодействий между фармацевтическими препаратами и иммунной системой затрудняет разработку лекарств, скрывает потенциально серьезные побочные эффекты продаваемых на рынке соединений 12–14 и ограничивает открытие лекарств, которые можно использовать для лечения иммунных заболеваний.
Опубликованные исследования воздействия лекарств на иммунные клетки в основном изучали последствия введения одного лекарственного средства на клетки одного типа 15,16 . Даже когда выполнялись высокопроизводительные экраны, они обычно фокусировались на конкретной цели или считывании (например, изменениях в выбранных маркерах клеточной поверхности) 17–19 и игнорировали другие возмущения в системе. В настоящем отчете мы основываемся на предыдущих подходах на системном уровне, которые сравнивают и интегрируют профили дифференциальной экспрессии заболевания с профилями пертурбации лекарств, чтобы обнаружить потенциальные показания к новым лекарствам 20–22 .Недавние крупномасштабные совместные усилия позволили подготовить сборники молекулярных профилей как фармацевтических препаратов 23 , так и иммунных клеток 24 . Насколько нам известно, систематическая интеграция и анализ хемогеномных и иммуногеномных данных не проводились.
Мы объединили данные о лекарственных пертурбациях, полученные на раковых клетках человека, и данные экспрессии генов, полученные на иммунных клетках мыши. Наш анализ количественно оценивает вероятность того, что лекарство влияет на изменение состояния иммунных клеток, в форме «оценки иммунодефицита».Всего мы сгенерировали 304 изменения состояний иммунных клеток из 221 типа иммунных клеток. Мы изучили все комбинации из 1309 препаратов и 304 изменений состояний иммунных клеток и обнаружили 69 995 значимых взаимодействий (из 397 936 возможных взаимодействий). На основе этих взаимодействий мы построили фармакологическую карту иммунных клеток (IP) предсказанных связей между лекарствами и иммунными клетками, которая включает как известные, так и новые взаимодействия. Чтобы устранить опасения по поводу интеграции данных по видам, прогнозы были изучены как на мышах, так и на людях.Мы выполнили in vivo экспериментальной проверки 3 предсказаний и получили 100% согласие. Кроме того, мы нашли доказательства в данных о пациентах, которые подтверждали наши предсказанные взаимодействия между лекарствами и иммунными клетками в двух независимых наборах электронных медицинских записей. Наши результаты показывают, что интегративный вычислительный анализ может улучшить понимание эффектов лекарств на иммунную систему и обеспечить основу для рационального управления этими эффектами.
РЕЗУЛЬТАТЫ
Генерация молекулярных сигнатур иммунных клеток
Проект «Иммунологический геном» (ImmGen) является крупнейшим общедоступным сборником полногеномных профилей транскрипционной экспрессии для более чем 250 различных иммунологических состояний клеток у мышей 25–27 .Данные включают 14 категорий типов иммунных клеток, собранных из 25 участков ткани (дополнительный рисунок 1). Эти состояния отражают различные стадии дифференцировки клонов, собранные из различных тканей с использованием набора генетических вариантов, в ответ на стимуляцию химическими веществами, бактериями или вирусами и на отдельных эффекторных стадиях. Одна из проблем с использованием данных ImmGen для исследования иммунных нарушений заключается в том, что профили экспрессии генов фиксировались в одном состоянии, что дает ограниченную информацию о клеточном ответе на внешние стимулы.Таким образом, мы создали набор данных, который отражает ответы иммунных клеток на пертурбации путем создания сигнатур дифференциально экспрессируемых генов между двумя иммунологическими состояниями, которые различаются одним параметром (например, типы клеток с идентичными поверхностными маркерами, выделенными из разных тканей, или два типа клеток, которые отличаются один поверхностный маркер, такой как наивные против CD4 + Т-клеток памяти).
Мы собрали набор из 304 сигнатур изменения состояния иммунных клеток из 221 уникального типа клеток в компендиуме ImmGen, чтобы изучить, как лекарственные нарушения влияют на иммунную систему (
Дополнительная таблица 1).Полные ранжированные списки представлены в дополнительной таблице 2. Эти сигнатуры группируются по схожим типам клеток при кластеризации по расстоянию Жаккара между наборами генов крайних складок (дополнительный рис. 2). Средние расстояния Жаккара между родственными типами клеток превышают общее среднее фоновое расстояние (дополнительный рис. 3) и показали значительные различия между подмножествами иммунных клеток (p-значение = 6 × 10 -15 , ANOVA).
Конструирование взаимодействия «лекарство-клетка»
( a ) Схематический обзор этапов интеграции и обработки данных.( b ) Схематическое изображение алгоритма сопоставления и распределения баллов. ( c ) Резюме изученных иммунологических изменений состояния клеток. ( d ) Мультяшная диаграмма влияния лекарств на изменения состояния иммунных клеток, предсказываемых знаком оценки иммуномода.
Создание хемогеномных профилей лекарств
Карта подключений (CMap) — это хранилище данных профилей транскрипционной экспрессии в масштабе всего генома, собранных в 6100 экспериментальных условиях 1309 уникальных соединений, примененных к линиям клеток человека 23 .Каждое возмущение представлено списком дифференциально экспрессируемых генов, ранжированных нами на основе кратности изменения. Чтобы зафиксировать согласованный профиль соединения в разных условиях, мы объединили несколько экспериментов (т. Е. С разными концентрациями лекарств или клеточными линиями) для одного и того же соединения в единый ранжированный список прототипов (PRL), используя иерархическую схему большинства голосов 28,29 (). Коллекция ПРЛ создала всеобъемлющий ресурс для разработки инструмента систематического скрининга для поиска связей между лекарственными нарушениями и иммунологическими состояниями (дополнительная таблица 3).
Построение IP-карты
Мы создали общесистемную карту взаимодействия между лекарствами и иммунными клетками, сопоставив 1309 профилей пертурбации лекарств в CMap с 304 изменениями состояния иммунных клеток, которые мы курировали из сборника ImmGen. Наш алгоритм сопоставления оценивает сходство между двумя паттернами транскрипционной экспрессии путем сравнения генов с верхним и нижним ранжированием из обоих профилей 20,21 (дополнительный рис. 4 и методы). В частности, мы проверили сходство между профилями изменения иммунологического состояния (состояние B vs.состояние A) для каждого из профилей нарушения лекарственного средства (леченых против необработанных) путем вычисления показателя иммунодефицита на основании перекрытия генов, занимающих верхние и нижние позиции в каждом профиле. Положительная оценка иммунофосфата указывает на то, что профиль лечения конкретным лекарственным средством подобен состоянию иммунных клеток B и предполагает, что лекарство смещает иммунную клетку в сторону состояния B, тогда как отрицательная оценка свидетельствует о том, что лечение препаратом сдвигает клетку в состояние A ().
Чтобы оценить значимость наших предсказанных взаимодействий между лекарственными средствами и клетками, мы сгенерировали случайные профили пертурбаций лекарственных средств для каждого соединения и повторили анализ 1000 раз для каждого изменения состояния иммунных клеток (дополнительный рис.4а и методы). Полная вычислительная интеграция наборов данных CMap и ImmGen дала 397 936 потенциальных связей между лекарствами и изменениями состояния иммунных клеток. Чтобы оценить, была ли предсказанная связь надежной, мы варьировали размер набора генов с верхним и нижним рейтингом, используемых для алгоритма сопоставления, и пересчитали все ~ 400 000 пар «оценка-p-значение» иммуномода. Пропорция каждого взаимодействия лекарственного средства с клеткой была значительной среди всех размеров набора генов, обеспечивающая относительный вес для каждого предсказанного взаимодействия (дополнительный рис.4б, в). Большие веса указывают на то, что данное взаимодействие лекарственное средство-клетка меньше зависит от размера набора, выбранного для расчета оценки иммунодефицита, и означает надежную связь. Этот процесс выбора позволил обнаружить ранее неизвестные взаимодействия при минимизации ложных соединений (дополнительный рисунок 5).
Используя значимые и надежные взаимодействия, мы установили связи между лекарствами и изменениями состояния иммунных клеток для создания всеобъемлющей IP-карты. Карта IP содержит 69 995 соединений (дополнительная таблица 4), которые значимы при FDR менее 5% и появляются в> 85% размеров набора генов.Хотя каждое лекарство показало значительную связь по крайней мере с одним из 304 изменений иммунологического состояния, наиболее частое количество переходов между состояниями составляет 26, и 144 препарата влияют на 100 или более изменений состояния (дополнительный рисунок 6). Лекарства, которые, по прогнозам, влияют на наибольшее количество переходов состояний иммунных клеток, включают мощные иммуномодуляторы, многие из которых вызывают значительную иммуносупрессию (). Лекарства с иммуномодулирующей активностью (например, противовоспалительные средства, антигистамины и иммунодепрессанты) демонстрируют значительное улучшение взаимодействия иммунных клеток ( E = 1.5, P = 0,002, E = 1,4, P = 0,04, E = 2,1, P = 0,02 , соответственно, и дополнительная таблица 5).
Таблица 1
Предполагается, что лекарственные препараты влияют на наибольшее количество изменений иммунного статуса.
| Лекарство | Состояние изменения | Статус | Класс лекарственного средства | |||
|---|---|---|---|---|---|---|
| Пуромицин | 138 | Экспериментальный | Аминонуклеозидный ингибитор | Квинтозид | ||
| Дептропин | 129 | Одобренный | Антигистаминный | |||
| Гликлазид | 127 | Одобренный | Антидиабетический | |||
| Антидиабетический | ||||||
| Психиатрический | ||||||
| Иринотекан | 127 | Одобренный | Ингибитор топоизомеразы | |||
| Пирвиний | 126 | Экспериментальный | Антигельминтный | |||
| Даунорубицин | 126 | Одобренный | Антрациклин | |||
| Целастрол | 125 | Экспериментальный | Противовоспалительное | Противовоспалительное | Противовоспалительное | |
| Пимозид | 124 | Одобрен | Антипсихотический |
Глобальные свойства IP-карты
Чтобы изучить глобальный ландшафт IP-карты, мы использовали оценку иммунодефицита в качестве метрики сходства и организовали полную набор взаимодействий лекарств и иммунных клеток посредством неконтролируемой иерархической кластеризации ().Мы обнаружили, что препараты со схожими терапевтическими классами группируются вместе. Например, антипсихотические препараты (клозапин, локсапин, галоперидол и флуфеназин) образовали кластер, так же как и аналоги пурина (меркаптопурин и тиогуанин) и блокаторы кальциевых каналов (дексверапамил, бепридил и пергексилин). Предполагается, что эти три кластера будут взаимодействовать с наибольшим числом переходов подмножества иммунных клеток. Кластеры лекарств также показали обогащение по той же молекулярной мишени. Например, противодиабетические препараты троглитазон и розиглитазон нацелены на PPARG и ACSL4 как часть их механизма действия по снижению уровня глюкозы в крови.Основываясь на их показателях иммунодефицита, предполагается, что эти препараты будут влиять на наивные CD4 + Т-клетки и NK-клетки, что дает потенциальное объяснение терапевтических преимуществ, наблюдаемых у пациентов с аутоиммунным заболеванием 32,33 .
Обзор IP-карты
( a ) Кластерная тепловая карта лекарств и изменений состояния иммунных клеток, организованная по счету иммуномода. Диаграммы Венна отражают количество лекарств, которые изменяют состояния иммунных клеток в определенном или неспецифическом направлении.( b ) Двумерная тепловая карта стабильных кластеров клеток и лекарств со значительным обогащением по крайней мере для одного типа клеток (строки) или терапевтического класса уровня 1 (столбцы). К терапевтическим классам относятся: H = системные гормональные препараты, искл. половые гормоны и инсулины, V = различные, B = кровь и кроветворные органы, P = противопаразитарные продукты, M = костно-мышечная система, L = противоопухолевые и иммуномодулирующие средства, G = мочеполовая система и половые гормоны , R = дыхательная система, A = пищеварительный тракт и обмен веществ, D = дерматологические препараты, J = противоинфекционные препараты для системного применения, S = органы чувств, N = нервная система и C = сердечно-сосудистая система.Области соответствующих кружков представляют количество клеток или лекарства в кластере (2–14 клеток, 2–13 препаратов). Квадраты серого цвета указывают на предсказанное взаимодействие по крайней мере между одной парой клеток-лекарств в парах кластеров.
Мы идентифицировали 28 лекарств, связанных с более поздними стадиями развития клонов нескольких типов клеток (например, стволовые / предшественники и пре-В-клетки; дополнительная таблица 6). Эти лекарства включают соединения, используемые для лечения заболеваний обмена веществ и нервной, скелетно-мышечной и респираторной систем, или являются противоинфекционными средствами.Более того, эти 28 препаратов обогащены (i) агентами с иммунодепрессивной, антипсориатической и дофаминергической активностью и (ii) соединениями, которые нацелены на связанный с хроматином фермент PARP1, который является ключевой регуляторной молекулой для дифференцировки и пролиферации 34, 35 . Напротив, 17 соединений влияют на субпопуляции незрелых гемопоэтических клеток (дополнительная таблица 7). Эти соединения не относятся к одному терапевтическому классу, но их молекулярные мишени обогащены процессами, связанными с активностью оксидоредуктазы и репарацией алкилирования, которые важны для дифференцировки и поддержания целостности стволовых клеток 36,37 .
Чтобы дополнительно охарактеризовать взаимодействие лекарств и иммунных клеток, мы выполнили неконтролируемую иерархическую кластеризацию с многоуровневой загрузочной повторной выборкой 38 . Из 143 изменений типов ячеек 119 соответствуют одному из 25 стабильных кластеров ячеек ( P <0,05, многомасштабный бутстрап-анализ) (дополнительная таблица 8). Почти половина (13/25) стабильных кластеров клеток демонстрирует значительное избыточное обогащение (E> 2, P <0,05) для одного или нескольких типов клеток (дополнительная таблица 9).Для сравнения, 1089 лекарств из 1309 в общей сложности попали в один из 409 стабильных кластеров лекарств ( P <0,05, многомасштабный анализ начальной загрузки) (дополнительная таблица 10). Почти 87% (356/409) стабильных кластеров лекарств показали значительное избыточное обогащение (E> 4, P <0,05) для одного или нескольких терапевтических классов (уровни классификации ATC 1-3) или молекулярной мишени, Дополнительная таблица 11). Например, 88 кластеров лекарственных средств значительно обогатились по крайней мере для одного описания уровня 1 системы классификации анатомо-терапевтических химических веществ (АТХ).Обогащение обусловлено обилием антитромботических агентов или витамина К и других кровоостанавливающих средств (B), контрастных агентов или диагностических радиофармпрепаратов (V), а также алкилирующих агентов, цитотоксических антибиотиков, гормональных антагонистов или иммунодепрессантов (L) (дополнительные Рис.7).
Чтобы изучить особенности стабильных кластеров более подробно, мы идентифицировали 53 кластера лекарств, обогащенных для терапевтического класса и молекулярной мишени, и пересекли эти кластеры с 13 кластерами клеток, обогащенными для одного или нескольких типов клеток ().Пересекающиеся кластеры показали, что определенные подмножества иммунных клеток (например, пре-лимфоциты, моноциты, NKT-клетки и гамма-дельта-Т-клетки) перекрываются с несколькими категориями лекарств, тогда как другие подмножества (например, В-клетки и макрофаги) пересекаются с парные категории. Несколько кластеров лекарств (например, cl195, cl335) влияли на несколько типов клеток, тогда как другие кластеры (например, cl2, cl48, cl49, cl97) влияли на один тип клеток. Кластер лекарств с наибольшим перекрытием иммунных клеток (cl195) был обогащен противоопухолевыми препаратами, которые являются цитотоксическими антибиотиками (например, доксорубицином и митоксантроном).
Мы обнаружили сильную положительную связь между количеством молекулярных мишеней для данного лекарственного средства и количеством предполагаемых взаимодействий, влияющих на переходы иммунологического состояния ( P = 1,7 × 10 −5 , линейная регрессия). Когда мы изучали неблагоприятные лекарственные взаимодействия с использованием ресурса по побочным эффектам (версия 2) 1 , мы не обнаружили взаимосвязи между сообщаемым количеством побочных эффектов для лекарства и количеством взаимодействий с иммунными клетками ( P = 0.8, линейная регрессия). Однако, поскольку данные о побочных эффектах имеют широкое частотное распределение и их трудно точно измерить 2 , это отсутствие корреляции может отражать вариацию, присущую систематической ошибке регистрации и сообщения о побочных эффектах.
Соединения и субструктуры в IP-карте
Чтобы изучить возможные иммунологические результаты, которые могут возникнуть в результате соединений в IP-карте, мы сосредоточились на изменениях состояния иммунных клеток между субпопуляциями клеток или тканями. Переходы между лекарственными средствами и клетками были организованы по терапевтическим классам и категориям перехода состояний иммунных клеток (например,g., внутри подмножества или между тканями), чтобы обеспечить обзор всех предсказанных связей, которые являются статистически значимыми (дополнительный рис. 8). Мы идентифицировали неразборчивые наркотики по их взаимодействию с большим количеством переходов подмножества (). Учитывая неравномерное распределение типов клеток в пределах подмножества изменений состояния (дополнительная таблица 1), мы определили концентраторы лекарств на основе взаимодействий с наибольшим количеством типов клеток, которые, как мы предполагаем, могут иметь наибольшее влияние на иммунную систему.Напротив, островки лекарств были определены на основе взаимодействия с наименьшим количеством клеток ().
Прогнозирование влияния иммунных клеток на основе IP-карты
( a ) Круговая схема прогнозируемых связей между лекарствами и типами клеток (все связи статистически значимы P <0,05 с FDR <5%, см. Методы). Ширина линии соответствует количеству взаимодействий. Диаграмма была организована путем сортировки типов клеток против часовой стрелки (лекарства по часовой стрелке) в порядке убывания количества соединений.Однобуквенные коды для каждого препарата соответствуют системе анатомической терапевтической классификации, как описано в. ( b ) Подсеть, показывающая концентраторы и островки лекарств (квадратные узлы в центре и на периферии соответственно) и их предсказанные взаимодействия с подмножествами иммунных клеток (кружки). Каждый квадратный узел представляет собой одно лекарство (например, четыре центральных узла, обозначенных буквой L, представляют собой против часовой стрелки сверху, препараты даунорубицин, азацитидин, вориностат и метотрексат). ( c ) Лекарства, идентифицированные на IP-карте на основе их иммунодефицитной оценки и, по прогнозам, увеличивают частоту нейтрофилов и моноцитов в крови.( d ) Подтверждение предсказания лекарств в иммунных клетках человека. Влияние лекарств (+ = лекарство, — = отсутствие лекарственного средства) на количество клеток, измеренное на основании лабораторных значений пациентов в электронных медицинских записях Mount Sinai (количество и частота клеток). Высота столбцов представляет собой среднее количество (нейтрофилы) или частоту (моноциты), а нижняя / верхняя граница столбцов ошибок отражают межквартильные диапазоны (от 25% до 75% данных соответственно). Значимость оценивалась с помощью критерия суммы рангов Вилкоксона.
Таблица 2
Предполагается, что лекарственные препараты повлияют на наибольшее количество изменений иммунной подгруппы.
| Лекарство | Изменения в подгруппе | Статус | Класс лекарства | |||
|---|---|---|---|---|---|---|
| Иринотекан | 60 | Утверждено | Пурпоизомеразный антибиотик | Пурпоизомеразный антибиотик | ||
| Дептропин | 55 | Одобрено | Антигистамин | |||
| Тирфостин AG-825 | 54 | Экспериментальный | Экспериментальный | Ингибитор тирозинкиназы | ||
| Даунорубицин | 54 | Одобренный | Антрациклин | |||
| Медризон | 53 | Одобрен | Кортикостероид | блокатор | ||
| Этакриновая кислота | 52 | Одобрено | Петлевой диуретик | |||
| Альстерпауллон | 52 | Экспериментальный | Циклин-хвинзависимый | |||
| Прокаин | 50 | Одобрено | Местный анестетик | |||
| Гликлазид | 50 | Одобренный | Антидиабетический | Антидиабетический | ||
| 50 | Одобрено | Антихолинергические |
Хабы были обогащены противоопухолевыми препаратами (E = 13.8, P <1 × 10 -5 ) (дополнительный рис. 9), чего можно было ожидать, учитывая влияние этих соединений на иммунные клетки 1,2 . Хабы также были обогащены соединениями нервной системы, такими как селективный ингибитор обратного захвата серотонина зимелдин (E = 1,3, P <0,04), который был снят с продажи из-за редкой, но серьезной побочной реакции, приводящей к аутоиммунному состоянию, известному как Синдром Гийена-Барре 39 и противосудорожный препарат топирамат, который оказался эффективным средством лечения воспалительного заболевания кишечника на доклинической модели 21 (дополнительный рис.10а). Напротив, островки лекарств были обогащены метаболическими лекарствами, которые включали антидиабетические соединения гликидон и метформин (дополнительный рис. 10b). Этот метаболический остров, который мы идентифицировали на карте IP, отражает низкую связность, обнаруженную при метаболических заболеваниях в сети болезней человека 40 .
Чтобы исследовать препараты, которые, по прогнозам, будут влиять на часть адаптивной иммунной системы, мы определили подсеть, основанную на наибольшей величине иммунных оценок для субпопуляций Т-клеток и тканей (дополнительный рис.11). Эта подсеть включает более тысячи соединений, которые, по прогнозам, будут влиять на подмножества CD4 + или CD8 + , причем 113 и 202 соединения уникальны для каждой группы соответственно. Наивысший показатель иммунодефицита для этой подсети находится между CD4 + FoxP3 + Т-клетками и гуанфацином (дополнительные рисунки 12, 13а). Гуанфацин — агонист рецептора α2A (ADRA2A), используемый для снижения артериального давления и лечения СДВГ 41 .
Чтобы убедиться, что оценка иммуномода определяет влияние препарата на конкретную субпопуляцию клеток, мы вводили антигипертензивный препарат гуанфацин мышам и измеряли процент регуляторных субпопуляций Т-клеток, выделенных из селезенки.Основываясь на оценке иммуномода, мы пришли к выводу, что частота регуляторных Т-клеток должна увеличиваться после лечения гуанфацином. По сравнению с необработанными мышами, обработанные мыши показали 5% увеличение средней частоты клеток CD62L + в компартменте Т-клеток CD4 + FoxP3 + (42,0% против 37,0%: n = 15 обработанных против n = 14 необработанных, P = 0,01, дополнительный рисунок 13b).
Когда мы исследовали подмножества CD8 + , наивысший балл по иммунным модам был у антипаркинсонического препарата тригексифенидил.Одной из молекулярных мишеней тригексифенидила является мускариновый ацетилхолиновый рецептор M1 (CHRM1). Когда ген, кодирующий эту молекулярную мишень, нокаутирован в модели на мышах, клетки CD8 + этих мышей проявляют дефектную цитотоксическую способность 42 .
Подтверждение взаимодействия лекарств с иммунными клетками у людей
Данные об иммунных клетках были собраны у мышей, а данные о лекарственных нарушениях были собраны из линий раковых клеток человека. Одна из проблем, связанных с интеграцией этих данных, заключается в том, применимы ли результаты, полученные на мышах, для людей.Мы проверили, могут ли взаимодействия, предсказанные картой IP, наблюдаться у людей, изучив количество иммунных клеток у пациентов, которым вводили лекарство, по сравнению с пациентами, не получавшими лечения. Чтобы сравнить популяции пациентов, мы изучили полные анализы крови для более чем 2,3 миллиона электронных медицинских карт в системе больниц Mount Sinai и отобрали людей, которые прошли лечение и у которых был собран анализ клеток крови в течение одного месяца после приема лекарства.
Учитывая ограничения обычных клинических лабораторных тестов, обнаруживаемые в электронных медицинских записях, мы ограничили предсказания IP-карты двумя распространенными препаратами, которые, по прогнозам, влияют на моноциты и нейтрофилы.IP-карта предсказывала, что общий анестетик пропофол и антигипертензивный спиронолактон будут увеличивать количество нейтрофилов и моноцитов соответственно (). Пропофол увеличивал количество нейтрофилов на 2500 клеток / мм 3 , а спиронолактон увеличивал частоту моноцитов на 1,6% (). Хотя изменения клеточной популяции были небольшими, оба сдвига были значительными ( P <1 × 10 −100 , сумма рангов Вилкоксона). Более того, увеличение количества нейтрофилов у большинства пациентов привело к выходу за верхний предел нормы.Чтобы подтвердить эти наблюдения, мы исследовали те же пары лекарств и иммунных клеток в электронных медицинских записях Медицинского центра Колумбийского университета. Этот независимый источник данных показал одинаковую направленность и значимость обоих препаратов и их прогнозируемого влияния на иммунные клетки (дополнительная таблица 12).
Подтверждение влияния клиохинола на миграцию нейтрофилов
Для оценки точности и специфичности предсказанного взаимодействия на карте IP мы экспериментально подтвердили влияние лекарственного препарата клиохинол на миграцию нейтрофилов из костного мозга в кровь.Эта гипотеза возникла из прогноза с наивысшим показателем иммунодефицита (), а также из желания идентифицировать лекарство, которое могло бы изменять динамику иммунной системы между тканями и которое было бы просто оценить с обильным типом клеток in vivo . Более того, регуляция нейтрофилов играет решающую роль в здоровье и болезнях, поэтому новые лекарства, изменяющие их кинетику, могут иметь терапевтический потенциал 43–45 .
Влияние на миграцию иммунных клеток с использованием IP-карты
Показатели Immunemod для влияния на иммунные клетки между тканями с использованием ( a ) клиохинола или ( b ) амантадина.Этикетки указывают направление влияния лекарственного средства на тип клеток между тканями x -> y, а ширина столбца представляет собой величину оценки иммунодефицита. Показаны значительные и устойчивые взаимодействия лекарств с клетками. Оранжевые стрелки отражают предполагаемое максимальное взаимодействие с клиохинолом и отсутствие взаимодействия с амантадином. Фиолетовые стрелки указывают на предсказанные взаимодействия с дополнительной экспериментальной проверкой. ( c ) Представленные графики биаксиальной проточной цитометрии клеток Gr-Ly6G + и CD11b + , собранных из различных тканей обработанных и необработанных мышей.Клетки гейтировали в популяции CD45 + DAPI —. ( d ) Частоты Ly6G + CD11b + нейтрофилов клеток, собранных из крови, костного мозга и брюшной полости ( n = 8 на группу). Черные столбцы отражают медианное выражение всех образцов в каждом состоянии, а нижняя / верхняя части прямоугольников представляют 25 -го и 75 -го процентилей соответственно. Данные представляют от трех до четырех экспериментов. Значимость оценивается ANOVA.( e ) Количественный анализ экспрессии маркерных генов нейтрофилов. Содержание каждого транскрипта в селезенке, печени, легких и костном мозге (BM) рассчитывали относительно соответствующего контроля (PEG400 для клиохинола или PBS для амантадина). Каждое экспериментальное условие включает 8 образцов. Значимость оценивается ANOVA. ( f ) Деревья SPADE данных CyTOF, собранные из клеток селезенки. Стрелками выделено увеличение популяции Gr-Ly6G + CD11b + после лечения клиохинолом.Горизонтальные цветовые шкалы представляют собой среднюю интенсивность указанного маркера (синий = низкий, красный = высокий).
Мы выбрали два препарата для эксперимента на основе их иммунных оценок и p-значений. Эти статистические показатели определили наивысший балл иммунодефицита и соответствующее самое низкое значение p для прогнозируемого сочетания нейтрофилов и клиохинола (). Клиохинол является противогрибковым и противопротозойным лекарственным средством без известного механизма действия, но это соединение было протестировано на доклинической модели болезни Альцгеймера 46,47 .В качестве контроля мы выбрали противовирусный и противопаркинсонический препарат амантадин в качестве контрольного препарата, поскольку наш алгоритм предсказал нулевую оценку иммуномода для взаимодействия амантадин-нейтрофил (). Основываясь на показателях иммунопрофилактики, мы пришли к выводу, что клиохинол может влиять на миграцию нейтрофилов из костного мозга в кровь, тогда как амантадин не влияет на миграцию нейтрофилов ().
Чтобы оценить прогнозируемое влияние клиохинола на нейтрофилы in vivo , мы вводили мышам C57BL / 6 клиохинол или контрольный носитель ( n, = 8 обработанных и n = 8 необработанных).После лечения клиохинолом, но не контролем, нейтрофилы рекрутировались в брюшную полость (дополнительный рис. 14). У мышей, получавших клиохинол, более 70% гематопоэтических клеток в полости были нейтрофилами, тогда как у мышей, получавших только носитель, менее 5% были нейтрофилами, как и у необработанных мышей. Это рекрутирование совпало с мобилизацией нейтрофилов из костного мозга в кровь (дополнительный рис. 14). Более того, анализ кПЦР собранных образцов ткани выявил повышенное количество транскриптов нейтрофил-специфических хемокинов, таких как Cxcl1, Cxcl2 и Cxcl5 ().Мы также обнаружили транскрипт Cxcr2 , что свидетельствует об инфильтрации нейтрофилов в анализируемых образцах.
Как и предполагалось, у мышей, получавших амантадин, не было значительного изменения частоты нейтрофилов в крови, костном мозге или брюшной полости (). Чтобы изучить более широкий спектр изменений иммунных клеток после лечения, мы выполнили массовую цитометрию (CyTOF) с использованием панели из 19 маркеров для оценки клеточных различий в селезенке мышей, получавших клиохинол или контрольный носитель.В соответствии с тем, что мы наблюдали с помощью проточной цитометрии, количество нейтрофилов увеличилось (Ly6G + CD11b + клетки) после лечения клиохинолом (). Кроме того, когда мы исследовали полный набор маркеров с использованием деревьев SPADE 48 , мы обнаружили увеличение количества наивных CD8 + клеток (CD45 + CD3 + CD4 — CD8 + Thy1.2 + TCRb + CD62L hi CD44 lo ) (дополнительный рис. 15), что также было предсказано нашим алгоритмом, хотя и с более низким показателем иммунодефицита ().
ОБСУЖДЕНИЕ
Мы описываем интегративный вычислительный подход для картирования эффектов лекарств на иммунную функцию. Мы сравнили хемогеномный и иммуногеномный профили и создали показатель иммунодефицита для количественной оценки вероятного влияния лекарственного воздействия на иммунную клетку на основе перекрытия их транскрипционных профилей. Хотя полный набор взаимодействий между лекарствами и иммунными клетками больше, чем то, что мы смоделировали здесь, наше систематическое изучение почти 400 000 потенциальных взаимодействий является шагом к картированию этого огромного пространства. In vivo эксперименты по подтверждению одного прогноза — что селективный агонист альфа-2A адренергических рецепторов гуанфацин увеличивает долю регуляторных Т-клеток — предположили, что лекарство, используемое для лечения гипертонии и тревоги, может быть перепрофилировано для стимулирования периферической толерантности. Чтобы изучить полезность использования IP-карты для выявления лекарств с наивысшими показателями иммунодефицита для данного перехода иммунологического состояния, мы предсказали, что на изменение соотношения нейтрофилов между кровью и костным мозгом больше всего повлияет лекарственный препарат клиохинол.Этот вывод подтверждается пропорциями нейтрофилов, собранных из крови и костного мозга, и характером специфичных для нейтрофилов генов, экспрессируемых в различных тканях. Предыдущее исследование, в котором использовались соединения для управления уровнями экспрессии Cxcr2 и Cxcr4 , показало паттерны мобилизации нейтрофилов, аналогичные тем, которые мы наблюдали 49 . Хотя клиохинол обладает нейротоксическим действием, эти результаты предполагают его потенциальное использование в качестве краткосрочного усилителя нейтрофилов в определенных контекстах.Кроме того, это открытие предполагает, что наш подход может позволить открытие соединений, контролирующих кинетику нейтрофилов, для устранения воспалительных реакций 50 .
Ограничение IP-карты состоит в том, что она объединяет наборы данных от мыши и человека, и поэтому предсказанные связи могут не транслироваться в иммунные клетки человека. Несколько недавних исследований показали как сходство, так и различия между профилями транскрипции иммунных клеток у мышей и людей 51–54 .Однако оба наших прогноза были подтверждены в электронных медицинских записях на горе Синай и в независимом наборе данных Колумбийского университета. Взятые вместе, наши вычислительные анализы и экспериментальные результаты показывают, что IP-карта фиксирует иммунные ответы как у людей, так и у мышей.
Еще одним ограничением является то, что профили препаратов CMap были созданы на ограниченном наборе линий раковых клеток с использованием полногеномного транскрипционного профилирования. Хотя усилиями проекта LINCS (http: // www.lincsproject.org) значительно расширит количество соединений и включит больше клеточных линий, вероятно, имеет смысл генерировать иммуноспецифические сигнатуры CMap по крайней мере для подмножества типов иммунных клеток для дальнейшей оценки и улучшения метода подсчета иммунных мод. Такие усилия, как обширное транскрипционное профилирование дифференцировки человеческих клеток 55 , должны быть расширены для более полной картины человеческого иммунитета, что поможет лучше понять, как данные ImmGen будут транслироваться между видами.Мы не использовали информацию о химической структуре и признаем, что включение структурной информации и данных, отличных от профилей транскрипции 56,57 , предоставит более полную картину сложности воздействия лекарств на иммунную систему.
Метод статистической биоинформатики, который мы использовали для систематического изучения взаимодействий лекарств и иммунных клеток, следует подходу Колмогорова-Смирнова (KS), аналогичному тому, который использовался во многих других исследованиях 20,23,58 . Этот метод был полезен при идентификации многочисленных биологических связей, которые впоследствии были подтверждены экспериментально.Однако ограничение традиционного подхода KS с использованием транскрипционных данных является предположением о статистической независимости транскриптов. Другие недавно предложили возможные решения для этого ограничения 59–62 . Когда мы реализовали в наших методах подход на основе PCA 59 , p-значения действительно выросли, как и ожидалось. В рамках этой альтернативной нулевой модели количество значимых взаимодействий уменьшается примерно в 3 раза по сравнению с методом независимого перемешивания (дополнительный рис.5). Однако кажется, что коррекция на основе PCA может быть излишне пессимистичной при низких порогах FDR 59 . Это наблюдение, по-видимому, отражено в нашем собственном анализе, где мы обнаруживаем, что все экспериментально проверенные и подтвержденные взаимодействия падают выше порога значимости после перестановки с поправкой на PCA. Насколько нам известно, до сих пор не проводился систематический анализ различных предложенных методов обогащения на основе набора генов с поправкой на независимость на хемогеномных данных.Систематическая оценка подходов к перестановке и декорреляции экспрессии для крупномасштабного картирования хемогеномных связей является плодотворной областью для будущих исследований, особенно в связи с тем, что хемогеномное сообщество использует уменьшенные наборы наборов зондов с использованием платформы L1000.
Очевидно неизвестные взаимодействия, идентифицированные на IP-карте, могут включать многие, требующие экспериментального наблюдения. Другие возможные применения наших данных включают изучение вклада иммунных клеток в побочные реакции на лекарства, роль подмножеств иммунных клеток в развитии рака и других заболеваний, а также комбинированную лекарственную терапию.Более того, глобальные тенденции, извлеченные из наших данных, могут предоставить руководящие принципы и конкретные прогнозы о том, как манипулировать иммунными клетками, раскрыть механизмы действия лекарств и выбрать альтернативные соединения из той же терапевтической категории с меньшим количеством побочных эффектов иммунных клеток.
МЕТОДЫ
Данные по экспрессии генов лекарств и иммунных клеток
Изменения профиля транскрипции, вызванные лекарственными средствами, определенные на линиях раковых клеток человека, были получены из базы данных 23 карты связи (CMap).Мы обработали и проанализировали версию 2, которая включала 6 100 экспериментов с 1309 соединениями. Этапы предварительной обработки и нормализации были выполнены, как описано ранее 23 . Чтобы сделать кросс-платформенные сравнения совместимыми, мы стандартизировали идентификаторы генов от идентификаторов зондов, специфичных для микрочипов, до идентификаторов NCBI GeneID, выбрав максимальное значение для отдельных значений экспрессии зонда. Чтобы создать единый ранжированный профиль экспрессии для каждого из 1309 соединений, мы объединили несколько экспериментов для одного и того же соединения в единый ранжированный список прототипов (PRL) после обработки, описанной ранее 28,29 .Окончательный набор данных включал 13 071 значение дифференциальной экспрессии генов для каждого из 1309 соединений.
Данные по экспрессии генов иммунных клеток, собранные из стационарного профилирования 249 различных типов клеток, были получены из ImmGen 24 . Предварительная обработка и нормализация были выполнены, как описано ранее 64 . Поскольку профили клеток были собраны в установившемся состоянии, мы выбрали 221 уникальный тип клеток и создали 304 сигнатуры дифференциального состояния из разницы между двумя профилями устойчивого состояния (дополнительная таблица 13).Чтобы сделать межвидовые и кросс-платформенные сравнения разумными, мы стандартизировали идентификаторы генов от идентификаторов зондов, специфичных для микрочипов, до идентификаторов NCBI GeneID, сопоставили идентификаторы GeneID мыши с их человеческим ортологом и выбрали максимум для отдельных значений экспрессии зонда. Наконец, мы преобразовали профили дифференциального состояния в ранжированные списки, упорядоченные по значениям дифференциальной экспрессии, создав набор данных с 11 153 значениями дифференциальной экспрессии генов для каждого из 304 изменений иммунологического состояния.
Построение IP-карты
Мы построили матрицу предсказанных взаимодействий между каждым из 1309 лекарств и 304 изменений иммунологического состояния, используя ранговую стратегию сопоставления с образцом, описанную ранее 20 . Вкратце, для каждого трио размера набора лекарств, клеток и генов ( d, c, s ) мы рассчитали показатель Immunemod Score ( ImS ), основанный на степени перекрытия между наборами генов лекарственного средства и иммунных клеток в крайних случаях. двух ранжированных подписей. Чтобы получить меру значимости для оценки Immunemod, мы перетасовали гены в сигнатуре ранга лекарств и вычислили перестановку Immunemod Score ( ImS * ) для каждого лекарства, клетки и триплета набора генов [ ImS * (d i). , c j , s k ) ].Мы рассчитали p-значение для каждого ImS , подсчитав количество рандомизированных оценок ImS * (d i , c j , s k ) , которые были больше или равны абсолютному значению фактические оценки ImS (d i , c j , s k ) и деление на количество перестановок ( n perms = 1000 ). Эта стратегия перестановки устанавливает нижнюю границу для p-значений на уровне 0,001, что дает смещенную оценку количества ложных срабатываний с учетом количества рассматриваемых гипотез.Чтобы обеспечить точные p-значения в нижнем диапазоне, в то же время ограничивая вычислительные затраты, мы использовали обобщенное распределение Парето для моделирования распределения p-значений и вычислили улучшенные оценки для низких p-значений (количество <1/100) на основе распределения баллы пермутированного иммунодефицита 30 . Мы скорректировали p-значения 65 и выбрали FDR 5% в качестве порога значимости. Для контроля ложных взаимодействий на основе размера набора генов, используемого для сопоставления, мы варьировали размер набора сопоставлений от 100 до 250 генов для каждого из верхних и нижних крайних значений и пересчитывали все оценки иммуномода, пары значений p для каждого лекарство-клеточное взаимодействие.Доля случаев, когда каждое взаимодействие лекарство-клетка было значимым среди всех размеров наборов генов, обеспечивает относительную силу для любого данного взаимодействия. Прогнозируемое взаимодействие считалось сильным и стабильным, если оно было значимым для 85% или более размеров набора.
Анализ данных
Чтобы оценить сходство между профилями экспрессии подмножеств иммунных клеток, мы рассчитали расстояние Жаккара среди всех пар генов с экстремальной кратностью изменений и использовали ANOVA для оценки различий между подмножествами иммунных клеток.Мы исследовали серию диагностических графиков и не обнаружили значительных отклонений, которые нарушали бы предположения о нормальности или гомоскедастичности.
Чтобы организовать препараты и иммунные клетки беспристрастным образом, мы применили иерархическую кластеризацию к полной матрице взаимодействия, используя вычисленный коэффициент корреляции Пирсона в качестве метрики расстояния между оценками иммунодефицита и полной кластеризацией сцепления для агломерации лекарств или клеток. Мы использовали пакет pvclust R 38 для вычисления начального анализа кластеров и идентифицировали значительный кластер, если приблизительно несмещенная вероятность была> 95%.
Чтобы определить обогащение категории анатомического терапевтического класса, мы рассчитали кратное изменение и p-значение. Кратковременное обогащение (E) рассчитывалось как отношение соотношений E = (a / b) / (c / d), где a — количество лекарств с определенной категорией (например, «L») в кластере. Представляет интерес, b — количество лекарств с этой категорией в общем наборе данных, c — общее количество лекарств в кластере, а d — общее количество лекарств в целом. Мы использовали гипергеометрическое распределение для расчета p-значения и оценки значимости каждого вычисления обогащения.
Чтобы изучить связь между химическими характеристиками (например, молекулярными мишенями и побочными эффектами лекарств) и количеством взаимодействий иммунных клеток, мы реализовали простую модель линейной регрессии. Химические характеристики следовали асимметричному распределению, поэтому мы преобразовали данные в логарифм, в результате чего значения скорректировали так, чтобы они следовали нормальному распределению. Основываясь на диагностических графиках преобразованных данных, мы не обнаружили отклонений, которые нарушали бы предположения о нормальности и гомоскедастичности, которые являются центральными для регрессионных моделей.
Чтобы проверить, вызывает ли медикаментозное лечение клиохинолом или амантадином какие-либо различия в частотах нейтрофильных клеток в различных тканевых компартментах, мы использовали модель ANOVA для сравнения групп лечения. Множественное групповое тестирование и p-значения оценивались с использованием достоверной значимой разницы Тьюки. Для всех тестов ANOVA мы создали серию диагностических графиков для изучения: (i) остаточных ошибок для выбросов, (ii) графиков QQ для нормальности и (iii) квадратного корня из стандартизованных остатков для гетероскедастичности.Во всех случаях мы не обнаружили значительных отклонений, которые нарушили бы предположения, используемые в модели ANOVA. Для сравнения мы оценили экспериментальную и контрольную группы непосредственно с помощью теста суммы рангов Вилкоксона и обнаружили, что медианные различия между лечением (клиохинол, амантадин) и контролями (PEG400, PBS) соответствуют точно такой же схеме, полученной с использованием ANOVA, с аналогичными максимальное значение p для значимых различий ( P ≤ 0,01). Чтобы проверить, влияет ли гуанфацин на частоту регуляторных Т-клеток, мы использовали стратегию метаанализа 63 для объединения экспериментальных условий и групп, что позволило нам установить, были ли общие различия в каждом независимом эксперименте надежными и значительными.
Электронная медицинская карта
Мы извлекли из электронной медицинской карты Mount Sinai все записи о пациентах, которые содержали данные полного анализа крови на нейтрофилы и моноциты (всего более 2,3 миллиона записей). Чтобы определить, связаны ли пропофол или спиронолактон с изменением количества клеток, мы определили записи пациентов, у которых были лабораторные значения, измеренные в течение 30 дней после введения лекарства, по сравнению с записями пациентов, которые никогда не получали лекарства. Мы проверили различия на уровне группы с помощью непараметрического критерия суммы рангов Вилкоксона.Результаты были подтверждены с использованием электронных медицинских записей Медицинского центра Колумбийского университета, где мы использовали те же критерии для отбора пациентов и выполнили тест суммы рангов Вилкоксона для групповых различий.
Визуализация
Графики Circos, созданные с использованием пакета circlize R (версия 0.0.7 https://github.com/jokergoo/circlize). Сетевые диаграммы, созданные с использованием Cytoscape 66 и деревьев SPADE, сгенерированных с помощью CytoSPADE 67 . Все остальные графики созданы с использованием статистического пакета R.
Мыши и лекарственное лечение
Самок мышей C57Bl / c в возрасте 6–12 недель были получены из Jackson Laboratories. Мышам вводили внутрибрюшинно 3 раза каждые 12 ч клиохинол, амантадин (оба в дозе 30 мг / кг, Sigma Aldrich) или соответствующий контроль. Уровень и частота дозирования были выбраны на основе предыдущих экспериментов с использованием клиохинола на мышах 47,68 и периодом полувыведения препарата (11–14 ч). Клиохинол растворяли в 8% PEG400 / PBS, нагретом до 37 ° C; амантадин растворяли в PBS.Перед инъекцией растворы несколько раз встряхивали. Мышей умерщвляли для сбора ткани между 2,5 и 3 часами после последней обработки. Кровь брали из хвоста. Для лечения гуанфацином мышам вводили начальную инъекцию 5 мг / кг лекарственного средства или контрольного носителя (PBS) в день 1, после чего следовали две (эксперимент 1) или шесть (эксперименты 2–5) внутрибрюшинные инъекции по 2 мг / кг каждые 12 ч. начиная со дня 2. Мышей умерщвляли для сбора ткани через 12 ч после последней обработки.Все процедуры с животными выполнялись в соответствии с протоколами, утвержденными Комитетом по уходу и использованию животных Института медицины Mount Sinai.
Проточная цитометрия
Клетки брюшной полости собирали промыванием холодным PBS, содержащим 4% FBS. Одноклеточные суспензии костного мозга получали промыванием бедренных костей с последующей фильтрацией через сетчатый фильтр для клеток 100 мкм (BD Biosciences). Эритроциты лизировали в течение 2 мин при комнатной температуре с использованием буфера для лизиса эритроцитов (eBioscience).Образцы окрашивали следующими антителами (все от eBioscience): CD45, конъюгированный с аллофикоцианином-eFluor780 (30-F11), конъюгированный с перидинином хлорофиллом и белком-цианином 5.5 CD11b (M1 / 70), конъюгированный с фикоэритрином Ly6G (RE6-8Cyth5), конъюгированный CD3 (145-2C11), конъюгированный с перидинином хлорофиллом белок-цианин 5.5 CD25 (PC61.5), конъюгированный с флуоресцеином изотиоцианат CD62L (MEL-14), конъюгированный с аллофикоцианином FoxP3 (FJK-16s), eFluor450-конъюгированный CD1 .5), аллофикоцианин-eFluor780-конъюгированный CD8a (53–6.7) и CD44, конъюгированный с аллофикоцианином (клон IM7, BD Pharmingen). DAPI использовался для маркировки мертвых клеток. LSR Fortessa использовалась для сбора образцов, а программное обеспечение FlowJo — для анализа данных.
Выделение РНК и количественная ПЦР
Общую РНК экстрагировали из кусочков клеток легких, печени, селезенки и костного мозга с использованием реагента QIAzol Lysis Reagent (Qiagen) и гликогенового синего (Ambion, Life Technologies) в соответствии с инструкциями производителя. Для синтеза кДНК 2 мкг общей РНК подвергали обратной транскрипции в течение 1 ч при 37 ° C с помощью набора для преобразования РНК в кДНК (Applied Biosystems).Для количественной ПЦР использовали мастер-микс SYBR green qPCR 2 ° (Fermentas, Thermo Scientific) и следующие праймеры: мышиный Actb , прямой, 5′-CTAAGGCCAACCGTGAAAAG-3 ‘и обратный, 5′-ACCAGAGGCATACAGGGACA-3’; мышь Cxcl1 вперед, 5′-GTGTTGCCCTCAGGGCC-3 ‘и обратный, 5′-GCCTCGCGACCATTCTTG-3’; мышь Cxcl2 , прямой, 5′-ACGCCCCCAGGACCC-3 ‘и обратный, 5′-CTTTTTGACCGCCCTTGAGA-3’; мышь Cxcl5 вперед, 5′-CTCGCCATTCATGCGGAT-3 ‘и обратно, 5′-CTTCAGCTAGATGCTGCGGC-3’; мышь Cxcr2 вперед, 5′-CTTTGCCCTGACCTTGCCT-3 ‘и обратный, 5′-GCACAGGGTTGAGCCAAAA-3’; мышь Cxcr4 вперед, 5′-TGGCCTTCATCAGCCTGG-3 ‘и обратный, 5′-TTGGCCTTTGACTGTTGGTG-3’.
Анализ селезенки мыши методом масс-цитометрии (CyTOF)
Для получения суспензии отдельных клеток селезенки переваривали в течение 20 мин при 37 ° C в HBSS, содержащем 8% FBS и 0,2 мг / мл коллагеназы IV (Sigma Aldrich). После фильтрации через сетчатый фильтр для клеток 100 мкм эритроциты лизировали в течение 2 мин при комнатной температуре с буфером для лизиса эритроцитов. Клетки (5 × 10 6 на образец) были окрашены на следующие поверхностные маркеры: 141Pr-Ly6G, 153Eu-PDCA1, 162Dy-Ly6C, 166Er-CD138 (все приготовленные на месте) и 142Nd-CD11c, 147Sm-CD45, 148Nd-CD11b, 149Sm-CD19, 151Eu-CD25, 152Sm-CD3e, 156Gd-Thy1.2, 160Gd-CD62L, 168Er-CD8, 169Tm-TCRb, 170Er-NK1.1, 171Yb-CD44, 172Yb-CD4, 174Yb-MHCII и 176Yb-B220 (все из DVS Sciences). Цисплатин добавляли на последние 5 минут для мечения мертвых клеток, и образцы фиксировали с использованием буфера Fix и Perm (DVS Sciences). Непосредственно перед инъекцией добавляли калибровочные шарики EQ Four Element Calibration и образцы обрабатывали на массовом цитометре CyTOF 2 (DVS Sciences) за три 10-минутных цикла сбора данных. Данные были нормализованы к EQ Beads и файлам, объединенным с помощью программного обеспечения DVS.
Определение, лечение и что это такое
Обзор
Что такое иммунодепрессанты?
Иммунодепрессанты — это лекарства, которые контролируют вашу иммунную систему.
Иммунная система организма помогает бороться с инфекциями, вызывающими болезни. Но иногда иммунная система по ошибке атакует здоровые клетки и ткани. Иммунодепрессанты могут замедлить или остановить этот ответ.
Кому нужны иммунодепрессанты?
Ваш лечащий врач может порекомендовать иммунодепрессанты, если у вас есть:
Какова роль иммунодепрессантов при аутоиммунных заболеваниях?
Когда у вас аутоиммунное заболевание, иммунная система принимает здоровые ткани и клетки за чужеродных захватчиков (например, микробы).Иммунная система по существу поворачивается против тела и атакует его. В зависимости от того, какая часть тела подвергается атаке, эта реакция может привести к разным типам аутоиммунных заболеваний.
Иммунодепрессанты сдерживают иммунную систему, помогая предотвратить повреждение клеток и воспаление. Эти препараты минимизируют симптомы. Они могут даже вызвать ремиссию аутоиммунного заболевания (у вас нет никаких признаков болезни).
Если у вас одно из этих аутоиммунных заболеваний, вам могут потребоваться иммунодепрессанты:
Какова роль иммунодепрессантов при трансплантации органов?
Иммунодепрессанты помогают людям, перенесшим трансплантацию органов, предотвратить отторжение органов.Ваша иммунная система знает, что новый орган не является частью вашего первоначального тела. Он воспринимает новый орган как угрозу и попытается его уничтожить. Иммунодепрессанты контролируют эту реакцию, защищая новый орган.
Вы получите сильные дозы иммунодепрессантов (индукционных агентов) во время трансплантации органа. Это помогает обеспечить успех трансплантации. Чтобы предотвратить отторжение органов, вам нужно будет принимать иммунодепрессанты (поддерживающие препараты) каждый день на всю жизнь.
Дозировка лекарства может со временем уменьшаться, поскольку ваша иммунная система приспосабливается к новому органу.Медицинские работники обычно назначают преднизон для трансплантации органов.
Какова роль иммунодепрессантов при трансплантации стволовых клеток (костного мозга)?
Трансплантация стволовых клеток может лечить множество заболеваний, в том числе:
Некоторые трансплантаты стволовых клеток используют ваши собственные клетки (аутологичная трансплантация). Людям, которым сделали аутотрансплантат, не нужны иммунодепрессанты.
Аллогенные трансплантаты стволовых клеток заменяют больные клетки в вашем организме здоровыми от донора (так называемого трансплантата).После трансплантации донорские клетки начинают выстраивать новую иммунную систему в вашем организме (хозяине).
Иногда эта новая иммунная система рассматривает ваше тело как чужеродное. Иммунная система может атаковать здоровые ткани и органы. Это приводит к болезни «трансплантат против хозяина» (РТПХ).
Иммунодепрессанты снижают вероятность РТПХ. Вы получаете различные внутривенные (IV) или пероральные иммунодепрессанты в течение нескольких недель или месяцев во время и после трансплантации стволовых клеток. Возможно, вам придется годами принимать иммунодепрессанты, пока новая иммунная система не стабилизируется.
Какие типы иммунодепрессантов?
Кортикостероиды, такие как преднизон, являются одними из наиболее распространенных иммунодепрессантов, которые прописывают медицинские работники. Но есть много видов иммунодепрессантов. Ваш врач выберет лекарство (или комбинацию иммунодепрессантов) в зависимости от вашего конкретного состояния и симптомов.
Вы можете получать иммунодепрессанты в виде таблеток или жидкости, внутривенно или в виде инъекции (инъекции). Типы иммунодепрессантов включают:
- Биологические препараты, такие как адалимумаб (Humira®) и инфликсимаб (Remicade®).
- Ингибиторы кальциневрина, такие как такролимус (Энварсус XR® или Протопик) и циклоспорин (Генграф®, Неорал® или Сандиммун®).
- Кортикостероиды (преднизон).
- Ингибиторы инозинмонофосфатдегидрогеназы (IMDH), такие как микофенолятмофетил (CellCept®).
- Ингибиторы киназы Янус, такие как тофацитиниб (Xeljanz®).
- Механическая мишень ингибиторов рапамицина (mTOR), таких как сиролимус (Rapamune®).
- Моноклональные антитела, такие как базиликсимаб (Simulect®).
Риски / преимущества
Каковы возможные побочные эффекты иммунодепрессантов?
Иммунодепрессанты могут оказывать сильное воздействие на организм. Ваш лечащий врач назначит регулярные анализы крови, чтобы убедиться, что уровень лекарств не слишком высок. Высокие дозы могут вызвать серьезные побочные эффекты.
Побочные эффекты зависят от типа иммунодепрессанта. Эти препараты могут вызывать:
Каковы потенциальные риски или осложнения иммунодепрессантов?
Подавленная иммунная система с трудом борется с инфекциями. У вас повышенный риск развития:
Когда звонить доктору
Когда мне следует позвонить своему врачу?
Вы должны позвонить своему врачу, если у вас возникли проблемы:
дополнительные детали
Какое последующее наблюдение мне потребуется при приеме иммунодепрессантов?
Вы будете чаще сдавать анализы крови, чтобы отслеживать эффективность лекарств и побочные эффекты.Ваш лечащий врач может увеличить или уменьшить дозировку в зависимости от симптомов и побочных эффектов.
Люди с аутоиммунными заболеваниями и после трансплантации органов часто принимают эти лекарства пожизненно. Реципиенты трансплантата стволовых клеток могут прекратить прием препаратов после прохождения риска РТПХ.
Как мне принимать иммунодепрессанты?
Иммунодепрессанты обладают мощным действием. Важно следовать указаниям вашего лечащего врача. Вы должны принимать прописанное лекарство ежедневно, желательно в одно и то же время каждый день.
Пропуск приема лекарства на один день может вызвать обострение аутоиммунного заболевания (возвращение или ухудшение симптомов). Для реципиентов пропущенная доза может подвергнуть вас риску отторжения органа или осложнений РТПХ.

