Можно ли мочить манту — Лайфхакер
Многие считают, будто вода, попавшая на место пробы Манту, может повлиять на реакцию организма. Папула (уплотнение, которое появляется в зоне укола) увеличится в размерах, и результат теста посчитают положительным — то есть припишут вам туберкулёз.
Это заблуждение. Хотя купаться, сделав пробу Манту, в некоторых случаях действительно не стоит.
Что такое проба Манту
Так называют диагностический укол в предплечье, который помогает установить, есть ли в вашем организме туберкулёзная инфекция. Методику этого внутрикожного теста в 1912 году разработал французский врач Шарль Манту — и он же подарил пробе своё имя. Второе её название — туберкулиновая.
Работает манту так. В кожу тонкой иголкой вводится вещество туберкулин. Оно является белковой производной бактерий M. tuberculosis (они же — палочка Коха) — тех, что вызывают туберкулёз. Сам по себе туберкулин абсолютно безопасен, в нём нет ни следа живых бактерий. Но есть их узнаваемые части.
Если ваш организм уже сталкивался с туберкулёзом, он отреагирует на пробу Манту кожной реакцией — появлением заметного красного уплотнения в районе укола.
Иммунная система зафиксирует знакомые кусочки M. tuberculosis и отправит в атакованную, как ей кажется, туберкулёзом зону Т‑лимфоциты. Основное назначение этих клеток — уничтожать опасных «вторженцев». Там, где Т‑лимфоциты особенно активны, возникают воспаление и отёк.
Когда врач видит такую реакцию на месте туберкулиновой пробы, он понимает, что организм знаком с туберкулёзом. Возможно, вы однажды контактировали с тем, кто болел, и теперь опасная инфекция дремлет в вашем теле. Медики в таких случаях говорят, что туберкулёз находится в латентной (скрытой) форме. Но его всё равно надо лечить.
А вот если отёка нет — размеры папулы не превышают 15 миллиметров , вы здоровы.
Сейчас читают 🔥
Можно ли мочить манту
Да. Как понятно из назначения пробы, иммунитет реагирует на признаки палочки Коха, а не на воду.
Как понятно из назначения пробы, иммунитет реагирует на признаки палочки Коха, а не на воду.
К тому же туберкулин вводится в кожу. При обычном купании вода так глубоко проникнуть не может. А значит, точно не повлияет на результат теста.
В медицинских рекомендациях авторитетных организаций — положим, американских Центров по контролю и профилактике заболеваний (CDC) — нет никаких ограничений по поводу купания после пробы Манту. А некоторые медсервисы и вовсе напоминают, что телу необходима гигиена. «Вы можете вымыть и аккуратно высушить руку», — сообщает Департамент здравоохранения штата Миннесота (США).
Почему много лет говорили, что мочить манту нельзя
Во время купания кожа не только намокает. Кто‑то яростно трёт её мочалкой. Другие слишком энергично вытираются грубыми полотенцами.
Такие действия могут повредить место укола и вызвать раздражение — а значит, есть риск, что проба Манту даст ложноположительный результат. Чтобы этого не случилось, во время водных процедур надо быть аккуратнее.
Мочить можно, нельзя расчёсывать. Теребить нельзя, тереть мочалкой .
Ирина Васильева
главный внештатный фтизиатр Минздрава, в комментарии информационному агентству ТАСС
Итак, принимать душ, купаться в ванне и даже плавать в бассейне или открытом водоёме — на здоровье. Главное — обойтись без мочалок. Чтобы убрать влагу, бережно промокните кожу мягким полотенцем или салфеткой.
А вот если без массажа купание для вас немыслимо, место инъекции действительно лучше не мочить. Потерпите три дня, чтобы удостовериться, что вы здоровы.
Читайте также 💉🚿🦠
что будет, изменится ли результат?
Для чего делать ДСТ и какие побочные эффекты
«Диаскинтест» на туберкулез позволит выявить присутствие в крови патогенных организмов, которые провоцируют развитие этого опасного заболевания. В отличие от рентгена и прочих инструментальных методов диагностики, такой способ считается самым безвредным, поскольку исключает облучение.
Вероятность возникновения аллергии или побочных эффектов при проведении пробы «Диаскинтест» сведена к минимуму.
В некоторых случаях инъекция может вызывать такие проявления:
- головную боль;
- незначительные колебания температуры тела;
- сонливость и слабость.
Хотя вакцина считается практически безвредной и разрешена для введения в период вынашивания плода, а также в детском и пожилом возрасте, существует ряд противопоказаний.
К ним относят следующие состояния:
- эпилепсию;
- заболевания инфекционного происхождения;
- простуды, сопровождающиеся повышением температуры, насморком и кашлем;
- некоторые хронические нарушения в период обострений;
- дерматологические проблемы;
- склонность к аллергии.
Внимание! Ещё одним противопоказанием к проведению теста считается действие иных вакцин. Интервал между прививками должен составлять не меньше 30 суток.
Можно ли мочить руку водой при пробе Диаскинтест на туберкулез
«Диаскинтест» стал широко применяться относительно недавно, и многие далекие от медицины обыватели не знают, что разрешено и запрещено делать в первые сутки после вакцинации. В частности, пациенты интересуются, через какое время можно мочить руку водой.
В частности, пациенты интересуются, через какое время можно мочить руку водой.
Беречь место инъекции от влаги нужно на протяжении 3 дней, после чего проводится оценка результата. Впоследствии можно принимать гигиенические процедуры в обычном режиме.
Если на место укола случайно попало небольшое количество воды, это не особенно исказит результат. В таких ситуациях стоит осторожно, не растирая, промокнуть капли сухим полотенцем.
Важно! Если в течение трех суток после введения вакцины место прививки было случайно намочено, при проверке результатов стоит сообщить об этом врачу. Не исключено, что под воздействием влаги тест может выдать ложный положительный результат.
Можно ли мочить руку
Проверку теста проводят на 3 сутки после введения препарата. Чтобы результат был максимально корректным, следует придерживаться мер предосторожности:
- Можно мыться при Диаскинтесте, если после введения препарата прошло 72 часа. Если проверка пробы не проводилась, любые водные процедуры следует проводить осторожно, чтобы не мочить прививку.

- На 3 дня откажитесь от похода в бассейн. Хлорированная вода может спровоцировать аллергическую реакцию. Рекомендуется ограничить посещение бани и сауны – горячий влажный воздух также может повлиять на результат теста.
- Полностью отказываться от гигиенических процедур не обязательно. Не следует только мочить водой место инъекции в течение 48-72 часов после проведения теста. Можно мыться после Диаскинтеста в ванной или душе, но купаться в открытых водоемах не рекомендуется.
- Не закрывать место укола – от раздражения кожи может возникнуть нежелательная реакция. Если нет возможности принять удобную позу, чтобы никак не намочить пробу в душе, следует аккуратно промокнуть место введения теста сухой тканью.
Важная информация: Что такое папула пробы Манту и как измеряют покраснение
Сколько нельзя мочить пробу, следует уточнить у медработника. Тест проверяют не ранее 48 и не позднее 72 часов после введения.
Что будет, если намочить
Если на пробу попадет вода, нужно промокнуть руку сухим полотенцем или марлей. Если область укола намочили простой водой, это не приведет к искажению результатов. Нельзя подвергать место инъекции на руке воздействию озерной, речной или морской воды. В этом случае может понадобиться проведение повторного теста.
Если область укола намочили простой водой, это не приведет к искажению результатов. Нельзя подвергать место инъекции на руке воздействию озерной, речной или морской воды. В этом случае может понадобиться проведение повторного теста.
Через сколько можно есть сладкое, и какие продукты исключить из рациона
Проведение ДСТ не требует особенных ограничений в питании, можно есть сладкое и привычные продукты. Но при этом стоит несколько ограничить потребление шоколада, цитрусовых и орехов, а также красных сортов яблок.
Если пациент склонен к аллергическим реакциям, в это время ему нельзя употреблять продукты, способные вызвать такие негативные проявления. Часто именно невоздержанность в еде и становится причиной образования гематом и покраснений на месте укола, что приводит к неверному толкованию при оценке теста.
На заметку. Перед проведением «Диаскинтеста» аллергикам специалисты советуют принимать антигистаминные препараты на протяжении 5 – 7 суток до ведения вакцины.
Однако не стоит назначать их самостоятельно, лучше проконсультироваться с врачом, который пропишет наиболее подходящее средство.
Что будет если намочить место?
Если намочить руку при диаскинтесте, конечно, ничего страшного не произойдет, но повлиять на правдивость полученных результатов это может.
В воде могут находиться различные элементы, и даже палочка Коха. Поэтому, мочить руку после диаскинтеста не рекомендуется. Если по неаккуратности произошло попадание воды на место укола и появилось покраснение или папула, целесообразно провести повторную пробу.
Иногда возможно заражение места, куда попала вода (при условии, что она была грязной). В таком случае придется заниматься еще и дополнительно лечением раны, а после снова делать диаскинтест, так как увидеть реакцию на туберкулин будет нереально.
Кроме того, тем людям, которые склонны к аллергическим реакциям и имеют чувствительную кожу также нежелательно мочить руку, куда вводилась вакцина. Что произойдет после этого, остается только гадать.
Что произойдет после этого, остается только гадать.
Можно ли мочить диаскинтест на туберкулез через три дня и более? Да, если на руку взглянул врач и занес увиденные результаты в амбулаторную карту.
Но, стоит заметить, что в большинстве случаев намокание диаскинтеста не вызывала никакой реакции. Если человек не инфицирован, то и вода не мешала показать тесту достоверные результаты. Воздержание от купания – это мера, которая позволит обезопасить человека и предупредить возможные нежелательные последствия.
Что делать, если на улице лето и ребенок пришел домой перепачканный? В таком случае мама должна помыть свое чадо так, чтобы место диаскинтеста не намокло. Вода не должна затронуть руку. Возможно придется аккуратно замотать предплечье, чтобы ничего туда не попало. Сильное и длительное передавливание категорически запрещено.
Правила поведения после прививки
Корректность результата тестирования на туберкулез во многом зависит от поведения пациента в течение 3 суток после вакцинации.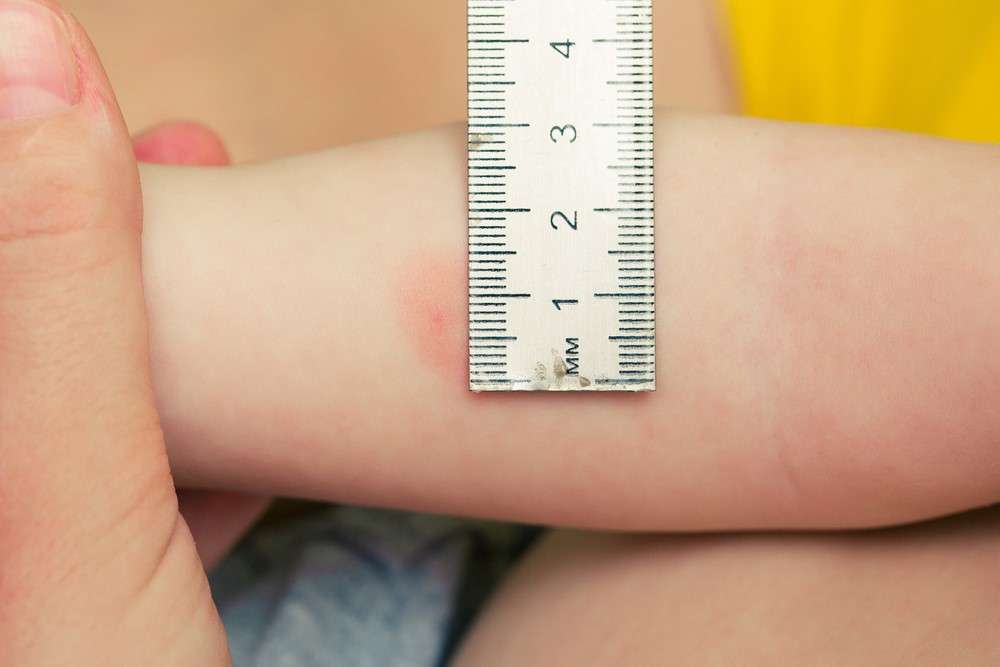
Запрет налагается на проведение следующих процедур и манипуляций:
- мытье места инъекции;
- посещение бань и саун;
- купание в бассейне и открытых водоемах;
- расчесывание укола;
- обработку прививки антисептическими растворами спреями или мазями;
- длительное нахождение под солнечными лучами;
- физические нагрузки и прочие занятия, приводящие к повышенному потоотделению;
- прогулки на улице при температуре воздуха ниже 0.
На заметку. Алкогольные напитки не влияют на результаты «Диаскинтеста», поэтому запрет на них не налагается. Но следует знать, что спиртное может привести к возникновению побочных эффектов, которые проявляются повышением температуры, головной болью и скачками давления.
Оценка результатов диаскинтеста
Оценивать реакцию на «Диаскинтест» можно через 48 – 72 часа после проведения вакцинации. Результаты проверки, сделанной раньше или позже обозначенного времени, будут некорректными.
Отрицательной считается реакция, когда папула на месте укола не видна или не превышает 2 мм, а также отсутствуют отёки, гематомы и покраснения.
Результат расценивается как сомнительный, если на месте укола образовалась небольшая язвочка. В этом случае назначают дополнительные диагностические мероприятия для исключения или подтверждения наличия в организме палочек Коха.
Положительными называют реакции, при которых на месте инъекции образуется папула от 0,5 до 1 см.
При этом результат классифицируют по степени выраженности:
- слабый — до 0,5 см;
- умеренный — до 0,9 см;
- ярко выраженный — больше 1 см.
Если размеры образования на месте укола достигают 15 мм и в нем присутствуют клетки крови и лимфы, это состояние называют гиперергической реакцией. Причиной такого явления может стать лимфаденит, но для подтверждения потребуется провести повторную вакцинацию.
Сделать «Диаскинтест» ещё раз можно будет только через 2 месяца.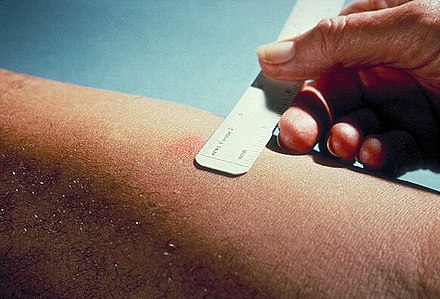 Иначе тестирование выдаст некорректный результат, который окажется бесполезным при постановке диагноза.
Иначе тестирование выдаст некорректный результат, который окажется бесполезным при постановке диагноза.
Отличия Диаскинтеста и Манту
Манту, как и «Диаскинтест», помогает определить присутствие возбудителей туберкулеза в составе крови. Принцип действия этих вакцин одинаков, но последняя является наиболее усовершенствованным способом диагностики и, к тому же, вызывает побочные эффекты и аллергическую реакцию значительно реже.
Еще одним отличием «Диаскинтеста» является то, что он выдаёт положительный результат только при наличии болезнетворных бактерий в крови в настоящий момент. Он способен распознать их даже в случаях, когда они ещё неактивны, и могут нанести урон организму в будущем.
Проба Манту выдаст положительный результат даже в случаях, когда палочки Коха в настоящий момент не обнаружены, но паразитировали в крови ранее, при этом неважно, сколько времени прошло.
Помимо того, «Диаскинтест» не выдает реакции на последствия вакцины БЦЖ, тогда как при введении пробы Манту человеку, которому была проведена такая прививка, не исключен ложный положительный результат.
Из вышесказанного можно заключить, что «Диаскинтест» является не только более современным способом диагностики, но и превосходит Манту по точности. Кроме того, этот препарат считается практически безопасным, тогда как вакцина, использующаяся с незапамятных времён, способна вызывать ряд побочных проявлений, а также провоцирует аллергические реакции разной степени выраженности.
Что такое диаскинтест?
Реакция манту, которая многие годы позволяла выявить инфицированных детей и вовремя их пролечить, чтобы инфекция не развивалась и не распространялась, очень часто вызывала ложно положительную реакцию из-за вакцинации БЦЖ, которую обязательно проводили в роддоме и позже, при отсутствии защиты из-за истощения пула антител к вакцине (проявлялась отрицательной реакцией на манту) делают ревакцинацию детям в школе. Положительный ответ на Манту сразу после вакцинации это норма.
Вместо пробы Манту появился Диаскинтест, реакция на который будет положительной только в случае инфицирования Mycobacterium tuberculosis, тогда как вакцинация БЦЖ проводится ослабленным штаммом Mycobacterium bovis (коровий туберкулез).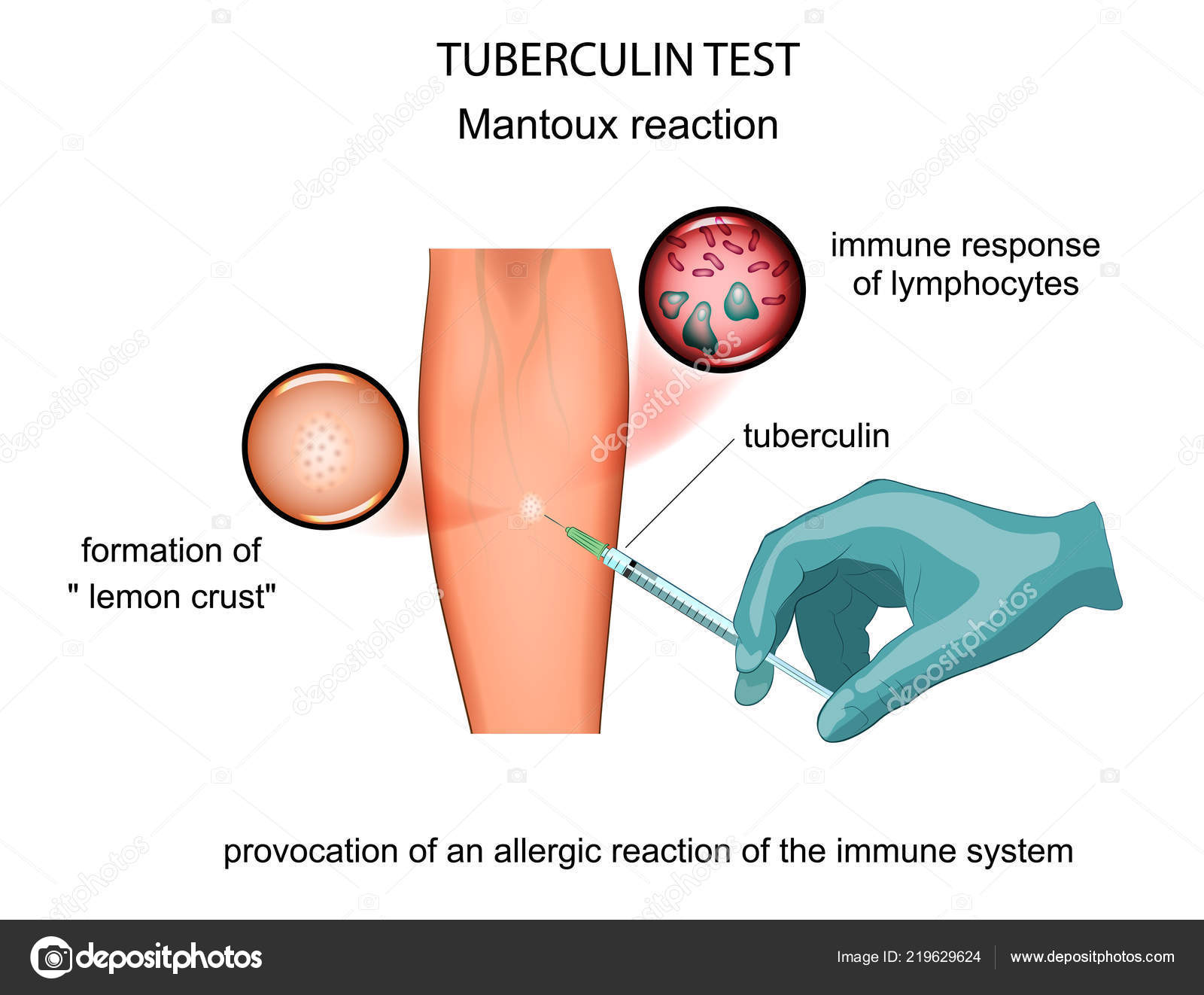
В ответ на строго внутрикожную инъекцию аллергена может возникнуть клеточная реакция на антиген, которая проявляется в виде инфильтрата или покраснения на месте введения. Это гиперчувствительность замедленного типа, которая не может не появиться, если в организме есть активный туберкулезный процесс. Т.е., если организм в настоящий момент борется с микобактерией туберкулеза, то он покажет это, отреагировав на диаскинтест. Если реакция сохраняется через 72 часа, то значит кожный тест положителен.
почему нельзя мочить манту: как оценить результат пробы
На чтение 8 мин Просмотров 3.3к. Опубликовано
Проба Манту – процедура, направленная на выявление туберкулезной инфекции в организме. В профилактических целях прививку делают, преимущественно, детям, чтобы выявить зараженных. На достоверность результатов пробы влияет множество факторов, в особенности воздействие жидкости на место инъекции. Следует рассмотреть, почему нельзя мочить манту и как это влияет на результаты диагностики.
Следует рассмотреть, почему нельзя мочить манту и как это влияет на результаты диагностики.
Можно ли мочить манту
Изначально врачи категорически запрещали мочить место инъекции. Это объясняется тем, что попадание жидкости провоцирует интенсивную кожную реакцию, из-за которой результат прививки манту будет недостоверным.
Сейчас большинство медиков склоняются к единому мнению о том, что нельзя мочить прививку только в первый день. Для проведения пробы используют усовершенствованные препараты с туберкулином, результативность которых меньше зависит от внешних факторов. Некоторые врачи и вовсе утверждают о том, что можно мочить руку даже в первые сутки после процедуры.
Что представляет собой проба манту
Чтобы выяснить, можно ли мочить пробу манту, следует выяснить принцип действия этого метода диагностики.
Процедура состоит из двух этапов:
- Инъекция. Под кожу вводят препарат с туберкулином. Туберкулин – это препарат, содержащий небольшое количество бактерий, вызывающих туберкулез.
 Обычно это палочки Коха. Эти микроорганизмы недееспособны, поэтому не могут инфицировать пациента и спровоцировать болезнь.
Обычно это палочки Коха. Эти микроорганизмы недееспособны, поэтому не могут инфицировать пациента и спровоцировать болезнь. - Интерпретация результатов. После введения туберкулина под кожу образуется небольшая папула, а вокруг нее отмечается покраснение кожи. Интенсивная реакция кожи после контакта с палочкой Коха указывает на то, что в организме уже присутствует туберкулезная инфекция, то есть пациент заражен. Если кожная реакция выражена слабо и покраснения практически нет – это свидетельствует об отсутствии бактерий.
На месте введения туберкулина иногда возникает небольшая гематома
На размер папулы в месте инъекции и на площадь покраснения вокруг влияет множество факторов. Поэтому не всегда процедура дает достоверные результаты.
Размеры пробы манту
Результаты реакции интерпретирует врач. Самостоятельно сравнивать показатели не рекомендуется, чтобы исключить ошибочный диагноз. Показатели нормы отличаются в зависимости от возраста пациента.
| Возраста пациента | Размер папулы в месте инъекции (мм) | Размер покраснения вокруг инъекции | ||
| Нормальная реакция (мм) | Сомнительная реакция (мм) | Высокая вероятность заражения (мм) | ||
| 1 год | 6-10 | 5-15 | 16 | От 17 |
| 2 года | Не важно | 5-15 | 14-16 | 16-22 |
| 3-5 лет | Не важно | 5-8 | 14-18 | 18-28 (От 12, если проба поставлена впервые) |
| 6-7 лет | Не важно | От 1 до 4 | 5 | 6и больше |
| 8-9 лет | 3-6 | От 10 до 16 | 17-18 | Больше 18 |
| 10-12 лет | 3-4 | От 5 до 6 | 7-8 | Больше 8 |
| 13-14 лет | Не важно | 2-4 | От 4 | 18-20 |
| 15-18 лет | Не важно | 3-6 | 7-9 | 9и более |
| У взрослых | Не важно | До 5 | 5-14 | 15 и более |
Взрослым реакцию манту проводят крайне редко.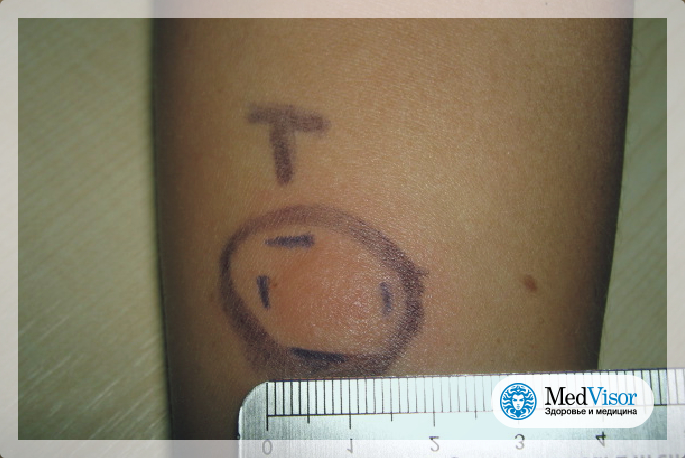 Такой метод диагностики используют, преимущественно, для детей. От 18 лет целесообразно проводить флюорографию.
Такой метод диагностики используют, преимущественно, для детей. От 18 лет целесообразно проводить флюорографию.
Можно ли купаться и принимать душ
Сама по себе жидкость не влияет на реакцию манту. Туберкулин вводят по кожу, где он не контактирует с водой. Иная ситуация обстоит в случае, если в место инъекции проникает загрязненная жидкость. В укол может попасть инфекция, которая отразится на результатах процедуры, а в некоторых случаях может привести к появлению язвы или гнойника на руке.
При попадании бактерий манту воспаляется с первого дня
Врачи не запрещают купаться и принимать душ, так как манту можно мочить. Но вода во время гигиенических процедур не должна быть горячей. Не следует посещать парные и бани, так как это может усилить кожную реакцию.
Сколько дней нельзя мочить место укола взрослому и ребенку
Правила гигиены после манту одинаковы для любого возраста. Не рекомендуется мочить прививку в первые сутки. В этот период место инъекции особо чувствительно, поэтому манту нельзя подвергать контакту с горячей водой, источникам загрязнения.
Важно знать! Еще одна причина запрета в том, что при контакте с жидкостью в месте укола появляется зуд. Прививку категорически запрещено чесать, однако ребенок может сделать это неосознанно.
На второй день можно без сомнений отправляться в душевую или принять ванную. Главное – это не расчесать прививку во время обтирания полотенцем.
Что будет если случайно намочить манту
Не стоит ожидать каких-либо сильно выраженных негативных явлений. В большинстве случаев прививка на контакт с водой никак не реагирует.
Ранка от укола затягивается в течение 2-3 часов
Побочные реакции возможны только в редких случаях, при наличии индивидуальных факторов или предрасположенности к аллергическим реакциям.
Последствия попадания воды в первый день
Наибольшую опасность представляет контакт с водой в первые 4 часа после инъекции. Туберкулин, введенный под кожу, не успел рассосаться с кровью. Вода вымывает его, в результате чего диагностику можно считать недостоверной.
Посетить душ можно уже через 6-8 часов после прививки. Место инъекции в этот момент затягивается и риск вымывания туберкулинового препарата исключен.
Если намочили во второй день
Контакт с водой на 2 день не отразится на состоянии манту. Напротив, врачи осторожно мыть прививку, чтобы предотвратить попадание патогенных микроорганизмов. Это особенно актуально для малышей, так как дети во время активных игр занести инфекцию.
Попадание воды не приводит к аллергическим реакциям
В редких случаях в детском возрасте на второй день развивается аллергия. Она сопровождается сильным покраснением вокруг инъекции, уплотнением папулы, умеренным болевым синдромом. Однако это происходит не из-за попадания воды, а по другим причинам.
Среди них:
- попадание инфекции под кожу;
- наличие острых или хронических заболеваний;
- гельминтоз;
- одновременный прием некоторых медикаментов;
- врожденная гиперчувствительность кожи.
Перечисленные факторы являются противопоказаниями для проведения манту.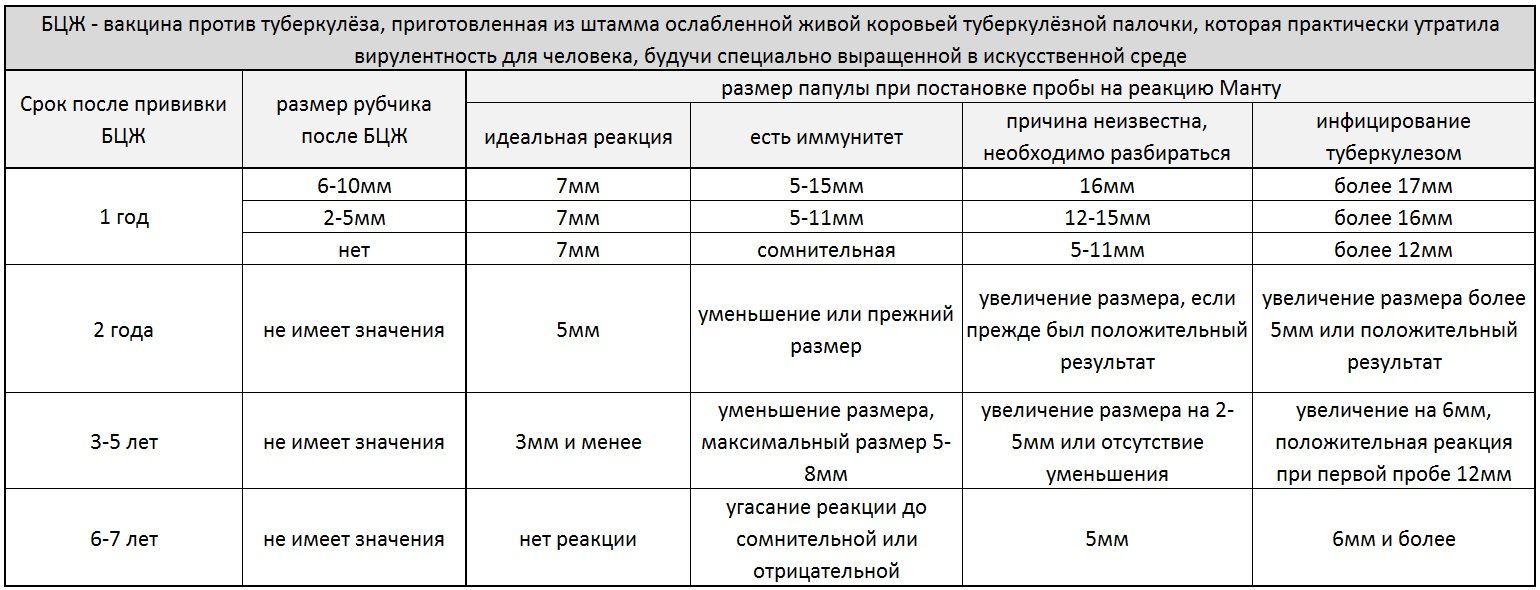 Аллергическая реакция ошибочно расценивают как положительный результат.
Аллергическая реакция ошибочно расценивают как положительный результат.
Можно ли мочить на третий день
Через 3 дня после прививки проверяют результат. В этот период пробу можно мочить, это никак не отразиться на результате туберкулинодиагностики.
После замеров и интерпретации результатов все ограничения снимают
Не рекомендуется расчесывать манту, так как риск попадания инфекции сохраняется. Обычно на третий день зуд полностью проходит.
Нужно ли ограничивать место инъекции от попадания воды
Намеренно закрывать папулу, чтобы предотвратить контакт с жидкостью, не следует. Некоторые думают, что это обеспечит достоверный результат. На самом деле это нет.
Причины:
- Место инъекции должно иметь доступ к кислороду. Тогда кожа в месте введения инъекции заживет быстрее.
- Повязки препятствуют полноценному кровоснабжению в месте прививки. Это негативно влияет на состояние кожных покровов.
- Повязки и прочие защитные средства способствуют размножению патогенных микроорганизмов.
 Увеличивается риск заражения ранки.
Увеличивается риск заражения ранки.
Категорически запрещено закрывать прививку воздухонепроницаемым материалом
Чтобы защитить прививку от намокания, достаточно не подставлять руку под проточную воду. Ограничивать место инъекции другим способ не рекомендуется.
Стоит ли заклеивать обычным пластырем
Заклеивать манту пластырем нельзя. Клейкое вещество проникает под кожу и влияет на реакцию сосудов. Пластырь может стать источником инфекции. К тому же он не защищает от воды должным образом, и часто оказывается бесполезным.
Другие факторы которые могут повлиять на результат манту
Выяснив, можно ли мочить манту, следует рассмотреть что еще влияет на достоверность туберкулиновой пробы. Факторов много, поэтому при интерпретации результатов врач изучает анамнез пациента.
На результаты влияют:
- употребление в пищу цитрусовых, кондитерских изделий, спиртосодержащих продуктов;
- повышенная чувствительность кожи к инъекциям;
- недавно перенесенная ветрянка;
- аллергия на отдельные продукты;
- врожденные аутоиммунные заболевания;
- некоторые препараты;
- проведенная вакцинация бцж и других заболеваний;
- переохлаждение или перегрев тела;
- ожоги в месте инъекции.

Если результат диагностики положительный – это не означает что у ребенка туберкулез. Назначают дополнительное обследование для подтверждения диагноза и последующее лечение.
Общие рекомендации после манту
После прививки рекомендуется скорректировать рацион ребенка. Необходимо исключить продукты, на которые у пациента может быть аллергия. Рацион щадящий, чтобы не перегружать пищеварительную систему.
Посетить ванну или душ следует перед сдачей анализа
Важно знать! После манту не рекомендуется носить плотно прилегающую одежду. Иначе папулу можно случайно расчесать.
Врачи советуют отказаться от чрезмерных нагрузок в первые 2 суток после инъекции. Исключают активные игры, занятия спортом и другие виды физической активности.
Почему всегда говорили, что мочить манту нельзя
Туберкулиновую пробу в СССР с использовали 70х годов XX века. До этого применяли пробу Пирке. Это тест, при котором туберкулин наносили на поврежденную кожу. Мочить место категорически запрещалось, иначе раствор смоется.
Манту вводят под кожу. Поэтому вода не наносит прививке никакого вреда.
Мнение Комаровского
По мнению доктора Комаровского, манту по праву считают самым эффективным методом диагностики туберкулеза в раннем возрасте. Мочить пробу не запрещено, но преднамеренно обливать ее водой не нужно.
Для ребенка с манту опасность представляет инфекция, которая может попасть в ранку после инъекции. Этот риск можно исключить, если соблюдать личную гигиену и не расчесывать прививку.
Чего нельзя делать ни в коем случае
Есть ряд обязательных ограничений, которые обязательны после пробы. Иначе результат диагностики будет ошибочным.
После манту категорически запрещено:
- заклеивать пуговку;
- чесать место укола;
- обрабатывать прививку спиртосодержащими антисептиками;
- давить на папулу;
- допускать попадание грязи;
- подвергать кожу перегреву, переохлаждению.

Покраснение кожи может быть вызвано индивидуальной реакцией организма на препарат
При возникновении аллергических реакций нельзя лечить ребенка самостоятельно. Необходимо обратиться за медицинской помощью.
Итог
Проба Манту – основной метод диагностики туберкулеза в детском возрасте. Ранее считалось, что место инъекции запрещено мочить водой. На самом деле, если прививка намокнет, это не отразится на результатах диагностики. Несмотря на это, есть ряд ограничений, которые должен соблюдать каждый пациент после проведения пробы.
Очень важный есть вопрос: «Нужен вам туберкулёз?»
Очень важный есть вопрос: «Нужен вам туберкулёз?»
Туберкулез — это инфекционная болезнь, вызываемая микобактерией туберкулеза. Наиболее часто поражаются при этом заболевании органы дыхания, лимфатические узлы, мочеполовая система, кости, суставы.
Особой формой болезни у детей является туберкулезная интоксикация, когда не выявляется какого-то определенного очага воспаления.
Микобактерии туберкулеза самые устойчивые к воздействию окружающей среды:
- в уличной пыли они сохраняются до 10 дней,
- на страницах книг — до 3 месяцев,
- в воде — до 5 месяцев,
- под влиянием солнечного света туберкулезные палочки погибают лишь через 90 минут.
Основной источник инфекции — больной туберкулезом:
— при кашле, чихании или отхаркивании люди с легочным туберкулезом выделяют в воздух бактерии туберкулеза;
— для инфицирования человеку достаточно вдохнуть лишь незначительное количество таких бактерий.
Однако инфицирование организма бактериями далеко не всегда приводит к болезни, это зависит от состояния иммунитета.
Туберкулёз у детей имеет ряд характерных особенностей: протекает более тяжело, чем у взрослых и протекает со множеством осложнений.
Детская иммунная система окончательно не сформирована, её активность снижена, и потому, сразу отграничить очаг инфекции она не способна.
У детей до 2-х лет сразу после заражения возможно массивное распространение инфекции: милиарный туберкулез, туберкулезный менингит, туберкулезный сепсис и др.
У детей постарше иммунная система успевает локализовать инфекцию на уровне легких, поэтому у них чаще развивается туберкулез лёгких.
При неосложненном туберкулезе лёгких основные симптомы болезни:
- кашель (более 3 недель),
- длительное повышение температуры,
- утомляемость,
- снижение внимания, отставание в учебе,
- потеря аппетита и похудание.
Для милиарного туберкулеза или туберкулезного менингита характерны более выраженные симптомы интоксикации:
- нарушение сознания,
- высокое повышение температуры,
- признаки раздражения мозговых оболочек,
- одышка.
Симптомы туберкулеза легких у ребенка по ошибке могут быть приняты за симптомы обычной простуды, ОРЗ или бронхита. Для того чтобы заподозрить туберкулез следует обратить внимание на длительность кашля и температуры, а также на общее состояние ребенка (для туберкулеза характерно длительное присутствие кашля и температуры).
Для того чтобы заподозрить туберкулез следует обратить внимание на длительность кашля и температуры, а также на общее состояние ребенка (для туберкулеза характерно длительное присутствие кашля и температуры).
Как защитить своего ребенка от заболевания туберкулезом?
- Прежде всего – это вакцинация БЦЖ. Такую прививку малыши получают еще в родильном доме на 3-7 сутки жизни.
- Флюорографическое обследование окруженияребенка (мамы, папы, бабушки, дедушки и др.), проживающих вместе в одной квартире.
- Для ранней диагностики туберкулеза ежегодно всем детям в возрасте от 1 года до 7 лет включительно проводится проба Манту,а с 8 до 17 лет Диаскин-тест.
| ВОПРОС | ОТВЕТ |
|
Зачем нужна флюорография?
|
Флюорография является одним из основных методов выявления туберкулеза.
Проведение флюорографических осмотров населения обеспечивает раннее выявление туберкулеза и резкое снижение запущенных и распространенных форм туберкулеза. Флюорографические обследования проводятся на стационарных флюорографах, установленных в поликлиниках или на передвижных флюорографических установках.
|
|
Почему раньше флюорографию требовалось проходить 1 раз в 2 года, а теперь нужно 1 раз в год?
| Периодичность прохождения профилактических медицинских осмотров населения от 15 лет и старше (рентгенофлюорографические осмотры населения 1 раз в год) регламентирована требованиями санитарных правил СП 3.1.2.3114-13 «Профилактика туберкулеза» в связи с высоким показателем заболеваемости туберкулезом по г. Екатеринбургу (более 60 случаев на 100 тыс. населения). |
|
Вредно ли облучение, полученное от флюорографии?
|
Эффективная доза облучения зависит от марки и чувствительности флюорографического аппарата.
Конкретную дозу можно узнать при прохождении флюорографического осмотра у врача-рентгенолога.
В соответствии с нормативными документами техническое состояние ФЛГ аппаратов подлежит регулярному контролю.
Существуют противопоказания для проведения флюорографии: возраст (дети до 15 лет), беременность, ряд заболеваний, при которых все обследования согласуются с лечащим врачом.
|
|
Где можно пройти флюорографию и сколько это стоит?
|
Флюорографию можно пройти в поликлинике по месту жительства бесплатно при наличии паспорта и медицинского полиса.
Флюорографическое обследование проводится без посещения врача.
|
|
Почему взрослые проходят флюорографию, а детям ставят Манту?
|
Рентгеновское обследование детям до 15 лет проводится строго по медицинским показаниям.
С целью раннего выявления туберкулеза у детей до 7 лет включительно проводится ежегодная туберкулинодиагностика путем постановки пробы Манту.
|
|
Зачем нужно ставить пробу Манту?
|
Проба Манту проводится в плановом порядке детям с целью выявления первичного инфицирования туберкулезом. Данная проба не является прививкой, а только аллергопробой. Это позволяет диагностировать случаи заболевания туберкулезом на ранних стадиях, когда ещё нет патологических изменений в легочной ткани.
|
| Можно ли мочить место постановки пробы Манту? |
После постановки ребенку пробы Манту, в процедурном кабинете Вам дают рекомендации не мочить руку в течении 72 часов.
Эта рекомендуется для того, чтобы при определении результатов получить достоверную картину проведенного исследования.
|
| Что такое Диаскин-тест? |
Диаскинтест — это внутрикожный диагностический тест на туберкулез. Его относят к экспресс-методам диагностики туберкулеза.
Данный тест не является прививкой, а только аллергопробой для диагностики туберкулеза и проводится для выявления клеточного иммунного ответа на специфические раздражители. Обладает высокой чувствительностью при определении вероятной инфекции туберкулеза, в том числе в начальной (скрытой) стадии. Техника постановки и учет результатов данного теста идентичны пробе Манту. Диаскинтест используется в возрастной группе от 8 до 17 лет, у детей групп риска, что позволяет уменьшить число случаев позднего выявления туберкулеза.
|
|
Ребенку в школе/детском саду проводили туберкулинодиагностику (Манту или Диаскин -тест), сказали, что у нас положительная реакция.
Что это значит?
|
Положительная реакция на внутрикожную пробу с туберкулином (проба Манту или Диаскин-тест) возможна при первичном инфицировании организма микобактерией туберкулеза.
Дети с выявленной положительной реакцией направляются на консультацию к фтизиатру в противотуберкулезный диспансер для исключения диагноза «Туберкулез».
|
| Туберкулез – приговор? | Нет!Своевременное выявление туберкулеза на ранних стадиях, постановка больного на диспансерный учет и проведение адекватного и полного лечения дают положительный прогноз. |
Чтобы обезопасить себя и своих близких от туберкулезной инфекции, необходимо помнить о соблюдении ряда правил:
- Вовремя прививаться вакциной БЦЖ;
- Ежегодно проходить флюорографическое обследование;
- Следить за регулярностью и сбалансированностью режима питания, давать организму ежедневные адекватные физические нагрузки, отказавшись по возможности от вредных привычек.

Врач-эпидемиолог
Бызова Наталья Алексеевна
зачем нас пугали в детстве и почему этот запрет не имеет смысла
Доктор Комаровский о пробе Манту
Иногда пробу Манту, в народе именуемую «пуговкой» ошибочно считают прививкой. А когда мамам кто-то доходчиво объясняет, то, что укололи в школе, садике или в процедурном кабинете отпрыску в ручку, является не вакциной, а тестом, пробой, то возникает масса вопросов. Известный детский врач Евгений Комаровский рассказывает, что собой представляет Манту и зачем такой укол делают.
Что это такое
Туберкулиновая проба является методом диагностики, тестом на наличие в организме микроба, вызывающего туберкулез, – туберкулезной палочки. Для этих целей ребенку вводят подкожно специальный препарат, который имеет в своей основе микросреду обитания возбудителя болезни – туберкулин. Затем специалисты оценивают реакцию организма на введенное вещество. Дело в том, что люди, страдающие туберкулезом, инфицированные, и те, кто здоров, диаметрально противоположно реагируют на туберкулин. Реакция эта схожа с проявлениями аллергии: если в человеке есть микроб-возбудитель туберкулеза, туберкулин вызывает определенный неадекватный аллергический (иммунный) ответ, если палочки-возбудителя у ребенка нет, ничего не происходит.
Реакция эта схожа с проявлениями аллергии: если в человеке есть микроб-возбудитель туберкулеза, туберкулин вызывает определенный неадекватный аллергический (иммунный) ответ, если палочки-возбудителя у ребенка нет, ничего не происходит.
Более подробно и основательно все вопросы на тему манту детям расскажет доктор Комаровский в следующем видео.
На сегодняшний день проба Манту во всем мире считается эффективным методом диагностики. Альтернативные способы выяснить, болен ли ребенок туберкулезом, тоже существуют, но их мало. Одна из современных проб – «Диаскинтест» еще только внедряется. В России препарат зарегистрирован и сертифицирован совершенно официально. Его диагностическое действие основано на выделении некоторых специфических белков-антигенов, которые чувствительны только к агрессивному возбудителю туберкулеза. Если обычная проба Манту может дать реакцию на компоненты вакцины БЦЖ, то «Диаскинтест» дает положительную реакцию исключительно на микробов, которые являются болезнетворными. С этой точки зрения, новый тест более совершенен. Если он отрицательный — болезни нет, если положительный – болезнь есть.
Зачем это делать
Прививку, направленную на то, чтобы у ребенка выработался противотуберкулезный иммунитет, делают еще в роддоме. Она называется БЦЖ. Однако несмотря на вакцинацию, ребенок может заразиться туберкулезом, хотя вакцина существенно снижает эту вероятность. Это связано с постепенным уменьшением антител к туберкулезной палочке. Если у малыша вообще не выработался иммунитет после первой прививки, ему делают повторную — перед школой, в возрасте 7 лет.
В нашем окружении всегда есть кто-то, кто является носителем туберкулезной палочки, с такими людьми мы сталкиваемся в транспорте, в магазине, на улице, ведь политика российского государства не предусматривает жесткой изоляции людей с таким диагнозом от общества.
Проводить пробу Манту нужно раз в год, начиная с момента, когда ребенку исполнится 1 год. Если проба дает отрицательный результат, это трактуется, как то, что иммунитет к туберкулезной палочке после роддомовской вакцины не сформировался, и таким малышам доктор вправе рекомендовать проведение туберкулинового теста не один, а 2 раза в год, чтобы не «прозевать» заболевание.
Делать пробы по существующим правилам нужно в разные руки. Если в этом году ребенку сделали в левую, то через год нужно делать в правую. Место для введения туберкулина всегда одинаковое — внутренняя поверхность предплечья, средняя его треть. Если вы увидели, что проба сделана в другую треть предплечья, на верный результат можно не рассчитывать.
Правила проведения пробы
Как и перед вакцинацией, перед пробой Манту, примерно за месяц, следует убедиться, что малыш чувствует себя хорошо. Он должен быть здоров, у него не должно наблюдаться никаких острых заболеваний и проявлений аллергии. Если у ребенка повышена температура, лучше перенести дату проведения пробы на более поздний срок.
Нельзя делать пробу, если у ребенка имеются кожные заболевания, особенно в период обострения, если у него в анамнезе имеются диагнозы «Бронхиальная астма» или «Ревматизм», а также если в детском коллективе, который посещает чадо, на данный момент объявлен карантин. Все это — строгие противопоказания.
После любой очередной календарной прививки проводить пробу Манту следует не раньше, чем через месяц. Также более 30 дней должно пройти после болезни. Если правильно подготовиться к диагностической пробе, то результаты с наименьшей вероятностью будут ложными или ошибочными.
Можно ли купаться
Часто можно услышать мнение, что ребенка после проведенной пробы Манту нельзя купать 3—4 дня. Евгений Комаровский утверждает, что это не так, и мыться совершенно не противопоказано, мочить место введения туберкулина можно. Но ряд ограничений и запретов в отношении той самой «пуговки» все-таки имеется:
- Место введения туберкулина нельзя интенсивно чесать и тереть (в том числе и мочалкой).
- Место укола категорически запрещено смазывать антисептиками, йодом, а также мазями.
- На пробу Манту нельзя наклеивать пластырь, повязывать бинт, делать компрессы и примочки.
- Нельзя на ребенка надевать одежду с длинными рукавами не по погоде, так как выделение пота и трение ткани о место пробы могут вызвать выраженноположительную ошибочную реакцию.
Результаты пробы
Проводить оценку реакции организма на туберкулин должен квалифицированный медицинский работник. Однако мамам обычно не терпится самостоятельно разобраться в тонкостях диагностики. Их желание вполне объяснимо и понятно, говорит Евгений Комаровский. Специально для мам и пап он объясняет, о чем же может поведать реакция Манту.
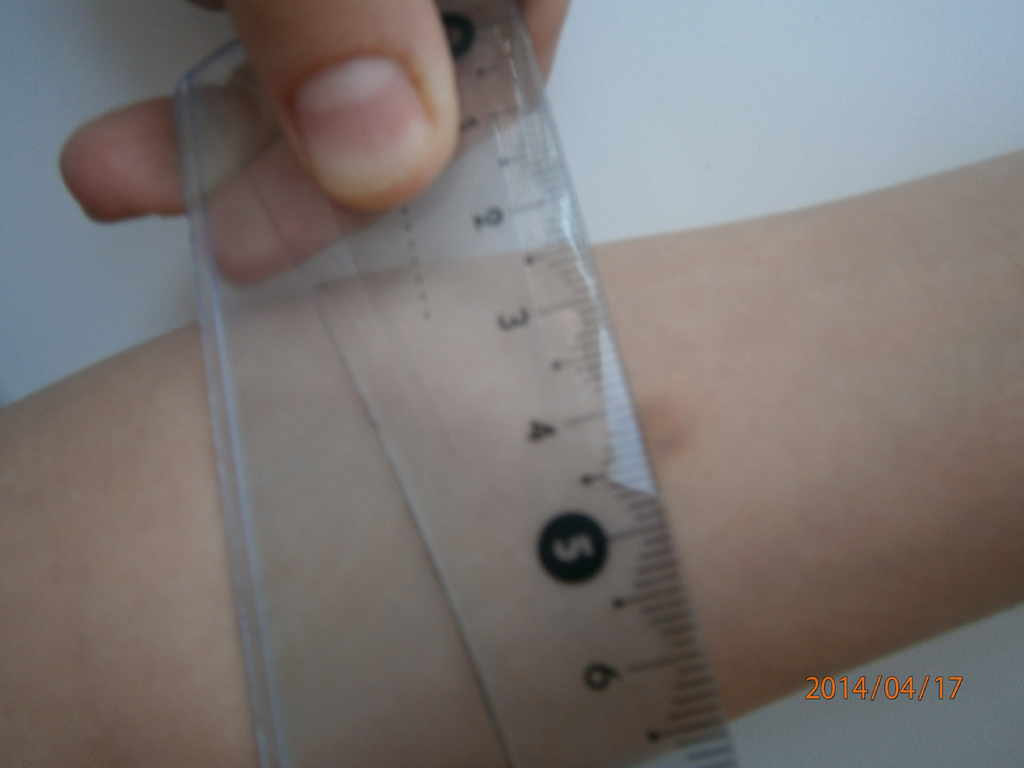
Учет проводят через 72 часа после проведения пробы. Поэтому наиболее удобный день для проведения диагностики — пятница, в большинстве российских поликлиник именно этот день выбран, чтобы у врача была возможность ровно через 72 часа (в понедельник) оценить результат. Место введения туберкулина за это время меняется. Иногда наблюдается покраснение (гиперемия). Часто наблюдается некоторая припухлость, увеличение в размерах, уплотнение в месте введения препарата, Его называют – папула. Медработник измеряет не покраснение, а увеличенную папулу, для этого обязательно используют прозрачную линейку.
Реакция может быть такой:
- Отрицательная. Если какие-либо покраснения, увеличения в районе укола отсутствуют.
- Сомнительная, спорная. Если имеется покраснение (гиперемия) или папула размером не более 2-4 мм. В этой ситуации доктор, оценив общее состояние ребенка и посмотрев его медицинскую карту, может как приравнять результат к отрицательному, так и назначить дополнительные диагностические исследования.
- Положительная. Слабовыраженный результат определяется, если размер папулы от 5 до 9 мм. Средневыраженный результат – папула имеет размеры от 10 до 14 мм. Выраженный результат— папула в поперечнике более 15 -16 мм.
- Чрезмерная. Размер папулы при таком результате всегда более 17 мм. Кроме этого наблюдается общая реакция организма — увеличение лимфатических узлов, появление язвочек на коже, признаки воспалительного процесса в самой папуле. Такой результат в высокой долей вероятности может говорить о развивающемся туберкулезе.
Тревожные результаты
Иногда родители сталкиваются с такой ситуацией, когда проба, ранее всегда бывшая отрицательной, преобразуется в положительную (а прививки БЦЖ не было). В медицине это явление получило название «вираж туберкулиновой пробы». Если он произошел, это может означать, что произошло инфицирование ребенка туберкулезной палочкой. Чаду будет назначена консультация врача-фтизиатра, понадобится сделать рентген легких и пройти дополнительные исследования, после чего ребенку будет назначено лечение.
Заражение опасным заболеванием можно заподозрить и в том случае, если проба Манту после положительного результата (после прививки БЦЖ), постепенно ежегодно уменьшалась, а потом вдруг резко выросла (была 5 мм, стала 9 мм). Такие изменения размеров папулы – тоже основание для проведения дополнительного обследования и назначения лечения при необходимости.
Если на протяжении 4-5 лет проба Манту остается выраженной (более 12 мм при поперечном измерении), это тоже может говорить о развитии туберкулеза легких.
Если родители отказываются от пробы
В последнее время появляется масса непрофессиональной и недостоверной информации о вреде пробы Манту. Так, в интернете по социальным сетям «гуляют» страшные рассказы о токсичности этой диагностической пробы из-за содержащегося в ней фенола. Поэтому число родителей, которые отказываются делать своим детям пробы, возросло в разы. Евгений Комаровский утверждает, что введение туберкулина ни в коей мере не представляет для ребенка никакой опасности.
Фенол в качестве консерванта действительно содержится в препарате, который вводят внутрикожно, но его количество очень мало (примерно столько же содержится в 5-6 мл. мочи). Кстати, фенол является естественным для организма человека веществом, он, как продукт распада определенных соединений, выделяется с мочой. Чтобы ребенок оказался подвержен токсичному влиянию туберкулина ему нужно за сутки ввести около тысячи доз!
Советы
Очень часто у родителей возникает вопрос, надо ли давать перед тестом ребенку антигистаминные препараты. Евгений Комаровский утверждает, что делать этого нельзя. Поскольку основная задача пробы Манту — увидеть, есть ли аллергическая реакция на туберкулин, антигистаминные средства могут помешать это сделать.
Понятия единая «норма» при проведении туберкулиновой пробы у детей не существует.
- Доктор Комаровский
- Реакция
- Диаскинтест
медицинский обозреватель, специалист по психосоматике, мама 4х детей
Можно ли мочить пробу Манту?
Ежегодно детям начиная с 12 месяцев, делается проба Манту. Это диагностическое мероприятие позволяет определить, болен ли ребенок туберкулезом. У медицинского персонала не хватает времени, чтобы объяснить правила ухода за местом инъекции. Поэтому родители часто интересуются, можно ли мочить Манту. Стоит подробнее разобраться в данном вопросе.
Что представляет собой реакция Манту?
Проба Манту относится к распространенным методам ранней диагностики туберкулеза. Обследование предполагает введение в среднюю часть предплечья с внутренней стороны туберкулина внутрикожно. Инъекцию делают одноразовым шприцем с тонкой иголкой с косым срезом. После введения диагностического препарата на месте укола появляется небольшое уплотнение, похожее на пуговицу.
Важно! Реакцию Манту делают детям каждый год с 12 месяцев и до 14-летнего возраста.
Оценку результатов пробы проводят спустя 3 суток с помощью линейки. Размер папулы заносят в медицинскую карту ребенка. Нормой считается, если диаметр пуговки не превышает 4 мм. Папула на месте инъекции аномально больших размеров (5-16 мм) возникает, если пациент имел контакт с микобактериями Бовис, которые вызывают туберкулез. В подобных случаях детей направляют на консультацию к фтизиатру для проведения углубленной диагностики.
Можно ли мочить место укола?
Некоторые врачи утверждают, что нельзя мочить Манту, ведь это приведет к получению ложноположительного результата. Однако подобный запрет является необоснованным. Проба Манту предполагает внутрикожное введение туберкулина, поэтому контакт воды с препаратом возможен только при попадании жидкости внутрь кожи. Для этого потребуется сделать инъекцию. Исключительно в данном случае возможна аллергическая реакция.
Но почему врачи поголовно запрещают мочить место укола? Это связано с историей методов диагностики туберкулеза. В начале семидесятых реакцию организма на микобактерии Бовис отслеживали с помощью накожных проб: проба Пирке или Коха. Эти методы заключались в помещении раствора диагностического препарата на кожу, где впоследствии делались тонкие насечки. Результаты такой пробы действительно могли измениться, если человек имел контакт с водой, которая способна вымыть аллерген из царапин.
Важно! Если ребенок случайно намочил руку, где поставлена реакция Манту, то не следует паниковать. Достаточно просто вытереть намокшее место салфеткой или дать воде высохнуть.
Что будет, если намочить пробу
Итак, можно ли мочить Манту? Кратковременный контакт места введения туберкулина с водой не способен исказить результаты обследования. Поэтому ребенка можно купать в любой день после постановки пробы. Однако лучше ограничить контакт места укола и воды, которая вероятно способна спровоцировать аллергическую реакцию.
Почему нельзя мочить Манту? В редких случаях после водных процедур папула способна резко увеличиваться в размере. Необходимо сразу уведомить об этом лечащего врача. В данном случае туберкулиновая проба будет неинформативной, придется провести обследование повторно.
Сколько нельзя мочить Манту? Врачи утверждают, что не стоит контактировать с жидкостью сразу после инъекции препарата. Ведь вода может проникнуть в кожу посредством не затянувшегося прокола. Поэтому рекомендуют исключить любые контакты с влагой в течение часа после посещения процедурного кабинета. Этого времени вполне достаточно для того, чтобы место укола забилось свернувшейся кровью.
Что категорически нельзя делать?
Изменить результаты пробы Манту могут следующие факторы:
- Перегрев ребенка и длительное пребывание в душном помещении с повышенной влажностью. Поэтому на 3 суток рекомендуют отказаться от посещения сауны, бассейна, бани. Ведь тепло и влага способствуют расширению пор кожи, поэтому внутрь дермы может проникнуть вода;
- Механические повреждения кожи. Важно постоянно следить за ребенком после инъекции туберкулина, чтобы предотвратить попытки расчесывания, растирания или выдавливания «пуговки». Это может привести к проникновению воды, развитию ложноположительной реакции;
- Наложение повязок, заклеивание места укола лейкопластырем. Это приводит к накоплению в месте укола пота и кожного жира, искажает результаты;
- Шерстяные вещи или одежда из грубых тканей способны привести к развитию раздражения;
- Профилактические прививки. Вакцинация способна исказить иммунологический статус, поэтому рекомендуют делать пробу до иммунизации или спустя 30 дней;
- Йод, спирт, перекись водорода и прочие антисептики, крема, мыло, гель для душа способны спровоцировать возникновение аллергической реакции;
- На время проведения туберкулиновой пробы рекомендуют отказаться от продуктов, которые могут спровоцировать возникновение аллергии: рыба, цитрусовые, шоколад, пряности, сладкое;
- Купание в общественных водоемах, которое может спровоцировать присоединение вторичной инфекции.
Кому нельзя делать Манту?
Туберкулиновая проба, как и любые диагностические мероприятия, имеет определенные противопоказания. Врачи рекомендуют отказаться от обследования в таких случаях:
- Наличие проблем с кожей бактериального или аллергического генеза;
- Период усиления хронических патологий;
- Острые инфекционные заболевания;
- Наличие бронхиальной астмы в анамнезе;
- Активное течение ревматизма;
- Наличие судорожной готовности или эпилептические припадки в анамнезе.
Некоторые из перечисленных ограничений являются относительными, поэтому пробу проводят после улучшения самочувствия пациента.
Туберкулиновая проба не способна защитить человека от заражения туберкулезом. Она относится к диагностическим мероприятиям, которые определяют наличие туберкулезной инфекции. Можно ли мочить Манту? Попадание влаги на место укола не способно исказить результаты диагностики. Однако для собственного спокойствия рекомендуют исключить любые контакты с водой в течение 3 суток после инъекции туберкулина.
Манту запрещают мыть не просто так
Не все врачи сразу объясняют, почему нельзя мочить манту. При этом, в большинстве случаев они стремятся запретить водные процедуры. Связана ли необходимость дополнительного обследования в тубдиспансере с намоченной коже сразу после манту? Или все-таки врачи оперируются другими понятиями? — Данная волнует многих родителей, так что стоит разобраться в ней поглубже.
Мыться с «пуговкой» или нет?
Полемику в деталях по данному вопросу можно вести достаточно долго. Вначале стоит вспомнить, имеет ли манту право называться прививкой. Стоит со всей определенностью сказать, что манту отнюдь не относится к прививкам, так как во время нее не вносится достаточно малое количество живых (которые должны быть угнетенными и весьма ослабленными) или мертвых клеток возбудителей различных болезней с важной целью — запустить иммунитет на выработку антител. Так что манту следует называть всего лишь диагностической инъекцией.
Вот теперь можно перейти к главному. Разрешается ли мочить прививку? В подавляющем большинстве медицинских учреждений делать подобное категорически запрещают.
Если вспомнить о прививках АКДС (вакцина, которая включает компоненты коклюша, дифтерии и столбняка), то всегда упоминают о большом стрессе не только для больного, но и для здорового организма. Малыши переживают подобные прививки еще тяжелее, чем взрослые. Попытки скомбинировать купание и прививку могут изменить активность занесенных («привитых») болезнетворных вирусов.
Также в открытую ранку возможно попадание вредных веществ из загрязненного водопровода. Реакция на подобные эксперименты может быть непредсказуемой. По этой причине настоятельно рекомендуют хотя бы в первые сутки отказаться от купания и не мочить прививку.
А что же манту? Как уже говорилось выше, ее нельзя отнести к прививкам. Шарль Манту разработал туберкулиновую пробу, называемую в народе «пуговка», для постановки диагноза. Сама по себе она ничего не лечит и даже не может застраховать от серьезного заболевания. Ее основная цель — помочь врачам поставить точный диагноз, а также выявить наличие либо полное отсутствие явно выраженной аллергической реакции на близкий контакт с веществом «туберкулин».
Так почему же запрещается мочить манту? Подобное табу является абсолютно необоснованным. Так как туберкулиновая проба является внутрикожной, то для попадания воды вовнутрь пробы потребуется ввести ее шприцем под давлением. Конечно же, ни один родитель в здравом уме не будет заниматься подобным. Во всех остальных случаях аллергическая реакция на воду произойти не может.
По какой же причине практически все практикующие нынче педиатры и медсестры запрещают мочить пробу? Ответ скрывается в истории. Приблизительно до конца шестидесятых и, в редких случаях, в начале семидесятых годов вместо внутрикожной пробы Манту использовали накожные пробы (например, пробу Пирке или пробу Коха).
На кожу сверху капали раствор препарата, а затем через него делали тонкие насечки (царапины). Естественно, что именно эта проба действительно могла очень сильно отреагировать на купание. В первые 24 часа контакт с водой мог вымыть аллерген из царапин, что делало бессмысленным ожидание правдивой реакции.
В медицине достаточно сложно происходят изменения. Проще продолжать всем запрещать купаться, чем внести в консервативный устой некоторые изменения. Десятки лет стереотипов не прошли даром.
На самом деле, желательно отказаться от механического воздействия на манту. Нельзя ее растирать, замазывать чем-либо, заклеивать лейкопластырем, обрабатывать раствором перекиси или зарисовывать зеленкой. Просто мыться можно, но все же следует отказаться от похода в баню или воздействия мочалкой на данный участок кожи.
Как долго оберегать руку?
Можно отбросить все эти рассуждения в сторону и просто потерпеть некоторое время без купания. Мало ли, вдруг на самом деле вода может проникнуть в подкожный слой. Какой же срок является самым «опасным» для манту? Достаточно подумать о том, через какой срок измеряется папула (пуговка). Обычно говорят придти через 48-72 часа для контроля над ситуацией. Так что трое суток — самое оптимальное время, когда к руке с манту лучше лишний раз не прикасаться и не мочить.
Следует понимать, что даже положительная туберкулиновая проба дает лишь малую часть информации о заболевании. Для выяснения того, насколько распространен туберкулез или где он локализован, понадобится дополнительное обследование. В некоторых случаях выясняется ошибка во время проведения первого теста. Так что рекомендуется отказаться от паники при вынесении «неутешительного вердикта» сразу после изучения одной лишь манту.
О том, можно ли делить на ноль, читайте в нашей следующей статье.
Почему нельзя мочить Манту?
Туберкулез – одно из опаснейших заболеваний. Несмотря на все старания современной медицины, болезнь активно распространяется, угрожая в первую очередь людям с ослабленным иммунитетом, живущим в скученности, имеющим скудное питание. Чтобы избавиться от заболевания, необходимо проходить длительное лечение, при этом важно выявить его на ранних стадиях. Дети относятся к уязвимой категории населения, врачи стремятся проверять их регулярно, проводя аллергологический тест, который носит название реакция Манту. Он позволяет обнаружить факт наличия палочки Коха, являющейся возбудителем туберкулеза, в организме.
Место укола мочить нельзя, об этом врачи предупреждают родителей и самого малыша каждый раз, когда проводится тест. Но почему нельзя допускать попадания воды, и что будет, если влага все же попадет на кожу в месте инъекции? Что еще нельзя делать до того момента, когда произведут замеры участка покраснения? На эти вопросы необходимо дать ответ.
Что будет, если вода попадет на Манту?
Причина, из-за которой нельзя мочить кожу на месте укола, очень проста. Попадание жидкости может привести к разбуханию. Покраснение распространится на значительную поверхность, что даст ложноположительный результат. Придется проходить дополнительные мероприятия для уточнения ситуации и постановки правильного диагноза, что вынудит потратить лишнее время и нервы. Чтобы не сталкиваться с этими и другими проблемами, стоит сделать все возможное, чтобы не мочить место укола до того момента, пока врачи не сделают замеры. Даже руки стоит мыть с осторожностью, под наблюдением родителей.
Как делают тест на туберкулез?
Данную методику проверки на туберкулез ввел французский врач Шарль Манту, она названа в его честь. Тест проводят путем внутрикожной инъекции препарата, это совершенно безопасно для ребенка. Средство представляет собой не живые, а уничтоженные палочки Коха, по сути, это экстракт из них. В антигенном плане он полностью идентичен бактериям, иммунная система человека распознает вещество именно как непосредственных возбудителей туберкулеза. Реакция организма на введенный препарат позволяет провести диагностику, определить, кто из детей болен, а кто здоров. Укол делают в предплечье, во внутреннюю верхнюю часть, затем выжидается период в 3 суток, в течение которого нельзя мочить кожу.
За данный период успевает сработать иммунная система, на месте укола возникает аллергическое проявление в виде красного пятна, которое постепенно рассасывается. Спустя трое суток врачи делают замер результата, отмечая как размеры пятна, так и его яркость. Если в течение этого периода ребенок хоть раз намочил место укола, результат может оказаться недостоверным.
Оценка реакции Манту
Казалось бы, чем меньший размер имеет аллергическое пятно, тем лучше. Но это не совсем верно. Если его нет, либо если диаметр покраснения составляет менее 0.5 мм – значит, отсутствует и защитная реакция. Подобная ситуация означает, что иммунная система ребенка «не знает» о наличии данного возбудителя – это случается, когда малышу не поставили в роддоме прививку БЦЖ, или если ее сделали неправильно. Если пятно имеет больше 5 мм в диаметре, необходима дополнительная консультация и обследование, чтобы выяснить, болен ребенок или нет. Сразу впадать в панику не нужно, поскольку существует целый ряд факторов, способных дать ложноположительный результат. Несмотря на всю информативность этого диагностического мероприятия, в ряде случаев оно может дать неточный результат.
В каких еще случаях результат будет неточным?
Неверный результат может проявиться в случае, когда ребенок перегревался или долго пребывал в душном помещении. Повышенная влажность воздуха, пар сауны или бани, попытка чесать место укола могут изменить результат и дать ложноположительную реакцию. Тоже самое касается попыток давить место укола, выдавливать папулу. Необходимо объяснить это ребенку и наблюдать за ним в течение периода, предшествующего проверке. Большинству малышей достаточно бывает сказать, что при несоблюдении мер, названных врачом, надо будет ставить новый укол.
Опасно ли попадание воды на Манту? Что делать, если это произошло?
Помимо ложноположительного результата, особых опасностей не отмечается. Есть, разве что, риск воспаления, если ребенок будет купаться в открытом водоеме, или на место укола попадет грязная вода – микроорганизмы могут попасть в ранку. Единственное, что необходимо делать, когда ребенок все же намочил область покраснения – промокнуть воду стерильной салфеткой. Дезинфицировать это место нельзя.
Почему нельзя мочить Манту?
Туберкулиновая проба Манту – один из самых распространенных методов диагностики туберкулеза у детей и подростков. Это также тест, который помогает проверить наличие аллергии к антигенам микобактерий туберкулеза до вакцинации против туберкулеза (БЦЖ).
Всем детям делают в школе так называемую реакцию Манту. И при этом медсестра всегда предупреждает: мочить руку нельзя в ближайшие 3 дня, пока врачи не оценят результат пробы. Конечно же, любой запрет интригует и вызывает интерес у малышей и их родителей. Так почему нам говорят, что нельзя мочить Манту?
В чем смысл пробы Манту?
Этот тест достаточно простой: испытуемому вводят 0,1 мл туберкулина (специально созданный фильтрат микобактерии туберкулеза) в центральной части левого переднего предплечья. После инъекции на руке появляется беловатый пористый пузырь, имеющий диаметр 7-9 мм, который исчезает через несколько минут.
Результат теста на туберкулин считывается после 3 дней (72 часов). С помощью специальной высокоточной миллиметровой линейки врач или медсестра замеряет диаметр кожной реакции. Если он больше, чем требует норма, человека направляют в диспансер для дополнительных обследований.
Если вам укололи неправильное количество туберкулина, он введен слишком глубоко или на месте инъекции появилась кровь, тест необходимо повторить в тот же день, на другом месте тела.
В европейских странах после введения туберкулиновой пробы пациенту запрещают:
- закрывать место укола пластырем;
- касаться руками появившегося пузыря;
- выдавливать место укола.
Ни о каких запретах на контакт с водой речь не идет. Мочить Манту запрещают только в постсоветских странах. Почему?
Пережитки старины
До 70-х годов прошлого века в нашей стране для диагностики туберкулеза детям делали накожную пробу Пирке. Суть ее заключалась в следующем: на кожу наносился реагент с туберкулином, эпидермис в этом месте «расцарапывался», через несколько дней можно было оценить результаты. Естественно, накожную пробу ни в коем случае нельзя было мочить, чтобы попросту не смыть действующее вещество.
Позже в арсенале врачей появился более удобный тест, который делался внутрикожно – проба Манту. Ее смыть невозможно, да и результаты исследования интерпретируются более точно. Укол от туберкулиновой пробы, на самом деле, можно мочить водой, ведь действующее вещество «запрятано» в глубинах кожи, куда вода просто не попадает. Но медицинский персонал по старой привычке (или «на всякий случай») продолжал предупреждать деток, чтобы они не мочили место инъекции. Традиции – вещь упертая. Поэтому до сих пор у нас сохранились эти пережитки старины.
Так где же правда?
Врачи, когда советуют не мочить Манту, оберегают пациентов от действий, которые действительно могут помешать правдивости теста.
- Если просто мыть руку, на которой сделана инъекция, это никак не повлияет на результаты пробы. Но если человек решит сходить в баню или сауну, это будет уже неправильно. Под воздействием высоких температур и пара кровообращение становится слишком интенсивным, поэтому организм может дать непредсказуемую реакцию. Все-таки укол – это вмешательство. Поэтому лучше в эти три дня отказаться от бассейнов, поездок к морю и походов в баню.
- Каждая кожа уникальна. У некоторых людей она очень чувствительна. Поэтому туберкулиновую пробу не рекомендуется растирать мочалкой – вдруг организм ответит на это аллергической реакцией или раздражением?
- По этой же причине нельзя наклеивать пластырь на место укола – ведь под ним скопится влага, жир и пот, а они довольно агрессивно действуют на кожу.
- Некоторые детки могут выдавить Манту – это вообще самое плохое, что можно сделать для своей кожи. Реагент неравномерно «расползется» по кожным тканям, что приведет к воспалению, раздражению, а в некоторых случаях – и к нагноению. Не говоря уже о том, что нужно будет делать еще одну туберкулиновую пробу.
Мнение доктора Комаровского (видео):
Итак, мы с вами разобрались, почему врачи любят говорить, что нельзя мочить Манту. Они руководствуются исключительно нашими с вами интересами, и хотят, чтобы тест показал объективный результат.
«Ушла эпоха»: россияне ошеломлены известием о том, что Миндзрав разрешил мочить Манту
Мир больше никогда не будет прежним.
Главный внештатный специалист-фтизиатр Министерства здравоохранения России Ирина Васильева заявила в интервью ТАСС, что пробу Манту (или если по-научному – туберкулинодиагностика, она же реакция Манту, она же проба Пирке)) можно мочить, но нельзя механически повреждать.
Пробу Манту делают детям, чтобы оценить реакцию организма на попадание в него антигена возбудителя туберкулеза.
Оказывается, по словам Васильевой, медработники все эти десятилетия не разрешали мочить место пробы Манту из-за того, что обычно люди вытирают намокшее место полотенцем, а это и есть механическое повреждение.
«Нельзя расчесывать. Теребить нельзя, тереть мочалкой»
«С пробой Манту все не так строго — просто нельзя раздражать кожу», — уточнила Ирина Васильева.
В советской, а затем и российской истории отечественного здравоохранения знание о том, что Манту можно мочить, тщательно скрывалось. «Намочить Манту» — было одним из самых страшных нарушений табу у многих поколений детей в России. Существует даже специальная фраза, характеризующая крайнюю степень подросткового бунтарства — «специально намочить Манту».
Именно поэтому реакцию на новость от Минздрава про Манту можно охарактеризовать как абсолютный шок. «Росбалт Like» сделал подборку комментариев из соцсетей к этому переломному в жизни поколений россиян событию.
«Главный фтизиатр Минздрава разрешил детям мочить пробу Манту»
>Главный фтизиатр Минздрава разрешила мочить пробу Манту
ВСЯ МОЯ ЖИЗНЬ
ЛОЖЬ
МЕНЯ ОБМАНЫВАЛИ ВСЕ ЭТО ВРЕМЯ
сейчас пойду, сделаю манту и НАМОЧУ
Минздрав разрешил мочить Манту! Ну все, теперь нас не остановить. #манту
А вы думали, что в российской медицине не будет новых прорывов? А хрен вы угадали.
– В Минздраве разрешили мочить Манту! pic.twitter.com/lV23rVRosz
Слышали главную новость этого года? Оказывается манту можно мочить! И ничего не будет! ?
“Минздрав разрешил россиянам мочить пробу манту”
Гаврила замочил в сортире
Манту. Министр разрешил.
УРА! Это день наконец то настал. В Минздраве разрешили мочить Манту
С победы Путина не прошло и 5 дней, а Минздрав уже разрешил мочить Манту. Что дальше?
Мочите манту сегодня, завтра этот аттракцион неслыханной щедрости могут и прикрыть
Оттепель, свобода! Не зря выбирали!
в России разрешили мочить манту и трогать журналисток за лобок
Что значит манту мочить можно?
Это что же – все те тысячи смертей были напрасными?!
Мой брат теребил, отец теребил, деды ещё как теребили. И мы обтеребимся
ТЕРЕБИТЬ НЕЛЬЗЯ? Это че за страна такая?!
Стоит отметить, что разоблачение мифа о том, что нельзя мочить место укола для реакции Манту, на официальном уровне недавно сделал и Минздрав Украины. И.о. министра здравоохранения Ульяна Супрун написала в Facebook, что вода на коже никак не может повлиять на пробу Манту, так как инъекция туберкулина вводится внутрикожно, куда вода сама по себе не проникает. «В рекомендациях западных организаций, таких как CDC, нет никаких ограничений на этот счет», — сообщила она. Это заявление было сделано 25 февраля этого года.
Почему десятки лет, и в СССР, а потом и в постсоветский период истории, ни в одной из стран СНГ не был официально разоблачен миф про «намочить Манту» до нынешнего года — неизвестно.
можно ли мочить руку водой и есть сладкое? 8 правил, которые важно соблюдать при проведении пробы на туберкулез
На протяжении более 100 лет одним из надежных способов выявления туберкулеза считалась проба Манту. Но с 2009 года медики начали использовать для этих целей «Диаскинтест». Этот метод позволяет определить наличие палочек Коха в организме тогда, когда болезнь еще не начала заявлять о себе какими-либо характерными симптомами. Рассмотрим детально, что такое «Диаскинтест», и можно ли мочить место укола после введения вакцины.
Для чего делать ДСТ и какие побочные эффекты
«Диаскинтест» на туберкулез позволит выявить присутствие в крови патогенных организмов, которые провоцируют развитие этого опасного заболевания. В отличие от рентгена и прочих инструментальных методов диагностики, такой способ считается самым безвредным, поскольку исключает облучение.
Вероятность возникновения аллергии или побочных эффектов при проведении пробы «Диаскинтест» сведена к минимуму.
В некоторых случаях инъекция может вызывать такие проявления:
- головную боль;
- незначительные колебания температуры тела;
- сонливость и слабость.
Хотя вакцина считается практически безвредной и разрешена для введения в период вынашивания плода, а также в детском и пожилом возрасте, существует ряд противопоказаний.
К ним относят следующие состояния:
- эпилепсию;
- заболевания инфекционного происхождения;
- простуды, сопровождающиеся повышением температуры, насморком и кашлем;
- некоторые хронические нарушения в период обострений;
- дерматологические проблемы;
- склонность к аллергии.
Внимание! Ещё одним противопоказанием к проведению теста считается действие иных вакцин. Интервал между прививками должен составлять не меньше 30 суток.
Можно ли мочить руку водой при пробе Диаскинтест на туберкулез
«Диаскинтест» стал широко применяться относительно недавно, и многие далекие от медицины обыватели не знают, что разрешено и запрещено делать в первые сутки после вакцинации. В частности, пациенты интересуются, через какое время можно мочить руку водой.
Беречь место инъекции от влаги нужно на протяжении 3 дней, после чего проводится оценка результата. Впоследствии можно принимать гигиенические процедуры в обычном режиме.
Если на место укола случайно попало небольшое количество воды, это не особенно исказит результат. В таких ситуациях стоит осторожно, не растирая, промокнуть капли сухим полотенцем.
Важно! Если в течение трех суток после введения вакцины место прививки было случайно намочено, при проверке результатов стоит сообщить об этом врачу. Не исключено, что под воздействием влаги тест может выдать ложный положительный результат.
Через сколько можно есть сладкое, и какие продукты исключить из рациона
Проведение ДСТ не требует особенных ограничений в питании, можно есть сладкое и привычные продукты. Но при этом стоит несколько ограничить потребление шоколада, цитрусовых и орехов, а также красных сортов яблок.
Если пациент склонен к аллергическим реакциям, в это время ему нельзя употреблять продукты, способные вызвать такие негативные проявления. Часто именно невоздержанность в еде и становится причиной образования гематом и покраснений на месте укола, что приводит к неверному толкованию при оценке теста.
На заметку. Перед проведением «Диаскинтеста» аллергикам специалисты советуют принимать антигистаминные препараты на протяжении 5 – 7 суток до ведения вакцины.
Однако не стоит назначать их самостоятельно, лучше проконсультироваться с врачом, который пропишет наиболее подходящее средство.
Правила поведения после прививки
Корректность результата тестирования на туберкулез во многом зависит от поведения пациента в течение 3 суток после вакцинации.
Запрет налагается на проведение следующих процедур и манипуляций:
- мытье места инъекции;
- посещение бань и саун;
- купание в бассейне и открытых водоемах;
- расчесывание укола;
- обработку прививки антисептическими растворами, спреями или мазями;
- длительное нахождение под солнечными лучами;
- физические нагрузки и прочие занятия, приводящие к повышенному потоотделению;
- прогулки на улице при температуре воздуха ниже 0.
На заметку. Алкогольные напитки не влияют на результаты «Диаскинтеста», поэтому запрет на них не налагается. Но следует знать, что спиртное может привести к возникновению побочных эффектов, которые проявляются повышением температуры, головной болью и скачками давления.
Оценка результатов диаскинтеста
Оценивать реакцию на «Диаскинтест» можно через 48 – 72 часа после проведения вакцинации. Результаты проверки, сделанной раньше или позже обозначенного времени, будут некорректными.
Отрицательной считается реакция, когда папула на месте укола не видна или не превышает 2 мм, а также отсутствуют отёки, гематомы и покраснения.
Результат расценивается как сомнительный, если на месте укола образовалась небольшая язвочка. В этом случае назначают дополнительные диагностические мероприятия для исключения или подтверждения наличия в организме палочек Коха.
Положительными называют реакции, при которых на месте инъекции образуется папула от 0,5 до 1 см.
При этом результат классифицируют по степени выраженности:
- слабый — до 0,5 см;
- умеренный — до 0,9 см;
- ярко выраженный — больше 1 см.
Если размеры образования на месте укола достигают 15 мм и в нем присутствуют клетки крови и лимфы, это состояние называют гиперергической реакцией. Причиной такого явления может стать лимфаденит, но для подтверждения потребуется провести повторную вакцинацию.
Сделать «Диаскинтест» ещё раз можно будет только через 2 месяца. Иначе тестирование выдаст некорректный результат, который окажется бесполезным при постановке диагноза.
Отличия Диаскинтеста и Манту
Манту, как и «Диаскинтест», помогает определить присутствие возбудителей туберкулеза в составе крови. Принцип действия этих вакцин одинаков, но последняя является наиболее усовершенствованным способом диагностики и, к тому же, вызывает побочные эффекты и аллергическую реакцию значительно реже.
Еще одним отличием «Диаскинтеста» является то, что он выдаёт положительный результат только при наличии болезнетворных бактерий в крови в настоящий момент. Он способен распознать их даже в случаях, когда они ещё неактивны, и могут нанести урон организму в будущем.
Проба Манту выдаст положительный результат даже в случаях, когда палочки Коха в настоящий момент не обнаружены, но паразитировали в крови ранее, при этом неважно, сколько времени прошло.
Помимо того, «Диаскинтест» не выдает реакции на последствия вакцины БЦЖ, тогда как при введении пробы Манту человеку, которому была проведена такая прививка, не исключен ложный положительный результат.
Из вышесказанного можно заключить, что «Диаскинтест» является не только более современным способом диагностики, но и превосходит Манту по точности. Кроме того, этот препарат считается практически безопасным, тогда как вакцина, использующаяся с незапамятных времён, способна вызывать ряд побочных проявлений, а также провоцирует аллергические реакции разной степени выраженности.
Правда ли, что нельзя мочить Манту?
Вконтакте
Когда нам в школе ставили туберкулиновую пробу (она же реакция Манту), то каждый раз не забывали напомнить: место укола ни в коем случае нельзя мочить. Неужели нас всё это время обманывали?
Существуют две разновидности туберкулинодиагностики: проба Пирке и более известная и современная реакция Манту. Обе нацелены на то, чтобы проверить устойчивость иммунитета к возбудителям туберкулёза, но методика тестов разная. Проба Пирке подразумевает скарификацию — нанесение небольшой царапины на кожу, через которую в организм и вводят туберкулин. При проведении реакции Манту раствор вводят под кожу, а потом просят не мочить это место.
С реакцией Манту связано сразу несколько мифов. Например, с момента введения туберкулина до измерения размера «пуговки» якобы нельзя есть сладкое или принимать противоаллергические препараты. Но, безусловно, самый распространённый — это недопустимость попадания воды на участок кожи, где был сделан укол.
По всей видимости, связано это с тем, что проба Пирке — более устаревшая технология — подразумевала царапание кожи и именно в царапину могла попасть жидкость. Поэтому пациентов и просили не мочить это место. Как отмечает Дик Мензис, исследователь Медицинского центра Университета МакГилла в Канаде, мочить Манту можно уже спустя 15 минут после укола. Внимательным нужно быть уже после того, как вы помыли руки или приняли душ: участок кожи, на котором проведена проба, нельзя тереть, поэтому его стоит аккуратно промокнуть салфеткой или мягким полотенцем.
Зарубежных коллег поддерживают и российские специалисты. В 2018 году главный фтизиатр (то есть специалист по диагностике и лечению туберкулёза) Минздрава России заявила, что попадание на кожу воды не влияет на результат исследования. Анна Васильева сказала: «Намочить можно, потом просто промокнуть и всё. <…> С пробой Манту всё не так строго – просто нельзя раздражать кожу».
Фейк
Что означают наши вердикты?
Почитать по теме:
- https://ru.wikipedia.org/wiki/Туберкулиновая_проба
- https://tass.ru/obschestvo/5059581
- https://meduza.io/cards/v-novostyah-opyat-pishut-chto-probu-mantu-nelzya-mochit-eto-pravda-spoyler-da-mochite-ee-na-zdorovie
Если вы нашли ошибку, пожалуйста, выделите фрагмент текста (до 140 символов) и нажмите Ctrl+Enter.
Интересное по теме: Лженаука
Правда ли, что морковь, улучшающая зрение, — миф, придуманный британцами с целью скрыть использование радара?
Опубликовано 15.05.2021
Павел Солахян
Согласно распространённой информации, история о невероятной пользе моркови для зрения — фейк, появившийся в годы Второй мировой. Во время налётов немецкой авиации британские лётчики использовали передовую для своего времени вещь — бортовые радары, но скрывали этот факт, ссылаясь на уникальные свойства поедаемой ими моркови. Мы проверили, так ли это было.
Правда ли, что исследователь из Стэнфордского университета опроверг необходимость ношения маски?
Опубликовано 26.04.2021
Даниил Федкевич
Противники использования медицинских масок в повседневной жизни утверждают, что недавно к их мнению присоединился учёный из одного из самых авторитетных университетов мира. Мы проверили, так ли это на самом деле.
Правда ли, что нефть образовалась из останков динозавров?
Опубликовано 14.04.2021
Павел Солахян
Нередко пишут о том, что в образовании «чёрного золота» важнейшую роль сыграли продукты разложения древних обитателей нашей планеты — динозавров. Мы проверили, так ли это.
Индурация или эритема диаметром не менее 5 мм по результатам кожной пробы с рекомбинантным слитым белком ESAT6-CFP10 для выявления инфекции M. tuberculosis | BMC Infectious Diseases
Характеристики участников
Всего в исследовании приняли участие 743 пациента с туберкулезом; им было 38,77 ± 14,11 лет, 513 человек (69,04%) были мужчинами, а 118 пациентов имели анамнез или семейный анамнез ТБ. Всего было 1514 здоровых добровольцев в возрасте 45,43 ± 9,57 лет, 398 человек (26.29%) были мужчинами. Среди них 777 добровольцев имели шрамы от вакцинации БЦЖ (были вакцинированы в младенчестве, что было основной политикой здравоохранения в Китае). БЦЖ очень эффективна в профилактике тяжелого туберкулеза у детей, но менее эффективна у взрослых [25,26,27]. Таким образом, здоровые взрослые, вакцинированные БЦЖ в младенчестве, считались в целом здоровым населением без защиты БЦЖ. Для оценки специфичности кожного теста ЭК в популяции вакцинированных БЦЖ 315 здоровых добровольцев были отобраны для вакцинации БЦЖ в соответствии с целью клинического испытания.Остальные характеристики приведены в таблице 1.
Таблица 1 Характеристики зарегистрированных больных ТБ и здоровых добровольцев
Диаметр уплотнения и эритемы после кожной пробы ЭК
У больных ТБ средний диаметр уплотнения составлял 14,23 мм, 22,68 мм и 21,00 мм через 24 часа 48 ч и 72 ч после кожной пробы ЭК, при этом максимальный диаметр составлял 82,50 мм, 96,00 мм и 112,50 мм соответственно. Более того, средний диаметр эритемы составлял 24,72 мм, 37,55 мм и 37 мм.64 мм через 24 часа, 48 часов и 72 часа после кожной пробы ЭК, а максимальный диаметр составлял 108,00 мм, 153,50 мм и 158,50 мм соответственно (рис. 1а).
Рис. 1
Диаметр уплотнения и эритемы после кожной пробы ЭК. a Диаметр уплотнения и эритемы у больных туберкулезом. b Диаметр уплотнения и эритемы у здоровых добровольцев
У здоровых добровольцев средний диаметр уплотнения составлял 0,36 мм и 1,81 мм через 24 и 48 часов после кожной пробы ЭК, в то время как максимальный диаметр составлял 30.50 мм и 60,50 мм соответственно; средний диаметр эритемы составлял 1,23 мм и 3,86 мм через 24 и 48 часов после кожной пробы ЭК, а максимальный диаметр составлял 73,00 мм и 124,00 мм соответственно (рис. 1b).
Диагностическая ценность уплотнения и эритемы после кожной пробы ЭК
Чувствительность измерения уплотнения составила 72,14, 84,25 и 83,78% через 24 часа, 48 часов и 72 часа после кожной пробы ЭК, соответственно; чувствительность была наименьшей через 24 ч (χ 2 = 43,80, P <0.01), при этом статистической разницы между чувствительностью 48 и 72 часов не было (χ 2 = 0,06, P = 0,81). Специфичность измерения уплотнения составила 97,49 и 91,15% через 24 и 48 часов после кожной пробы ЭК, соответственно; специфичность была ниже через 48 ч (χ 2 = 56,81, P <0,01). Значение Каппа составило 0,75 через 48 часов. Последовательность 24 и 48 часов после кожной пробы между уплотнением и клиническим диагнозом была близка к 90% (χ 2 = 0.08, P = 0,78). Остальные результаты показаны в таблице 2.
Таблица 2 Диагностическая оценка уплотнения и эритемы после кожной пробы ЭК
Чувствительность измерения эритемы составила 85,33, 90,85 и 91,08% через 24 часа, 48 часов и 72 часа после кожной пробы ЭК, соответственно; Чувствительность была самой низкой через 24 часа (χ 2 = 16,18, P <0,01), и не было статистической разницы между чувствительностью через 48 и 72 часа (χ 2 = 0.03, P = 0,88). Специфичность измерения эритемы составила 95,38 и 89,83% через 24 и 48 часов после кожной пробы ЭК, соответственно; специфичность была ниже через 48 ч (χ 2 = 34,02, P <0,01). Значения каппа составляли 0,82 через 24 часа и 0,78 через 48 часов. Последовательность через 24 и 48 часов после кожной пробы между эритемой и клиническим диагнозом была более 90%; через 48 часов после кожной пробы консистенция была немного ниже, чем через 24 часа после кожной пробы (χ 2 = 5.06, P = 0,02). Остальные результаты показаны в Таблице 2.
При сравнении согласованности между уплотнением с клиническим диагнозом и эритемой с клиническим диагнозом, через 24 часа после кожной пробы ЭК была выявлена значительная разница (χ 2 = 11,34, P <0,01), и никакой разницы через 48 ч после кожной пробы (χ 2 = 1,99, P = 0,16). Согласованность эритемы с клиническим диагнозом была выше, чем у уплотнения с клиническим диагнозом через 24 часа после кожной пробы, и не было никакой разницы в консистенции между двумя из них через 48 часов после кожной пробы.
Сравнение чувствительности и специфичности между уплотнением и эритемой
У больных ТБ было больше пациентов с положительным ответом на эритему, чем с положительным ответом на уплотнение. Чувствительность при оценке уплотнения и эритемы сравнивали в трех временных точках: P <0,01 (χ 2 24 ч = 38,60, χ 2 48 ч = 14,82, χ 2 72 ч = 17,93) (таблица 3). Эти результаты продемонстрировали, что чувствительность измерения эритемы была значительно выше, чем чувствительность измерения уплотнения.У бактериологически положительных больных ТБ чувствительность измерения эритемы была выше, чем у индурации, P <0,01 (χ 2 24 ч = 20,72, χ 2 48 ч = 11,16, χ 2 72 ч = 16,58) (таблица 3). У бактериологически отрицательных пациентов с ТБ и пациентов с внелегочным ТБ не было различий в чувствительности между измерениями уплотнения и эритемы через 48 и 72 часа после кожной пробы, P ≥ 0.05 (таблица 3).
Таблица 3 Чувствительность и специфичность уплотнения и эритемы после кожного теста ЭК
Среди здоровых добровольцев было больше субъектов с отрицательной реакцией уплотнения, чем с отрицательной реакцией на эритему. Сравнивали специфичность анализа уплотнения и эритемы. Наблюдалась значительная разница через 24 ч после кожной пробы ЭК (χ 2 = 9,83, P <0,01) и отсутствие разницы через 48 ч после кожной пробы ЭК (χ 2 = 1.54, P = 0,22) (таблица 3), из чего следует, что специфичность измерения эритемы была ниже, чем уплотнение через 24 часа после кожной пробы, но не через 48 часов после кожной пробы.
У добровольцев, вакцинированных БЦЖ, специфичность измерения уплотнения и эритемы была> 90%, и специфичность сравнивалась в двух временных точках: P > 0,05 (χ 2 24 ч = 1,79, χ 2 48 ч = 1,01). Это доказало отсутствие разницы в специфичности между уплотнением и эритемой (таблица 3).
Сравнение стойкости уплотнения и эритемы
У больных ТБ CR + (χ 2 = 31,99, P <0,01), значение Каппа и консистенция (χ 2 = 18,36, P <0,01) между уплотнением и эритемой были ниже через 24 часа после кожной пробы, чем через 48 и 72 часа. У бактериологически положительных больных ТБ CR + (χ 2 = 8,62, P = 0,01) и постоянство (χ 2 = 8.19, P = 0,02) между уплотнением и эритемой были ниже через 24 часа после кожной пробы, в то время как значение Каппа было выше через 48 часов после кожной пробы. У пациентов с бактериологически отрицательным ТБ CR + (χ 2 = 27,02, P <0,01), значение Каппа и постоянство (χ 2 = 27,27, P <0,01) были ниже через 24 ч после кожная проба. У пациентов с внелегочным туберкулезом значение Каппа было выше через 48 ч после кожной пробы. У здоровых добровольцев CR + (χ 2 = 30.84, P <0,01) и значение Каппа через 24 часа после кожной пробы были ниже, чем через 48 часов после кожной пробы. Результаты сравнений представлены в таблице 4.
Таблица 4 Сравнение согласованности между уплотнением и эритемой после кожного теста EC
Прежде всего, уплотнение и эритема могут быть использованы для обнаружения M. tuberculosis . Эти данные свидетельствуют о том, что лучшая чувствительность, специфичность и другие диагностические результаты достигаются через 48 часов после проведения кожной пробы.
Сравнение диагностических показателей кожного теста ЭК
Мы выбрали уплотнение, эритему, уплотнение или эритему, уплотнение и эритему в качестве диагностических индикаторов кожного теста ЭК и сравнили диагностические эффекты этих четырех индикаторов у разных типов пациентов. через 48 ч после кожной пробы ЭК.
У разных типов пациентов чувствительность измерения уплотнения или эритемы была самой высокой, чувствительность измерения уплотнения и эритемы была самой низкой, однако у пациентов с внелегочным туберкулезом не было различий в чувствительности четырех показателей.Специфичность измерения уплотнения или эритемы была самой низкой, специфичность измерения уплотнения и эритемы была самой высокой, однако не было никакой разницы в специфичности четырех показателей. У разных испытуемых не было различий в согласованности четырех показателей с клиническим диагнозом. Подробные данные представлены в таблице 5.
Таблица 5 Сравнение четырех диагностических индикаторов кожной пробы ЕС
Синергия между туберкулиновой кожной пробой и пролиферативными Т-клеточными ответами на PPD или клеточные мембранные антигены Mycobacterium tuberculosis для выявления латентной инфекции ТБ в условиях высокого бремени болезни
Abstract
Туберкулиновая кожная проба (ТКП) наиболее широко используется для выявления латентной туберкулезной инфекции (ЛТИ), даже несмотря на то, что данные свидетельствуют о том, что она могла занижать распространенность ЛТИ, особенно в условиях высокого бремени болезни.Мы исследовали, могут ли in vivo (TST) и in vitro (пролиферативные) Т-клеточные ответы на PPD служить дополнительными мерами. Кроме того, мы также исследовали, может ли in vitro Т-клеточный ответ на клеточные мембранные антигены (Mem) Mycobacterium tuberculosis (MTB) служить биомаркером для LTBI. Объектами исследования были 43 медицинских работника (МР), а 9 больных туберкулезом с положительным мазком мокроты служили «контрольными». Чтобы измерить пролиферативные Т-клеточные ответы, 0.1 мл крови (разведенной 1:10) инкубировали (5 дней) с тестируемым или контрольным антигеном. Клетки окрашивали флуоресцентными антителами к поверхностным маркерам Т-клеток (CD3 + / CD4 + / CD8 +) и, после фиксации и пермеабилизации, к маркеру ядерной пролиферации Ki67. Данные были получены на проточном цитометре. Медработники, имевшие интимный контакт с МТБ, показали значительно более высокую положительную реакцию на ТКП (85%), чем остальные (43%), несмотря на их статус вакцинации БЦЖ. Пролиферативные ответы субпопуляций CD4 + и CD8 + Т-клеток были сопоставимы.Шестьдесят семь и 100% TST-отрицательных медицинских работников, соответственно, были положительны в отношении пролиферативного Т-клеточного ответа на PPD и MTBMem. Кумулятивная положительность (TST или in vitro ) составила 86% для PPD и 100% для MTBMem, что указывает на комплементарность двух ответов. Как автономный тест in vitro , MTBMem показал значительно более высокую положительность (95%), чем PPD (67%). Т-клеточные ответы у больных ТБ были «в целом» подавленными, что имело значение для разработки иммунологических тестов на «прогрессирующий» ЛТИ.В целом, эти результаты демонстрируют, что in vivo и in vitro Т-клеточные ответы на PPD являются комплементарными, а in vitro ответ на MTBMem может быть разработан как высокочувствительный биомаркер для LTBI.
Образец цитирования: Арья С., Кумар С.К., Нат А., Капур П., Аггарвал А., Мисра Р. и др. (2018) Синергизм между туберкулиновой кожной пробой и пролиферативными Т-клеточными ответами на PPD или антигены клеточных мембран Mycobacterium tuberculosis для выявления латентной инфекции ТБ в условиях высокого бремени болезни.PLoS ONE 13 (9):
e0204429.
https://doi.org/10.1371/journal.pone.0204429
Редактор: Сейед Этешам Хаснаин, Индийский технологический институт, Дели, ИНДИЯ
Поступила: 26 мая 2018 г .; Одобрена: 9 сентября 2018 г .; Опубликовано: 24 сентября 2018 г.
Авторские права: © 2018 Arya et al. Это статья в открытом доступе, распространяемая в соответствии с условиями лицензии Creative Commons Attribution License, которая разрешает неограниченное использование, распространение и воспроизведение на любом носителе при условии указания автора и источника.
Доступность данных: Все соответствующие данные находятся в документе и его файлах с вспомогательной информацией.
Финансирование: Авторы не получали специального финансирования на эту работу.
Конкурирующие интересы: Авторы заявили, что никаких конкурирующих интересов не существует.
Введение
Подавляющее большинство людей, живущих в странах с высоким бременем туберкулеза (ТБ), имеют скрытую инфекцию ТБ (ЛТИ), определяемую как «состояние стойкого иммунного ответа на Mycobacterium tuberculosis (MTB) без клинических проявлений заболевания» [1 ].Примерно у 10% людей с ЛТИ может развиться активный ТБ в течение 2–5 лет [2]. В 2016 году во всем мире было зарегистрировано 6,3 миллиона новых больных туберкулезом против примерно 10,4 миллиона, что означает, что почти 4 миллиона случаев «пропали» из записей [2]. На одну только Индию приходится четверть пропавших без вести случаев, которые могут выступать в качестве «скрытых» очагов инфекции. Выявление инфекции MTB, предпочтительно на «доклинической» стадии, считается важным для успеха стратегии «Положить конец туберкулезу» [2].
В отсутствие «золотого стандарта» наиболее широко используемым тестом для выявления ЛТИ является «Туберкулиновая кожная проба (ТКП)».Основная критика TST заключается в том, что результаты теста искажены из-за предшествующей вакцинации БЦЖ или контакта с «нетуберкулезными» микобактериями (НТМ). Однако имеющиеся данные говорят об обратном. В метаанализе 24 исследований с участием 240 203 субъектов, положительный результат ТКП был выявлен у <1% субъектов, вакцинированных БЦЖ в младенчестве и прошедших тестирование через 10 лет [3]. В том же метаанализе не было обнаружено, что NTM является существенным фактором, влияющим на TST. В 18 исследованиях с участием 1169105 субъектов ложноположительный результат теста на тест-пробы на НТМ варьировался от 0.От 1 до 2,3%. Следовательно, в таких странах, как Индия, которые следуют политике ВОЗ по вакцинации БЦЖ в младенчестве [2], ТКП ≥10 мм у подростков и взрослых можно рассматривать как надежный индикатор инфекции MTB [4, 5]. Прямое сравнение ТКП с «анализами высвобождения гамма-интерферона (IGRA)» не показало никаких доказательств того, что один тест лучше другого [1]. Фактически, вопреки ожиданиям, некоторые исследования показали, что TST имеет преимущество перед IGRA [6, 7].
Хотя TST и IGRA могут обнаруживать инфекцию MTB с разумной специфичностью, оба, очевидно, не достигают желаемой чувствительности, поскольку они часто не могут выявлять даже бактериологически подтвержденные случаи ТБ [8].Это вызывает озабоченность относительно того, достаточно ли чувствительны эти анализы для выявления ЛТИ. В недавнем исследовании [9] эффективность TST и IGRA оценивалась у более чем 1500 контактов с туберкулезом из Дели. За время наблюдения у 76 контактов развился активный туберкулез. Поразительно, что частота случаев положительных и отрицательных контактов TST или IGRA была сопоставимой, что позволяет предположить, что в обоих тестах могла отсутствовать большая часть пациентов, инфицированных MTB, живущих в районах с высоким бременем болезни.
Учитывая, что циркулирующие Т-клетки могут демонстрировать более широкое фенотипическое разнообразие, чем те, что находятся в коже, были предприняты исследования, чтобы выяснить, будут ли Т-клетки крови TST-отрицательных людей реагировать на PPD.Действительно, PPD может индуцировать пролиферацию Т-клеток у пациентов с ТБ, не отвечающих на ТКП [10]. PPD (и другие антигены MTB) также индуцировали синтез IFN-γ в Т-клетках TST-отрицательных здоровых людей из эндемичных по ТБ районов [11, 12]. Эти сообщения предполагают, что in vivo (TST) и in vitro Т-клеточные ответы на PPD могут дополнять друг друга. Кроме того, полногеномный поиск выявил 82 белка MTB, содержащих иммунодоминантные эпитопы для Т-клеток LTBI-позитивных субъектов [13].Интересно, что ESAT-6 и CFP-10 (ключевые компоненты IGRA) не фигурировали среди тех антигенов, которые в основном состоят из мембранно-ассоциированных белков MTB. Иммунодоминантность белков мембран микобактерий для Т- и В-клеток человека также сообщалась нами [14, 15], а также другими [16, 17].
Продолжающаяся эпидемия туберкулеза вызвана резким увеличением количества уведомлений о случаях заболевания из Индии [2]. Кроме того, недавний отчет IUATLD показывает, что в Индии самый высокий уровень заболеваемости детским туберкулезом [18].Эти данные предполагают, что истинное распространение ЛТИ или «ежегодного риска заражения туберкулезом (ОРТИ)» в Индии может быть намного выше, чем оценки, которые почти полностью основаны на исследованиях ТКП [4, 19]. Примечательно, что в большинстве опросов сообщается об аналогичных показателях положительной реакции на ТКП (~ 50%) в общей популяции и в тесных контактах с туберкулезом [20, 21], даже несмотря на то, что люди в последней категории подвергаются более высокому риску заражения инфекцией [9, 22]. . Наша цель в этом исследовании состояла в том, чтобы изучить, могут ли (а) in vitro и in vivo Т-клеточные ответы на PPD служить дополнительными показателями LTBI и (b) in vitro Т-клеточный ответ на антигены клеточной мембраны MTB можно использовать как чувствительный биомаркер для LTBI.Объектами исследования были медицинские работники (МР) крупной больницы третичного уровня на севере Индии, а «контроль болезни» включал пациентов с туберкулезом с положительным мазком мокроты. В нескольких исследованиях [2], в том числе в Индии [23], сообщается, что медработники подвергаются большему риску заражения MTB-инфекцией, чем население в целом.
Материалы и методы
Настройка исследования
Исследование проводилось в Институте последипломного образования медицинских наук имени Санджая Ганди (SGPGIMS), который представляет собой крупную (более 1000 коек) специализированную медицинскую школу в городе Лакхнау на севере Индии.В DOT-клинике SGPGIMS ежегодно проходят лечение около 300 больных туберкулезом.
Предметы исследования
В состав исследовательской группы вошли 43 медработника (преподаватели, студенты и сотрудники) SGPGIMS (таблица 1 в разделе «Результаты»). Кроме того, 9 пациентов с легочным туберкулезом (3 женщины, 6 мужчин, 23–55 лет) были включены в «контрольную группу». Все пациенты имели активное заболевание с положительными мазками мокроты (от 2+ до 3+) на кислотоустойчивые бациллы (КУБ). Шесть из них не принимали лекарственные препараты, а остальные 3 получали комбинированную терапию в течение <3 недель [2].Ни у одного из испытуемых не было подозрений на инфицирование или положительный результат теста на ВИЧ. Протокол исследования был одобрен Комитетом по этике Института последипломного образования медицинских наук им. Санджая Ганди, и все участники предоставили письменное информированное согласие. Все клинические исследования проводились в соответствии с руководящими принципами «Хельсинкской декларации» [24].
Материалы
Подробная информация о закупленных материалах приведена в разделе «Вспомогательная информация» (текст S1).
Получение антигенов мембран бактериальных клеток
Мембраны МТБ (MTBMem) и E . coli были выделены с использованием ранее описанного протокола [14] с некоторыми модификациями. Вкратце, трехнедельные культуры MTB (на среде Левенштейна-Йенсена) или 24-часовые культуры E . Собирали coli (в бульоне Лурия-Бертани), бактериальные отложения промывали и суспендировали в PBS (0,2 г сырого веса / мл). Лизаты клеток, полученные обработкой ультразвуком (20 мин), центрифугировали (23000 г х 20 мин) для осаждения неразрушенных клеток и остатков клеточной стенки. Супернатанты повторно центрифугировали (150 000 г х 90 мин) для получения мембраны (осадка) и цитозоля (супернатант).Мембраны промывали и восстанавливали PBS. Оценка белков проводилась модифицированным методом Лоури [25], а профили белков определялись с помощью SDS-PAGE (S1 фиг.). Подходящие аликвоты хранили при -80 ° C.
ТСТ
Пять туберкулиновых единиц PPD (0,1 мл) вводили внутрикожно в ладонную часть левого предплечья. Через 48–72 часа максимальный диаметр пальпируемого уплотнения измеряли штангенциркулем [26]. ТКП считалась положительной, если уплотнение составляло 10 мм и более.
Образцы крови
Кровь собирали в пробирки с гепарином натрия стандартной венепункцией. Образцы хранили при комнатной температуре (RT) до использования для настройки анализов (в течение 4 часов после сбора).
Анализ пролиферации Т-клеток
Кровь разбавляли (1:10) в среде RPMI и разливали в 24-луночные культуральные планшеты (1 мл / лунку). В отдельные лунки добавляли среду (отрицательный контроль), PHA (5 мкг, положительный контроль) или тестовые антигены — PPD (5 TU или 0,1 мкг) и MTBMem (5 мкг) и инкубировали в течение 5 дней в инкубаторе CO 2 . .Для некоторых анализов E . Мембрана coli (5 мкг) также использовалась в качестве «отрицательного» контроля. На 5 день клетки обрабатывали ЭДТА (2 мМ, 15 мин), собирали в пробирки для FACS и центрифугировали (400 г х 5 мин). К перемешанным осадкам клеток добавляли заданные количества флуоресцентно меченных антител к поверхностным маркерам Т-клеток (CD3 / CD4 / CD8) и инкубировали (30 мин, RT, в темноте). Эритроциты лизировали лизирующим раствором BD FACS (2 мл / пробирка, 15 мин, RT, в темноте) с последующим центрифугированием.WBC (осадок), промытые PBS, фиксировали (15 мин, RT, в темноте) 2% параформальдегидом. Позже клетки промывали PBS, содержащим 0,05% BSA (PBS-BSA), и повышали проницаемость (15 мин, RT, в темноте) с помощью 0,2% Triton X100. Клетки снова промывали PBS-BSA и инкубировали (45 мин, RT, в темноте) с флуоресцентно-меченными антителами к Ki67 (ядерный белок, сверхэкспрессируемый во время синтеза ДНК) [27]. Наконец, клетки промывали PBS-BSA и ресуспендировали в PBS. Данные о 10 5 клетках в «воротах лимфоцитов» были получены на проточном цитометре FACS Canto-II (BD) и проанализированы с использованием программного обеспечения Flowjo v10.0,7 (Tree Star, США). Отсечка для положительного клеточно-пролиферативного ответа была определена как 0,75% (= среднее + 3 x SD всех ответов на среду RPMI).
Стратегия стробирования изображена на рис. S2. Дополнительные данные по оптимизации метода приведены в файле S1.
Статистический анализ
t-критерий Стьюдента (парный / непарный) был использован для вычисления различий между двумя популяциями, а точный критерий Фишера (с использованием таблиц сопряженности 2×2) был использован для вычисления различий между двумя пропорциями.Значения P <0,05 считались значимыми. Статистический анализ проводили с использованием программного обеспечения GraphPad Prism.
Результаты
Предметы исследования
Демография субъектов исследования представлена в Таблице 1. Из 43 медицинских работников 30 не проживали с больным туберкулезом в своей семье и были классифицированы как «профессиональные контакты (ОК)». Восемь медработников, которые прожили с больным туберкулезом с бактериологически положительным диагнозом не менее 3 месяцев, были классифицированы как «домашние контактные лица (HC)».Пять медицинских работников имели в анамнезе излеченный туберкулез (2 легочных, 2 лимфаденита и 1 кожный). Рубцы от БЦЖ присутствовали у 81% пациентов, и 56% дали положительный результат на TST.
Ответы TST отражали воздействие MTB независимо от вакцинации БЦЖ
Как показано в Таблице 1 (и Таблице S1), 43% субъектов в категории ОК (n = 30) были положительными на ТКП. Тем не менее, процент положительных результатов (85%) был значительно выше (P <0,05) у медработников, которые были подвержены или инфицированы MTB (HC и излеченный TB, n = 13).Кожные уплотнения у этих субъектов также были значительно больше, чем ОК (рис. 1А, таблица S1). С другой стороны, частота положительных результатов ТКП у медработников, которые получали (57%, 20/35) или не получали (50%, 4/8) вакцину БЦЖ (определяется по наличию рубца от БЦЖ), существенно не различалась. Кожные уплотнения в обеих группах также были сопоставимы (рис. 1B, таблица S2). Эти результаты свидетельствуют о том, что индивидуальные ответы на ТКП могут отражать воздействие MTB, независимо от вакцины БЦЖ, принятой в младенчестве.
Рис. 1. Ответ медицинских работников на TST.
[A] Ответы (уплотнение кожи) домашних контактов (HC) и излеченных больных туберкулезом (CTB) были значительно сильнее, чем у профессиональных контактов (OC), и [B] ответы субъектов с (+) или без (-) Шрам БЦЖ был сопоставим. Отображаются средние +/- SEM значений в каждом столбце, а значения P отображаются в верхней части соответствующих столбцов. Пунктирные горизонтальные линии обозначают границу положительного ответа (= уплотнение 10 мм).
https: // doi.org / 10.1371 / journal.pone.0204429.g001
Антигены MTB индуцировали пролиферативные ответы в субпопуляциях CD4 +, а также CD8 + Т-клеток
Первоначально мы сравнили пролиферативные ответы клеток CD4 + и CD8 + на антигены PPD и MTBMem, поскольку оба подмножества T (CD3 +) клеток вносят вклад в общий T-клеточный иммунитет против MTB [28]. Оба показали сопоставимые ответы на PPD и PHA (митоген Т-клеток), хотя реакция на MTBMem значительно различалась (P <0,05, рис. 2 и таблица S3).Эти результаты и подтверждающие доказательства [29] побудили нас принять пролиферацию Т-клеток в качестве индикатора ответа Т-клеток. Эти результаты также указали на более высокую стимулирующую способность MTBMem к Т-клеткам, чем у PPD, что было неизменной особенностью исследования.
Рис. 2. Пролиферативные ответы Т-клеток (CD3 +) и субпопуляций Т-клеток (CD4 + и CD8 +) на антигены MTB (PPD и MTBMem) или контроли (среда и PHA).
Верхняя панель: Типовые диаграммы потоков для одного из медработников. На каждом графике в верхнем правом квадранте находятся клетки респондента (Ki67 +).Нижняя панель: индивидуальные ответы Т-клеток (ключ) 5 медработников. P Показано значение для одиночной разницы.
https://doi.org/10.1371/journal.pone.0204429.g002
In vivo и in vitro Т-клеточные ответы на PPD были комплементарными
Пролиферативные Т-клеточные ответы медработников на PPD вместе с соответствующими уплотнениями TST показаны на фиг. 3 (и в таблице S4). Положительность ответа in vivo (TST) составила 56% (таблица 1), а ответ in vitro — 67% (29/43).Кумулятивный положительный результат (для любого теста) составил 86% (37/43), что было значительно выше (P <0,01), чем положительный результат только для TST. Субъекты, не ответившие на PPD (квадрант C, рис. 3), принадлежали в основном к категории ОК. Эти результаты показали, что in vivo и in vitro Т-клеточные ответы на PPD могут служить дополнительными мерами.
Рис. 3. Комплементарность in vivo, и in vitro, Т-клеточных ответов на PPD.
Пороговые значения положительной кожной реакции (уплотнение 10 мм) и пролиферации клеток (0.75% отвечающих клеток) показаны пунктирными линиями. Квадранты AD содержат субъектов, которые были [A] отрицательными для in vivo , но положительными для in vitro ответ , [B] положительными для обоих ответов, [C] отрицательными для обоих ответов и [D] положительными для in vivo но отрицательный для in vitro ответ . Рисунок на вставке (таблица S5) показывает абсолютные числа в каждой категории.
https://doi.org/10.1371/journal.pone.0204429.g003
Мембрана МТБ была мощным активатором микобактерий-специфичных Т-клеток
Положительный пролиферативный ответ Т-клеток на MTBMem наблюдался у 88% (21/24) TST-положительных и 100% (19/19) TST-отрицательных медицинских работников (рис. 4 и таблица S4).Положительность любого анализа (TST / in vitro ) составляла 100%. В качестве антигена для «автономного» анализа in vitro MTBMem давал значительно более высокую (P <0,01) положительную реакцию (95%, фиг. 4), чем PPD (67%, фиг. 3). Количество MTBMem-реактивных Т-клеток у медработников также было значительно выше, чем у PPD-реактивных (рис. 5А). Слабая, хотя и значимая корреляция (r = 0,33, P <0,05) между ответами на оба антигена (рис. 5B) предполагает, что их уникальные белки [14, 30] могли запускать Т-клетки с различной антигенной специфичностью.В целом, эти результаты указывают на более сильную способность MTBMem индуцировать Т-клетки, чем PPD.
Рис. 4. Комплементарность TST и in vitro Т-клеточных ответов на MTBMem.
Пороговые значения положительной кожной реакции (уплотнение 10 мм) и пролиферации клеток (0,75% отвечающих клеток) показаны пунктирными линиями. Квадранты AD содержат субъектов, которые были [A] отрицательными для in vivo , но положительными для in vitro ответ , [B] положительными для обоих ответов, [C] отрицательными для обоих ответов и [D] положительными для in vivo но отрицательный для in vitro ответ .На вставке (таблица S6) показаны абсолютные числа в каждой категории.
https://doi.org/10.1371/journal.pone.0204429.g004
Рис. 5. Относительная эффективность и специфичность Т-клеточного ответа, индуцированного MTBMem.
Пунктирные линии обозначают границу положительного клеточно-пролиферативного ответа (= 0,75% отвечающих клеток). [A] MTBMem давал значительно более высокий (P <0,01) ответ, чем PPD. [B] Слабая (r = 0,33), но значимая (P <0,05) корреляция наблюдалась между ответами на MTBMem и PPD.[C] MTBMem также давал значительно более высокий (P <0,01) ответ, чем E . Мембрана coli (ECMem).
https://doi.org/10.1371/journal.pone.0204429.g005
Чтобы оценить специфичность ответа Т-клеток, индуцированного MTBMem, мы сравнили его с ответом на E . Мембрана coli (рис. 5C, таблица S7). Все, кроме одного пролиферативного ответа на E . coli антиген был отрицательным, и разница между ответами на два антигена была значительной (P <0.01). Эти результаты позволяют предположить, что ответ Т-клеток, индуцированный MTBMem, был, по крайней мере, «микобактерий-специфичным», если не MTB-специфичным.
Ответы Т-клеток снизились с увеличением воздействия MTB
Интересная картина возникла, когда Т-клеточные ответы медработников сравнивали с ответами больных туберкулезом, которые служили «контролем болезни» в этом исследовании. Хотя ответы на антигены MTB были незначительно выше при HC (чем OC), они были ниже у субъектов с излеченным туберкулезом и, в большей степени, у пациентов с активным туберкулезом (рис. 6, таблица S8).В некоторых случаях снижение ответа достигло статистической значимости. Примечательно, что реакция больных ТБ на митоген Т-клеток (ФГА) также была значительно ниже, чем соответствующая реакция медработников (во всех трех категориях). Эти результаты свидетельствуют о том, что возрастающее бремя антигена MTB или инфекции у человека может вызывать MTB-специфическое и, в конечном итоге, «генерализованное» подавление ответов Т-клеток.
Рис. 6. Пролиферативные Т-клеточные ответы на антигены MTB и митоген (ключевой) снижались с увеличением воздействия инфекции.
Диаграммы в виде прямоугольников и усов показывают индивидуальные ответы профессиональных контактов (ОК), домашних контактов (HC), излеченных (CTB) и активных (ATB) пациентов. Отсечка для положительного ответа (0,75% отвечающих клеток) изображена пунктирной линией. P Значения значительных различий показаны вверху соответствующих столбцов.
https://doi.org/10.1371/journal.pone.0204429.g006
Обсуждение
TST используется для выявления LTBI уже почти столетие, и ВОЗ также рекомендует не заменять его на IGRA [1, 2].Тем не менее, доступность и качество PPD для исследований TST остаются предметом озабоченности [31]. Еще одна проблема, вызывающая беспокойство, — это широкие вариации в используемой «силе» (TU) PPD [4, 19–22]. Эти переменные могли привести к серьезным расхождениям в сообщаемых данных о распространенности ЛТИ [32]. При выборе 5 TU PPD в качестве тестовой дозы мы руководствовались рекомендациями IUATLD и ВОЗ [26], а также некоторыми исследованиями, проведенными на Индийском субконтиненте [22, 33]. Частота положительных результатов ТКП у наших медработников была сопоставима с таковой в других регионах Индии [20, 23].Стратификация медработников показала, что повышенное воздействие МТБ может привести к более высокому уровню положительной реакции на ТКП, что согласуется с сообщениями из Дели [22] и Карачи [33]. Позитивность медицинских работников в отношении рубца от БЦЖ была также сопоставима с другими сообщениями из Индии, в которых, как и в случае с нами, не наблюдалось какого-либо влияния вакцины БЦЖ на результаты ТКП [9, 21].
Несмотря на то, что чувствительность к TST может увеличиваться с увеличением контакта с инфекцией, случаи туберкулеза могут возникать в субпопуляциях TST-отрицательных [4, 9].Чтобы определить, может ли in vitro Т-клеточный ответ на PPD дополнять ответ in vivo (TST), мы использовали один и тот же препарат антигена для обоих анализов. Действительно, оба анализа казались комплементарными, поскольку две трети TST-отрицательных медицинских работников показали положительную реакцию на пролиферацию Т-клеток. Напротив, у одной трети TST-положительных субъектов не было ответа in vitro на . Сходные противоречивые ответы in vivo и in vitro также сообщались ранее [11, 12].По разным причинам люди могут проявлять стойкую невосприимчивость к ТКП, несмотря на то, что они проживают в гиперэндемичных по ТБ районах. Например, отсутствие экспрессии «кожного лимфоцитарного антигена» на резидентных коже Т-клетках считается причиной отсутствия ответа на ТКП [34]. Дефицит продукции фактора ингибирования миграции макрофагов (MIF) кожными макрофагами также может способствовать плохому ответу на TST [35]. Наиболее вероятной причиной отсутствия пролиферативного ответа у подгруппы TST-положительных медицинских работников может быть избыточная продукция TGF-β в культурах клеток, индуцированная PPD [36].Как «главный регулятор» иммунных ответов, TGF-β может подавлять пролиферативный Т-клеточный ответ, с одной стороны, и, с другой стороны, он может способствовать ответу TST, способствуя созреванию резидентных в коже Т-клеток памяти и антигенпрезентирующих дендритных клеток. [37].
Т-клеток почти всех медработников, в том числе TST-отрицательных, ответили на MTBMem. Несмотря на то, что составляющие мембраны микобактериальных клеток являются мощными индукторами Т- и В-клеток человека [13–17], такие высокие показатели положительности вызывают озабоченность по поводу специфичности ответа.Поэтому мы сравнили его с ответом на мембранные антигены E . coli — грамотрицательная бактерия, колонизирующая желудочно-кишечный и мочеполовой тракты человека. Незначительный Т-клеточный ответ на мембрану E coli предполагает, что ответ на MTBMem можно рассматривать как «микобактерии-специфичный», в то время как необходимо более глубокое исследование (с использованием антигенов от других микробов и микобактерий, которым индейцы подвергаются «с экологической точки зрения»). чтобы доказать, что он также специфичен для МТБ.Ранее также сообщалось о сопоставимых Т-клеточных ответах здоровых индейцев на антигены MTB. В исследовании, проведенном в Мумбаи [38], Т-клетки 80% добровольцев ответили на ESAT-6 и CFP-10, а уровень положительности повысился до 98% при использовании PPD в качестве антигена. Поскольку подгруппа пациентов из Оксфорда также ответила на PPD, авторы предположили, что последняя реакция могла быть связана с БЦЖ. Тем не менее, учитывая, что влияние БЦЖ ослабевает в более поздние годы жизни [3], возможно, что у PPD-положительных субъектов действительно был LTBI [5].В другом родственном исследовании [39] 96% лиц, контактировавших с больными туберкулезом, были признаны LTBI-положительными, поскольку у них были антитела к ESAT-6 и CFP-10.
Наши результаты с пациентами с туберкулезом согласуются с отчетами, показывающими депрессивный MTB-специфический, а также общий ответ Т-клеток у сильно инфицированных людей. Хотя мы не проводили ТКП нашим пациентам (поскольку их диагноз мог быть установлен с помощью микроскопии мазка), большинство пациентов с ТБ на запущенной стадии не реагируют на ТКП [33, 38, 40]. Ответы Т-клеток на антигены IGRA также снижаются с увеличением бактериальной нагрузки [29].В том же исследовании [29] нарушение пролиферации Т-клеток положительно коррелировало с частотой полифункциональных (IFN-γ + IL-2 + TNF-α +) и отрицательно с монофункциональными (TNF-α +) Т-клетками. Кроме того, авторы наблюдали восстановление MTB-специфических ответов после химиотерапии. Излеченные случаи туберкулеза в нашем исследовании также показали более высокий ответ Т-клеток, чем активные случаи. Возможной причиной подавленных Т-клеточных ответов у активных пациентов может быть «компартментализация» Т-клеток. Schwander и др. [41] сообщили о значительно более высоком индуцированном PPD синтезе ДНК и IFN-γ в бронхоальвеолярных клетках, чем в клетках крови больных туберкулезом.Другой возможной причиной может быть индуцированная МТБ гиперпродукция Т-клеточного регуляторного цитокина TGF-β у пациентов [36, 37]. Эти и наши результаты имеют важное значение для развития Т-клеточной диагностики туберкулеза. Хотя частота MTB-реактивных Т-клеток может быть высокой при LTBI, она может снижаться по мере прогрессирования инфекции. Это может затруднить различие между «субклинической» и «доклинической» стадиями инфекции.
Мы стремились использовать методы и протоколы, которые при необходимости можно было бы адаптировать для крупномасштабных исследований.Пролиферация Т-клеток является таким же хорошим коррелятом иммунитета, как и уровни множественных цитокинов «типа 1» [29, 42]. Выбор цельной крови по сравнению с мононуклеарными клетками устранил необходимость забора больших объемов крови и ее «предварительной обработки». Хотя мы использовали 0,1 мл венозной крови для каждой точки анализа, с появлением более чувствительных и простых версий проточных цитометров станет возможным работать с меньшими объемами капиллярной крови (укола пальцем). Необходимая лабораторная установка находится в допустимых пределах для нового диагностического теста на ТБ [43].
По определению, тест на LTBI предоставляет доказательства иммунного ответа памяти против MTB, а не подтверждает наличие жизнеспособной или активной инфекции. С этой точки зрения наши (и некоторые более ранние) результаты позволяют предположить, что почти все жители гиперэндемичного региона по ТБ могут считаться ЛТИ-положительными. Тогда как выбрать тех субъектов, у которых может развиться активная форма туберкулеза? Меняющаяся парадигма LTBI как «спектра» требует, чтобы любой диагностический тест проводился в нескольких временных точках [43].Для включения в такие лонгитюдные исследования было бы более полезно включить в исследование тех людей, которые не только имеют положительный тест на исходном уровне, но также имеют высокую частоту МТВ-реактивных Т-клеток. Например, при пороговом значении позитивности 0,75%, значительное количество наших медработников показало в 4 раза больше (> 3%) клеток-респондентов. В этом контексте уже сообщалось, что большие реакции на ТКП являются лучшими предикторами возникновения туберкулеза [4].
Относительно небольшой размер выборки можно рассматривать как ограничение исследования.Применяемые критерии не позволяли нам набирать большее количество субъектов в категориях HC и излеченного туберкулеза. Точно так же преобладающая политика вакцинации затрудняла набор пациентов из категории БЦЖ-отрицательных. При отборе больных туберкулезом мы также уделяли внимание донорам с положительным мазком мокроты и донорам, не получавшим лечения. Тем не менее, наши результаты хорошо подтверждаются некоторыми предыдущими исследованиями [9, 11, 12, 20–23, 29, 33, 38, 40]. Другие требования, которые могут быть выполнены в ходе будущих исследований, включают (а) данные о выполнении анализов in vitro, особенно с использованием MTBMem, в регионах с низкой эндемичностью ТБ и (б) молекулярную характеристику антигенов в MTBMem [13, 14 ].В заключение, это исследование, проводимое на фоне неослабевающей эпидемии туберкулеза, требует критической оценки методов и протоколов, используемых в настоящее время для выявления ЛТИ.
Благодарности
Мы благодарны принимающему институту (SGPGIMS) за очную поддержку. SS является почетным ученым-медиком, а SKK — старшим научным сотрудником Индийского совета медицинских исследований.
Список литературы
- 1.
КТО. 2015. Руководство по ведению латентной туберкулезной инфекции.Женева: Всемирная организация здравоохранения; 2015 г. (WHO / HTM / TB / 2015.01). - 2.
КТО. 2017. Global Tuberculosis Report, 2017. - 3.
Фархат М., Гринуэй К., Пай М., Мензис Д. Ложноположительные туберкулиновые кожные пробы: каков абсолютный эффект БЦЖ и нетуберкулезных микобактерий? Int J Tuberc Lung Dis, 2006; 10: 1192–204. pmid: 17131776 - 4.
Научный центр туберкулеза. Связь начальной чувствительности к туберкулину, возраста и пола с заболеваемостью туберкулезом в южной Индии: 15-летнее наблюдение.Int J Tuberc Lung Dis, 2003; 7: 1083–1091. pmid: 14598969 - 5.
Седдон Дж. А., Патон Дж., Надеми З., Кин Д., Уильямс Б., Уильямс А. и др. Влияние вакцинации БЦЖ на реакцию детей на туберкулиновую кожную пробу зависит от возраста: данные, которые следует учитывать при скрининге детей на туберкулезную инфекцию. Thorax, 2016; 71: 932–9 pmid: 27335104 - 6.
Hill PC, Brookes RH, Fox A, Jackson-Sillah D, Lugos MD, Jeffries DJ и др. Удивительно высокая специфичность кожного теста PPD на M.tuberculosis в результате недавнего заражения в Гамбии. PLoS ONE, 2008 г .; 1: e68 - 7.
Макмаллен С.Е., Пегес Д.А., Шофер Ф.С., Шеллер А.С., Винер Э.Б. Проведение теста QuantiFERON-TB Gold и туберкулиновой кожи относительно риска заражения туберкулезом у субъектов. Clin Infect Dis, 2014; 58: 1260–6. pmid: 24585559 - 8.
Lagrange PH, Thangaraj SK, Dayal R, Deshpande A, Ganguly NK, Girardi B и др. Набор инструментов для диагностики туберкулеза (ТБ): индийское многоцентровое исследование (2006–2008 гг.).Оценка QuantiFERON-TB Gold в пробирке для диагностики ТБ. PLoS ONE, 2013 г .; 8: e73579. pmid: 24039990 - 9.
Шарма С.К., Вашишта Р., Чаухан Л.С., Шринивас В., Сет Д. Сравнение TST и IGRA в диагностике латентной туберкулезной инфекции в условиях высокого бремени ТБ. PLoS ONE, 2017; 12: e0169539. pmid: 28060926 - 10.
Смит Дж. А., Райхман Л.Б. Трансформация лимфоцитов. Помощь в диагностике пациентов с нереактивными кожными пробами. Амер Рев Респ Дис, 1972 год; 106: 194–201.pmid: 4626099 - 11.
Black GF, Fine PEM, Warndorff DK, Floyd S, Weir RE, Blackwell JM и др. Взаимосвязь между IFN-γ и чувствительностью кожной пробы к PPD Mycobacterium tuberculosis у здоровых молодых людей, не вакцинированных БЦЖ, в северной части Малави. Int J Tuberc Lung Dis, 2001; 5: 664–672. pmid: 11467373 - 12.
Галлант CJ, Cobat A, Simkin L, Black GF, Stanley K, Hughes J и др. Туберкулиновая кожная проба и анализы in vitro обеспечивают дополнительные измерения противомикобактериального иммунитета у детей и подростков.Сундук, 2010 г .; 137: 1071–1077. pmid: 20040612 - 13.
Lindestam ACS, Герасимова А., Меле Ф, Хендерсон Р., Суонн Дж., Гринбаум Дж. А. и др. Т-клетки памяти при латентной инфекции Mycobacterium tuberculosis направлены против трех антигенных островов и в основном содержатся в субпопуляции CXCR3 + CCR6 + Th2. PLoS Pathog, 2013; 9: e1003130. pmid: 23358848 - 14.
Синха С., Косалаи К., Арора С., Намане А., Шарма П., Гайквад А. Н. и др. Иммуногенные мембранно-ассоциированные белки Mycobacterium tuberculosis, выявленные с помощью протеомики.Микробиология, 2005; 151: 2411–19. pmid: 16000731 - 15.
Кумар С.К., Сингх П., Синха С. Естественно продуцируемые опсонизирующие антитела ограничивают выживание Mycobacterium tuberculosis в макрофагах человека за счет увеличения созревания фагосом. Открытая Биол, 2015; 5: 150171. pmid: 26674415 - 16.
Адекамби Т., Ибегбу С.К., Кейгл С., Калохе А.С., Ван Ю.Ф., Ху Ю.и др. Биомаркеры Т-клеток пациента позволяют диагностировать активный туберкулез и контролировать реакцию на лечение. J Clin Invest, 2015; 125: 1827–38.pmid: 25822019 - 17.
Kunnath-Velayudhan S, Salamon H, Wang HY, Davidow AL, Molina DM, Huynh VT, et al. Динамические ответы антител на протеом Mycobacterium tuberculosis. Proc Natl Acad Sci USA, 2010; 107: 14703–14708. pmid: 20668240 - 18.
Международный союз борьбы с туберкулезом и болезнями легких, 2018. Тихая эпидемия: призыв к действиям против детского туберкулеза. - 19.
Чадха В.К., Сарин Р., Наранг П., Джон К.Р., Чопра К.К., Джитендра Р. и др.Тенденции ежегодного риска туберкулезной инфекции в Индии. Int J Tuberc Lung Dis, 2013; 17: 312–319. pmid: 23321394 - 20.
Narasimhan P, MacIntyrea CR, Mathaib D, Wood J. Высокие показатели латентной инфекции туберкулеза среди контактов и более широкого сообщества в Южной Индии. Trans R Soc Trop Med Hyg, 2017; 111: 55–61. pmid: 28407146 - 21.
Пай М., Гокхале К., Джоши Р., Догра С., Калантри С., Мендиратта Д. К. и др. Инфекция Mycobacterium tuberculosis у медицинских работников в сельских районах Индии: Сравнение анализа интерферона-g цельной крови с кожным туберкулиновым тестом.JAMA, 2005; 293: 2746–2755. pmid: 15941804 - 22.
Сингла Н., Сингла Р., Джайн Г., Хабиб Л., Бехера Д. Туберкулез среди домашних контактов больных туберкулезом с множественной лекарственной устойчивостью в Дели, Индия. Int J Tuberc Lung Dis, 2011; 15: 1326–1330. pmid: 22283889 - 23.
Хайям К.Ю., Патра С., Сарин Р., Бехера Д. Туберкулез среди медицинских работников в институте третичной помощи при респираторных заболеваниях в Нью-Дели. Индийский J Tuberc. 2010, 57: 192–98. pmid: 21141337 - 24.Всемирная медицинская ассоциация. Хельсинкская декларация ВМА — Этические принципы медицинских исследований с участием людей. https://www.wma.net/policies-post/wma-declaration-of-helsinki-ethical-principles-for-medical-research-involving-human-subjects/ (по состоянию на 27 августа 2018 г.).
- 25.
Марквелл М.А., Хаас С.М., Бибер Л.Л., Толберт Н.Е. Модификация процедуры Лоури для упрощения определения белка в образцах мембран и липопротеинов. Анальная биохимия, 1978; 87: 206–210.pmid: 98070 - 26.
Rieder HL, Chadha VK, Nagelkerke NJD, van Leth F, van der Werf MJ. Руководство по проведению обследований кожных проб в странах с высокой распространенностью. Int J Tuberc Lung Dis, 2011; 15: S1 – S25. pmid: 21276325 - 27.
Соарес А., Говендер Л., Хьюз Дж., Мавакла В., де Кок М., Барнард С. и др. Новое применение Ki67 для количественной оценки антиген-специфической лимфопролиферации in vitro. J Immunol Methods, 2010; 362: 43–50. pmid: 20800066 - 28.
Левинсон Д.А., Сварбрик Г.М., Парк Б., Канслер М.Э., Нулл М.Д., Торен К.Г. и др.Комплексное определение иммунодоминантных антигенов CD8 человека при туберкулезе. NPJ Vaccines, 2017; 2: 8. pmid: 28775896 - 29.
Day CL, Abrahams DA, Lerumo L, Janse van Rensburg E, Stone L, O’rie T. и др. Функциональная способность Mycobacterium tuberculosis-специфических Т-клеточных ответов у людей связана с микобактериальной нагрузкой. J Immunol, 2011; 187: 2222–2232. pmid: 21775682 - 30.
Чо Ю.С., Добос К.М., Пренни Дж., Ян Х., Хесс А., Розенкрандс И. и др. Расшифровка протеома диагностического реагента in vivo «очищенное производное белка» от Mycobacterium tuberculosis.Протеомика, 2012; 12: 979–991. pmid: 22522804 - 31.
Тебрюгге М., Буонсенсо Д., Бринкманн Ф., Ногера-Джулиан А., Павич I, Арборе А.С. и др. Дефицит очищенных производных белка в Европе и его влияние на практику скрининга на туберкулез. Int J Tuberc Lung Dis, 2016; 20: 1293–1299. pmid: 27725037 - 32.
Rieder HL. Методологические вопросы оценки проблемы туберкулеза по данным туберкулиновых обследований. Tuberc Lung Dis, 1995; 76: 114–21. - 33.Хуссейн Р., Туси З., Хасан Р., Джамиль Б., Давуд Г., Элльнер Дж. Дж. Профиль иммунного ответа у пациентов с активным туберкулезом в зоне вакцинации БЦЖ. Юго-Восточная Азия J Trop Med Public Health, 1997; 28: 764–773. pmid: 9656400
- 34.
Акбар А.Н., Рид Дж. Р., Лейси К. Э., Джексон С. Е., Вукманович-Стеич М., Рустин М. Х. Исследование кожного ответа на отзыв антигена у людей in vivo. Clin Exp Immunol, 2013; 173: 163–172. pmid: 23607634 - 35.
Бернхаген Дж., Бахер М., Каландра Т., Мец К.Н., Доти С.Б., Доннелли Т. и др.Существенная роль фактора ингибирования миграции макрофагов в реакции гиперчувствительности замедленного типа к туберкулину. J Exp Med, 1996; 183: 277–82. pmid: 8551232 - 36.
Тусси З., Янг Ти-Джи, Аверилл Л.Э., Гамильтон Б.Д., Ширацучи Х., Элльнер Дж.Дж. Индукция трансформирующего фактора роста β1 очищенным производным белка Mycobacterium tuberculosis. Infect Immun, 1995; 63: 224–228 pmid: 7806361 - 37.
Келли А., Хьюстон С.А., Шервуд Е., Казулли Дж., Трэвис М.А. Регуляция врожденного и адаптивного иммунитета с помощью TGF-β.Успехи Иммунол, 2017; 134: 137–233 - 38.
Лалвани А., Нагвенкар П., Удвадиа З., Патан А.А., Уилкинсон К.А., Шастри Дж.С. и др. Подсчет Т-клеток, специфичных к антигенам, кодируемым RD1, свидетельствует о высокой распространенности латентной инфекции Mycobacterium tuberculosis у здоровых городских индейцев. J. Infect Dis, 2001; 183: 469–77. pmid: 11133379 - 39.
Хофф С.Т., Абебе М., Равн П., Диапазон N, Маленганишо В., Родрикес Д.С. и др. Оценка специфических антител к Mycobacterium tuberculosis в популяциях с различными уровнями воздействия из Танзании, Эфиопии, Бразилии и Дании.Clin Infect Dis, 2007; 45: 575–582. pmid: 17682991 - 40.
Санчес ФО, Родригес Джи, Агудело Джи, Гарсия Л.Ф. Иммунная реакция и продукция лимфокинов у пациентов с туберкулезом и здоровых людей из контрольной группы. Infect Immun, 1994; 62: 5673–5678. pmid: 7960152 - 41.
Швандер С.К., Торрес М., Сада Э., Карранса С., Рамос Э., Тари-Леманн М. и др. Повышенная реакция альвеолярных лимфоцитов человека на антигены Mycobacterium tuberculosis во время активного туберкулеза легких.J. Infect Dis, 1998; 178: 1434–45. pmid: 9780265 - 42.
Sutherland JS, Adetifa IM, Hill PC, Adegbola RA, Ota MO. Характер и разнообразие продукции цитокинов различают инфекцию Mycobacterium tuberculosis и болезнь. Евро. J. Immunol, 2009; 39: 723–729. pmid: 19224636 - 43.
КТО. 2017a. Отчет о консенсусной встрече: разработка профиля целевого продукта (TPP) и основы для оценки теста для прогнозирования прогрессирования туберкулезной инфекции в активную болезнь.Женева: Всемирная организация здравоохранения; 2017 г. (WHO / HTM / TB / 2017.18).
Контактный дерматит: Сводка | Всемирная организация по аллергии
Обновлено: декабрь 2020 г.
Сообщение: август 2004 г.,
Luz Fonacier, MD, FACAAI, FAAAAI
Заведующий отделением аллергии отделения ревматологии и иммунологии
NYU Langone Hospital — Long Island
Профессор медицины — Медицинская школа Лонг-Айленда Нью-Йоркского университета,
Минеола, Нью-Йорк, США
Элеонора Фельдман, MD
Аллергия и иммунология
Больница NYU Langone — Лонг-Айленд
Введение
Контактный дерматит, вызывающий раздражение
Контактный дерматит (КД) — заболевание кожи, характеризующееся покраснением, зудом и пузырьками.В хронических случаях также может присутствовать чешуйчатое шелушение и лихенификация. CD возникает в результате контакта с веществами окружающей среды, вызывающими аллергическую и / или раздражающую реакцию. Высокое клиническое подозрение на аллергический контактный дерматит (АКД) — это первый шаг в постановке диагноза. Патч-тест показан любому пациенту с острым или хроническим дерматитом, если есть подозрение на первичный или вторичный ACD.
ВВЕДЕНИЕ
CD — это распространенное кожное заболевание с оценкой 5.7 миллионов посещений врача в год. Затронуты все возрастные группы, с небольшим преобладанием женщин. Хотя истинная распространенность и заболеваемость неизвестны, на долю CD приходится примерно 85-95% всех профессиональных кожных заболеваний в промышленно развитых странах. Дерматит кистей рук — наиболее частое клиническое проявление, которым страдают от 2 до 6% этой популяции. Фундаментальной характеристикой CD является его отношение к воздействию окружающей среды, которое может быть определено по месту и форме поражения кожи, а также по подробному анамнезу.
РАЗДРАЖАЮЩИЙ КОНТАКТНЫЙ ДЕРМАТИТ
Раздражающий контактный дерматит (ИКД), наиболее распространенный тип контактного дерматита, чаще всего поражает руки. У детей пеленочный дерматит и дерматит сухой кожи являются наиболее частыми формами МКБ. Эти поражения кожи развиваются при длительном и многократном воздействии веществ, которые химически истирают, физически раздражают или повреждают кожу (например, едкие вещества, детергенты). У детей поражения часто возникают в результате многократного контакта с водой (облизывания губ или сосания большого пальца).Поражения часто бывают хорошо очерченными и выглядят глянцевыми, засохшими или ошпаренными. Патч-тест обычно дает отрицательный результат, и поражения быстро исчезают после прекращения действия возбудителя. Хотя воспалительные клетки играют роль в развитии дерматита, аллерген-специфические иммунные лимфоциты не участвуют в патогенезе, поэтому предварительная сенсибилизация не требуется. Восприимчивость к раздражителям у разных людей разная, но при достаточном воздействии почти у любого может развиться ИКД.
АЛЛЕРГИЧЕСКИЙ КОНТАКТНЫЙ ДЕРМАТИТ
Аллергический контактный дерматит (АКД) возникает в результате воспаления, вызванного в основном гиперчувствительностью (замедленным) клеточным иммунным ответом типа IV. Острые поражения характеризуются папулами и / или пузырьками, которые вызывают мокнутие, образование корок, эритему, отек и зуд. (См. Рисунок A ниже). Предварительная сенсибилизация важна, и быстрое развитие дерматита происходит при повторном воздействии низких концентраций аллергена. У сенсибилизированных людей это обычно происходит в течение 6–12 часов.Хронические поражения могут проявляться в виде трещин, утолщения кожи, лихенификации, угревой сыпи, гипо- или гиперпигментации. ACD был зарегистрирован у младенцев уже в возрасте одной недели, хотя сенсибилизация обычно происходит в возрасте 6 месяцев.
Рисунок A
КОМБИНАЦИЯ АЛЛЕРГИЧЕСКОГО И РАЗДРАЖАТЕЛЬНОГО КОНТАКТНОГО ДЕРМАТИТА
Одновременное воздействие раздражающих и контактных аллергенов может вызывать аддитивные, синергические или антагонистические реакции.Если присутствуют в более высоких концентрациях, аллергены, участвующие в ACD, могут устанавливать ICD за счет активации провоспалительных цитокинов и / или усиления проникновения аллергена через кожу.
ФОТОДЕРМАТИТ
Фотодерматит может вызывать фототоксические или фотоаллергические реакции. Фотодерматоз обычно поражает открытые солнцу участки, такие как лицо, «V» передней части шеи, тыльную сторону кистей и предплечья. Обычно щадят верхние веки, верхнюю губу, подподбородочные и постурикулярные области.Другими причинами дерматита в этом анатомическом распределении являются высыпания от фототоксичных лекарств, высыпания от фотоаллергических лекарств и системные заболевания, такие как красная волчанка. Фотоаллергическая реакция может развиться, когда УФ-свет взаимодействует с химическими веществами (например, ароматизаторами, парааминобензойной кислотой, растениями, пастернаком, инжиром или некоторыми пероральными лекарствами), вызывая различные формы фотосенсибилизации. Например, фототоксические и фотоаллергические поражения могут развиваться на коже, подвергшейся воздействию солнечных лучей при системном введении агентов (т.е. лекарства). Напротив, когда сенсибилизирующий агент наносится непосредственно на кожу (например, ароматизаторы), на месте нанесения после воздействия солнечного света развиваются поражения.
СИСТЕМНЫЙ КОНТАКТНЫЙ ДЕРМАТИТ
Аллергический системный контактный дерматит (ВСС) может проявляться как генерализованный дерматит или экзантема в интертригинозных и изгибных областях (синдром бабуина). Вспышки могут также развиться на участках предыдущих CD или положительных патч-тестов при системном воздействии известного контактного сенсибилизатора (например,g., прием внутрь, инфузия или чрескожное воздействие). Патофизиология похожа на ACD, с инициированием воспалительной реакции при активации аллерген-специфических Т-лимфоцитов. Наиболее частые причины SCD включают металлы (ртуть, никель, золото), лекарства (антибактериальные аминогликозиды, кортикостероиды, аминофиллин), растения и растительные продукты (бальзамы Перу, семейства растений Compositae и Anacardiaceae).
ДИФФЕРЕНЦИАЛЬНАЯ ДИАГНОСТИКА
CD можно заподозрить на основании клинического проявления и распределения поражений, отсутствия сопутствующих системных симптомов и отсутствия другой вероятной этиологии.Гистологически БК характеризуется межклеточным отеком эпидермиса (спонгиоз) и различной степенью утолщения базального и шиповатого слоя эпидермиса (акантоз). Также присутствуют поверхностные периваскулярные, лимфогистиоцитарные инфильтраты. По клиническим и гистологическим признакам трудно отличить ACD от ICD. Однако дифференцировать эти два состояния важно, особенно при профессиональном дерматите. ИКД может позволить пациенту продолжить работу с соответствующей защитой кожи.Требуется подробный анамнез домашних, профессиональных, спортивных и развлекательных лиц, контактировавших с ними, а также результаты патч-тестов.
Дифференциальный диагноз CD включает другие воспалительные заболевания кожи. Атопический дерматит (АД) обычно проявляется в раннем возрасте и носит более хронический характер. У этих пациентов также есть личный или семейный анамнез атопии. Поражения обычно распространяются на лице в младенчестве, на разгибателях в раннем детстве и на изгибных областях в подростковом возрасте и у взрослых.Патч-тестирование (PT) должно проводиться у пациентов с AD при определенных обстоятельствах: при отсутствии улучшения с помощью местной терапии, пациентах с атипичным распространением дерматита, экземе рук, устойчивой к терапии, у взрослых или подростков с началом AD и / или перед началом системного иммунного ответа. подавители для лечения AD. Себорейный дерматит обычно возникает на коже черепа, околопориаурикулярной области, лице (медиальные брови, глабель, носогубные складки), предсердной и межлопаточной области. Поражения резко разграничены, имеют тусклый желтовато-красный цвет, который может быть покрыт жирными чешуйками.Дисгидротическая экзема должна рассматриваться как дифференциальный диагноз АКД с поражением рук. Клинические признаки включают симметричные мелкие глубоко расположенные пузырьки на ладонях, подошвах и / или боковых сторонах пальцев. Везикулы также сильно зудят. Грибковые микозы (MF) и кожная Т-клеточная лимфома также являются важными условиями, которые следует исключить при оценке ACD. Эти заболевания характеризуются пятнами, которые имеют тонкий, морщинистый вид, часто с сетчатой пигментацией (см. Рисунок B ниже).Часто они присутствуют на нижней части туловища и ягодицах. Эти условия также могут проявляться бляшками и узелками. Из-за этой вариабельности для подтверждения требуется биопсия кожи. Зуд различается у разных людей, но чаще встречается в премикотической фазе и может предшествовать МФ на несколько лет.
Рисунок B: Mycosis Fungoides
ОБЫЧНЫЕ АЛЛЕРГЕНЫ, ВЫЗЫВАЮЩИЕ АЛЛЕРГИЧЕСКИЙ КОНТАКТНЫЙ ДЕРМАТИТ
Никель
Никель — самая частая причина ACD как у детей, так и у взрослых во многих странах.Аллергия на никель обычно поражает уши из-за контакта с серьгами, кожей под пряжками ремня и руками. Это также может повлиять на лицо от случайного распространения от рук. Никель широко используется в ортодонтии. Пациентам с известной чувствительностью к никелю может потребоваться избегать использования некоторых гибких титан-никелевых дуг, которые выделяют повышенное количество никеля по сравнению с нержавеющей сталью. Никель также является частой причиной SCD. У женщин чувствительность к никелю может увеличить риск развития экземы рук.
Пирсинг (пирсинг ушей) связан с повышением сенсибилизации никелем. В Европе правила относительно количества никеля, присутствующего в потребительских товарах, были введены более 20 лет назад. В результате последующие исследования продемонстрировали резкое снижение уровня сенсибилизации к никелю в этих странах. Присутствие высвобождаемого никеля с поверхности объекта можно обнаружить с помощью пробы с диметилглиоксимом; розовый цвет указывает на наличие> 0.5 мкг никеля / см2 / неделя.
Хроматы
Воздействие хромата калия часто встречается в кожевенной промышленности (т. Е. В процессе дубления) и в строительстве (воздействие цемента). ACD к хромату, присутствующий в кожаной обуви, может развиваться в более теплом климате, поскольку потоотделение способствует высвобождению аллергена. Чувствительность к хроматам может быть связана с дерматитом рук или ног, который может сохраняться даже после избегания хроматирования.
Резиновые ускорители: тиурамы, карбаматы, меркаптобензотиазол
ACD к резине обычно развивается из-за сенсибилизации от резиновых изделий, которые носят близко к коже.Примерами являются резинки нижнего белья, перчаток, обуви и барьерных противозачаточных средств (см. Рисунок C ниже). Общие аллергены каучука включают карбаматы, тиурамы и меркаптобензотиазол. Карбаматы также содержатся в садовых фунгицидах. В частности, аллергия на черный каучук также может быть связана с сенсибилизацией к парафенилендиаминовому красителю, а не к самому каучуковому компоненту. Кроме того, пациенты с подозрением на ACD каучука также должны быть проверены на смешанные диалкилтиомочевины (диэтилтиомочевину и дибутилтиомочевину), поскольку большинство пациентов, сенсибилизированных тиомочевиной, не реагируют на общие аллергены каучука при тестировании пластыря.
Смешанные диалкилтиомочевины (MDTU) используются в качестве ускорителя каучука и антиоксиданта при производстве неопрена. Сообщалось о ACD из неопрена при использовании ортопедических скоб, протезов, шин и опор для ног; спортивная обувь; резиновые маски, плавательные очки и гидрокостюмы; компьютерные упоры для запястий; неопреновые перчатки; и материалы на основе резины в автомобилях. Кроме того, латексный каучук также может вызывать аллергическую контактную крапивницу и анафилаксию, которая является опосредованной IgE реакцией на аллергены латексного белка.
Смешанные диалкилтиомочевины (MDTU) используются в качестве ускорителя каучука и антиоксиданта при производстве неопрена. Сообщалось о ACD из неопрена при использовании ортопедических скоб, протезов, шин и опор для ног; спортивная обувь; резиновые маски, плавательные очки и гидрокостюмы; компьютерные упоры для запястий; неопреновые перчатки; и материалы на основе резины в автомобилях. Кроме того, латексный каучук также может вызывать аллергическую контактную крапивницу и анафилаксию, которая является опосредованной IgE реакцией на аллергены латексного белка.
Рисунок C : ACD к перчаткам
Ароматы
Ароматы — это сложные вещества, содержащие сотни различных химических веществ. Некоторые примеры — бальзам Перу, коричный альдегид, коричный спирт, гидроксицитронеллаль, гераниол, изоэвгенол, эвгенол и дубовый мох. Эти химические вещества составляют наиболее частую причину появления АКД в косметике. Они также присутствуют во многих препаратах для местного применения, мыле, парфюмерии, зубных пастах и других продуктах личной гигиены.Сенсибилизированные пациенты должны использовать продукты, не содержащие отдушек. Продукты без запаха не подходят, так как они могут содержать маскирующие ароматизаторы. Однако важно отметить, что продукты без отдушек могут содержать большое количество растительных экстрактов. Эти экстракты используются для улучшения запаха продукта, но также могут быть источником сенсибилизаторов. Необходимо провести патч-тестирование с достаточным количеством химикатов, чтобы выявить замедленную гиперчувствительность к ароматизаторам. После того, как диагностирована аллергия на запахи, следует разработать план лечения, чтобы избежать воздействия запахов, содержащихся в продуктах.
Консерванты
Консерванты используются в большинстве косметических средств на водной основе и в средствах личной гигиены для предотвращения прогорклости и микробного загрязнения. Эти консерванты, как правило, делятся на 2 большие категории: высвобождающие формальдегид (продукты, выделяющие формальдегид) и неформальдегидные высвобождающие средства.
Формальдегид — один из самых распространенных аллергенов в окружающей среде. Он присутствует в фиксаторах, клеях, консервантах и дезинфицирующих средствах.Многие косметические и дезинфицирующие средства содержат высвобождающие формальдегид или формальдегид (имидазолидинилмочевину, DMDM, гидантоин, диазолидинилмочевину и кватерниум-15). Формальдегид также содержится в тканях, особенно в «небрежной» одежде, чтобы помочь сохранить их форму. Однако многие пациенты с повышенной чувствительностью к формальдегиду могут переносить эти типы одежды, если их стирали несколько раз.
Неформальдегидный высвобождающий агент, метилдибромглютеронитрил (MDG / PE), недавно стал важным косметическим аллергеном, связанным с дерматитом рук.Другой неформальдегидный высвобождающий агент, метилхоризотиазолинон / метилизотиазолинон (MCI / MI), является распространенным консервантом в косметике и продуктах личной гигиены. MCI / MI обычно встречается в комбинации 3: 1, однако использование одного MI увеличивается (например, шампуни, кондиционеры, детское мыло и моющие средства, влажные салфетки, влажные салфетки и влажная туалетная бумага). Смесь MCI / MI в патч-тестах пропускает примерно 40% аллергии на MI, вероятно, из-за низкой концентрации MI в смеси MCI / MI.
Парабены в косметике также могут вызывать ACD.Сенсибилизация к парабенам также часто наблюдается при применении местных антибактериальных препаратов, особенно при нанесении на поврежденную кожу в таких условиях, как длительный дерматит и застойные язвы.
Парафенилендиамин
Парафенилендиамин (PPD) является активным ингредиентом многих перманентных и полуперманентных красок для волос. Это основная причина ACD среди парикмахеров. Хотя краска для волос является наиболее распространенным источником воздействия, современные тенденции, такие как бодиарт и временные татуировки, приводят к другим путям воздействия.ACD от PPD может быть тяжелым, так как он также может проявляться ангионевротическим отеком.
PPD также используется в качестве антиоксиданта в маслах и консистентных смазках, а также в качестве компонента проявителей цветной пленки. Он также используется в качестве красителя для кожи, меха, текстиля, резинотехнических изделий и татуировок черной хной. Также сообщалось о перекрестной реактивности с другими пара-аминосоединениями, такими как бензокаин, пара-аминобензойная кислота (PABA), сульфамидные препараты, аминоазобензол, изопропил-пара-фенилендиамин (IPPD) и азокрасители.
Кокоамидопропилбетаин
Кокоамидопропилбетаин (CAPB) — это поверхностно-активное вещество, которое часто используется в шампунях, средствах для ванн, жидких гелях для душа, шариковых дезодорантах, средствах для чистки глаз и лица, жидких моющих средствах, средствах для чистки поверхностей, средствах для ухода за домашними животными и других средствах по уходу за кожей и волосами. Контактный дерматит от CAPB может проявляться как дерматит век, лица, кожи головы и / или шеи.
Лекарства
Бензокаин, производное ПАБК, является сенсибилизатором и присутствует во многих лекарствах, отпускаемых без рецепта, таких как препараты для лечения геморроя и ожогов, а также в качестве местного анестетика.Возможны перекрестные реакции с прокаином, бутакаином, тетракаином, пропоксикаином, метабутетамином, меприлкаином и изобукаином.
Антибактериальный агент, неомицин, является частой причиной ACD. Он перекрестно реагирует с паромомицином, бутирозином, фрамицетином, тобрамицином, канамицином и гентамицином. Пациенты с аллергией на неомицин также могут иметь сопутствующую сенсибилизацию к бацитрацину. Лекарства для лечения язв на ногах могут вызвать дерматит ног (см. Рисунок D ниже). Пациенты с застойным дерматитом, язвами ног, аногенитальным дерматитом и наружным отитом подвергаются более высокому риску развития АКД на фоне приема этих антибиотиков.
Рисунок D : Острая ACD, вызванная лекарством
Кортикостероиды для местного применения (TCS) можно разделить на различные группы в зависимости от активности и аллергенности. Эффективность и побочные эффекты TCS связаны с насыщением глюкокортикоидов в различных типах клеток и могут быть классифицированы как супер-, высокая, умеренная и низкая активность. (Таблица 1) Аллергенность основана на 2 сайтах иммунного распознавания — заменах C 6/9 и C16 / 17 — и может быть разделена на класс / группы A, B, C, D-1, D-2. Класс A содержит группы пивалата гидрокортизона и тиксокортола; Класс B содержит ацетониды, а Класс C содержит неэтерифицированный бетаметазон. Класс D1 Стероиды имеют метильную группу C16 и галогенированное кольцо B. Класс D2 Стероиды представляют собой лабильные сложные эфиры без метильной группы C16 и галогенового замещения в кольце B. (Таблица 2) ACD к TCS следует подозревать, если сыпь не реагирует или сначала реагирует, а затем ухудшается при длительной терапии.Хотя редко, у пациентов с ACD до TCS может развиться SCD при системном воздействии кортикостероидов (т. Е. Ингаляционных, пероральных, внутривенных, парентеральных). Из-за перекрестной реактивности внутри и между группами рекомендуется избегать группы TCS, если аллергия на одного члена группы подтверждается патч-тестом. Носитель и консерванты в местных препаратах кортикостероидов также являются частыми причинами ACD. Обычными ингредиентами носителя являются пропиленгликоль, сесквиолеат сорбитана, консерванты, высвобождающие формальдегид, парабены, MCI / MI и ланолин.
Если патч-тестирование недоступно, рекомендуется использовать стероид класса C с носителем без «обычных» аллергенов (например, дезоксиметазон) или местными ингибиторами кальциневрина.
ДИАГНОСТИКА И ОЦЕНКА КОНТАКТНОГО ДЕРМАТИТА
Патч-тестирование
PT — золотой стандарт диагностики ACD. ПВ показана любому пациенту с острым или хроническим, зудящим, экзематозным или лихенифицированным дерматитом, у которого есть подозрение на лежащий в основе или вторичный ACD.Дерматит, если он обширен, следует лечить до PT. В идеале пациенты не должны принимать иммунодепрессанты, такие как системные кортикостероиды, циклоспорин и / или микофенолят, до ПВ. Однако, если прием пероральных кортикостероидов нельзя отменить, некоторые исследования показали, что ПВ у пациентов, принимающих низкие дозы преднизона (менее 20 мг / день) и циклоспорина, все же может давать клинически значимые результаты. TCS и местные ингибиторы кальциневрина не следует наносить на тестируемый участок за 5–7 дней до тестирования.Пациентам также следует воздерживаться от солнечных ванн или использования солярия за 2-4 недели до PT. Не рекомендуется беременным или кормящим грудью пациенткам, которые кормят грудью.
Патч-тест на аллергены
По возможности важно использовать стандартизированные аллергены для окклюзированной ПП, поскольку они были тщательно протестированы и показали, что они не вызывают раздражения или сенсибилизации кожи. Большинство этих аллергенов продаются в виде вазелиновых смесей. Те, которые нельзя диспергировать в белом петролатуме из-за химической стабильности, доступны в водной форме.
Стандартные и / или дополнительные серии аллергенов PT продаются компаниями, работающими в тесном сотрудничестве с Международной исследовательской группой контактного дерматита (ICDRG), а также другими международными и национальными группами. Ядро или базовая серия антигенов PT, таких как те, которые используются NACDG, T.R.U.E. Можно использовать панель Test ™ или серию Core Allergen, рекомендованную Американским обществом контактного дерматита (ACDS). Однако, полагаясь только на эти серии, можно не идентифицировать причинный аллерген у всех пациентов, что приводит к заниженной диагностике ACD.Следовательно, может потребоваться добавление дополнительных аллергенов PT в зависимости от конкретного воздействия на пациента и личных продуктов пациента. При дерматите век, губ и лица может потребоваться использование личных продуктов пациента. Как правило, несмываемые продукты (например, помада, румяна, увлажняющий крем, тональный крем), одежду и перчатки можно тестировать без каких-либо изменений. Продукты для смывания (например, шампунь, кондиционеры, антиперспиранты) следует разбавлять (10-2 или 10-3), так как более высокие концентрации могут вызвать раздражающую реакцию.Другие нестандартизированные аллергены, бытовые чистящие средства и промышленные продукты должны проверяться только врачами, имеющими опыт проведения этого типа тестирования, после оценки информации в паспорте безопасности материалов.
Несколько исследований также показали повышенную распространенность ACD по отношению к конкретным аллергенам у пациентов с БА, включая металлы, ароматизаторы, консерванты, растения (например, композиты), антисептики (например, хлоргексидин), смягчающие средства (например, ланолин), лекарства для местного применения (например, , неомицин, кортикостероиды), поверхностно-активные вещества (т.е., кокамидопропилбетаин) и ускорители каучука.
Верхняя часть спины является предпочтительным местом для ПК, поскольку концентрация стандартных аллергенов определялась только для кожи в этой области. В некоторых случаях можно использовать верхнюю часть руки.
Пластыри хранятся на месте в течение 48 часов после их нанесения. Тесты считываются через 20-30 минут после удаления пятен, чтобы позволить эритеме из-за давления окклюзии или снятия ленты и / или камеры исчезнуть.Второе чтение следует провести через 3-7 дней после подачи заявки. Раздражающие реакции, возникающие в течение первых 48 часов, имеют тенденцию исчезать (эффект декрещендо) к 96 часам, тогда как аллергические реакции имеют тенденцию к усилению (эффект крещендо), поэтому важность третьего посещения. Могут образовываться контактирующие вещества, контактирующие с патч-тестом, такие как металлы (сульфат никеля, тиосульфат натрия, золото, хлорид палладия, дихромат калия, хлорид кобальта), некоторые антибиотики (неомицин), TCS (тиксокортол-21-пивалат, будесонид) и красители (пара-фенилендиамин). более 7 дней спустя.Позднее чтение через 7-10 дней после применения ПК также может быть рассмотрено, если тестирование не позволяет идентифицировать вызывающий аллерген, но история болезни убедительно подтверждает сенсибилизацию.
Интерпретация реакций патч-теста
> Все патч-тесты следует интерпретировать с учетом истории болезни пациента и морфологии кожных повреждений. Положительные патч-тесты могут не иметь отношения к текущему клиническому состоянию пациента и могут просто представлять собой сенсибилизацию.Пот и влага являются важными факторами в развитии контактного дерматита, способствуя утечке аллергена из контактного материала. Поэтому у некоторых пациентов поражения кожи могут возникать только в жаркую погоду.
Оценка патч-тестов
Международная исследовательская группа по контактному дерматиту опубликовала описательную систему оценки для стандартизации показаний пластырей.
(-) Отрицательная реакция
(? +) Сомнительная реакция только со слабой эритемой
(1+) Слабая положительная реакция с невезикулярной эритемой, инфильтрацией, возможно папулами
(2+) Сильная положительная реакция с пузырчатой эритемой, инфильтрацией и папулами
(3+) Чрезвычайно положительная реакция с интенсивной эритемой и инфильтрацией, сливающимися пузырьками, буллезной реакцией
(IR) Раздражающая реакция
(NT) Не тестировалось
Ложноположительные реакции патч-теста
Причины ложноположительных тестовых реакций:
- Вазелин может вызвать легкий фолликулит, некоторую эритему и иногда пустулы.Однако эта реакция концентрируется вокруг волосяных фолликулов и неравномерно распределяется по тестовой области.
- От окклюзионной ленты могут возникнуть аллергические или раздражающие реакции. Эти реакции возникают в непосредственной близости от места наложения окклюзионной ленты, а не в месте проведения теста на пластырь.
- «Синдром гневной спины» определяется как ложноположительные реакции, соседствующие с крупными истинно положительными реакциями, которые вызывают воспаление и раздражительность кожи на близлежащих участках тестирования.Основные механизмы до конца не изучены. Повторная оценка ложноположительных реакций может быть рассмотрена, если есть сомнения в ее достоверности. Тесты на эти специфические аллергены следует повторять и проводить на большем расстоянии друг от друга или последовательно.
- При PT пациенте с AD следует помнить, что раздражающие реакции, особенно на металлы, ароматизаторы, формальдегид, ланолин и средства для ополаскивания, являются обычными и могут быть ошибочно приняты за аллергические реакции.Между измерениями пластыря типичный паттерн «крещендо» не наблюдается в той же степени у пациентов с БА.
Ложноотрицательные реакции патч-теста
Причины ложноотрицательных тестовых реакций:
- Антигены тестировали при концентрациях, которые были слишком низкими, чтобы вызвать ответ.
- Неправильный носитель может привести к недостаточному проникновению аллергена через кожу.
- Предварительное воздействие ультрафиолетового света (т.е.е. солнце, солярии), нанесение TCS и местных ингибиторов кальциневрина на область PT, а также сопутствующая иммуносупрессивная терапия могут подавлять положительный ответ на пластырь.
- Факторы, связанные с методологией: недостаточная окклюзия, невыполнение отсроченных чтений и невыполнение фото ПК.
Определение релевантности положительной реакции патч-теста
Оценка положительной реакции на пластырь должна быть соотнесена с анамнезом и физическим осмотром, чтобы установить ее клиническую значимость.Положительная реакция на пластырь может иметь клиническое значение в зависимости от текущего или прошлого воздействия.
В настоящее время релевантность в PT определяется как:
Определено: , если пластырь или тест с предполагаемым аллергеном положительный.
Вероятно: , если аллерген присутствует в продуктах для местного применения в настоящем или прошлом и клинические проявления соответствуют этому воздействию.
Возможно: , если вероятен контакт кожи с материалами, которые, как известно, содержат аллерген.
Актуальность в прошлом: , если участок пробы положительный, но контакт с аллергеном был в прошлом, а не недавно.
ЛЕЧЕНИЕ КОНТАКТНОГО ДЕРМАТИТА
Избегание
После того, как аллерген или раздражитель был идентифицирован, предотвращение контакта с аллергеном является ключом к успешному лечению ACD. Если ПК смог идентифицировать конкретные аллергены в личных продуктах пациента, пациента следует проинформировать об аллергенах и проконсультировать по поводу их избегания.Следует обсудить список аллергенов, синонимов, а также их перекрестные реакторы. Соблюдение требований будет улучшено, если пациентам будет предоставлен список продуктов, которые они могут использовать, не содержащих идентифицированных аллергенов.
Пациентам с аллергией на никель можно использовать диметилглиоксимовый тест для определения выделения никеля металлическими предметами. Тест на кобальтовые пятна выявляет присутствие динатрий-1-нитрозо-2-нафтол-3,6-дисульфоната и может использоваться для оценки воздействия кобальта на кожу.Использование этих тестов для обнаружения присутствия этих металлов в продуктах может помочь избежать этого.
Кортикостероиды местного действия
В дополнение к предотвращению воздействия аллергенов в качестве дополнительных мер могут использоваться медицинские методы лечения. Эти методы лечения включают TCS, фототерапию, пероральные ретиноиды и иммунодепрессанты.
TCS широко используются для лечения острых и хронических дерматитов и могут быть достаточными при локализованных поражениях. Автомобиль, однако, является важным фактором.Гели сушат и предпочтительны при остром везикулярном дерматите, тогда как мази наиболее эффективны при хроническом лихенифицированном дерматите. С другой стороны, кремы часто используются, когда пациенты не переносят мази по эстетическим причинам. Следует избегать применения мазей и сильнодействующих фторированных ТКС у маленьких детей и на участках с более тонкой кожей, таких как интертригинозные области, веки и лицо.
Системное лечение
Системные методы лечения могут быть рассмотрены при контактном дерматите, поражающем большую площадь тела или мешающем выполнять важные аспекты повседневной жизни.Острый, обширный и тяжелый дерматит, такой как обширный дерматит Toxicodendron , может потребовать системной терапии, такой как пероральные кортикостероиды. Пациенты должны быть проинформированы о нежелательных эффектах системного лечения кортикостероидами, включая потерю плотности костной ткани, повышение артериального давления, гипергликемию, увеличение веса, катаракту и восприимчивость к инфекции.
Другие методы лечения, включая циклоспорин, азатиоприн и псорален плюс ультрафиолет А, использовались для лечения резистентных к стероидам ACD, таких как хронический дерматит рук.Тем не менее, пациент должен быть проинформирован о рисках и преимуществах этих методов лечения.
Профилактика
Защита кожи может быть полезной, особенно при профессиональном дерматите. Это включает использование средств индивидуальной защиты, таких как перчатки, защитные очки, защитные маски, униформа и хлопковые подкладки под перчатки. В некоторых случаях можно рассмотреть возможность использования специальных кремов для кожи, таких как защитные кремы. Также может быть полезен режим ухода за кожей с увлажняющими средствами для защиты барьерной функции кожи.Для педиатров особенно важно восстановить липидный и водный барьер кожи, чтобы предотвратить трансэпидермальную потерю от повторяющегося влажно-сухого воздействия.
Антигистаминные препараты
Ни зуд, ни воспаление контактного дерматита не поддаются антигистаминной терапии. Однако седативные антигистаминные препараты, такие как дифенгидрамин и гидроксизин, часто назначают, чтобы помочь пациенту спать всю ночь. Актуальные антигистаминные препараты не рекомендуются, так как они могут быть сильными сенсибилизаторами.
Продукты с низким уровнем контакта с аллергенами
До PT или если PT невозможно, устранение наиболее распространенных аллергенов может улучшить дерматит у некоторых пациентов. Сюда входят:
- Аромат (бальзам Перу, смесь ароматов I и II)
- Консерванты, высвобождающие формальдегид (формальдегид, Quaternium-15, диазолидинилмочевина, имидазолидинилмочевина, бронопол, DMDM Hydantoin
- Консервант без формальдегида (MDG / PE)
- MCI / MI и MI
- Ланолин
- CAPB
- Бензофенон-3
У детей, по оценкам, 1/3 детей с ACD потенциально выиграют от стратегии превентивного избегания (P.E.A.S.) [Hill H, Goldenberg A. et al, Стратегия упреждающего избегания (P.E.A.S.) Стратегия упреждающего избегания (P.E.A.S.) — лечение аллергического контактного дерматита в педиатрии; лечение аллергического контактного дерматита в педиатрической популяции. Jour Expert Review of Clinical Immunology 2016, Vol 12 p 551-561] Сюда входит отказ от неомицина, формальдегида, перуанского бальзама, кортикостероидов, смеси ароматизаторов, MCI / MI, ланолина, пропиленгликоля, кокамидопропилбетаина и бензалкония хлорида
Таблица 1: Классификация активности препаратов кортикостероидов для местного применения
Таблица 2: Классификация препаратов кортикостероидов для местного применения на основе структурных свойств (на основе 2 сайтов иммунного распознавания — замены C 6/9 и C16 / 17)
A C17 или C21 сложный эфир с короткой цепью
Гидрокортизон, тиксокортол, клопреднол, дихлоризона ацетат, флудрокортизона ацетат, фторметолон, флупреднизолона ацетат, медризон, мепреднизон, метилпреднизолона ацетат, преднизон натрия фосфат, преднизолона ацетат
B Добавки цис-кеталя C16, C17 или -диола
Амцинонид, будесонид, дезонид, флуоцинолона ацетонид, флуоцинонид, флумоксонид, флунизолид, галцинонид, триамцинолона ацетонид
C C16 метильная группа
Бетаметазон фосфат натрия, дезоксиметазон, дексаметазон-фосфат натрия, дифлюокортолон, флуметазон, флуокортин бутил, флуокортолон, флупрениденацетат, галометазон
D1 C16 метильная группа и галогенированное кольцо B
Дипропионат аклометазона, валерат бетаметазона 17, дипропионат бетаметазона, пропионат клобетазола, бутират клобетазона 17, диацетат дифлоразона, пропионат флутиказона, галобетазол
D2 Лабильные сложные эфиры без метильной группы C16 или галогенированного кольца B
Гидрокортизона ацепонат, гидрокортизона 17-бутират, гидрокортизон-17-валерат, предникарбат, метилпреднизолона ацепонат
Гипериммунное молозиво крупного рогатого скота как недорогой крупномасштабный источник антител против COVID-19
% PDF-1.7
%
1 0 объект
>
эндобдж
72 0 объект
> поток
application / pdf
2021-05-23T10: 09: 02-07: 002021-05-23T10: 09: 02-07: 002021-05-23T10: 09: 02-07: 00uuid: 4fa83f4e-1dd2-11b2-0a00-a80827fd5800uuid: 4fa83f51- 1dd2-11b2-0a00-6a0000000000
конечный поток
эндобдж
2 0 obj
>
эндобдж
3 0 obj
> / MediaBox [0 0 612 792] / Родитель 2 0 R / Ресурсы> / ProcSet [/ PDF / Text] >> / Тип / Страница >>
эндобдж
4 0 obj
> / MediaBox [0 0 612 792] / Родитель 2 0 R / Ресурсы> / ProcSet [/ PDF / Text] >> / Тип / Страница >>
эндобдж
5 0 obj
> / MediaBox [0 0 612 792] / Родитель 2 0 R / Ресурсы> / ProcSet [/ PDF / Text] >> / Тип / Страница >>
эндобдж
6 0 obj
> / MediaBox [0 0 612 792] / Родитель 2 0 R / Ресурсы> / ProcSet [/ PDF / Text] >> / Тип / Страница >>
эндобдж
7 0 объект
> / MediaBox [0 0 612 792] / Родитель 2 0 R / Ресурсы> / ProcSet [/ PDF / Text] >> / Тип / Страница >>
эндобдж
8 0 объект
> / MediaBox [0 0 612 792] / Родитель 2 0 R / Ресурсы> / ProcSet [/ PDF / Text] >> / Тип / Страница >>
эндобдж
9 0 объект
> / MediaBox [0 0 612 792] / Родитель 2 0 R / Ресурсы> / ProcSet [/ PDF / Text] >> / Тип / Страница >>
эндобдж
10 0 obj
> / MediaBox [0 0 612 792] / Родитель 2 0 R / Ресурсы> / ProcSet [/ PDF / Text] >> / Тип / Страница >>
эндобдж
11 0 объект
> / MediaBox [0 0 612 792] / Родитель 2 0 R / Resources> / ProcSet [/ PDF / Text / ImageC] / XObject >>> / Type / Page >>
эндобдж
12 0 объект
> / MediaBox [0 0 612 792] / Родитель 2 0 R / Ресурсы> / ProcSet [/ PDF / Text] >> / Тип / Страница >>
эндобдж
13 0 объект
> / MediaBox [0 0 612 792] / Родитель 2 0 R / Ресурсы> / ProcSet [/ PDF / Text] >> / Тип / Страница >>
эндобдж
14 0 объект
> / MediaBox [0 0 612 792] / Родитель 2 0 R / Ресурсы> / ProcSet [/ PDF / Text] >> / Тип / Страница >>
эндобдж
15 0 объект
> / MediaBox [0 0 612 792] / Родитель 2 0 R / Ресурсы> / ProcSet [/ PDF / Text] >> / Тип / Страница >>
эндобдж
16 0 объект
> / MediaBox [0 0 612 792] / Родитель 2 0 R / Ресурсы> / ProcSet [/ PDF / Text] >> / Тип / Страница >>
эндобдж
17 0 объект
> / MediaBox [0 0 612 792] / Родитель 2 0 R / Ресурсы> / ProcSet [/ PDF / Text] >> / Тип / Страница >>
эндобдж
18 0 объект
> / MediaBox [0 0 612 792] / Родитель 2 0 R / Ресурсы> / ProcSet [/ PDF / Text] >> / Тип / Страница >>
эндобдж
19 0 объект
> / MediaBox [0 0 612 792] / Родитель 2 0 R / Ресурсы> / ProcSet [/ PDF / Text] >> / Тип / Страница >>
эндобдж
20 0 объект
> / MediaBox [0 0 612 792] / Родитель 2 0 R / Ресурсы> / ProcSet [/ PDF / Text] >> / Тип / Страница >>
эндобдж
21 0 объект
> / MediaBox [0 0 612 792] / Родитель 2 0 R / Ресурсы> / ProcSet [/ PDF / Text] >> / Тип / Страница >>
эндобдж
22 0 объект
> / MediaBox [0 0 612 792] / Родитель 2 0 R / Ресурсы> / ProcSet [/ PDF / Text] >> / Тип / Страница >>
эндобдж
23 0 объект
> / MediaBox [0 0 612 792] / Родитель 2 0 R / Ресурсы> / ProcSet [/ PDF / Text] >> / Тип / Страница >>
эндобдж
24 0 объект
> / MediaBox [0 0 612 792] / Родитель 2 0 R / Ресурсы> / ProcSet [/ PDF / Text] >> / Тип / Страница >>
эндобдж
25 0 объект
> / MediaBox [0 0 612 792] / Родитель 2 0 R / Ресурсы> / ProcSet [/ PDF / Text] >> / Тип / Страница >>
эндобдж
26 0 объект
> / MediaBox [0 0 612 792] / Родитель 2 0 R / Ресурсы> / ProcSet [/ PDF / Text] >> / Тип / Страница >>
эндобдж
27 0 объект
> / MediaBox [0 0 612 792] / Родитель 2 0 R / Ресурсы> / ProcSet [/ PDF / Text] >> / Тип / Страница >>
эндобдж
122 0 объект
[124 0 R 125 0 R]
эндобдж
123 0 объект
> поток
HVYoF ~ OT +.Iln`1 (JdLrr% U8i
o & -Et; # Ey @! nw + X] «EyW˹a + -4’iB = c څ RRiGGX * Xi6W ܊ Siϴo + t
t {bÄR] 1FO39ǁг ~ DKI / Вт
Ȍ iDR ܃ G] u ~) WL2QI # s’X = NAmsfa`V
(PDF) Системы доставки для внутрикожной вакцинации
Ding Z, Van Riet E, Romeijn S, Kersten GFA, Jiskoot W, Bouwstra JA (2009a) Модуляция Immune
адъювантами в сочетании с дифтерийным анатоксином, вводимым местно мышам BALB / c
после предварительной обработки набора микроигл. Pharm Res 26: 1635–1643
Ding Z, Verbaan FJ, Bivas-Benita M, Bungener L, Huckriede A, van den Berg DJ, Kersten G,
Bouwstra JA (2009b) Массивы микроигл для чрескожной иммунизации дифтерии
и грипп у мышей BALB / c.J Control Release 136: 71–78
Donnelly RF, Singh TRR, Tunney MM, Morrow DIJ, McCarron PA, O’Mahony C, Woolfson AD
(2009) Массивы микроигл обеспечивают меньшее проникновение микробов, чем иглы для подкожных инъекций в
vitro . Pharm Res 26: 2513–2522
Drabick JJ, Glasspool-Malone J, King A, Malone RW (2001) Кожная трансфекция и иммунные ответы
на внутрикожную вакцинацию нуклеиновой кислотой значительно усиливаются за счет электропермеабилизации in vivo
.Mol Ther 3: 249–255
Drape RJ, Macklin MD, Barr LJ, Jones S, Haynes JR, Dean HJ (2006) Эпидермальная ДНК-вакцина
от гриппа иммуногенна для человека. Vaccine 24: 4475–4481
Epstein JE, Gorak EJ, Charoenvit Y, Wang R, Freydberg N, Osinowo O, Richie TL, Stoltz EL,
Trespalacios F, Nerges J, Ng J, Fallarme-Majam V, Abot E , Goh L, Parker S, Kumar S,
Hedstrom RC, Norman J, Stout R, Hoffman SL (2002) Безопасность, переносимость и отсутствие ответов антител
после введения вакцины против малярии ДНК PfCSP с помощью иглы или
безыгольная струйная инъекция и сравнение внутримышечных и комбинированных внутримышечных /
внутрикожных путей.Hum Gene Ther 13: 1551–1560
Eriksson E, Yao F, Svensjo T, Winkler T, Slama J, Macklin MD, Andree C, McGregor M,
Hinshaw V, Swain WF (1998) Перенос гена in vivo на кожу и рана микропосевом.
J Surg Res 78: 85–91
Etchart N, Hennino A, Friede M, Dahel K, Dupouy M, Goujon-Henry C, Nicolas JF, Kaiserlian D
(2007) Безопасность и эффективность чрескожной вакцинации с использованием пластырь с живой аттенуированной противокоревой вакциной
для человека.Vaccine 25: 6891–6899
Fernando GJP, Chen XF, Prow TW, Crichton ML, Fairmaid EJ, Roberts MS, Frazer IH, Brown
LE, Kendall MAF (2010) Сильный иммунитет к низким дозам гриппозной вакцины по вероятностной оценке
управляемая микротаргетированная доставка кожи в модели мыши. PLoS One 5: e10266
Fishbein DB, Pacer RE, Holmes DF, Ley AB, Yager P, Tong TC (1987) Предэкспозиция бешенства
Профилактика бешенства вакциной против бешенства диплоидными клетками человека: исследование доза-ответ. J Infect Dis
156: 50–55
Flynn PM, Shenep JL, Mao L, Crawford R, Williams BF, Williams BG (1994) Влияние калибра иглы
на кожные пробы Манту.Chest 106: 1463–1465
Foldvari M, Babiuk S, Badea I (2006) Доставка ДНК для вакцинации и лечения через кожу
. Curr Drug Deliv 3: 17–28
Frech SA, Kenney RT, Spyr CA, Lazar H, Viret JF, Herzog C, Gluck R, Glenn GM (2005)
Улучшенный иммунный ответ на вакцинацию против гриппа у пожилых людей с использованием иммуностимулятора
Патч
. Vaccine 23: 946–950
Frech SA, Dupont HL, Bourgeois AL, McKenzie R, Belkind-Gerson J, Figueroa JF, Okhuysen
PC, Guerrero NH, Martinez-Sandoval FG, Melendez-Romero JH, Astur Jiang EJ,
Halpern J, Torres OR, Hoffman AS, Villar CP, Kassem RN, Flyer DC, Andersen BH,
Kazempour K, Breisch SA, Glenn GM (2008) Использование пластыря, содержащего термолабильный токсин из
Escherichia coli против диареи путешественников: рандомизированное двойное слепое плацебо-исследование фазы II.Lancet 371: 2019–2025
Frerichs DM, Ellingsworth LR, Frech SA, Flyer DC, Villar CP, Yu J, Glenn GM (2008)
Контролируемое одноэтапное разрушение рогового слоя в качестве предварительной обработки для иммунизации с помощью
Патч
. Vaccine 26: 2782–2787
Frey SE, Couch RB, Tacket CO, Treanor JJ, Wolff M, Newman FK, Atmar RL, Edelman R,
Nolan CM, Belshe RB (2002) Клинические реакции на неразбавленную и разбавленную противооспенную вакцину .
New Engl J Med 346: 1265–1274
Gardeniers HJGE, Luttge R, Berenschot EJW, de Boer MJ, Yeshurun SY, Hefetz M, van’t Oever
R, van den Berg A (2003) Силиконовая микромашинная полость микроиглы для трансдермальной жидкости
транспорт.J MEMS 12: 855–862
106 Y. C. Kim et al.
Дозировка и введение аплизола | Уровень здоровья
Флаконы с аплизолом
перед введением следует проверить визуально на предмет наличия твердых частиц и обесцвечивания и выбросить, если они обнаружены. Флаконы, использованные более 30 дней, следует выбросить.
Доза 0,1 мл аплизола (туберкулин PPD, разбавленный) эквивалентна дозе 5 туберкулиновых единиц (TU) туберкулина PPD, которая является стандартной дозой, используемой для внутрикожного пробы Манту.
стандартный метод (проба Манту)
Проба Манту выполняется путем внутрикожной инъекции в ладонную часть предплечья с помощью шприца и иглы точно 0,1 мл аплизола. Результат считывается через 48-72 часа, и при интерпретации теста учитывается только пальпируемое уплотнение. Индурация представляет собой твердую приподнятую область с четко определенными краями в месте инъекции и вокруг него (см. Интерпретация туберкулиновой реакции).В месте инъекции может развиться эритема, но она не имеет диагностического значения.
Стандартный тест выполняется следующим образом:
- Испытание проводится на ладонной или тыльной поверхности предплечья примерно на 4 дюйма ниже локтя. Могут использоваться и другие участки кожи, но предпочтительнее ладонная поверхность предплечья. Рекомендуется использовать участок кожи без повреждений и вдали от вен 7
- Кожу в месте инъекции промывают 70% спиртом и дают высохнуть.
- Исследуемый материал вводится с помощью туберкулинового шприца (0,5 или 1,0 мл), снабженного короткой (от 1/4 до 1/2 дюйма) иглой 27 калибра.
- Следует использовать отдельный стерильный одноразовый шприц и иглу.
- Диафрагму пробки флакона следует протереть 70% спиртом.
- Игла вводится через мембрану пробки перевернутого флакона. приняты для исключения пузырьков воздуха и для поддержания просвета иглы заполненным.
- Острие иглы вводится в самые поверхностные слои кожи кончиком иглы вверх. Когда вводится раствор туберкулина, над острием иглы поднимается бледный пузырек размером от 6 до 10 мм (1/3 дюйма). Он быстро впитывается, и повязка не требуется.
- Может быть капля крови когда игла извлечена. Это нормально. Используйте марлевую салфетку и осторожно промокните ее, чтобы удалить кровь. Не надавливайте, так как это может выдавить туберкулин и тем самым нарушить анализ.
В случае, если инъекция вводится подкожно (т. Е. Пузырек не образуется), или если значительная часть дозы вытекает из места инъекции, тест следует немедленно повторить в другом месте на расстоянии не менее 5 см (2 дюйма). ) удален из места первоначальной инъекции.
расшифровка туберкулиновой реакции
Показания реакций Манту должны проводиться квалифицированным медицинским работником в период от 48 до 72 часов после инъекции.При интерпретации теста следует учитывать только индукцию. Диаметр уплотнения следует измерять поперек продольной оси предплечья и записывать в миллиметрах. Эритема не имеет диагностической ценности и не должна приниматься во внимание. Присутствие и размер некроза и отека, если они есть, должны быть зарегистрированы, но не используются при интерпретации теста. При отсутствии уплотнения область эритемы более 10 мм в диаметре может указывать на то, что инъекция была сделана слишком глубоко и показано повторное исследование.Найдите края уплотнения, слегка проведя указательным или средним пальцем по реакционной поверхности. Кончик шариковой ручки, повернутый под углом 45 ° к месту инъекции, также остановится на краях уплотнения.
Диаметр уплотнения следует измерять (предпочтительно штангенциркулем) поперек длинной оси предплечья и записывать в миллиметрах.
Эритема не имеет диагностической ценности и не должна приниматься во внимание. Отсутствие уплотнения следует записывать как «0 мм», а не «отрицательно».
Реакции следует интерпретировать следующим образом (см. Самые последние рекомендации):
Исходя из текущих рекомендаций, 3,7,14, 19 интерпретация реакций следующая:
положительные реакции
| Реакция индурации ≥ 5 мм | Реакция индурации ≥ 10 мм | Реакция индурации ≥ 15 мм |
|---|---|---|
Вирус иммунодефицита человека (ВИЧ) -позитивные Недавние иммигранты (т.д., в течение последних 5 лет) из стран с высокой распространенностью | Лица без факторов риска ТБ | |
Недавние контакты больных туберкулезом (ТБ) | Потребители инъекционных наркотиков | |
Фиброзные изменения на рентгенограмме грудной клетки в соответствии с предшествующим туберкулезом | Жители и сотрудники следующих мест скопления повышенного риска: тюрьмы и тюрьмы, дома престарелых и другие учреждения для престарелых, больницы и др. медицинские учреждения, жилые дома для пациентов с синдромом приобретенного иммунодефицита (СПИД) и приюты для бездомных | |
Пациенты с трансплантатами органов и другие пациенты с ослабленным иммунитетом (получающие эквивалент ≥ 15 мг / сут преднизона в течение 1 мес. или больше) 90 005 | Персонал микобактериологической лаборатории | |
Лица со следующими клиническими состояниями, которые подвергают их высокому риску: силикоз, сахарный диабет, хроническая почечная недостаточность, некоторые гематологические нарушения (например,g., лейкемии и лимфомы), другие специфические злокачественные новообразования (например, карцинома головы или шеи и легких), потеря веса ≥ 10% от идеальной массы тела, гастрэктомия и тощей кишки | ||
Дети младше 4 лет или младенцы, дети и подростки, контактирующие со взрослыми из группы высокого риска |
преобразований кожных проб
- Для лиц с отрицательными реакциями кожных проб, которые проходят повторные кожные пробы (например,g., медицинские работники), увеличение размера реакции ≥ 10 мм в течение 2 лет следует рассматривать как конверсию кожной пробы, указывающую на недавнюю инфекцию M. tuberculosis. 19
- У некоторых людей, инфицированных нетуберкулезными микобактериями или прошедших вакцинацию БЦЖ, кожная проба может показать некоторую степень уплотнения. Для этих людей переход к положительному результату определяется как увеличение уплотнения на 10 мм при последующих тестах. 7
медицинские учреждения и другие учреждения высокого риска
- Для медицинских работников и служащих в других условиях высокого риска, не имеющих других факторов риска туберкулеза, отсечка уплотнения составляет 15 мм (вместо 10 мм) на туберкулиновой кожной пробе следует использовать для определения положительного исходного теста во время первоначального приема на работу.
- Увеличение размера реакции на ≥10 мм обычно считается положительным результатом теста при последующем тестировании, за исключением случаев, когда работник контактирует с больным туберкулезом, не имеет ВИЧ-инфекции или иным образом ослаблен иммунитет, и в этом случае результат ≥5 мм считается положительным. 21
отрицательная реакция
Отрицательная реакция — это уплотнение менее 15 мм у лиц без факторов риска туберкулеза. Это указывает на отсутствие гиперчувствительности к туберкулезу и туберкулезная инфекция маловероятна. 7
Следует отметить, что реактивность на туберкулин может подавляться или подавляться на срок до 5–6 недель вирусными инфекциями, живыми вирусными вакцинами (например, корью, оспой, полиомиелитом, краснухой и эпидемическим паротитом) или после прекращения приема препарата. терапии кортикостероидами или иммунодепрессантами.Недоедание также может иметь аналогичный эффект (см. ПРЕДУПРЕЖДЕНИЯ). При диагностической важности отрицательный результат теста следует рассматривать как доказательство отсутствия гиперчувствительности только после того, как будет продемонстрирована нормальная реактивность на неспецифические раздражители. Первичная инъекция туберкулина может, возможно, оказать стимулирующее действие на последующие туберкулиновые реакции. Педиатрический пациент, который, как известно, контактировал с больным туберкулезом, не должен считаться благополучным до тех пор, пока у этого пациента не появится отрицательная туберкулиновая реакция, по крайней мере, через десять недель после прекращения контакта с больным туберкулезом. 17 Ежегодное тестирование обычно рекомендуется для педиатрических пациентов из групп высокого риска, таких как люди из стран с высокой распространенностью туберкулеза и из групп с низким доходом. 18
Положительная реакция на туберкулин не обязательно означает наличие активного заболевания. Дальнейшие диагностические процедуры (например, рентгенография грудной клетки, мазок мокроты и / или исследование посева) должны быть выполнены до постановки диагноза туберкулеза. Небольшой процент респондентов, возможно, не был инфицирован M.tuberculosis, но некоторыми другими микобактериями. Отрицательный туберкулиновый кожный тест никогда не должен использоваться для исключения возможности активного туберкулеза у лиц, для которых рассматривается диагноз (симптомы, совместимые с туберкулезом).
бустерный эффект и двухэтапное тестирование
Заражение человека туберкулезными палочками или другими микобактериями или вакцинация БЦЖ приводит к замедленной реакции гиперчувствительности на туберкулин, что подтверждается кожной пробой.Отсроченная реакция гиперчувствительности может постепенно уменьшаться в течение нескольких лет. Если человек в это время проходит туберкулиновую пробу, значимой реакции может не выявиться. Однако стимул теста может усилить или увеличить размер реакции на второй тест, иногда вызывая явное преобразование или развитие чувствительности. Этот усиливающий эффект можно увидеть на втором тесте, проведенном через неделю после первоначального стимулирующего теста, и он может сохраняться в течение года, а возможно, и дольше. Когда проводится рутинное периодическое туберкулиновое тестирование взрослых, сначала следует рассмотреть возможность двухэтапного тестирования, чтобы свести к минимуму вероятность интерпретации усиленной реакции как конверсии. 7,15,16
В этом методе тестирования лица с отрицательным исходом кожной пробы проходят вторую туберкулиновую кожную пробу через 1-3 недели после первой. Оба теста следует прочитать и записать через 48–72 часа. Лица с положительной реакцией на второй тест должны считаться ранее инфицированными, а лица с отрицательной реакцией на второй тест должны считаться неинфицированными. У этих неинфицированных людей положительный результат любой будущей кожной пробы следует интерпретировать как конверсию кожной пробы. 7
Консенсусное заявление Испанского общества ревматологов по управлению рисками биологической терапии ревматических пациентов
Введение
Целью данной статьи является разработка рекомендаций по управлению рисками биологической терапии у пациентов с ревматическими заболеваниями, независимо от их причины. болезнь.
Согласно Европейскому агентству по лекарственным средствам, биологическая терапия предназначена для лечения заболеваний; препараты производятся методами биотехнологии, в основном клетки из клеточных банков, за исключением микробных метаболитов, таких как антибиотики, аминокислоты, углеводы и другие вещества с низкой молекулярной массой.Эти методы лечения предназначены специально для воздействия на важную терапевтическую цель, имеющую решающее значение для патогенного процесса заболевания.
В настоящее время в Испании одобрено несколько биологических методов лечения (таблица 1) с показаниями для лечения ревматоидного артрита (РА), анкилозирующего спондилита (АС), псориатического артрита (ПсА), ювенильного идиопатического артрита (ЮИА) и остеопороза (ОП). К ним относятся инфликсимаб (IFX), этанерцепт (ETN), адалимумаб (ADA), анакинра, абатацепт (ABT), ритуксимаб (RTX), тоцилизумаб (TCZ), цертолизумаб (CZP), голимумаб, деносумаб, терипаратид-1– и резус-фактор. 84.
Поскольку деносумаб, терипаратида и rh-ПТГ 1–84 имеют механизм действия и профиль безопасности, очень отличающиеся от других представленных здесь биологических методов лечения, и, учитывая, что они подробно обсуждаются в согласованном документе 2011 года по остеопорозу, этот консенсус будет только предоставлять основные данные о них. Для получения дополнительной информации читатель может обратиться к консенсусу BE 2011 по остеопорозу.
Наконец, мы должны отметить, что этот документ был написан с целью предоставить руководство для всех профессионалов, которые когда-то могут использовать биологическую терапию для лечения пациентов с ревматическими заболеваниями.
Методы
Этот консенсус был разработан на основе других согласованных документов SER, касающихся ведения биологической терапии при РА, 1 СА, ПсА, а также руководств по клинической практике GUIPCAR2 и ESPOGUIA, 3 и других публикаций, представляющих научный интерес. Было сочтено, что управление рисками пациентов, получающих биологическую терапию, — это раздел, который повторяется в различных опубликованных документах, а также зависит от изменчивости группы экспертов, которая его подготовила. Эта изменчивость может привести к противоречивым установкам, поэтому было сочтено целесообразным разработать единый консенсусный документ, отражающий, как следует управлять рисками использования биологической терапии.
Исходя из этого, была создана группа экспертов-ревматологов, которые участвовали в публикации руководств и / или консенсуса, упомянутого ранее. Затем все предыдущие рекомендации различных документов были собраны, изменены или обновлены (если сочтены целесообразными). Впоследствии путем тайного голосования была получена степень согласия (DA) по каждой из рекомендаций. Совокупные результаты этого голосования были показаны всем участникам дискуссии (с изменениями Delphi). Рекомендации, показывающие, что согласие составляет менее 70%, были повторно отредактированы, и голосование по ним проводилось во втором туре.
Уровень доказательности (LE) и степень рекомендации (DR) каждой рекомендации были установлены в соответствии с моделью Центра доказательной медицины Оксфорда7 членами исследовательского подразделения SER.
Предварительные соображения Фармаконадзор и управление рисками
Управление рисками при использовании лекарственных препаратов является важной частью фармаконадзора. Это, в свою очередь, можно определить как деятельность общественного здравоохранения, целями которой являются идентификация, количественная оценка, оценка и профилактика рисков, связанных с наркотиками, после того, как они поступят на рынок, как указано в королевском указе (RD) 1344/2007.
Более конкретно, управление рисками представляет собой набор мероприятий и вмешательств по фармаконадзору, предназначенных для выявления, характеристики и предотвращения или минимизации рисков, связанных с лекарственными средствами, и оценки эффективности таких вмешательств. Все — регулирующие органы / органы здравоохранения, фармацевтические компании, исследователи, медицинские работники и т. Д. — обязаны работать над всеми.
В последние годы, используя биологическую терапию, мы выявили ряд рисков, более или менее связанных с ними.Некоторые из них определены как значимые, то есть те, в отношении которых имеется достаточное свидетельство связи с препаратом, и они очень актуальны. Другие потенциальные риски важны, это означает, что есть основания для подозрений, но нет подтверждения. С другой стороны, следует отметить, что в настоящее время у нас нет достаточной информации по конкретным случаям, например, в так называемых особых ситуациях (беременность, кормление грудью и т. Д.).
На основании вышеизложенного, управление рисками в отношении использования биологической терапии осуществляется в следующие моменты / обстоятельства (обсуждаемые в документе): показания, начало лечения, мониторинг и оценка нежелательных явлений, возникающих во время лечение.В большинстве случаев / обстоятельств есть доказательства того, что лучше всего вести себя.
Нормативно-правовая база в отношении употребления наркотиков в Испании
Наконец, вспомните правовую базу, в которой мы живем. RD 1345/2007 регулирует разрешенное использование лекарств, а RD 1015/2009 — использование лекарств в особых ситуациях. Вся документация доступна на веб-сайте Испанского агентства по лекарственным средствам и изделиям медицинского назначения (AEMPS) .8
Одобренные лекарственные препараты
Лекарства можно использовать при состоянии, для которого имеется разрешенное показание (нормальное использование, лист показаний).
Лекарства в особых ситуациях Использование исследуемых препаратов
AEMPS может разрешить использование исследуемых препаратов до их продажи в Испании отдельным пациентам, не имеющим удовлетворительной терапевтической альтернативы, тем, кто не участвует в клинических испытаниях и находится в клинической ситуации, которая не может ждать по окончании исследования и новые методы лечения разрешены. Таким образом, доступ к этим лекарствам может быть запрошен индивидуально для пациента, как это делается до сих пор (использование из сострадания), или при получении временного разрешения на использование AEMPS для группы пациентов.
Использование лекарств для состояний, отличных от разрешенных.
Это относится к использованию лекарств по нелицензированным показаниям (использование не по назначению или вне разрешенных условий использования). За такое использование отвечает лечащий врач для индивидуального использования, но AEMPS, если сочтет это целесообразным, может регулировать его использование для этого нелицензированного показания. В этом случае рекомендации по использованию или неиспользованию будут иметь исковую силу.
Иностранные лекарства
AEMPS может разрешить использование отдельных лекарств, которые не разрешены в Испании, которые продаются в других странах и использование которых является существенным.
Управление рисками и показания к биологической терапии
Расчетная польза / риск для отдельного пациента должна основываться на всех доступных знаниях с момента показания. Следовательно:
Комиссия считает, что лечение биологическими препаратами должно проводиться опытными врачами, которые привыкли управлять заболеваниями, для которых они показаны (LE 5, DR D, DA 100%).
Пожалуйста, ознакомьтесь с официальным списком всех биологических агентов и соблюдайте его рекомендации перед их использованием в клинической практике (LE 5, DR D, DA 91%).
Имеются данные о том, что использование не по назначению может быть связано с большим количеством побочных эффектов, чем когда схема приема лекарств была одобрена для такого показания, и пациент, которому это прописано, должен быть как можно ближе к профилированному показанию.
Следует помнить, что назначение биологической терапии пациентам с увеитом в анамнезе в настоящее время не разрешено; следовательно, это будет означать нелицензионное указание. В этом контексте врач должен взвесить относительный риск, связанный с различными лекарствами, и проконсультироваться с офтальмологом, прежде чем решить, начинать ли лечение биологическими препаратами и если да, то какие.10,11
Сводка таблиц данных биологической терапии приведена в таблице 1.
Управление рисками перед началом лечения
Каждый пациент, начинающий лечение биологической терапией, должен пройти предварительную оценку для выявления и / или предотвращения потенциальных рисков и следует регулярно контролировать во время терапии (LE 5, DR D, DA 100%).
Перед тем, как начать прием первой дозы, врач должен собрать достаточно информации о потенциальных рисках для конкретного пациента, которому было прописано лекарство.Для этого мы советуем провести серию скрининговых или скрининговых мероприятий, направленных на выявление сопутствующих заболеваний, но также предлагаем активные меры для минимизации возможных побочных реакций, такие как предоставление достоверной информации пациентам и персоналу, который будет управлять терапией и профилактикой.
Мониторинг пациента должен быть регулярным и адаптированным к характеристикам пациента и организации отделения; рекомендуется проводить по крайней мере одну оценку в месяц, а затем каждые 1–4 месяца, независимо от того, кто ее проводит и как она проводится.
Каждый раз, когда начинается лечение биологической терапией, пациента следует проинструктировать о предупреждающих знаках, на которые следует обратить внимание, как о возможных индикаторах риска (УД 5, ДР D, DA 91%).
При назначении биологической терапии, независимо от заболевания, пациента следует проинструктировать о симптомах / признаках, на которые следует обратить внимание, и о том, что делать в случае их появления. Пациент должен знать и осознавать эти риски; по крайней мере, самые частые. Точно так же врач может указать изменения в образе жизни, которые помогут снизить некоторые риски.Вся эта информация доступна во многих ревматологических отделениях или на сайте SER12.
Врач, назначивший лекарство или назначенный для этой цели, должен направлять управление рисками лечения биологическими препаратами; однако в этом должен участвовать весь медицинский персонал, включая медсестер, семейных врачей, больничную аптеку и пациента (LE 5, DR D, DA 100%).
Информация врача, выписывающего рецепт, одного наблюдающего (если другой) и медсестры должна быть согласованной, для чего важно иметь поддержку письменной документации, определенных процессов и четких и точных процедур, брошюр, руководств по эксплуатации и т. Д. и т.п.
В Таблице 2 представлены действия по предварительной оценке, рекомендованные в начале лечения. Хотя профиль безопасности не совпадает с различными вариантами биологической терапии с имеющейся в настоящее время информацией, за исключением деносумаба, терипаратида и rh-PTH 1–84, комиссия считает, что следующие рекомендации применимы ко всем пациентам, которые будут проходить биологическую терапию. .
У пациента, который собирается начать биологическое лечение, оценить возможное наличие активной инфекции; их наличие является противопоказанием к биологической терапии (LE 2b, DR B, DA 96%).
Испанский регистр побочных реакций на биологические методы лечения (BIOBADASER) и другие записи и / или исследования выявили повышенную частоту инфекций у пациентов, получавших эти методы лечения, независимо от исходного заболевания.13–28
Использование биологических методов лечения в пациенты с рецидивирующими инфекциями, сепсисом или с высоким риском развития инфекции в анамнезе ненадежны и требуют соответствующего баланса риска и пользы и максимального наблюдения. Врачам также не следует начинать лечение этими препаратами при наличии активной, системной или локальной инфекции.В этом смысле наличие в анамнезе инфицированного протезного сустава требует до начала биологической терапии соответствующего терапевтического подхода (хирургическое вмешательство с радикальным удалением инфекции и, если показано, замена протеза).
В связи с ростом численности иммигрантов и в соответствии с их географическим происхождением рекомендуется оценить возможную реактивацию необычных инфекций в нашей окружающей среде.
После разрешения инфекции можно начинать биологическую терапию.
Комиссия считает необходимым исключить у любого пациента, которому предстоит пройти биологическую терапию, наличие активного туберкулеза или недавнего контакта с больными туберкулезом и изучить возможность латентной инфекции туберкулеза. Важно регистрировать в истории болезни любой недавний контакт с больными туберкулезом и туберкулезом и выполнять рентгенографию грудной клетки, чтобы исключить активный туберкулез или рентгенологические доказательства, соответствующие старой туберкулезной инфекции, а также выполнить кожную пробу на туберкулез (PPD). , который необходимо повторить (повторный тест) через 1-2 недели при
мм (LE 2b, DR B, DA 100%).
Более высокая заболеваемость туберкулезом (ТБ) была обнаружена у пациентов, получающих антагонисты ФНО, особенно моноклональные антитела.5,23,24,29-31 Кроме того, скрининг был связан со снижением риска реактивации латентного ТБ5,32 PPD считается положительным при повторном тесте или у пациента, подвергающегося иммуносупрессии, с уплотнением, превышающим или равным 5 мм, через 72 часа. Результат следует учитывать независимо от предыдущей вакцинации от туберкулеза. Также важно информировать пациентов о рисках, связанных с контактом с пациентами с активным туберкулезом.
Лечение латентной туберкулезной инфекции должно быть начато до начала биологической терапии в следующих случаях: (1) недавний контакт с пациентом с задокументированным туберкулезом, (2) история частично пролеченного туберкулеза, (3) или положительный тест PPD или повторный -контрольная работа; (4) остаточные поражения на рентгенограмме грудной клетки. Для лечения латентной туберкулезной инфекции предпочтительным вариантом является изониазид (от 5 мг / кг / день до 300 мг в день) с витамином B6 в течение 9 месяцев (LE 2b, DR B, 96 DA%).
В случае непереносимости изониазида рекомендуется применять рифампицин в дозах 10 мг / кг / день (максимум 600 мг в день) в течение четырех месяцев.Эффективность этих рекомендаций для предотвращения реактивации латентного туберкулеза была продемонстрирована32. Появляются исследования коротких курсов лечения33 с использованием различных препаратов, хотя мы ожидаем подтверждения их эффективности у пациентов с ослабленным иммунитетом.
Если пациент получил адекватное лечение латентной ТБ-инфекции, в активной профилактике или тестировании Манту нет необходимости (УД 5, ДР D, DA 96%). Однако за такими пациентами рекомендуется наблюдение.
Перед тем, как начать биологическое лечение, врач должен принять во внимание наличие злокачественных новообразований в анамнезе.Если в анамнезе имеется серьезная история рака, следует оценить его биологию и поведение, обсудив с онкологом и пациентом риск рецидива. Мы не рекомендуем использовать биологическую терапию у пациентов с лимфопролиферативными заболеваниями в анамнезе (LE 4, DR C, DA 91%).
В настоящее время нет доказательств повышенного риска солидных опухолей у пациентов, получающих биологическую терапию18,34,35, хотя, по-видимому, существует повышенный риск в отношении немеланоцитарных опухолей кожи (базальных), по крайней мере, у пациентов с РА.36 Таким образом, у пациентов с солидными опухолями в анамнезе показание к биологической терапии будет определяться ее рисками и преимуществами.
С другой стороны, существуют противоречивые данные относительно риска развития лимфопролиферативного заболевания при использовании антагонистов TNF (см. Таблицы данных) при РА, 37–41, и, похоже, существует связь в SA42. не совсем ясно, мы не рекомендуем использовать антагонисты TNF, если в анамнезе имеется лимфопролиферативное заболевание.
Перед началом биологического лечения пациентов следует обследовать на предмет сердечной недостаточности (уровень доказательности 4, уровень риска C, уровень DA 91%).
Хотя доступные данные (относительно антагонистов TNF и RTX) не совсем согласованы43–45 для пациентов с легкой сердечной недостаточностью, пациенты должны находиться под наблюдением и прекращение лечения в случае ухудшения сердечной недостаточности. Не начинайте лечение пациентов с функциональным классом III или IV по NYHA.
Как правило, биологическая терапия должна быть индивидуализирована для пациентов с основным интерстициальным заболеванием легких (No.4, GR C, GA 96%).
Использование биологической терапии у пациентов с интерстициальным заболеванием легких может быть связано с риском (хотя мало изученным и определенным) ухудшения или летального исхода.46,47 Этот риск может быть повышен у пациентов с предшествующим анамнезом заболевания легких, и наихудшие исходы были зарегистрированы у пациентов с обычным интерстициальным пневмонитом, поэтому следует уделять особое внимание этой информации.46,47 В ожидании дополнительных данных о его применении лечение этих пациентов должно быть индивидуальным.
Перед началом биологического лечения оцените наличие цитопений и не начинайте лечение, пока они не исчезнут (УД 2b, DR B, DA 74%).
В случаях тяжелой цитопении не рекомендуется начинать лечение до ее исчезновения. С другой стороны, поскольку цитопения может быть вызвана активностью основного заболевания, необходимо изучить их происхождение и принять соответствующие меры.
Перед тем, как начать биологическое лечение, оцените наличие демиелинизирующего заболевания и избегайте лечения пациентов с явным анамнезом таких процессов (уровень доказательности 2b, DR B, DA 91%).
Были сообщения о демиелинизирующих заболеваниях при использовании антагонистов TNF48-50, и, согласно их данным, существует потенциальный риск при TCZ и ABT, хотя неясно, действительно ли использование этих препаратов увеличивает риск Это. Этот скрининг может проводиться клинически, а в случае сомнений — консультироваться с неврологом или специалистом. В случае предшествующего демиелинизирующего заболевания показания к биологической терапии следует оценивать индивидуально с учетом ее рисков и преимуществ, но, как правило, этого следует избегать.
Обнаружение серологических маркеров рекомендуется для HCV и HBV (LE 4, DR C, DA 100%).
Сообщалось о случаях реактивации инфекции и даже печеночной недостаточности у пациентов с HBV и принимающих антагонисты TNF.51–53 Нет данных о реактивации54 относительно использования RTX. В случае HCV неясно, вызывает ли лечение антагонистами TNF или использование ABT ухудшение функции печени или повышение вирусной нагрузки, и улучшение даже было описано в некоторых функциональных тестах.55–59 Случай RTX не ясен. 60,61 В связи с вирусом иммунодефицита человека (ВИЧ) есть ряд случаев, в которых биологические агенты были эффективны, но которые также показали рост инфекций62. , мы считаем, что каждый случай должен быть индивидуализирован, а соотношение риск / польза должно оцениваться. И, особенно в случае HBV, мы рекомендуем предварительную совместную оценку гепатологом / специалистом по инфекционным заболеваниям для мониторинга риска реактивации и оценки решения о назначении и поддержании противовирусных препаратов.
Пациентам, проходящим биологическую терапию, рекомендуются следующие вакцины: пневмококковая вакцина и вакцина против гриппа (LE 3b, DR C, DA 96%).
С другой стороны, использование живых аттенуированных вакцин противопоказано. Учитывая степень иммуносупрессии, вызванную биологической терапией, потенциальный риск заражения при их назначении может быть важным, и их использование не рекомендуется.
В принципе, при отсутствии других факторов риска могут быть назначены другие вакцины.Более подробную информацию о вакцинах можно найти в Таблице 3.
Пациентам с отрицательными маркерами гепатита B вакцинация рекомендуется до начала биологической терапии (LE 3b, DR C, DA 78%).
Что касается вакцин, несколько публикаций показали хороший гуморальный ответ в случае антагонистов TNF и ABT для таких микроорганизмов, как вирус гриппа, пневмококк или столбнячный токсин, 63–66, но пока что противоречивый для RTX.67,68 В отношении других препаратов информации недостаточно.
В любом случае всегда учитывайте, что эти вакцины могут оказаться неэффективными, если у пациента наблюдается интенсивная иммуносупрессия. После начала терапии нельзя использовать биологические вакцины, содержащие живые бактерии. Для получения дополнительной информации см. Таблицу 3.
Не рекомендуется беременность и кормление грудью пациентам, которые будут начинать биологическую терапию; Применение деносумаба противопоказано при беременности и в период лактации (LE 3b, DR C, DA 91%).
В целом, хотя данных 69–71 недостаточно, использование биологической терапии во время беременности и кормления грудью не рекомендуется.Важно, чтобы пациенты и их врачи обсуждали планирование беременности в связи с использованием этих терапевтических средств.
Управление рисками во время последующего наблюдения
Во время воздействия лекарственного препарата временные интервалы для систематического мониторинга конкретных событий должны устанавливаться как можно более регулярно (LE 5, DR D, DA 100%).
Управление рисками во время лечения с помощью биологических методов лечения и клинической оценки включает физикальное обследование и лабораторные тесты (лабораторные, визуализационные и т. Д.)) в зависимости от каждого препарата и клинической ситуации (LE 5, DR D, DA 91%).
Лечение следует проводить в сотрудничестве и при общении с лечащим врачом (NE 5, GR D GA 96%).
Было показано, что тщательный и систематический мониторинг сводит к минимуму побочные эффекты любого препарата. Действительно, тщательный мониторинг является стандартом в клинических испытаниях, и побочные эффекты возникают реже. Любые средства для облегчения связи между первичной медицинской помощью и диспетчером, включая пациента с любым из них, приводят к ожидаемому положительному влиянию на безопасность пациента.
Во время последующего наблюдения особое внимание следует уделять скринингу на нежелательные явления, особенно инфекции, болезни легких, сердечную недостаточность, а также на конкретные случаи лабораторных отклонений (изменения крови, липидов, функции печени), а также мониторинг контакта с инфекционными больными (туберкулезом или ветряной оспой среди других) (LE 5, DR D, DA 96%).
Для получения более подробной информации об управлении риском во время лечения биологической терапией см. Таблицы 1 и 2.
Рекомендуется внимательно наблюдать за пациентами с активной инфекцией HBV, HCV или ВИЧ, если они начинают биологическую терапию (уровень доказательности 5; DR B, DA 100%).
Хотя доказательств все еще мало, 51,55–58,62, если врач наконец решит начать биологическую терапию у пациентов с HBV, HCV или ВИЧ, мониторинг должен включать, по крайней мере, серологию, вирусную нагрузку, количество CD4 и функцию печени. контрольная работа. В случае HBV необходимо оценить использование противовирусной терапии, а в случае ВИЧ биологическая терапия всегда должна быть связана с интенсивной антиретровирусной терапией (которая должна начинаться до начала лечения). Как уже говорилось выше, в случае сомнений мы рекомендуем проконсультироваться со специалистом.
Отношение к нежелательным явлениям
Врач должен обращать особое внимание на возможное развитие инфекций во время лечения. В этой ситуации необходимы диагностика и лечение случаев, а также временное прекращение биологической терапии. Как только инфекция исчезнет, лечение можно возобновить (УД 2b, DR B, DA 100%).
Инфекции — наиболее частые события. Иногда они могут быть сложными и / или серьезными, и важно всегда подозревать их наличие.13,20,29,72–76 При использовании TCZ сообщалось о случаях дивертикулита с перфорацией кишечника, 77 поэтому все пациенты с клиническими симптомами острый живот / подострое состояние следует оценить на предмет этой возможности.
Во время наблюдения рекомендуется узнать о возможности контакта с больными туберкулезом. Если положительный или сомнительный, повторите кожную пробу на туберкулез или лечите контакт изониазидом (LE 5, DR D, DA 91%).
Даже если перед лечением был проведен скрининг или фармакологическая профилактика туберкулеза, возможность заражения туберкулезом все еще существует, поэтому необходимо рассмотреть эту возможность для последующего наблюдения и действовать соответствующим образом.
Тест QuantiFERON — это иммунный экспресс-тест in vitro, измеряющий продукцию IFN-γ циркулирующими мононуклеарными клетками в ответ на антигены, и он более специфичен для выявления туберкулезной инфекции, чем PPD.Его использование у пациентов с иммуноопосредованными воспалительными заболеваниями показало сильную корреляцию с факторами риска туберкулеза и низкий процент неопределенных результатов. Однако необходимы дополнительные исследования для оценки его использования у пациентов, принимающих антагонисты TNF78.
Нет данных, подтверждающих минимальные сроки, необходимые для лечения туберкулеза до начала биологической терапии. Клинический опыт подсказывает, что рекомендуется применять его как можно дольше, всегда сохраняя активность болезни на достаточно низком уровне.
Если у пациента развивается рак во время лечения биологическим агентом, его следует прекратить (уровень доказательности 2b, DR B, DA 96%).
Особое внимание следует уделять выявлению злокачественных новообразований.36,39,42,79–82 Среди других ситуаций клиническое подозрение должно быть установлено, когда обнаруживается несоответствие между клиническими симптомами и уровнями в сыворотке реагентов острой фазы количество лейкоцитов или концентрация гемоглобина.83
Также рекомендуется объяснить пациенту важность наблюдения и сообщения о любых изменениях на коже.
Врач должен быть особенно осторожен с антагонистами TNF и RTX у пациентов с сердечной недостаточностью, так как это состояние может значительно ухудшиться, и в этом случае прием препарата следует прекратить (уровень доказательности 4, DR C, DA 91%).
Хотя это требует дополнительных доказательств, 43,44 в случае клинических и / или ультразвуковых доказательств ухудшения сердечной недостаточности лечение следует прекратить.
У пациентов с интерстициальным заболеванием легких, получавших биологическую терапию, следует строго контролировать клиническую и легочную функцию, а в случаях клинического ухудшения и расширения поражений биологическую терапию следует прекратить (уровень доказательности 4; DR C, DA 96%).
Сообщалось об ухудшении интерстициального заболевания легких с летальным исходом у пациентов, получавших антагонисты ФНО, 46,47 хотя недавно сообщалось, что смертность у пациентов с РА и интерстициальным заболеванием легких увеличивается при приеме антагонистов ФНО по сравнению с традиционными БПВП. Доля смертей, связанных с интерстициальным заболеванием легких, выше у пациентов, получавших антагонисты TNF, хотя может иметь место информационная погрешность.84 Это малоизученный предмет, в котором причинно-следственная связь плохо определена, поэтому пока ждем большего доказательства этого, соотношение риск / польза следует оценивать индивидуально.
В случае тяжелой цитопении во время лечения биологической терапией ее следует прекратить и изучить другие возможные причины, прежде чем связывать ее с биологической терапией. Как только этот вопрос будет решен, он может быть восстановлен (УД 4, DR C, DA 96%).
Были редкие случаи тяжелой лейкопении или тромбоцитопении и апластической анемии у пациентов, получающих биологическую терапию85; в этом случае и если это связано с этими препаратами, отмена препарата до исчезновения и оценка его повторного введения являются обязательными.Из-за своего механизма действия RTX может вызвать лимфопению, которая (сама по себе) не является причиной для приостановки. В случае TZC цитопения часто возникает из-за фармакодинамического эффекта, и существуют рекомендации по лечению (в литературе и ее технических данных). С другой стороны, анемия, лейкопения, лимфопения или тромбоцитопения могут быть результатом активности заболевания. В любом случае врач должен изучить их происхождение и выбрать курс действий, исходя из соотношения польза / риск.
В случае возникновения волчаночного синдрома или других аутоиммунных заболеваний необходимо прекратить соответствующее лечение биологической терапией (УД 2b, DR B, DA 96%).
Несмотря на то, что эти явления встречаются редко, их следует контролировать.86–88 Присутствие типичных антител к волчанке при отсутствии других признаков или симптомов является основанием для приостановки.
Антагонисты TNF и TCZ следует прекратить в случае, совместимом с демиелинизирующим невритом зрительного нерва (LE 2b, DR B, DA 96%).
Лечение антагонистами TNF и TCZ было связано с появлением неврита зрительного нерва, рассеянного склероза и других демиелинизирующих заболеваний, 49,50, поэтому в случае возникновения следует приостановить прием препаратов.
В случае активации или появления гепатита B, C или ВИЧ противовирусное лечение должно быть связано с биологической терапией (LE 4, DR C, DA 87%).
В самой большой на сегодняшний день серии: 14 пациентов с хронической инфекцией HBV, 19 пациентов, вакцинированных от HBV, и 19 пациентов с разрешенной инфекцией HBV получали пероральную противовирусную терапию в сочетании с антагонистами TNF. Во время лечения уровни поверхностных антител к HBV исчезли или снизились. Проблем с безопасностью не обнаружено.89 Однако нельзя исключать вариант временного прекращения биологической терапии до установления эффективного контроля репликации вируса.
В случае псориатических поражений у пациентов, получающих биологическую терапию, следует назначить соответствующее лечение поражений и оценить его приостановку в случае неудачи или серьезного поражения кожи (уровень доказательности 4, степень риска C, DA 96%).
Поступали сообщения о кожном псориазе, в основном на ладонях рук и подошвах ног, а также об обострении или изменении морфологии ранее существовавших псориатических поражений при применении этих препаратов 90–93, что требует бдительности в отношении их возможное появление.
Управление рисками в особых ситуациях
Если беременность наступает во время лечения биологической терапией, ее следует прекратить (уровень доказательности 4, DR C, DA 78%).
Если наступила беременность, прекратите лечение биологическим агентом.69,70,94 Для получения дополнительной информации см. Таблицу 4. У мужчин, в принципе, хотя предполагалась возможность ассоциации с астеноазооспермией и снижением подвижности сперматозоидов, 95–98 не является убедительным доказательством снижения фертильности у мужчин, принимающих антагонисты TNF.
Пациентам с биологической терапией, перенесшим обширную плановую операцию, рекомендуется временно приостановить лечение (LE 4, DR C, DA 96%).
Хотя убедительных доказательств нет, 99–103 группа рекомендует временно приостановить биологическую терапию, когда пациенту предстоит серьезная плановая операция.

 Увеличивается риск заражения ранки.
Увеличивается риск заражения ранки.