Синдром аспирации мекония — Meconium aspiration syndrome
Состояние здоровья новорожденных
| Синдром аспирации мекония | |
|---|---|
| Другие названия | Неонатальная аспирация мекония |
| Рентгеновский снимок, показывающий степень повреждения эпителия легких в ответ на меконий у новорожденных с синдромом аспирации мекония. | |
| Специальность | Неонатология |
Синдром аспирации мекония ( MAS ), также известный как неонатальная аспирация мекония, представляет собой заболевание, поражающее новорожденных. Он описывает спектр заболеваний и патофизиологию новорожденных, рожденных в околоплодных водах, окрашенных меконием (MSAF) и имеющих меконий в легких. Таким образом, MAS имеет широкий диапазон степени тяжести в зависимости от того, какие состояния и осложнения развиваются после родов. Более того, патофизиология MAS многофакторна и чрезвычайно сложна, поэтому она является ведущей причиной заболеваемости и смертности доношенных детей.
Более того, патофизиология MAS многофакторна и чрезвычайно сложна, поэтому она является ведущей причиной заболеваемости и смертности доношенных детей.
Слово меконий происходит от греческого слова mēkōnion, означающего сок из опийного мака, поскольку успокаивающее действие, которое он оказывал на плод, наблюдал Аристотель .
Меконий представляет собой липкое темно-зеленое вещество, которое содержит желудочно-кишечные выделения, околоплодные воды , желчные кислоты , желчь , кровь, слизь , холестерин , выделения поджелудочной железы, лануго , верникса казеозу и клеточный мусор. Меконий накапливается в желудочно-кишечном тракте плода в течение третьего триместра беременности, и это первые выделения из кишечника в течение первых 48 часов после рождения. Примечательно, что поскольку меконий и все содержимое желудочно-кишечного тракта расположены «экстракорпорально», его составляющие скрыты и обычно не распознаются иммунной системой плода.
Чтобы меконий в околоплодных водах мог успешно вызвать МАС, он должен попасть в дыхательную систему в период, когда заполненные жидкостью легкие превращаются в наполненный воздухом орган, способный к газообмену .
Причины
Основные теории прохождения мекония в околоплодные воды вызваны зрелостью плода или стрессом плода в результате гипоксии или инфекции. К другим факторам, способствующим прохождению мекония в утробе матери, относятся плацентарная недостаточность, гипертония у матери, преэклампсия и употребление табака и кокаина матерью . Однако точный механизм перехода мекония в амниотическую жидкость до конца не изучен, и это может быть комбинация нескольких факторов.
Переход мекония в результате дистресса плода
Может быть важная связь между дистрессом плода и гипоксией с MSAF. Считается, что дистресс плода перерастает в гипоксию плода, заставляя плод испражняться меконием, что приводит к MSAF, а затем, возможно, к MAS. К другим факторам стресса, вызывающим дистресс плода и, следовательно, переход мекония, относятся случаи, когда насыщение кислородом пупочной вены ниже 30%.
К другим факторам стресса, вызывающим дистресс плода и, следовательно, переход мекония, относятся случаи, когда насыщение кислородом пупочной вены ниже 30%.
Гипоксический стресс плода во время родов может стимулировать деятельность толстой кишки за счет усиления перистальтики кишечника и расслабления анального сфинктера, что приводит к прохождению мекония. Затем из-за внутриматочного вдоха или из-за первых нескольких вдохов после родов может развиться МАС. Кроме того, аспирация густого мекония приводит к обструкции дыхательных путей, что приводит к более тяжелой гипоксии .
Важно отметить, что связь между патологическим состоянием плода и пассажем мекония не является определенной причинно-следственной связью, поскольку более четверти детей с MSAF активны при рождении и не имеют дистресса или гипоксии. Кроме того, дистресс плода часто возникает без прохождения мекония.
Переход мекония в результате зрелости плода
Хотя меконий присутствует в желудочно-кишечном тракте на ранней стадии развития, MSAF редко возникает до 34 недель беременности .
Перистальтика кишечника плода присутствует уже на 8 неделе беременности, а анальный сфинктер развивается примерно на 20–22 неделе. Ранние механизмы контроля анального сфинктера изучены недостаточно, однако есть свидетельства того, что плод регулярно испражняется в амниотическую полость даже при отсутствии дистресса. Присутствие кишечных ферментов плода было обнаружено в околоплодных водах у женщин на сроке беременности 14–22 недели. Таким образом, предполагается, что кишечное содержимое свободно попадает в амниотическую жидкость.
Мотилин обнаруживается в более высоких концентрациях в желудочно-кишечном тракте плода после родов по сравнению с недоношенными. Точно так же кишечная парасимпатическая иннервация и миелинизация также усиливаются на более поздних сроках беременности. Следовательно, повышенная частота MAS при переношенных беременностях может отражать созревание и развитие перистальтики желудочно-кишечного тракта у новорожденного.
Патофизиология
Поскольку MAS описывает спектр заболеваний у новорожденных, рожденных через MSAF, без каких-либо врожденных респираторных нарушений или другой основной патологии, существует множество предполагаемых механизмов и причин возникновения этого синдрома.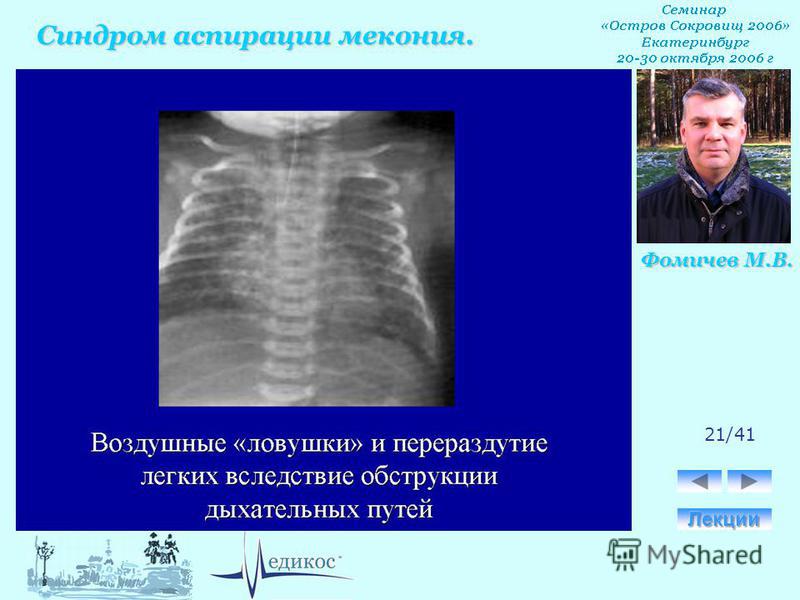 Эти расстройства могут иметь долгосрочные последствия, например, у младенцев, у которых развивается MAS, более высокая частота развития дефектов развития нервной системы из-за плохого дыхания.
Эти расстройства могут иметь долгосрочные последствия, например, у младенцев, у которых развивается MAS, более высокая частота развития дефектов развития нервной системы из-за плохого дыхания.
Обструкция дыхательных путей
В первые 15 минут аспирации мекония наблюдается обструкция более крупных дыхательных путей, которая вызывает повышенное сопротивление легких, снижение эластичности легких , острую гипоксемию , гиперкапнию , ателектаз и респираторный ацидоз . После 60 минут воздействия меконий попадает в более мелкие дыхательные пути. Попадая в конечные бронхиолы и альвеолы, меконий вызывает воспаление, отек легких , вазоконстрикцию , бронхоспазм , коллапс дыхательных путей и инактивацию сурфактанта .
Гипоксия плода
Области легких, которые не участвуют или участвуют лишь частично в вентиляции из-за обструкции и / или разрушения, станут гипоксичными, что может привести к воспалительной реакции. Частичная обструкция приведет к скоплению воздуха и гиперинфляции определенных участков легких, что может привести к пневмотораксу . Хроническая гипоксия приводит к повышению тонуса гладких мышц легочных сосудов и стойкой легочной гипертензии, вызывая нарушение дыхания и кровообращения.
Хроническая гипоксия приводит к повышению тонуса гладких мышц легочных сосудов и стойкой легочной гипертензии, вызывая нарушение дыхания и кровообращения.
Инфекционное заболевание
Микроорганизмы, чаще всего грамотрицательные палочки, и эндотоксины обнаруживаются в образцах MSAF чаще, чем в прозрачных околоплодных водах, например, у 46,9% пациентов с MSAF также присутствовали эндотоксины. Микробная инвазия в амниотическую полость (MIAC) чаще встречается у пациентов с MSAF, что в конечном итоге может привести к внутриамниотической воспалительной реакции. MIAC связан с высокими концентрациями цитокинов (таких как IL-6 ), хемокинов (таких как IL-8 и хемоаттрактантный белок-1 моноцитов ), комплемента , фосфолипазы A 2 и ферментов, разрушающих матрикс. Следовательно, эти вышеупомянутые медиаторы в околоплодных водах во время MIAC и внутриамниотической инфекции могут при аспирации в утробе матери вызвать воспаление легких у плода.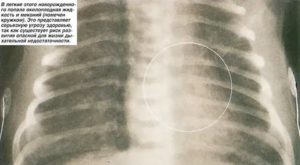
Легочное воспаление
Меконий имеет сложный химический состав, поэтому сложно выделить один агент, ответственный за несколько возникающих заболеваний. Поскольку меконий хранится внутри кишечника и частично не подвергается воздействию иммунной системы , при его аспирации врожденная иммунная система распознает чужеродное и опасное вещество. Иммунная система, которая присутствует при рождении, реагирует в течение нескольких минут с низкой специфичностью и без памяти, чтобы попытаться уничтожить микробы . Меконий, возможно, приводит к химическому пневмониту, поскольку он является мощным активатором медиаторов воспаления, которые включают цитокины , комплемент , простагландины и активные формы кислорода .
Меконий является источником провоспалительных цитокинов , в том числе фактора некроза опухоли (TNF) и интерлейкинов ( IL-1 , IL-6 , IL-8 ), а также медиаторов, продуцируемых нейтрофилами , макрофагами и эпителиальными клетками, которые могут напрямую поражать ткань легких.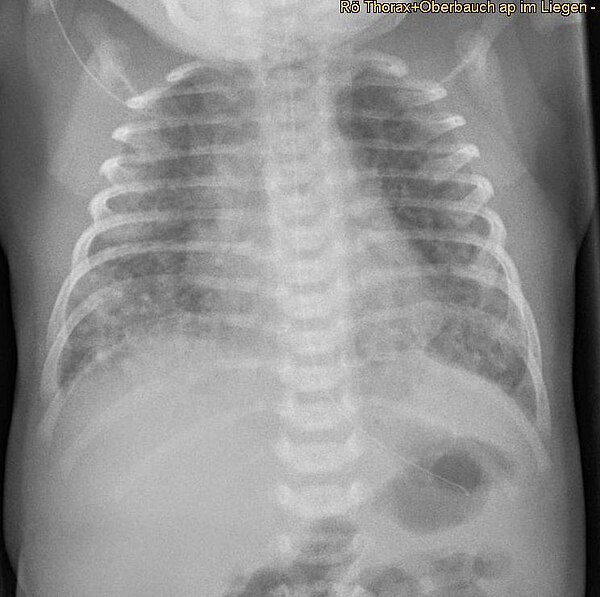 или косвенно. Например, протеолитические ферменты высвобождаются из нейтрофильных гранул, и они могут повредить легочную мембрану и сурфактантные белки. Кроме того, активированные лейкоциты и цитокины генерируют активные формы азота и кислорода, которые обладают цитотоксическим действием. Окислительный стресс приводит к сужению сосудов , бронхоспазму , агрегации тромбоцитов и ускоренному апоптозу клеток . Недавно была выдвинута гипотеза, что меконий является мощным активатором толл-подобных рецепторов (TLR) и комплемента , ключевых медиаторов воспаления, и, таким образом, может способствовать воспалительной реакции при MAS.
или косвенно. Например, протеолитические ферменты высвобождаются из нейтрофильных гранул, и они могут повредить легочную мембрану и сурфактантные белки. Кроме того, активированные лейкоциты и цитокины генерируют активные формы азота и кислорода, которые обладают цитотоксическим действием. Окислительный стресс приводит к сужению сосудов , бронхоспазму , агрегации тромбоцитов и ускоренному апоптозу клеток . Недавно была выдвинута гипотеза, что меконий является мощным активатором толл-подобных рецепторов (TLR) и комплемента , ключевых медиаторов воспаления, и, таким образом, может способствовать воспалительной реакции при MAS.
Меконий содержит большое количество фосфолипазы А 2 (PLA 2 ), мощного провоспалительного фермента, который может напрямую (или через стимуляцию арахидоновой кислоты ) приводить к дисфункции сурфактанта, разрушению эпителия легких, некрозу тканей и усилению апоптоза . Меконий также может активировать каскад коагуляции , выработку фактора активации тромбоцитов (PAF) и других вазоактивных веществ, что может привести к разрушению эндотелия капилляров и базальных мембран . Повреждение альвеолокапиллярной мембраны приводит к утечке жидкости, белков плазмы и клеток в интерстиций и альвеолярные пространства.
Меконий также может активировать каскад коагуляции , выработку фактора активации тромбоцитов (PAF) и других вазоактивных веществ, что может привести к разрушению эндотелия капилляров и базальных мембран . Повреждение альвеолокапиллярной мембраны приводит к утечке жидкости, белков плазмы и клеток в интерстиций и альвеолярные пространства.
Инактивация поверхностно-активного вещества
Поверхностно-активное вещество синтезируется альвеолярными клетками II типа и состоит из комплекса фосфолипидов , белков и сахаридов . Он действует для снижения поверхностного натяжения (для расширения легких во время вдоха ), стабилизации альвеол в конце выдоха (для предотвращения коллапса альвеол) и предотвращения отека легких . Поверхностно-активное вещество также способствует защите и защите легких, поскольку оно также является противовоспалительным агентом. Поверхностно-активное вещество способствует удалению вдыхаемых частиц и стареющих клеток из альвеолярной структуры.
Степень ингибирования поверхностно-активного вещества зависит как от концентрации поверхностно-активного вещества, так и от концентрации мекония. Если концентрация поверхностно-активного вещества низкая, даже очень сильно разбавленный меконий может ингибировать функцию поверхностно-активного вещества, тогда как при высоких концентрациях поверхностно-активного вещества действие мекония ограничено. Меконий может влиять на механизмы сурфактанта, предотвращая распространение сурфактанта по альвеолярной поверхности, уменьшая концентрацию сурфактантных белков ( SP-A и SP-B ), а также изменяя вязкость и структуру сурфактанта. После воздействия мекония происходит несколько морфологических изменений, наиболее заметными из которых являются отслоение эпителия дыхательных путей от стромы и выделение эпителиальных клеток в дыхательные пути. Это указывает на прямое пагубное воздействие на альвеолярные клетки легких из-за попадания мекония в легкие.
Стойкая легочная гипертензия
Стойкая легочная гипертензия (PPHN) — это неспособность кровообращения плода адаптироваться к внематочным условиям после рождения. PPHN ассоциируется с различными респираторными заболеваниями, включая MAS (поскольку у 15-20% младенцев с MAS развивается PPHN), а также с пневмонией и сепсисом . Сочетание гипоксии , легочной вазоконстрикции и несоответствия вентиляции / перфузии может вызвать PPHN в зависимости от концентрации мекония в дыхательных путях . PPHN у новорожденных является ведущей причиной смерти при МАС.
PPHN ассоциируется с различными респираторными заболеваниями, включая MAS (поскольку у 15-20% младенцев с MAS развивается PPHN), а также с пневмонией и сепсисом . Сочетание гипоксии , легочной вазоконстрикции и несоответствия вентиляции / перфузии может вызвать PPHN в зависимости от концентрации мекония в дыхательных путях . PPHN у новорожденных является ведущей причиной смерти при МАС.
Апоптоз
Апоптоз является важным механизмом очистки поврежденных клеток и восстановления тканей, однако слишком сильный апоптоз может нанести вред, например, острое повреждение легких. Меконий вызывает апоптоз и расщепление ДНК эпителиальных клеток дыхательных путей легких, что обнаруживается по присутствию фрагментированной ДНК в дыхательных путях и в ядрах альвеолярного эпителия. Меконий вызывает воспалительную реакцию в легких, поскольку после воздействия увеличивается количество аутофагоцитарных клеток и уровень каспазы 3 . После 8 часов воздействия мекония у плодов кроликов общее количество апоптотических клеток составляет 54%. Следовательно, большая часть повреждений легких, вызванных меконием, может быть вызвана апоптозом эпителия легких.
Следовательно, большая часть повреждений легких, вызванных меконием, может быть вызвана апоптозом эпителия легких.
Диагностика
Выброс мекония в амниотическую полость и затем внутриутробное дыхание у доношенных новорожденных может вызвать синдром аспирации мекония.
Дыхательной недостаточности у ребенка, родившегося в результате темного окраса MSAF, а также мекония, закупоривающего дыхательные пути, обычно достаточно для диагностики MAS. Кроме того, у новорожденных с МАС могут быть другие типы респираторного дистресса, такие как тахипноэ и гиперкапния . Иногда диагностировать МАС сложно, поскольку его можно спутать с другими заболеваниями, которые также вызывают респираторный дистресс, например, с пневмонией . Кроме того, рентген и УЗИ легких могут быть быстрыми, простыми и дешевыми методами визуализации для диагностики заболеваний легких, таких как MAS.
Профилактика
В целом, заболеваемость MAS значительно снизилась за последние два десятилетия, поскольку количество послеродовых родов сведено к минимуму.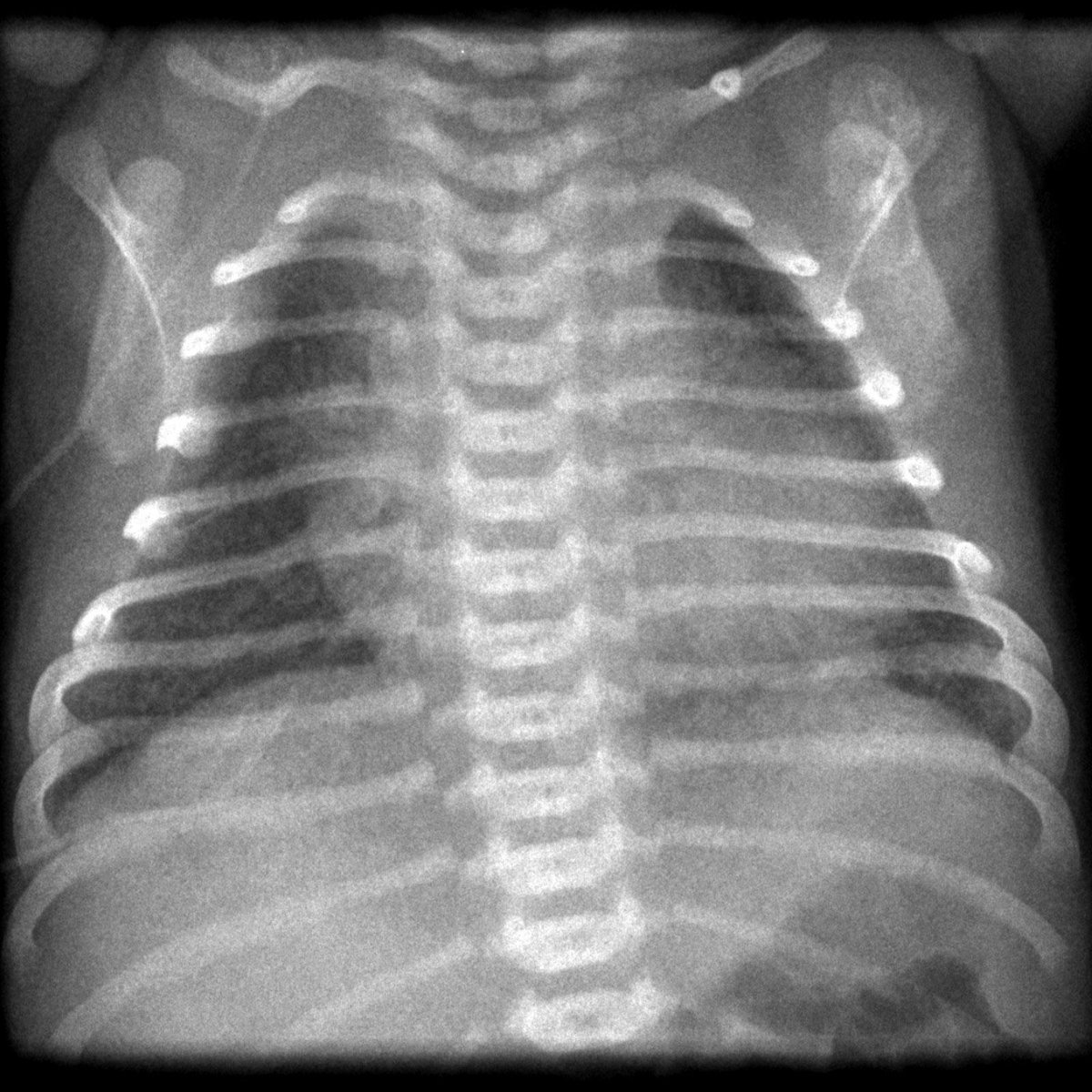 В настоящее время индуцируют роды у женщин, срок беременности которых превышает 41 неделю.
В настоящее время индуцируют роды у женщин, срок беременности которых превышает 41 неделю.
Профилактика при беременности
Профилактика во время беременности может включать амниоинфузию и антибиотики, но эффективность этих методов лечения сомнительна.
Профилактика во время родов
Как уже упоминалось ранее, отсасывание из ротоглотки и носоглотки не является идеальным профилактическим лечением как для энергичных, так и для детей с депрессией (не дышащих).
лечение
Большинство младенцев, рожденных в результате MSAF, не нуждаются в каком-либо лечении (кроме планового послеродового ухода), поскольку у них нет признаков респираторного дистресса, поскольку только примерно у 5% младенцев, рожденных в результате MSAF, развивается MAS. Тем не менее, младенцы, у которых действительно развивается МАС, должны быть помещены в неонатальное отделение, где за ними будут внимательно наблюдать и предоставлять любое необходимое лечение.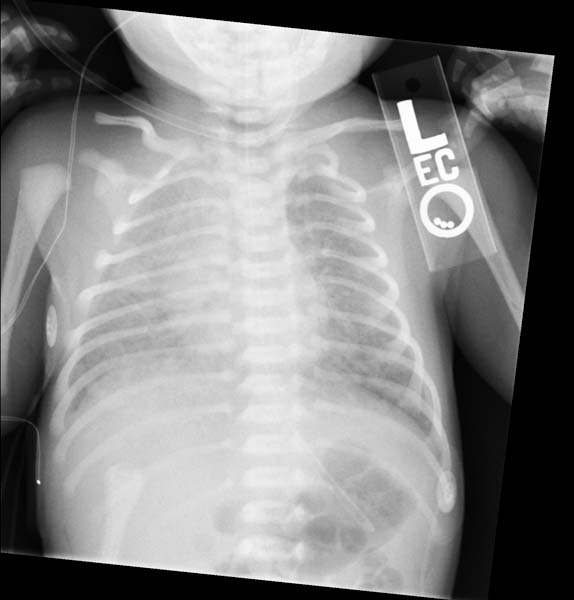 Наблюдения включают мониторинг частоты сердечных сокращений , частоты дыхания , сатурации кислорода и уровня глюкозы в крови (для выявления ухудшения респираторного ацидоза или развития гипогликемии ). В целом, лечение МАС носит более поддерживающий характер.
Наблюдения включают мониторинг частоты сердечных сокращений , частоты дыхания , сатурации кислорода и уровня глюкозы в крови (для выявления ухудшения респираторного ацидоза или развития гипогликемии ). В целом, лечение МАС носит более поддерживающий характер.
Техники вспомогательной вентиляции легких
Чтобы очистить дыхательные пути от мекония, можно использовать аспирацию из трахеи, однако эффективность этого метода под вопросом, и он может нанести вред.
В случае MAS существует потребность в дополнительном кислороде в течение как минимум 12 часов, чтобы поддерживать кислородное насыщение гемоглобина на уровне 92% или более. Тяжесть респираторного дистресс-синдрома может значительно различаться у новорожденных с МАС, поскольку некоторым из них требуется минимальная потребность в дополнительном кислороде или вообще не требуется, а в тяжелых случаях может потребоваться искусственная вентиляция легких. Желаемое насыщение кислородом составляет от 90 до 95%, а PaO 2 может достигать 90 мм рт.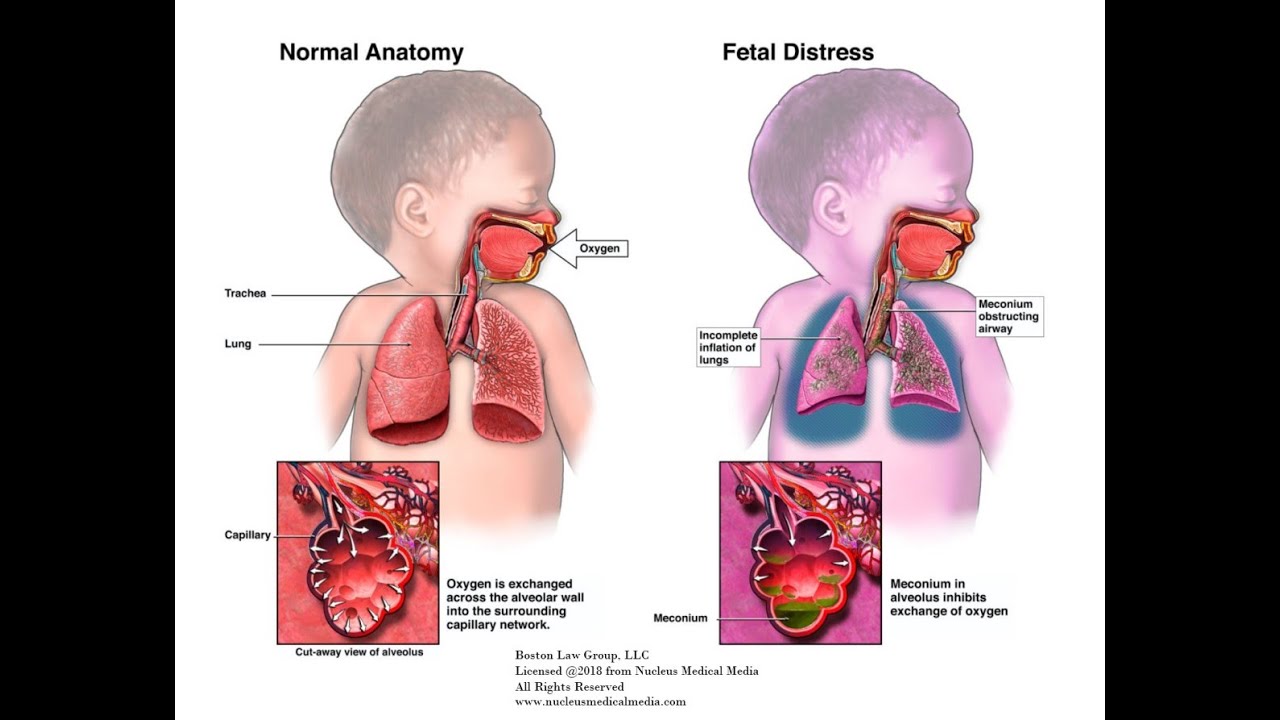 В случаях, когда глубоко в легких находится густой меконий, может потребоваться искусственная вентиляция легких . В крайних случаях экстракорпоральная мембранная оксигенация (ЭКМО) может использоваться у младенцев, которые не реагируют на вентиляционную терапию. Находясь на ЭКМО, организм может успеть поглотить меконий и разрешить все связанные с этим расстройства. Это лечение было отличным ответом, поскольку выживаемость MAS при ЭКМО составляет более 94%.
В случаях, когда глубоко в легких находится густой меконий, может потребоваться искусственная вентиляция легких . В крайних случаях экстракорпоральная мембранная оксигенация (ЭКМО) может использоваться у младенцев, которые не реагируют на вентиляционную терапию. Находясь на ЭКМО, организм может успеть поглотить меконий и разрешить все связанные с этим расстройства. Это лечение было отличным ответом, поскольку выживаемость MAS при ЭКМО составляет более 94%.
Вентиляция младенцев с MAS может быть сложной задачей, и, поскольку MAS может влиять на каждого человека по-разному, может потребоваться индивидуальная процедура вентиляции. У некоторых новорожденных с MAS могут быть однородные изменения в легких, а у других — непостоянные и неоднородные изменения в легких. Обычно седативные препараты и миорелаксанты используются для оптимизации вентиляции и сведения к минимуму риска пневмоторакса, связанного с диссинхронным дыханием.
Вдыхаемый оксид азота
Вдыхаемый оксид азота (iNO) действует на гладкие мышцы сосудов, вызывая избирательное расширение сосудов легких . Это идеальный вариант для лечения ПРГН, поскольку вызывает расширение сосудов в вентилируемых областях легких, уменьшая несоответствие вентиляции и перфузии и тем самым улучшая оксигенацию. Лечение с использованием iNO снижает потребность в ЭКМО и снижает смертность новорожденных с гипоксической дыхательной недостаточностью и PPHN в результате MAS. Однако примерно 30-50% младенцев с PPHN не отвечают на терапию iNO.
Это идеальный вариант для лечения ПРГН, поскольку вызывает расширение сосудов в вентилируемых областях легких, уменьшая несоответствие вентиляции и перфузии и тем самым улучшая оксигенацию. Лечение с использованием iNO снижает потребность в ЭКМО и снижает смертность новорожденных с гипоксической дыхательной недостаточностью и PPHN в результате MAS. Однако примерно 30-50% младенцев с PPHN не отвечают на терапию iNO.
Противовоспалительные
Поскольку воспаление является такой серьезной проблемой при MAS, лечение состояло из противовоспалительных средств.
Глюкокортикоиды
Глюкокортикоиды (ГК) обладают сильной противовоспалительной активностью и снижают миграцию и активацию нейтрофилов , эозинофилов , мононуклеаров и других клеток. ГК уменьшают миграцию нейтрофилов в легкие ergo, уменьшая их прилипание к эндотелию . Таким образом, снижается действие медиаторов, высвобождаемых из этих клеток, и, следовательно, уменьшается воспалительная реакция.
ШС также обладают геномный механизм действия , в котором после того , как связанный с глюкокортикоидного рецептора , активированного комплекса перемещается в ядро и ингибирует транскрипцию в мРНК . В конечном итоге, влияет на то, будут ли производиться различные белки или нет. Подавление транскрипции ядерного фактора ( NF-κB ) и активатора белка ( AP-1 ) ослабляет экспрессию провоспалительных цитокинов ( IL-1 , IL-6 , IL-8 и TNF и т. Д.), Ферментов ( PLA 2 , ЦОГ-2 , iNOs и др.) И другие биологически активные вещества. Противовоспалительный эффект ГК также проявляется в усилении активности липокортинов, которые ингибируют активность PLA 2 и, следовательно, уменьшают продукцию арахидоновой кислоты и медиаторов липоксигеназного и циклооксигеназного путей.
Противовоспалительные средства необходимо вводить как можно быстрее, так как действие этих препаратов может ослабнуть даже через час после аспирации мекония. Например, раннее введение дексаметазона значительно усилило газообмен , снизило давление на дыхание, уменьшило количество нейтрофилов в бронхоальвеолярной области, уменьшило образование отека и окислительное повреждение легких. Однако ГК могут увеличивать риск инфекции, и этот риск увеличивается с увеличением дозы и продолжительность лечения глюкокортикоидами. Могут возникнуть и другие проблемы, такие как обострение сахарного диабета , остеопороз , атрофия кожи и задержка роста у детей.
Например, раннее введение дексаметазона значительно усилило газообмен , снизило давление на дыхание, уменьшило количество нейтрофилов в бронхоальвеолярной области, уменьшило образование отека и окислительное повреждение легких. Однако ГК могут увеличивать риск инфекции, и этот риск увеличивается с увеличением дозы и продолжительность лечения глюкокортикоидами. Могут возникнуть и другие проблемы, такие как обострение сахарного диабета , остеопороз , атрофия кожи и задержка роста у детей.
Ингибиторы фосфодиэстеразы
Фосфодиэстеразы (ФДЭ) расщепляют цАМФ и цГМФ, и в дыхательной системе новорожденного с МАС могут быть задействованы различные изоформы ФДЭ из-за их провоспалительной и сократительной активности гладких мышц . Следовательно, неселективные и селективные ингибиторы ФДЭ потенциально могут использоваться в терапии МАС. Однако использование ингибиторов ФДЭ может вызвать побочные эффекты со стороны сердечно-сосудистой системы . Неселективные ингибиторы ФДЭ, такие как метилксантины , увеличивают концентрацию цАМФ и цГМФ в клетках, что приводит к бронходилатации и расширению сосудов . Кроме того, метилксантины снижают концентрацию кальция, ацетилхолина и моноаминов , что контролирует высвобождение различных медиаторов воспаления и бронхоспазма , включая простагландины . Селективные ингибиторы PDE нацелены на один подтип фосфодиэстеразы, и в MAS активность PDE-3 , PDE-4 , PDE-5 и PDE-7 может усиливаться. Например, милринон (селективный ингибитор PDE3) улучшал оксигенацию и выживаемость новорожденных с MAS.
Неселективные ингибиторы ФДЭ, такие как метилксантины , увеличивают концентрацию цАМФ и цГМФ в клетках, что приводит к бронходилатации и расширению сосудов . Кроме того, метилксантины снижают концентрацию кальция, ацетилхолина и моноаминов , что контролирует высвобождение различных медиаторов воспаления и бронхоспазма , включая простагландины . Селективные ингибиторы PDE нацелены на один подтип фосфодиэстеразы, и в MAS активность PDE-3 , PDE-4 , PDE-5 и PDE-7 может усиливаться. Например, милринон (селективный ингибитор PDE3) улучшал оксигенацию и выживаемость новорожденных с MAS.
Ингибиторы циклооксигеназы
Арахидоновая кислота метаболизируется через циклооксигеназу (ЦОГ) и липоксигеназу до различных веществ, включая простагландины и лейкотриены , которые обладают сильным провоспалительным и вазоактивным действием. Путем ингибирования ЦОГ, а точнее ЦОГ-2 (с помощью селективных или неселективных лекарств) можно уменьшить воспаление и отек. Однако ингибиторы ЦОГ могут вызывать пептические язвы и вызывать гиперкалиемию и гипернатриемию . Кроме того, ингибиторы ЦОГ не показали значительного ответа при лечении МАС.
Однако ингибиторы ЦОГ могут вызывать пептические язвы и вызывать гиперкалиемию и гипернатриемию . Кроме того, ингибиторы ЦОГ не показали значительного ответа при лечении МАС.
Антибиотики
Меконий обычно стерилен, однако он может содержать различные культуры бактерий, поэтому может потребоваться назначение соответствующих антибиотиков.
Обработка поверхностно-активными веществами
Промывание легких разбавленным сурфактантом — это новое лечение, дающее потенциально положительные результаты в зависимости от того, как рано его вводить новорожденным с МАС. Это лечение является многообещающим, поскольку оно оказывает значительное влияние на утечки воздуха, пневмоторакс , необходимость в ЭКМО и смерть. Раннее вмешательство и его использование у новорожденных с легким MAS более эффективно. Однако есть риски, поскольку закапывание большого объема жидкости в легкие новорожденного может быть опасным (особенно в случаях тяжелого MAS с легочной гипертензией ), поскольку оно может усугубить гипоксию и привести к смерти.
Предыдущие процедуры
Первоначально считалось, что MAS возник в результате физической блокировки дыхательных путей меконием. Таким образом, для предотвращения развития МАС у новорожденных, рожденных с помощью MSAF, в течение 20 лет использовалось отсасывание ротоглотки и носоглотки перед родами с последующей аспирацией трахеи . Это лечение считалось эффективным, поскольку сообщалось, что оно значительно снижает частоту возникновения MAS по сравнению с новорожденными, рожденными через MSAF, которые не получали лечения. Позже это утверждение было опровергнуто, и будущие исследования пришли к выводу, что отсасывание через ротоглотку и носоглотку перед родоразрешением у младенцев, рожденных в результате MSAF, не предотвращает MAS или его осложнения. Фактически, это может вызвать больше проблем и повреждений (например, повреждение слизистой оболочки ), поэтому это не рекомендуемое профилактическое лечение. Отсасывание не может значительно снизить частоту возникновения MAS, поскольку пассаж мекония и аспирация могут происходить внутриутробно.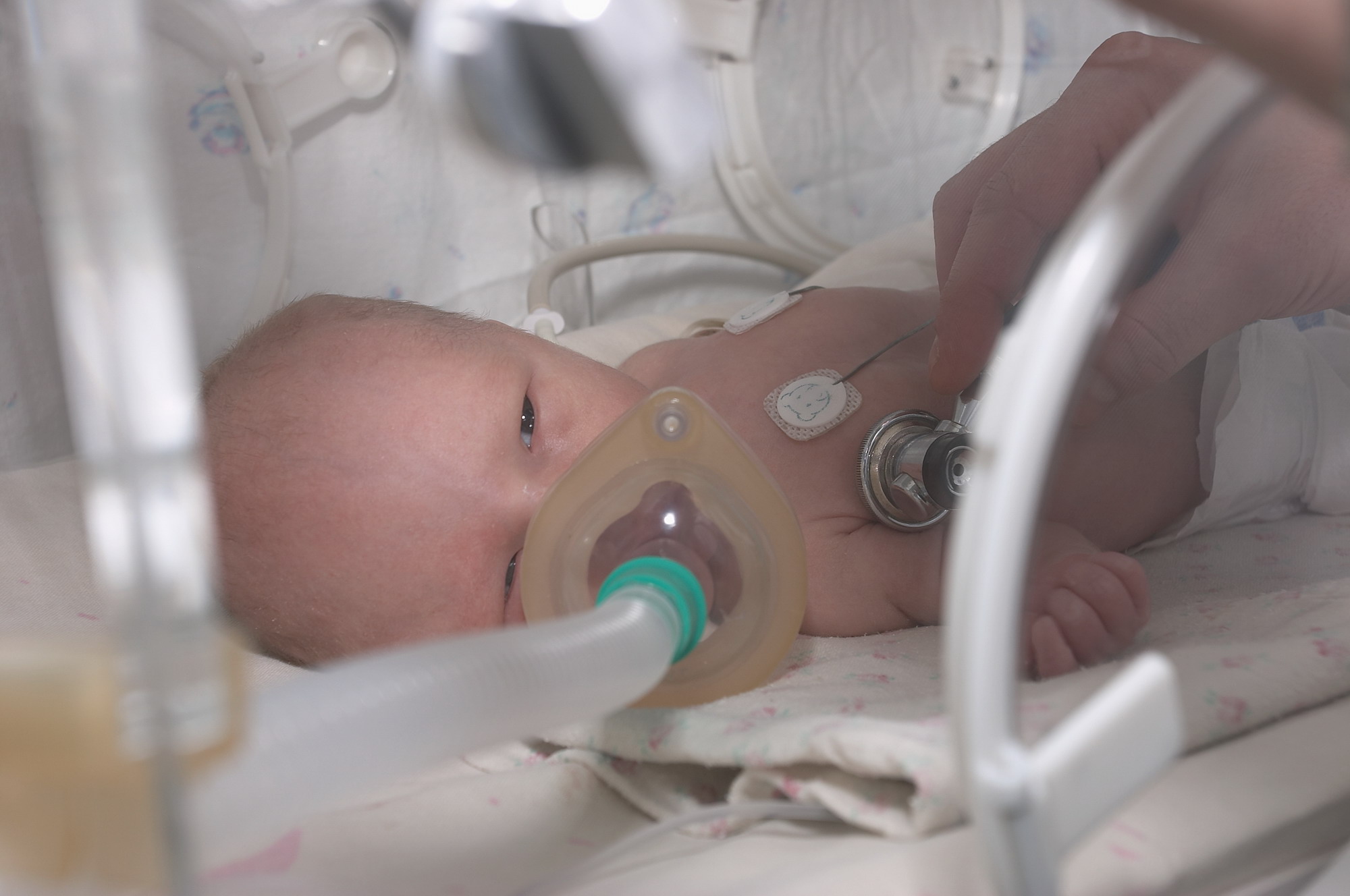 Таким образом, отсасывание становится ненужным и бесполезным, поскольку меконий может находиться глубоко в легких во время рождения.
Таким образом, отсасывание становится ненужным и бесполезным, поскольку меконий может находиться глубоко в легких во время рождения.
Исторически сложился так , амниоинфузия была использована , когда MSAF присутствовал, которая включает в себя трансцервикальное вливание жидкости во время родов. Идея заключалась в том, чтобы разбавить густой меконий, чтобы уменьшить его потенциальную патофизиологию и уменьшить количество случаев MAS, поскольку MAS более распространен в случаях густого мекония. Однако существуют сопутствующие риски, такие как выпадение пуповины и удлинение родов. Руководящие принципы Национального института здоровья и клинической практики Великобритании (NICE) не рекомендуют использовать амниоинфузию у женщин с MSAF.
Распространенность
У 1 из каждых 7 беременностей есть MSAF, и из этих случаев примерно у 5% этих младенцев развивается MAS. MSAF наблюдается в 23-52% беременностей на сроке 42 недели, поэтому частота MAS увеличивается по мере увеличения срока беременности , так что распространенность наиболее высока при беременности после родов . И наоборот, преждевременные роды не часто связаны с MSAF (только около 5% в общей сложности содержат MSAF). Частота MAS снижается в популяциях, в которых индуцируют роды у женщин, срок беременности которых превышает 41 неделю. Есть много предполагаемых факторов, предшествующих выбрасыванию, которые, как считается, увеличивают риск MAS. Например, риск MSAF выше у матерей афроамериканцев, африканцев и жителей островов Тихого океана по сравнению с матерями из других этнических групп.
И наоборот, преждевременные роды не часто связаны с MSAF (только около 5% в общей сложности содержат MSAF). Частота MAS снижается в популяциях, в которых индуцируют роды у женщин, срок беременности которых превышает 41 неделю. Есть много предполагаемых факторов, предшествующих выбрасыванию, которые, как считается, увеличивают риск MAS. Например, риск MSAF выше у матерей афроамериканцев, африканцев и жителей островов Тихого океана по сравнению с матерями из других этнических групп.
Будущие исследования
Исследования сосредоточены на разработке как успешного метода предотвращения MAS, так и эффективного лечения. Например, проводятся исследования эффективности противовоспалительных средств, заместительной терапии сурфактантами и терапии антибиотиками . Необходимо провести дополнительные исследования фармакологических свойств, например, глюкокортикоидов , включая дозировку, прием, время или любые взаимодействия с лекарствами. Кроме того, все еще проводятся исследования относительно того, является ли интубация и отсасывание мекония у новорожденных с MAS полезным, вредным или просто избыточным и устаревшим лечением. В целом до сих пор не существует общепринятого терапевтического протокола и эффективного плана лечения МАС.
В целом до сих пор не существует общепринятого терапевтического протокола и эффективного плана лечения МАС.
Смотрите также
Рекомендации
внешние ссылки
Влияние интеркуррентных заболеваний на биомеханическую функцию легких у новорожденных с тяжелой асфиксией на фоне проведения системной лечебной гипотермии
ГБОУ ВПО Иркутский государственный медицинский университет Минздрава России;
ОГАУЗ Иркутский городской перинатальный центр, Россия
Цель исследования. Определить влияние интеркуррентных состояний на биомеханическую функцию легких у новорожденных, перенесших тяжелую асфиксию в родах, на фоне проведения системной лечебной гипотермии.
Материал и методы. В исследование были включены 40 новорожденных с тяжелой асфиксией. В зависимости от вида интеркуррентного заболевания все дети разделены на 4 группы.
Результаты исследования. Синдром аспирации мекония (САМ) и внутриутробное инфицирование (ВУИ) достоверно увеличивают продолжительность госпитализации в условиях отделения реанимации и интенсивной терапии новорожденных и пролонгирование искусственной вентиляции легких (ИВЛ). При начале гипотермии FiO 2, MAP и RR снижались и доходили до минимума к концу 3-х суток у новорожденных без интеркуррентных заболеваний. К 12-му часу жизни у новорожденных с САМ и ВУИ наблюдались нарастание всех параметров ИВЛ, также у этих групп выявлен переход на высокочастотную ИВЛ и связь с реализацией персистирующей легочной гипертензии.
При начале гипотермии FiO 2, MAP и RR снижались и доходили до минимума к концу 3-х суток у новорожденных без интеркуррентных заболеваний. К 12-му часу жизни у новорожденных с САМ и ВУИ наблюдались нарастание всех параметров ИВЛ, также у этих групп выявлен переход на высокочастотную ИВЛ и связь с реализацией персистирующей легочной гипертензии.
Заключение. Оценивая комплаенс, FiO2, МАР и индекс оксигенации, можно оценить тяжесть поражения дыхательной системы и спрогнозировать длительность ИВЛ. Дети с САМ и ВУИ имеют более тяжелое поражение дыхательной системы, в связи с чем им требуется более тщательный контроль за кислотно-щелочным состоянием и параметрами ИВЛ. Во всех исследуемых группах летальных исходов не было.
синдром аспирации мекония
внутриутробная инфекция
гипоксически-ишемическая энцефалопатия
лечебная гипотермия
искусственная вентиляция легких
1. Kurinczuk J.J., White-Koning M., Badawi N. Epidemiology of neonatal encephalopathy and hypoxic-ischaemic encephalopathy. Early Hum. Dev. 2010; 86(6): 329-38.
Early Hum. Dev. 2010; 86(6): 329-38.
2. Gluckman P.D., Williams C.E. When and why do brain cells die? Dev. Med. Child Neurol. 1992; 34(11): 1010-4.
3. De Menezes M.S. Hypoxic-ischemic brain injury in the newborn. 2013. Available at: http:// emedicine.medscape.com/article/1183351
4. Platt M.J., Cans C., Johnson A., Surman G., Topp M. et al. Trends in cerebral palsy among infants of very low birthweight (
5. TOBY Protocol and handbook. Available at: https://www.npeu.ox.ac.uk/tobyregister/docs Accessed 25.11.2015.
6. Колганова А.А. Прогнозирование мекониальной аспирации у плода в анте- и интранатальном периодах: дисс. … канд. мед. наук. Ростов н/Д.; 2010. 160с.
7. Буштырева И.О., Чернавский В.В., Колганова А.А. Синдром аспирации мекония. Саратовский научно-медицинский журнал. 2010; 6(2): 378-83.
8. El Shahed A.I., Dargaville P., Ohlsson A., Soll R.F. Surfactant for meconium aspiration syndrome in full term/near term infants. Cochrane Database Syst. Rev. 2007; (3): CD002054.
Rev. 2007; (3): CD002054.
9. Zhang D.S., Chen C., Zhou W., Chen J., Mu D.Z. Pathogens and risk factors for ventilator-associated pneumonia in neonates. Zhongguo Dang Dai Er Ke Za Zhi. 2013; 15(1): 8-14.
10. Сурков Д.Н., Капустина О.Г., Иванов Д.О. Влияние искусственной вентиляции легких на церебральный статус у новорожденных в остром периоде гипоксически-ишемической энцефалопатии. Вестник современной клинической медицины. 2014; 7(6): 46-55. Available at: http://cyberleninka.ru/article/n/vliyanie-iskusstvennoy-ventilyatsii-legkih-na-tserebralnyy-status-u-novorozhdennyh-v-ostrom-periode-gipoksicheski-ishemicheskoy Accessed 11.02.2016.
11. Abbasi S., Sivieri E., Roberts R., Kirpalani H. Accuracy of tidal volume, compliance, and resistance measurements on neonatal ventilator displays: an in vitro assessment. Pediatr. Crit. Care Med. 2012; 13(4): 262-8.
12. Овсянников Д.Ю., Бойцова Е.В., Беляшова М.А., Ашерова И.К. Интерстициальные заболевания легких у младенцев. М.: РУДН; 2014. 182с.
М.: РУДН; 2014. 182с.
13. Clark D.A., Nieman G.F., Thompson J.E., Paskanik A.M., Rokhar J.E., Bredenberg C.E. Surfactant displacement by meconium free fatty acids: an alternative explanation for atelectasis in meconium aspiration syndrome. J. Pediatr. 1987; 110(5): 765-70.
14. Gautam A., Ganu S.S., Tegg O.J., Andresen D.N., Wilkins B.H., Schell D.N. Ventilator-associated pneumonia in a tertiary paediatric intensive care unit: a 1-year prospective observational study. Crit. Care Resusc. 2012; 14(4): 283-9.
15. Hill A., Volpe J.J. Neurologic disorders. In: Avery G.B., Fletcher M.A., MacDonald M.G., eds. Neonatology: pathophysiology and management of the newborn. Philadelphia: Lippincott-Raven Publ.; 1994: 1117-38.
16. Антонов А.Г. Методика проведения лечебной гипотермии детям, родившимся в состоянии асфиксии. Анестезиология и реаниматология. 2014; 6: 76-8.
17. American Academy of Pediatrics, American Heart Association. Textbook of neonatal resuscitation. 6th ed. American Heart Association; 2010.
6th ed. American Heart Association; 2010.
18. Александрович Ю.С., Блинов С.А., Пшениснов К.В., Паршин Е.В. Критерии тяжести поражения легких у новорожденных с респираторным дистресс-синдромом. Анестезиология и реаниматология. 2014; 1: 52-7. Available at: http://cyberleninka.ru/article/n/kriterii-tyazhesti-porazheniya-legkih-u-novorozhdennyh-s-respiratornym-distress-sindromom. Accessed 11.02.2016.
19. Wiswell T.E., Tuggle J.M., Turner B.S. Meconium aspiration syndrome: have we made a difference? Pediatrics. 1990; 85(5): 715-21.
20. Cleary G.M., Wiswell T.E. Meconium-stained amniotic fluid and the meconium aspiration syndrome. An update. Pediatr. Clin. North Am. 1998; 45(3): 511-29.
21. Зарубин А.А., Голуб И.Е., Богданова А.Д., Мельников В.А., Ионушене С.В., Федорова О.С. Применение лечебной гипотермии при лечении тяжелой интранатальной асфиксии. Universum: Медицина и фармакология. Электронный научный журнал. 2015; 11(22). Available at: http://7universum.com/ru/med/archive/item/2714 Accessed 10..jpg) 01.2016.
01.2016.
22. Бубнова Н.И., Тютюнник В.Л., Михайлова О.И. Репродуктивные потери при декомпенсированной форме плацентарной недостаточности, вызванной инфекцией. Акушерство и гинекология. 2010; 4: 55-8.
23. Шабалов Н.П. Неонатология. Учебное пособие. т.1. М.: МЕДпресс-информ; 2004. 608с.
24. Холичев Д.А., Стецкая Ю.Н., Сенькевич О.А. Искусственная вентиляция легких у детей с перинатально обусловленным аспирационным синдромом. Дальневосточный медицинский журнал. 2015; 2: 41-4. Available at: http://cyberleninka.ru/article/n/iskusstvennaya-ventilyatsiya-legkih-u-detey-s-perinatalno-obuslovlennym-aspiratsionnym-sindromom Accessed 11.02.2016.
25. Дассиос Т., Остин Т. Показатели функции внешнего дыхания у новорожденных, находящихся на искусственной вентиляции легких при проведении системной лечебной гипотермии. Неонатология: новости, мнения, обучение. 2014; 1: 65-70.
26. Lin H.C., Su B.H., Lin T.W., Peng C.T., Tsai C.H. Risk factors of mortality in meconium aspiration syndrome: review of 314 cases. Acta Paediatr. Taiwan. 2004; 45(1): 30-4.
Acta Paediatr. Taiwan. 2004; 45(1): 30-4.
27. Бондарев В.В., Горелик К.Д. Мекониальная аспирация, этиология, патоморфологические механизмы, оказание помощи на догоспитальном этапе. В кн.: Конференция, посвященная памяти профессора Э.К. Цыбулькина: Материалы. М.; 2004: 28-32.
28. Armstrong L., Stenson B.J. Use of umbilical cord blood gas analysis in the assessment of the newborn. Arch. Dis. Child. 2007; 92(6): F430-4.
Поступила 20.02.2016
Принята в печать 25.03.2016
Зарубин Александр Анатольевич, аспирант, ассистент кафедры анестезиологии и реаниматологии, ГБОУ ВПО Иркутский государственный медицинский университет Минздрава России; врач, ОГАУЗ Иркутский городской перинатальный центр. Адрес: 664003, Россия, г. Иркутск, ул. Красного Восстания, д. 1. Телефон: 8 (983) 249-39-49. E-mail: [email protected]
Голуб Игорь Ефимович, профессор, д.м.н., зав. кафедрой анестезиологии и реаниматологии, ГБОУ ВПО Иркутский государственный медицинский университет Минздрава России. Адрес: 664003, Россия, г. Иркутск, ул. Красного Восстания, д. 1
Адрес: 664003, Россия, г. Иркутск, ул. Красного Восстания, д. 1
Михеева Наталья Иннокентьевна, врач, ОГАУЗ Иркутский городской перинатальный центр. Адрес: 664025, Россия, г. Иркутск, ул. Сурикова, д. 16
Богданова Арина Дмитриевна, врач, ОГАУЗ Иркутский городской перинатальный центр. Адрес: 664025, Россия, г. Иркутск, ул. Сурикова, д. 16
Федорова Ольга Сергеевна, врач, ОГАУЗ Иркутский городской перинатальный центр. Адрес: 664025, Россия, г. Иркутск, ул. Сурикова, д. 16
Для цитирования: Зарубин А.А., Голуб И.Е., Михеева Н.И., Богданова А.Д., Федорова О.С. Влияние интеркуррентных заболеваний на биомеханическую функцию легких у новорожденных с тяжелой асфиксией на фоне проведения системной лечебной гипотермии. Акушерство и гинекология. 2016; 11: 101-5.
http://dx.doi.org/10.18565/aig.2016.11.101-5
СИНДРОМ АСПИРАЦИИ МЕКОНИЯ (САМ)
ный ДВС-синдром, некротический энтероколит, электролитные нарушения, бронхолегочная дисплазия, ретинопатия недоношенных.
Исходы. Случаи смерти при РДСН связаны с острым нарушением центральной гемодинамики или механической травмой лёгких в результате неадекватной ИВЛ. У 5-15% глубоконедоношенных детей с СДР может развиться хроническое заболевание лёгких – бронхолегочная дисплазия, у 10-70% неврологические нарушения. У детей после РДСН возможно развитие пневмонии.
Случаи смерти при РДСН связаны с острым нарушением центральной гемодинамики или механической травмой лёгких в результате неадекватной ИВЛ. У 5-15% глубоконедоношенных детей с СДР может развиться хроническое заболевание лёгких – бронхолегочная дисплазия, у 10-70% неврологические нарушения. У детей после РДСН возможно развитие пневмонии.
Прогноз при РДСН зависит от степени недоношенности, тяжести заболевания, характера и степени поражения внутренних органов и систем. При своевременном начале и высоком качестве интенсивной терапии прогноз благоприятный.
САМ – дыхательное расстройство, обусловленное попаданием мекония вместе с околоплодными водами в дыхательные пути ребенка до родов или в момент рождения.
Меконий встречается в околоплодных водах в 2-10% случаев, однако САМ выявляется в 5-10 раз реже. Он наблюдается преимущественно у переношенных (44%) или доношенных (5-10%) новорожденных, подвергшихся длительной внутриутробной или острой интранатальной гипоксии.
Этиология и патогенез. При наличии гипоксии развивается спазм сосудов брыжейки, усиление перистальтики кишечника, расслабление анального сфинктера и выход мекония в околоплодные воды. Это возможно даже при отсутствии асфиксии – при обвитии пуповины вокруг шеи, сдавлении ее, что стимулирует вагусную реакцию и в ы- ход мекония.
При наличии гипоксии развивается спазм сосудов брыжейки, усиление перистальтики кишечника, расслабление анального сфинктера и выход мекония в околоплодные воды. Это возможно даже при отсутствии асфиксии – при обвитии пуповины вокруг шеи, сдавлении ее, что стимулирует вагусную реакцию и в ы- ход мекония.
При внутриутробно САМ развиваются четыре основные эффекта: обструкция дыхательных путей, снижение активности сурфактанта, спазм легочных сосудов и воспаление, развивающееся в первые 48 ч жизни. Обструкция глубоких дыхательных путей приводит к формированию «воздушных ловушек», ателектазов. Ателектазы обусловлены как закупоркой бронхов, так и инактивацией сурфактанта, что приводит к спадению альвеол на выдохе. Результаты последних исследований выявили высокое содержание в крови новорожденных с САМ иммунореактивного эндотелина-1, который обладает выраженным сосудосуживающим эффектом, что способствует развитию легочной гипертензии и гиперактивности легочных сосудов. Аспирированный меконий вызывает воспалительную реакцию в трахее, бронхах, легочной
597
паренхиме за счет содержащихся в нем солей желчных кислот, протеолитических ферментов и его повышенной осмолярности.
Химическое повреждение бронхиального и альвеолярного эпителия создает предпосылки для развития бактериальной флоры, превращения асептических трахеобрнохита и пневмонии в инфекционный процесс. Помимо химического воспаления и ателектазов в легких возникает отек, перифокальная эмфизема с развитием легочной гипертензии, синдрома «утечки воздуха» (интерстициальная эмфизема, пневмоторакс, пневмомедиастинум, пневмоперикард). Летальность при САМ составляет по данным разных авторов от 4 до 19% и зависит от качества оказания первичной реанимационной помощи в родзале и уровня интенсивной терапии в первые 48 ч жизни.
Внутриутробная гипоксия
Спазм сосудов брыжейки, усиление перистальтики кишечника, расслабление анального сфинктера и выход мекония в околоплодные воды
| Обструкция дыхательных путей меконием |
|
| ||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
| Синдро- |
|
|
|
|
|
|
|
|
|
| ||
|
|
|
|
|
|
|
|
|
|
| |
|
|
|
|
|
|
|
|
|
|
| мы |
|
|
|
|
|
|
|
|
|
|
| «утечки |
Ателекта- |
|
|
|
| Химический |
| Дефицит сурфак- | ||||
|
|
|
|
|
| воздуха» | |||||
зы |
|
|
|
| пневмонит |
| танта |
| |||
|
|
|
|
|
|
| |||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Синдром пер- |
| Сердечная не- |
|
|
систирующей |
| достаточность |
|
|
легочной ги- |
|
|
|
|
|
|
|
| |
|
|
|
| |
пертензии |
|
|
|
|
|
|
|
| |
|
| Гипоксия, гипоксемия | ||
| ||||
|
|
|
|
|
Поражение ЦНС и других органов
Рис. 2.6. Схема патогенеза аспирации мекония
2.6. Схема патогенеза аспирации мекония
Исследования. Рентгенография органов грудной клетки; общий анализ крови и мочи, гематокрит, определение концентрации РаО2
598
РаСО2 в артериальной крови, показатели КОС, определение в крови уровней: общего белка, глюкозы, калия, натрия, кальция, мочевины, креатинина, магния, билирубина; показатели коагулограммы, ЭКГ, ЭхоКГ, НСГ.
Анамнез, клиника. Дети при САМ, как правило, рождаются с низкой оценкой по шкале Апгар. У переношенных детей часто имеется прокрашивание меконием ногтей, кожи, пуповины. Существуют два варианта клинического течения САМ:
1)у большинства детей с САМ с рождения отмечаются признаки дыхательных расстройств, притупление легочного звука, повышение ригидности грудной клетки, обильные разнокалиберные влажные хрипы в легких, у части – приступы вторичной асфиксии;
2)у некоторых детей с САМ после рождения имеется «светлый» промежуток, после которого (по мере продвижения мелких частиц мекония к мелким бронхам) возникает клиника тяжелой дыхательной недостаточности.
В наиболее тяжелых случаях САМ осложняется синдромом персистирующей легочной гипертензии. В процессе ИВЛ нередко выявляется синдром «утечки воздуха».
Через 24-48 часов после рождения у большинства детей развиваются с САМ клинические признаки аспирационной пневмонии.
Увсех новорожденных с тяжелой формой САМ развиваются функциональные изменения со стороны ЦНС: мышечная гипотония, угнетение физиологических рефлексов, фокальные судороги в первые дни жизни. Транзиторная дисфункция миокарда проявляется цианозом, тахикардией, систолическим шумом, иногда ритмом галопа, кардиомегалией, увеличением в размерах печени.
Диагноз. Для постановки диагноза САМ используют результаты оценки по шкале Даунса. Диагноз устанавливается на основании данных анамнеза, мекониального характера околоплодных вод клинических и рентгенологических данных. На обзорной рентгенограмме грудной клетки отмечается сочетание крупных участков затемнения, отходящих от корней легких, с участками эмфизематозных вздутий. Характерен симптом «снежной бури», кардиомегалия, в ряде случаев обнаруживаются признаки пневмоторакса. Диафрагма уплощена, переднезадний размер грудной клетки увеличен.
Характерен симптом «снежной бури», кардиомегалия, в ряде случаев обнаруживаются признаки пневмоторакса. Диафрагма уплощена, переднезадний размер грудной клетки увеличен.
Если в мекониальных водах обнаружены плотные фрагменты мекония, то вероятность аспирации мекония и пневмонии гораздо выше, чем когда околоплодные воды просто окрашены меконием.
599
Лабораторные исследования: выраженная гипоксемия и смешанный ацидоз.
Дифференциальный диагноз проводят с: РДСН, персистирующей легочной гипертензией, вызванной тяжелой асфиксией, сепсисом, транзиторным тахипноэ.
Табл. 2.48. Дифференциальный диагноз синдрома аспирации
мекония и РДСН
Признак | РДСН | Синдром аспирации |
|
| мекония |
Срок гестации | Менее 30 недель | Дети доношены или пе- |
|
| реношены |
Мекониального | Не характерен | Характерен |
характера около- |
|
|
плодных вод |
|
|
Раздувание щек | Характерно | Не характерно |
(дыхание трубача) |
|
|
Экспираторное | Характерно | Не характерно |
хрюканье |
|
|
Парадоксальное | Характерно | Не характерно |
дыхание |
|
|
Персистирующие | Характерно | Не характерно |
фетальные комму- |
|
|
никации |
|
|
Рентгенологические | Воздушная бронхо- | крупные участки затем- |
данные | грамма, снижение | нения, отходящих от |
| пневматизации лег- | корней легких, участки |
| ких | эмфиземы, симптом |
|
| «снежной бури» |
Лечение. Обязательна аспирация мекония из дыхательных путей сразу после рождения до начала вспомогательной вентиляции легких. Отсасывание мекония при необходимости повторяют неоднократно. Интенсивность и длительность респираторной терапии, а также особенности поддерживающей терапии зависят от тяжести клинической картины и имеют много общего с РДСН. При легких вариантах САМ проводится кислородотерапия при помощи кислородной палатки. Эффект от применения СРАР непредсказуем, его лучше не использовать, при необходимости перейти к ИВЛ (при РаО2<50, РаСО2>60, РН<7,2).
Обязательна аспирация мекония из дыхательных путей сразу после рождения до начала вспомогательной вентиляции легких. Отсасывание мекония при необходимости повторяют неоднократно. Интенсивность и длительность респираторной терапии, а также особенности поддерживающей терапии зависят от тяжести клинической картины и имеют много общего с РДСН. При легких вариантах САМ проводится кислородотерапия при помощи кислородной палатки. Эффект от применения СРАР непредсказуем, его лучше не использовать, при необходимости перейти к ИВЛ (при РаО2<50, РаСО2>60, РН<7,2).
600
Аспирация мекония при родах: личный опыт
Автор Дневников размноженца Павел Рябиков делится с читателями «Летидора» тем, какие сложности возникли при родах, а также просит читателей поделиться личным опытом профилактики бронхолегочных заболеваний у детей — к сожалению, его сын теперь будет иметь к ним склонность.
Честно говоря, долго откладывал написание этой колонки. 29 июля моя жена родила сына Никиту, но долгое время нам было совершенно не до колонок, как, впрочем, и до всего остального мира. В основном, мы общались с этим миром через меня, потому что моя жена не хотела брать трубку даже тогда, когда звонили ее родители. Причина проста — когда у тебя по-настоящему серьезное горе, рассказывать об этом горе опять и опять — означает переживать происшедшие события снова и снова.
В основном, мы общались с этим миром через меня, потому что моя жена не хотела брать трубку даже тогда, когда звонили ее родители. Причина проста — когда у тебя по-настоящему серьезное горе, рассказывать об этом горе опять и опять — означает переживать происшедшие события снова и снова.
А начиналось все очень хорошо, даже весело — просто в какой-то момент приложение на айфоне показало, что схватки уже не ложные, и пора в роддом. И мы двинули, собственно говоря, в роддом. Там нас определили в отделение патологии, которым заведует Евгения Анатольевна Зигуля. Евгения Романовна, моя красавица жена, лежала там уже на обследовании незадолго до родов, и ей там не просто понравилось — она это отделение определила как «несуществующий детский сад мечты моего детства». Действительно, там все, начиная с заведующей, хорошо относятся к пациентам. Как и во всем 32 роддоме, там чисто, много необходимой медицинской техники и квалифицированные врачи с медсестерами. Причем чрезвычайно любезно ведут себя все, включая санитарок. Как такое можно организовать в отечественном медицинском учреждении — для меня загадка.
Как такое можно организовать в отечественном медицинском учреждении — для меня загадка.
При том, что за всю беременность мы болели один раз ОРВИ, все обследования показывали норму, а беременность длилась 40 недель и 5 дней, воды были очень зелеными. И вот тут мы совершили ошибку — а точнее, эту ошибку совершил я. Заведующая отделением сказала, что надо делать кесарево, «хотя, если не хотите, давайте мы вас доведем до родов на КТГ. Если гипоксия у ребенка компенсированная, то ничего страшного». Надо было настоять на кесаревом сечении. Обязательно, если воды зеленые, и врачи раздумывают относительно кесарева сечения, настаивайте на кесаревом! Да, у кесарят высокие риски аллергии, матери сложнее начать кормить грудью и пр., но поверьте, когда ваш ребенок лежит вторую неделю на искусственной вентиляции легких, все сомнения кажутся абсолютно несущественным!
Роды длились часов двенадцать, но за счет вовремя сделанной эпидуральной анестезии жена моя почти не мучилась от схваток, исключая последние часа полтора непосредственно перед родами. Кстати, тысячепервая причина не набирать вес во время беременности — роженице в соседней палате эпидуралку так и не сделали — просто не смогли добраться до позвоночника через слой жира на спине.
Кстати, тысячепервая причина не набирать вес во время беременности — роженице в соседней палате эпидуралку так и не сделали — просто не смогли добраться до позвоночника через слой жира на спине.
Я, естественно, на родах был, и жена моя говорит, что мое присутствие ей помогло. Совет мужьям, которые рожают вместе с женами — найдите себе какую-то роль — там, держать ногу, массировать поясницу, короче, помогите акушерке, займитесь делом. Тогда все это воспринимается вполне нормально. Роды и роды. Вплоть до последнего момента все шло обычным для родов порядком, но когда Никита Палыч родился, стало ясно, что реанимация дежурила в палате не зря. Сразу же после родов ему воткнули в трахею трубку и стали откачивать.
Оказалось, что есть на свете такая вещь, как синдром аспирации мекониевыми водами. Дети, вообще, обычно нахлебываются околополодных вод при родах — вот только если воды эти с меконием, зеленые, то потом детит очень долго лежат на ИВЛ и болеют двусторонней пневмонией. Иногда от этого умирают. И не такая уж редкая штука этот синдром — насколько я потом погуглил, встречается в 1 проценте случаев от всех родов, при летальности в 10 процентов (не знаю, насколько точны сейчас эти цифры, специалисты меня поправят). При том, что зеленые воды — это 15-20 процентов всех случаев, наши шансы нарваться были довольно низкими, но в итоге нам не повезло. Говорят, что месяц назад в 32 роддоме уже был один такой случай, но все обошлось благополучно.
И не такая уж редкая штука этот синдром — насколько я потом погуглил, встречается в 1 проценте случаев от всех родов, при летальности в 10 процентов (не знаю, насколько точны сейчас эти цифры, специалисты меня поправят). При том, что зеленые воды — это 15-20 процентов всех случаев, наши шансы нарваться были довольно низкими, но в итоге нам не повезло. Говорят, что месяц назад в 32 роддоме уже был один такой случай, но все обошлось благополучно.
Три недели после родов был очень тяжелыми. Впрочем, нам удалось сохранить лактацию — в этом очень помог вовремя купленный электрический молокоотсос компании «здесь могла бы быть ваша реклама». Первые девять дней Евгения вместе с Никитой лежали в роддоме — это было психологически почти невыносимо, потому что там же все радостные, выписываются постоянно с салютом и танцами — а у нас радости особенной, как вы понимаете, не было.
Через девять дней Никиту перевели в реанимацию Филатовской больницы (хочется сказать «повезло», но на самом деле это не так — просто врачи из 32 роддома сделали все от них зависящее, чтобы Никита попал именно в эту больницу). Неизменно, каждый день мы выслушивали фразу о том, что «состояние ребенка очень тяжелое», и шли сцеживаться.
Неизменно, каждый день мы выслушивали фразу о том, что «состояние ребенка очень тяжелое», и шли сцеживаться.
В Филатовской, несмотря на то, что нам стало полегче — по крайней мере, мы оказались в такой же толпе хмуро сосредоточенных родителей в одноразовых халатах и масках и с футлярами для бутылочек с молоком — Никите стало потяжелее. У него в день переезда было легочное кровотечение, и выглядел в последующие дни он невесело — синеватый, с пятнами от кандидоза (пять антибиотиков одновременно), дышащий принудительно. Заведующая отделением реанимации «да, у нас отделение страшное» каждый день говорила про «состояние стабильно тяжелое». Жути нагнетало то, что в Филатовской врачи обращаются к родителям пациентов «папа» и «мама», что на психологическом состоянии этих родителей тоже сказывается не лучшим образом.
Переломный момент наступил неожиданно — я зашел в палату и увидел, что сигнал тревоги у аппарата ИВЛ отключен, но мигает вовсю (такой характерный колокольчик на дисплее перечеркнутый), и на датчике — ровная линия. Стал выяснять, что происходит, «вы что ли не видите, что сигнал отключен? И что он не дышит? спасите, помогите! — и услышал от медсестры: «Да не волнуйтесь вы так. Мы его с аппарата искусственного дыхания только что сняли. Идет на поправку».
Стал выяснять, что происходит, «вы что ли не видите, что сигнал отключен? И что он не дышит? спасите, помогите! — и услышал от медсестры: «Да не волнуйтесь вы так. Мы его с аппарата искусственного дыхания только что сняли. Идет на поправку».
Аспирация мекония у новорожденных — презентация онлайн
2. ОПРЕДЕЛЕНИЕ
Аспирация мекония — комплекс
патофизиологических событий,
характеризующихся механической
обструкцией дыхательных путей,
химическим пневмонитом и
инактивацией сурфактанта
Robertson В. Archives of Disease in childhood1996;75:F1-F3
содержимое кишечника младенца
при рождении, которое представляет собой продукт из амниотической
жидкости, фетальных волос, кишечного эпителия, гастроинтестинального секрета (70-80% воды, муцин,
желчные кислоты, холестерин, 3-9%
белка и активных энзимов)
у переношенных
родившихся в срок в состоянии
гипоксии
у младенцев с задержкой
внутриутробного развития
Синдром аспирации мекония редко
возникает при нормальном развитии
плода, если роды происходят раньше 34
недель гестации
5.
 Основные методы пренатальной диагностики меконеальных вод
Основные методы пренатальной диагностики меконеальных вод
• Амниоскопия и амниоцентез (Sailing,
1962), частота осложнений 0,5 – 2,5%
• Ультразвуковое сканирование:
определение количества
околоплодных вод и наличие в них
взвеси
• Допплерографическое сканирование
Меконий встречается в амниотической жидкости приблизительно
в 10% родов. В половине случаев
меконий будет присутствовать ниже
голосовых связок, и у 20% этих детей появится клиника дыхательной
недостаточности
7. Профилактика САМ
• Точное определение срока беременности
• Антенатальная диагностика мекония в
околоплодных водах
• Антенатальная диагностика гипоксических
состояний плода
• Интранатальная диагностика гипоксии (КТГ,
пульсоксиметрия)
• Ограничение родостимуляции
• Профилактическая амниоинфузия
• Санация носо- и ротоглотки до рождения
туловища, санация трахеи
Козлов В.П. Вопросы акушерства, гинекологии и перинатологии 2003. Т.2, N94, с.49-52
Т.2, N94, с.49-52
8. Применение амниоинфузии при мекониальных околоплодных водах
ВЫВОД: ПРОВЕДЕНИЕ
АМНИОИНФУЗИИ ПРИВОДИТ К
УЛУЧШЕНИЮ ПРОГНОЗА В
ПЕРИНАТАЛЬНОМ ПЕРИОДЕ
Hofmeyr GJ. Amninioinfusion for meconium-stained liquor in labour. The
Сосhraпе Database of Systematic Reviews 2002, Issue 1.
ФЕТАЛЬНАЯ ГИПОКСИЯ
МЕЗЕНТЕРИАЛЬНАЯ ВАЗОКОНСТРИКЦИЯ
РАЗДРАЖЕНИЕ ДЫХАТЕЛЬНОГО ЦЕНТРА
ИШЕМИЯ КИШЕЧНИКА
АТОНИЯ АНАЛЬНОГО
СФИНКТЕРА
ГИПЕРПЕРИСТАЛЬТИКА
В/УТРОБНОЕ ОТХОЖДЕНИЕ МЕКОНИЯ
АСПИРАЦИЯ МЕКОНИЯ
АТЕЛЕКТАЗЫ, ЭМФИЗЕМА, ХИМ. ПНЕВМОНИТ
ВНУТРИЛЕГОЧНОЕ
ШУНТИРОВАНИЕ
ПОВЫШЕНИЕ
РЕЗИСТЕНТНОСТИ
ДЫХ. ПУТЕЙ
СНИЖЕНИЕ
КОМПЛАЙНСА
ПУЛЬМОНАЛЬНАЯ ВАЗОКОНСТРИКЦИЯ
ГИПОКСИЯ
АЦИДОЗ
А — нормальная альвеола; В — полная обструкция и ателектазирование;
С, D — «эффект клапана»; Е — перерастяжение и разрыв альвеолы;
F — ателектазирование
Owens CM Meconium aspiration, p,51
Прокрашенные меконием кожа, ногтевые
фаланги, пуповина
Часто асфиксия при рождении
Тахипное, диспное, втяжение межреберий
Цианоз
Экспираторные стоны
Нарушение кардиоваскулярной
адаптации (гипо- или гипертензия, СН,
право-левый шунт, периферическая
гипоперфузия)
Участки крупных неправильной
формы затемнений, чередующиеся с
участками повышенной прозрачности
В ¼ случаев в плевре и междолевых
пространствах определяется жидкость
и воздух
При обильной аспирации – симптом
«снежной бури» и кардиомегалия
Участки крупных
неправильной формы затемнений, чередующиеся с участками повышенной прозрачности
Cимптом
«снежной бури»
Адекватная первичная реанимационная
помощь
«Minimal handling»
Адекватная респираторная поддержка
Седация и анальгезия
Коррекция кардиоваскулярных нарушений
Поддержание водно-электролитного баланса
Антибактериальная терапия
Сурфактантная терапия
Раннее энтеральное и парентеральное питание
Поддержание кислородной емкости крови
(коррекция анемии)
Физиотерапия (вибромассаж)
Опытный медицинский персонал
Термонейтральное окружение
Немедленная санация ротоглотки при
прорезывании головки
Интубация и санация трахеи по возможности до
первого вдоха (толстый катетер)
ИВЛ по строгим показаниям
При необходимости – противошоковые
мероприятия
Перевод в ОИТР после стабилизации
состояния
Беспокоить ребёнка как можно меньше;
Оптимизировать мероприятия по уходу за
ребёнком;
Наблюдать за ребёнком во время проведения
диагностических и терапевтических мероприятий,
при
необходимости
манипуляцию
прервать;
Неинвазивный постоянный мониторинг в большинстве случаев предпочтительнее, чем интермитирующее мануальное измерение;
Не забывать о локальной анестезии: мнение,
что недоношенные дети к боли нечувствительны, глубоко ошибочно, но широко распространено
1.
2.
3.
Показания к переводу на ИВЛ :
РаО2 – менее 50 мм Hg (при FiO2 более 0,7)
РаСО2 – более 50 мм Hg
Стартовые параметры:
ЧД 60-70 в минуту
Tin 0,25-0,35 сек.
Tin:Tex = 1:2
PEEP 0-3 см Н2О
PIP – до видимой экскурсии грудной клетки
Поток 12-16 л/мин.
При ПЛГ первые трое суток поддерживать оксигенацию
на высоком уровне (SatO2 не менее 95%, РаО2 не менее
65 мм Hg), медленная редукция параметров ИВЛ
При сопутствующей ПЛГ:
фентанил 1-2 мкг/кг в час
диазепам 0,5-1 мг/кг в час
релаксация (панкуроний 0,03 мг/кг
на введение каждые 3-4 часа)
фенобарбитал:
— стартовая доза 20 мг/кг в/венно,
— поддерживающая доза 5-10 мг/кг
каждые 6-8 часов
Не допускать снижения систолического
давления ниже 50 мм Hg, диастолического
– ниже 25 мм Hg
Кардиотоники:
дофамин 5-20 мкг/кг в мин.
добутамин 5-20 мкг/кг в мин.
норадреналин 0,01-0,05-5 мкг/кг в мин
При необходимости: ЭР-масса, СЗП
Постоянный мониторинг АД, ЧСС, SatO2
1 сутки: ЖП = 80-100 мл/кг
В последующем увеличение ЖП на 20
мл/кг в сутки до достижения 160 мл/кг
в сутки
Контроль удельного веса мочи 2 раза в
сутки (стремиться к значению 1010)
Внимание: гиперволемия может
ухудшить состояние ребенка
Дотация электролитов в суточной
потребности
Целесообразно использование комбинации антибиотиков широкого
спектра действия:
цефалоспорины III поколения +
аминогликозиды
При необходимости – включение в
антибактериальную терапию
метронидазола
При сопутствующей длительно
сохраняющейся персистирующей
легочной гипертензии доказан
положительный эффект многократного
(3-4 раза) введения препаратов
сурфактанта в дозе 100 мг/кг на
введение
Баротравма (пневмоторакс,
интерстициальная эмфизема)
Волюмтравма
Нозокомиальные инфекции
Токсическое действие О2
ВЖК
ПВЛ
БЛД
Аспирация мекония у новорожденных — синдром, последствия
Этот синдром является самостоятельной нозологией. Преимущественно аспирация мекония наблюдается у переношенных или доношенных детей, подвергшихся длительной внутриутробной или острой интранатальной гипоксии. Это приводит к спазму сосудов брыжейки, усилению перистальтики кишечника, расслаблению анального сфинктера и выходу мекония в околоплодные воды. Это возможно даже при отсутствии асфиксии — при обвитии пуповины вокруг шеи, сдавлении ее, что стимулирует вагусную реакцию и выход мекония. В этой статье мы расскажем о том, что такое аспирация мекония у новорожденных — синдром, последствия.
Преимущественно аспирация мекония наблюдается у переношенных или доношенных детей, подвергшихся длительной внутриутробной или острой интранатальной гипоксии. Это приводит к спазму сосудов брыжейки, усилению перистальтики кишечника, расслаблению анального сфинктера и выходу мекония в околоплодные воды. Это возможно даже при отсутствии асфиксии — при обвитии пуповины вокруг шеи, сдавлении ее, что стимулирует вагусную реакцию и выход мекония. В этой статье мы расскажем о том, что такое аспирация мекония у новорожденных — синдром, последствия.
Что собой представляет аспирация меконием?
Частота окрашивания околоплодных вод меконием колеблется от 8 до 20% от общего числа родов. У 50% из этих детей меконий обнаруживается в трахее и бронхах, но только у 1/3 новорожденных развивается синдром аспирации мекония.
Этиология
Гипоксия и другие формы внутриутробного стресса плода вызывают усиление перистальтики кишечника, расслабление наружного анального сфинктера и отхождение мекония.
Первые дыхательные движения плода обнаруживаются уже на 11 неделе гестационного периода. Периоды дыхания редко длятся более 10 минут и чередуются с апноэ продолжительностью до 1-2 часов. Гипоксия приводит к появлению преждевременных глубоких «вздохов», во время которых мекониальные околоплодные воды попадают в дыхательные пути. Перемещение мекония в дыхательные пути малого калибра происходит быстро, в течение часа после рождения.
Патогенез дыхательных расстройств при синдроме аспирации, в первую очередь, связан с нарушением проходимости дыхательных путей и механическим препятствием заполнению легких воздухом. При этом в любом отделе респираторного тракта может возникнуть полная или частичная обструкция с развитием клапанного механизма. При полной обструкции дыхательных путей воздух не может проникнуть в нижележащие отделы, в результате чего возникает коллабирование участков легкого с образованием субсегментарных ателектазов. Клапанный механизм обструкции заключается в том, что при вдохе воздух, обтекая препятствие, попадает в дистальные отделы респираторного тракта, а при выдохе препятствие полностью перекрывает просвет бронха и не дает воздуху выйти, поскольку просвет мелких воздухоносных путей увеличивается при вдохе и уменьшается при выдохе.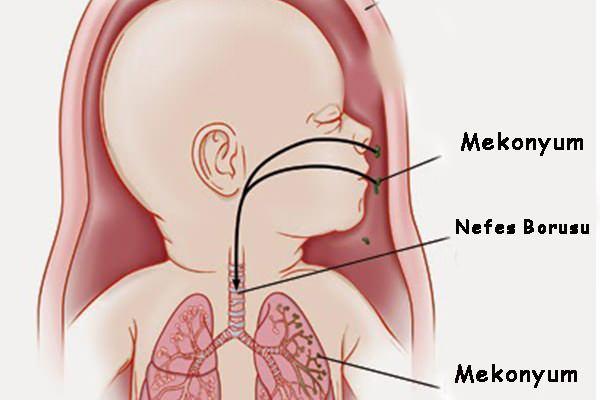
Задержка и накопление воздуха ниже места обструкции приводит к перерастяжению альвеол, образованию «воздушных ловушек» и эмфиземы. В результате снижается растяжимость легких, ухудшаются вентиляционно-перфузионные отношения, увеличиваются внутрилегочное шунтирование и сопротивление дыхательных путей. На фоне усиленного дыхания и неравномерной вентиляции может произойти разрыв альвеол, ведущий к утечке воздуха из легких.
Кроме механической обструкции, присутствие мекония, содержащего желчные соли и активные протеолитические ферменты, является причиной химического воспаления бронхиального и альвеолярного эпителия. Это создает предпосылки для развития бактериальной флоры и прогрессирования трахеобронхита и пневмонии.
Неравномерная вентиляция, нарушение вентиляционно-перфузионных отношений и присоединившийся пневмонит приводят к развитию гипоксемии, гиперкапнии и ацидоза.
При возникновении гипоксии и ацидоза развивается выраженный спазм легочных сосудов, что приводит к развитию вторичной легочной гипертензии. Величина давления в легочной артерии может достигать уровня системного и даже превышать его. Фетальные коммуникации не закрываются, а напротив, усиливается шунтирование крови через артериальный проток и овальное окно. Шунт крови справа — налево может достигать 70 — 80%.
Величина давления в легочной артерии может достигать уровня системного и даже превышать его. Фетальные коммуникации не закрываются, а напротив, усиливается шунтирование крови через артериальный проток и овальное окно. Шунт крови справа — налево может достигать 70 — 80%.
Легочная гипертензия, в свою очередь, оказывает отрицательное влияние на функцию правого, а затем и левого желудочков сердца. Острое увеличение постнагрузки правого желудочка сопровождается уменьшением фракции изгнания, что ведет к снижению преднагрузки левого желудочка и сердечного выброса.
По данным различных акушерских стационаров, присутствие мекония в околоплодных водах регистрируется в 2 — 10% случаев, однако синдром массивной мекониальной аспирации (MAC) встречается в 5 — 10 раз реже.
Чем опасна аспирация мекония у новорожденных?
Аспирированный меконий вызывает воспалительную реакцию в трахее, бронхах, легочной паренхиме за счет содержащихся в нем липидов, протеолитических ферментов и его повышенной осмолярности. Возникают также обструкция глубоких дыхательных путей, «воздушные ловушки», ателектазы из-за закупорки бронхов и инактивации сурфактанта, что приводит к спадению альвеол на выдохе. Помимо химического воспаления и ателектазов, в легких возникает отек, перифокальная эмфизема с развитием легочной гипертензии, пневмоторакс и другие виды «утечки воздуха».
Возникают также обструкция глубоких дыхательных путей, «воздушные ловушки», ателектазы из-за закупорки бронхов и инактивации сурфактанта, что приводит к спадению альвеол на выдохе. Помимо химического воспаления и ателектазов, в легких возникает отек, перифокальная эмфизема с развитием легочной гипертензии, пневмоторакс и другие виды «утечки воздуха».
Результаты последних исследований выявили высокое содержание в крови новорожденных с мекониальной аспирацией иммунореактивного эндотелина-1, который обладает выраженным сосудосуживающим эффектом, что способствует развитию легочной гипертензии и гиперреактивности легочных сосудов. Летальность при тяжелых формах мекониальной аспирации до недавнего времени составляла 50%. В настоящее время за счет совершенствования методов первичной реанимации и использования, в необходимых случаях, ВЧО ИВЛ летальность значительно снизилась.
Если меконий густой, в виде глыбок, следует очистить от него нос и ротоглотку новорожденного ещё до того, как грудная клетка выйдет из родового канала. Сразу же после рождения, как и при аспирации околоплодных вод, производят эндотрахеальную интубацию и отсасывают содержимое из трахеи до полного её очищения. Удаление заглоченного мекония из желудка предупреждает повторную аспирацию. Всем детям проводят оксигенотерапию, иногда вплоть до длительной искусственной вентиляции легких (в тяжёлых случаях). Мекониальная аспирация новорожденных лечится антибиотикотерапией.
Сразу же после рождения, как и при аспирации околоплодных вод, производят эндотрахеальную интубацию и отсасывают содержимое из трахеи до полного её очищения. Удаление заглоченного мекония из желудка предупреждает повторную аспирацию. Всем детям проводят оксигенотерапию, иногда вплоть до длительной искусственной вентиляции легких (в тяжёлых случаях). Мекониальная аспирация новорожденных лечится антибиотикотерапией.
Дети с синдромом аспирации мекония
Как правило, новорожденные рождаются с низкой оценкой по шкале Апгар. У переношенных детей часто имеется прокрашивание меконием
ногтей, кожи, пуповины.
Существует два варианта клинического течения мекониальной аспирации:
- С рождения у многих детей отмечаются признаки дыхательных расстройств, у части — приступы вторичной асфиксии, притупление легочного звука, повышение ригидности грудной клетки, обильные разнокалиберные влажные хрипы в легких.
- У части детей после рождения имеется «светлый» промежуток, после которого (по мере продвижения мелких частиц мекония к мелким бронхам) возникает клиника тяжелой дыхательной недостаточности.
 В наиболее тяжелых случаях мекониальная аспирация осложняется синдромом персистирующей легочной гипертензии (ПЛГ), при ИВЛ частым нередким осложнением является синдром «утечки воздуха». Через 24-48 часов большинство детей развивают клинику аспирационной пневмонии.
В наиболее тяжелых случаях мекониальная аспирация осложняется синдромом персистирующей легочной гипертензии (ПЛГ), при ИВЛ частым нередким осложнением является синдром «утечки воздуха». Через 24-48 часов большинство детей развивают клинику аспирационной пневмонии.
Диагностика
Чтобы диагностировать синдром аспирации мекония у новорожденных, врачам нужно провести тщательный анализ клинико-анамнестических данных.
После этого необходима рентгенограмма легких, выявляющая сочетание крупных участков затемнения, отходящих от корней легких, с участками эмфизематозных вздутий. Характерен симптом «снежной бури», кардиомегалия, реже — пневмоторакс. Диафрагма уплощена, переднезадний размер грудной клетки увеличен. Если в мекониальных водах обнаружены плотные фрагменты мекония, то вероятность мекониальнои аспирации и пневмонии гораздо выше, чем тогда, когда околоплодные воды просто окрашены меконием.
Лечение
Необходимо раннее отсасывание мекония из дыхательных путей сразу после рождения до начала вспомогательной вентиляции легких (Приложение 1 к Приказу МЗ РФ №372). Удалив содержимое желудка, интубируют трахею и проводят отсасывание мекония из нее, промывают трахею 1-2 мл стерильного изотонического раствора хлорида натрия и отсасывают. Затем начинают ИВЛ в течение 1-2 минут и снова повторяют процедуру промывания «до получения светлых вод» каждые 30 минут в первые 2 часа жизни. Интенсивность и длительность респираторной терапии, а также особенности поддерживающей терапии, зависят от тяжести клинической картины и имеют много общего с РДС. Из-за высокого риска пневмонии всем детям с синдромом аспирации мекония необходимо раннее назначение антибиотикотерапии.
Удалив содержимое желудка, интубируют трахею и проводят отсасывание мекония из нее, промывают трахею 1-2 мл стерильного изотонического раствора хлорида натрия и отсасывают. Затем начинают ИВЛ в течение 1-2 минут и снова повторяют процедуру промывания «до получения светлых вод» каждые 30 минут в первые 2 часа жизни. Интенсивность и длительность респираторной терапии, а также особенности поддерживающей терапии, зависят от тяжести клинической картины и имеют много общего с РДС. Из-за высокого риска пневмонии всем детям с синдромом аспирации мекония необходимо раннее назначение антибиотикотерапии.
Искусственная вентиляция легких
В первые двое суток ее обычно проводят в контролируемом режиме с частотой 50-70 вдохов в 1 минуту, максимальным давлением на вдохе 25-30 см вод. ст. и положительным давлением в конце выдоха +3-4 см вод. ст. Для предотвращения задержки воздуха в легких и развития эмфизематозных участков отношение времени вдоха к выдоху не должно быть больше, чем 1:2. При наличии симптомов легочной гипертензии оправдано поддержание умеренной гипервентиляции с уровнем PaCO2 — 33-30 мм рт. ст.
При наличии симптомов легочной гипертензии оправдано поддержание умеренной гипервентиляции с уровнем PaCO2 — 33-30 мм рт. ст.
1.
Для синхронизации дыхания ребенка с работой респиратора в этот период обязательно используются седативные препараты, центральные анальгетики и миорелаксанты (реланиум в дозе 0,5 мг/кг, промедол — 0,2-0,4 мг/кг, ардуан — 0,04-0,06 мг/кг).
2.
Дефицит циркулирующей крови у новорожденных с мекониальной аспирацией чаще всего связан с уменьшением плазменного объема. Поэтому в состав препаратов для инфузионной терапии включают плазму из расчета 10-15 мл/кг.
3.
Если несмотря на восполнение дефицита ОЦК у ребенка сохраняется гипотензия, то в качестве средства лечения назначают допамин в дозе 7-10 мкг/кг/мин.
Учитывая высокую вероятность развития пневмонии, детям для лечения сразу назначают антибиотики широкого спектра действия. В дальнейшем антибактериальная терапия меняется в соответствии с данными бактериального обследования и антибиотикограммы.
Последствия аспирации меконием. При несвоевременном удалении мекония из дыхательных путей и осложнении мекониальной аспирацией осложненной синдромом персистирующей легочной гипертензии летальность достигает 10%. При благоприятном течении даже при массивной аспирации рентгенограмма нормализуется к 2 неделям, но повышенная пневматизация легких и участки фиброза могут наблюдаться несколько месяцев.
Теперь вы знаете о том, что такое синдром аспирации мекония у новорожденных.
Практический опыт, который помогает предупредить тяжесть синдрома аспирации мекония
PERINATOLOGIYA I PEDIATRIYA.2015.4(64):61-63; doi 10.15574/PP.2015.64.61
Практический опыт, который помогает предупредить тяжесть синдрома аспирации мекония
Чуйко М. Н.
Львовский национальный медицинский университет имени Данила Галицкого, г. Львов, Украина
Львов, Украина
В статье приведены важные практические составляющие работы врача-неонатолога отделения новорожденных роддома в случаях риска рождения ребенка с синдромом аспирации мекония. Отмечено, что синдром аспирации мекония — это проблема не только доношенных и переношенных детей, но и недоношенных новорожденных. Представлена клиническая классификация степени тяжести синдрома аспирации мекония. Показано, с какими признаками ассоциируется летальность при синдроме аспирации мекония.
Ключевые слова: синдром аспирации мекония, новорожденные.
Литература:
1. Чуйко ММ. 2008. А. с. Міністерство освіти і науки України; Державний департамент інтелектуальної власності. Науково-прикладний твір «Стандартизована форма запису основних анамнестичних даних, клінічних, лабораторно-інструментальних даних новонароджених з ризиком внутрішньошлуночкових крововиливів (ВШК)». № 24 454; Опубл. 14.05.2008 р.
2. Запорожана ВМ, Аряєв МЛ, Добрянський ДО. 2013. Акушерство та гінекологія. Національний підручник. У 4 т. Кол авт. За ред акад НАМН України, проф ВМ Запорожана. Т2: Неонатологія. Київ, ВСВ «Медицина»: 928.
2013. Акушерство та гінекологія. Національний підручник. У 4 т. Кол авт. За ред акад НАМН України, проф ВМ Запорожана. Т2: Неонатологія. Київ, ВСВ «Медицина»: 928.
3. Клінічний протокол з акушерської допомоги «Дистрес плода при вагітності та під час пологів». Наказ МОЗ України від 27.12.2006 р. № 900. http://www.moz.gov.ua.
4. Лікувальні медичні заклади України. Як захиститись при порушенні прав пацієнта. Всеукраїнська громадська організація «Соціальна Україна». Київ, ТОВ «Інтерконтиненталь Україна». 2014: 81.
5. Полин РА, Спитцер АР. 2011. Секреты неонатологии и перинатологиий. Пер с англ. Москва, БИНОМ: 624.
6. Уніфікований клінічний протокол «Початкова, реанімаційна і після реанімаційна допомога новонародженим в Україні». Наказ МОЗ України від 28.14.2014 р. № 225. http://www.moz.gov.ua.
7. Cleary GM, Wiswell TE. 1998. Meconium-stained amniotic fluid and the meconium aspiration syndrome: an update. Pediatr Clin North Am. 45: 511—529.
8. Deepak L, Sourabn KM, Praven K. 2014. Predictors of Mortality in Neonates with Meconium Aspiration Syndrome. Indian pediatrics. 51: 638—640.
Deepak L, Sourabn KM, Praven K. 2014. Predictors of Mortality in Neonates with Meconium Aspiration Syndrome. Indian pediatrics. 51: 638—640.
9. Emmerson AJ-B. 2014. Predictors of Mortality in Neonates with Meconium Aspiration Syndrome. Indian pediatrics. 51: 610—611.
10. Fetal and neonatal brain injury. 4th ed. Еd by DK Stevenson, EW Benits, Philip Sunshine et al. New York, Cambridge University Press. 2009: 628.
11. Osava RH. Meconium-stained amniotic fluid and maternal and neonatal factors associated. Rev Saude Publica. Approved: 5/24/2012/Article available from: www.scielo.br/rsp.
Синдром аспирации мекония | Johns Hopkins Medicine
Что такое синдром аспирации мекония?
Меконий — это первый кал или стул новорожденного. Синдром аспирации мекония возникает, когда новорожденный вдыхает смесь мекония и околоплодных вод в легкие примерно во время родов. Синдром аспирации мекония, ведущая причина тяжелых заболеваний и смерти новорожденных, встречается примерно от 5 до 10 процентов рождений. Обычно это происходит, когда плод испытывает стресс во время родов, особенно когда у ребенка истек срок родов.
Обычно это происходит, когда плод испытывает стресс во время родов, особенно когда у ребенка истек срок родов.
Симптомы
- Голубоватый цвет кожи младенца
- Проблемы с дыханием
- Темное зеленоватое пятно или полосы околоплодных вод или очевидное присутствие мекония в околоплодных водах
- Вялость у новорожденного при рождении
Диагностика
- Перед родами монитор плода может показывать медленное сердцебиение.
- При рождении меконий можно увидеть в околоплодных водах. Самый точный тест для проверки возможной аспирации мекония заключается в поиске пятен мекония на голосовых связках с помощью ларингоскопа.
- Аномальные звуки дыхания, особенно грубые, потрескивающие, слышны через стетоскоп.
- Анализ газов крови показывает пониженную кислотность крови, пониженное содержание кислорода и повышенное содержание углекислого газа.
- Рентген грудной клетки может показать пятнистые или полосатые участки на легких.

Лечение
Рот новорожденного следует отсосать, как только во время родов будет видна голова. Дальнейшее лечение необходимо при сильном окрашивании мекония и дистрессе плода.Младенец может быть помещен в ясли особого ухода или отделение интенсивной терапии новорожденных. Другие методы лечения могут включать:
- Антибиотики для лечения инфекций
- Дыхательный аппарат для поддержания надутого состояния легких
- Использование грелки для поддержания температуры тела
- Постукивание по груди для отделения секрета
Если во время беременности не было никаких признаков дистресс-синдрома плода, а ребенок — здоровый доношенный новорожденный, специалисты рекомендуют не проводить глубокое отсасывание дыхательного горла из опасения вызвать определенный тип пневмонии.
Прогноз
В большинстве случаев прогноз отличный и нет серьезных побочных эффектов. В более тяжелых случаях могут возникнуть проблемы с дыханием, хотя обычно они проходят через два-четыре дня. Однако учащенное дыхание может сохраняться в течение нескольких дней. Младенец с тяжелой аспирацией, которому требуется дыхательный аппарат, может иметь более осторожный исход. Недостаток кислорода в матке или осложнения аспирации мекония могут привести к повреждению головного мозга. Аспирация мекония редко приводит к необратимому повреждению легких.
Однако учащенное дыхание может сохраняться в течение нескольких дней. Младенец с тяжелой аспирацией, которому требуется дыхательный аппарат, может иметь более осторожный исход. Недостаток кислорода в матке или осложнения аспирации мекония могут привести к повреждению головного мозга. Аспирация мекония редко приводит к необратимому повреждению легких.
Синдром аспирации мекония: история вопроса, патофизиология, этиология
Сингх Б.С., Кларк Р.Х., Пауэрс Р.Дж., Спитцер А.Р. Синдром аспирации мекония остается серьезной проблемой в отделении интенсивной терапии новорожденных: результаты и схемы лечения доношенных новорожденных, поступивших в реанимацию в течение десятилетнего периода. Дж Перинатол . 2009 июл.29 (7): 497-503. [Медлайн].
Янссен Д. Д., Карниелли В. П., Кого П. и др. Метаболизм поверхностно-активного фосфатидилхолина у новорожденных с синдромом аспирации мекония.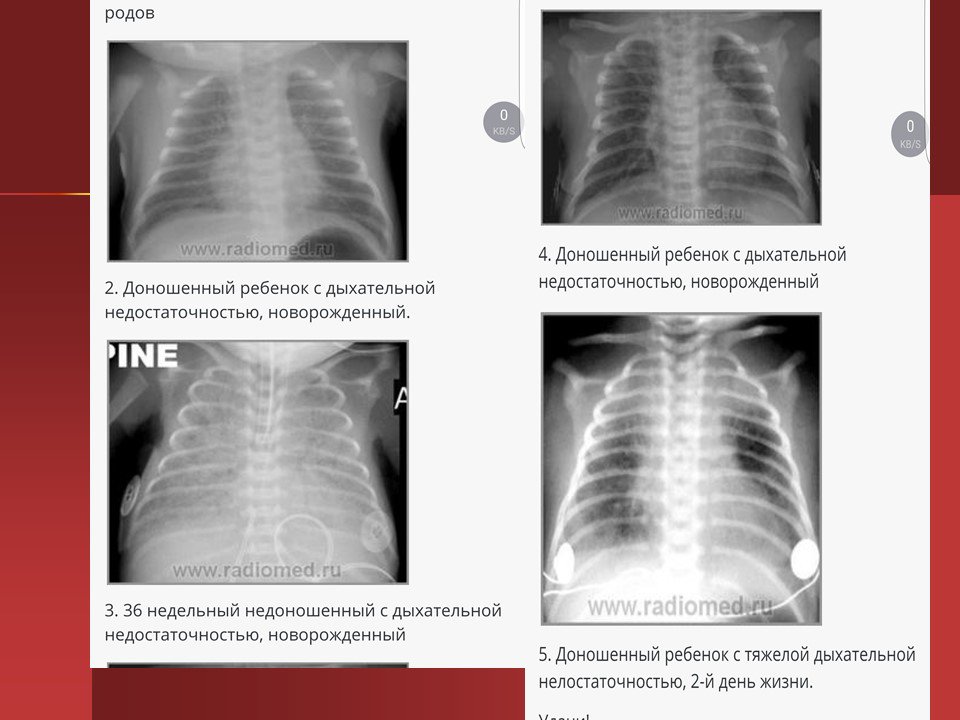 Дж. Педиатр . 2006 ноябрь 149 (5): 634-9. [Медлайн].
Дж. Педиатр . 2006 ноябрь 149 (5): 634-9. [Медлайн].
Кларк Д.А., Ниман Г.Ф., Томпсон Дж.Э., Пасканик А.М., Рохар Дж.Э., Бреденберг CE. Замещение поверхностно-активного вещества жирными кислотами, свободными от мекония: альтернативное объяснение ателектаза при синдроме аспирации мекония. Дж. Педиатр . 1987 май. 110 (5): 765-70. [Медлайн].
Терасака Д., Кларк Д.А., Сингх Б.Н., Рокар Дж. Свободные жирные кислоты мекония человека. Биол Новорожденных .1986. 50 (1): 16-20. [Медлайн].
Wiswell TE, Tuggle JM, Turner BS. Синдром аспирации мекония: что мы сделали? Педиатрия . 1990 Май. 85 (5): 715-21. [Медлайн].
Йодер Б.А., Кирш Е.А., Барт У.Г., Гордон М.С. Изменение акушерской практики, связанное со снижением заболеваемости синдромом аспирации мекония. Акушерский гинекол . 2002 май. 99 (5 пт 1): 731-9. [Медлайн].
Акушерский гинекол . 2002 май. 99 (5 пт 1): 731-9. [Медлайн].
Балчин И., Уиттакер Дж.С., Ламонт РФ, Стир П.Дж.Характеристики матери и плода, связанные с околоплодными водами, окрашенными меконием. Акушерский гинекол . 2011 Апрель 117 (4): 828-35. [Медлайн].
Macfarlane PI, Heaf DP. Легочная функция у детей после неонатального синдрома аспирации мекония. Арк Дис Детский . 1988 апр. 63 (4): 368-72. [Медлайн].
Ghidini A, Spong CY. Синдром тяжелой аспирации мекония не вызван аспирацией мекония. Am J Obstet Gynecol .2001 Октябрь 185 (4): 931-8. [Медлайн].
[Рекомендации] Wyckoff MH, Aziz K, Escobedo MB, et al. Часть 13: Реанимация новорожденных: Обновление рекомендаций Американской кардиологической ассоциации 2015 г. по сердечно-легочной реанимации и неотложной сердечно-сосудистой помощи. Тираж . 2015 г. 3 ноября. 132 (18 приложение 2): S543-60. [Медлайн].
по сердечно-легочной реанимации и неотложной сердечно-сосудистой помощи. Тираж . 2015 г. 3 ноября. 132 (18 приложение 2): S543-60. [Медлайн].
Американский колледж акушеров и гинекологов. Заключение комитета ACOG № 689 резюме: роды новорожденного с околоплодными водами, окрашенными меконием. Акушерский гинекол . 2017 Март 129 (3): 593-4. [Медлайн].
Nangia S, Pal MM, Saili A, Gupta U. Влияние внутриродовой ротоглоточной аспирации (IP-OP) на синдром аспирации мекония (MAS) в развивающихся странах: РКИ. Реанимация . 2015 Декабрь 97: 83-7. [Медлайн].
Boujenah J, Oliveira J, De La Hosseraye C, Benbara A, Tigaizin A, Bricou A, et al. Следует ли проводить забор крови с черепа плода в случае околоплодных вод, окрашенных меконием? J Matern Fetal Neonatal Med . 2016 29 декабря (23): 3875-8. [Медлайн].
[Медлайн].
Лю Дж., Цао Х.Й., Фу В. Ультрасонография легких для диагностики синдрома аспирации мекония у новорожденных. J Int Med Res . 2016 г. 1 ноября. [Medline].
Американский колледж акушеров и гинекологов. Заключение комитета ACOG № 579: определение срока беременности. Акушерский гинекол . 2013 ноябрь 122 (5): 1139-40. [Медлайн].
Американский колледж акушеров и гинекологов.Заключение комитета ACOG № 561: ранние роды по немедицинским показаниям. Акушерский гинекол . 2013 Апрель 121 (4): 911-5. [Медлайн].
Акушерская практика комитета ACOG. Заключение комитета ACOG № 346, октябрь 2006 г .: инфузия амниона не предотвращает синдром аспирации мекония. Акушерский гинекол . 2006 Октябрь 108 (4): 1053. [Медлайн].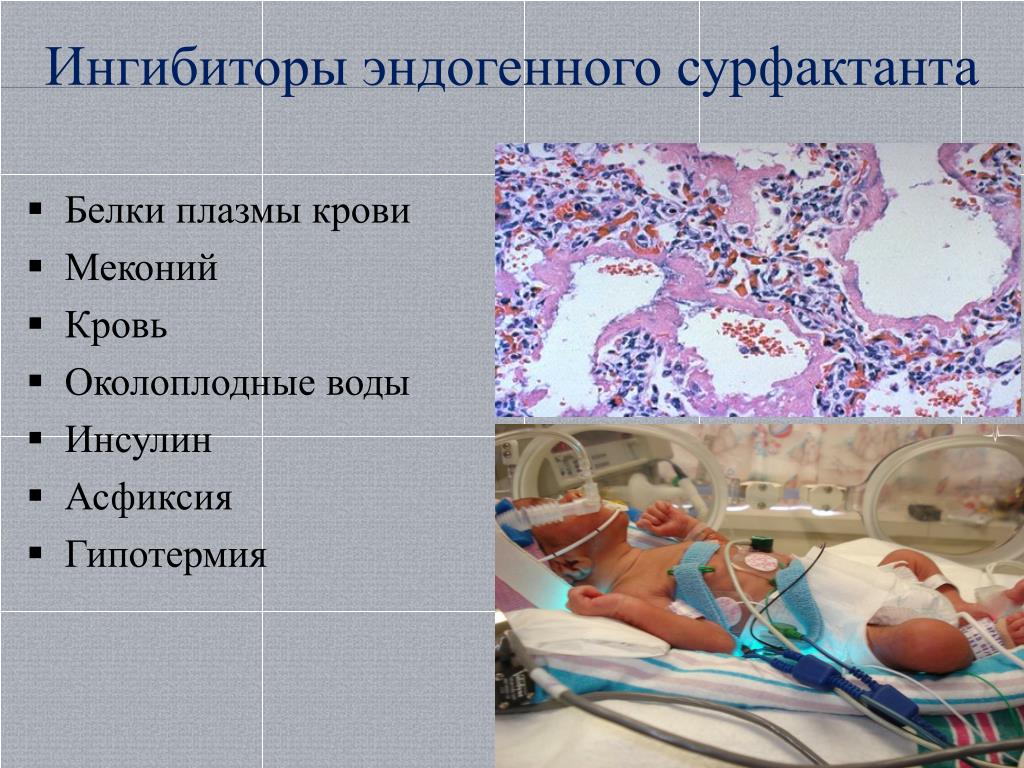
Велафи С., Видьясагар Д. Ведение младенцев, рожденных от матерей с околоплодными водами, окрашенными меконием: рекомендации, основанные на фактических данных. Клин Перинатол . 2006 Mar.33 (1): 29-42, v-vi. [Медлайн].
Hofmeyr GJ, Xu H. Амниоинфузия ликвора, окрашенного меконием, во время родов. Кокрановская база данных Syst Rev . 20 января 2010 г. CD000014. [Медлайн].
Fraser WD, Hofmeyr J, Lede R, et al, для группы испытаний амниоинфузии. Амниоинфузия для профилактики синдрома аспирации мекония. N Engl J Med . 2005 сентябрь 1. 353 (9): 909-17. [Медлайн].
Комитет по акушерской практике, Американский колледж акушеров и гинекологов.Заключение комитета ACOG № 379: ведение родов новорожденного с околоплодными водами, окрашенными меконием. Акушерский гинекол . 2007 Сентябрь 110 (3): 739. [Медлайн].
Акушерский гинекол . 2007 Сентябрь 110 (3): 739. [Медлайн].
Напрасный Н.Э., Шилд Е.Г., Прудент Л.М., Висвелл Т.Э., Агилар А.М., Вивас Н.И. Отсасывание из ротоглотки и носоглотки новорожденных, окрашенных меконием, перед родами: многоцентровое рандомизированное контролируемое исследование. Ланцет . 2004 14-20 августа. 364 (9434): 597-602. [Медлайн].
Chettri S, Bhat BV, Adhisivam B.Современные концепции лечения синдрома аспирации мекония. Индийский Дж. Педиатр . 2016 Октябрь 83 (10): 1125-30. [Медлайн].
Wiswell TE, Knight GR, Finer NN и др. Многоцентровое рандомизированное контролируемое исследование, сравнивающее лаваж сурфаксина (луцинактанта) со стандартными методами лечения синдрома аспирации мекония. Педиатрия . 2002 июн.109 (6): 1081-7. [Медлайн].
Dargaville PA. Нововведение в сурфактантной терапии I: лаваж сурфактанта и введение сурфактанта болюсом жидкости с использованием минимально инвазивных методов. Неонатология . 2012. 101 (4): 326-36. [Медлайн].
El Shahed AI, Dargaville PA, Ohlsson A, Soll R. Поверхностно-активное вещество при синдроме аспирации мекония у доношенных и поздних недоношенных детей. Кокрановская база данных Syst Rev .2014 14 декабря. CD002054. [Медлайн].
Коллинз М. П., Лоренц Дж. М., Джеттон Дж. Р., Панет Н. Гипокапния и другие связанные с вентиляцией факторы риска церебрального паралича у младенцев с низкой массой тела при рождении. Педиатр Рес . 2001 декабрь 50 (6): 712-9. [Медлайн].
2001 декабрь 50 (6): 712-9. [Медлайн].
Abman SH, Kinsella JP. Ингаляционная терапия оксидом азота при заболеваниях легких в педиатрии. Curr Opin Pediatr . 1998 июн.10 (3): 236-42. [Медлайн].
Ward M, Sinn J.Стероидная терапия синдрома аспирации мекония у новорожденных. Кокрановская база данных Syst Rev . 2003. CD003485. [Медлайн].
Sarkar S, Hussain N, Herson V. Фибриновый клей для стойкого пневмоторакса у новорожденных. Дж Перинатол . 2003 января 23 (1): 82-4. [Медлайн].
El Shahed AI, Dargaville P, Ohlsson A, Soll RF. Поверхностно-активное вещество при синдроме аспирации мекония у доношенных / недоношенных детей. Кокрановская база данных Syst Rev .18 июля 2007 г. 2: CD002054. [Медлайн]. [Полный текст].
[Рекомендации] Американская кардиологическая ассоциация, Американская академия педиатрии. Руководство Американской кардиологической ассоциации (AHA) 2005 г. по сердечно-легочной реанимации (CPR) и неотложной сердечно-сосудистой помощи (ECC) педиатрическим и неонатальным пациентам: рекомендации по реанимации новорожденных. Педиатрия . 2006 май. 117 (5): e1029-38. [Медлайн].
Cialone PR, Sherer DM, Ryan RM, Sinkin RA, Abramowicz JS.Амниоинфузия во время родов, осложненных околоплодными водами, окрашенными частицами мекония, снижает неонатальную заболеваемость. Am J Obstet Gynecol . 1994 Март 170 (3): 842-9. [Медлайн].
Dargaville PA, Copnell B, и Австралийская и Новозеландская сеть новорожденных. Эпидемиология синдрома аспирации мекония: заболеваемость, факторы риска, методы лечения и исходы. Педиатрия . 2006 май. 117 (5): 1712-21. [Медлайн].
Педиатрия . 2006 май. 117 (5): 1712-21. [Медлайн].
Dargaville PA, South M, McDougall PN.Сурфактанты и ингибиторы сурфактантов при синдроме аспирации мекония. Дж. Педиатр . 2001, январь 138 (1): 113-5. [Медлайн].
Glantz JC, Woods JR. Значение мекония околоплодных вод. В: Creasy RK, Resnick R, eds. Медицина матери и плода . 4-е изд. Филадельфия, Пенсильвания: У. Б. Сондерс; 1999. 393-403.
Kattwinkel J, Niermeyer S, Denson SE, ред. Учебник по реанимации новорожденных . 4-е изд. Чикаго, штат Иллинойс: Американская академия педиатрии; 2000 г.
Кинселла JP. Синдром аспирации мекония: ответ на вопрос — промывание сурфактантом ?. Am J Respir Crit Care Med . 2003 15 августа. 168 (4): 413-4. [Медлайн]..jpg)
Korones SB, Bada-Ellzey HS. Аспирация мекония. Принятие решений в неонатальном периоде (принятие клинических решений) . Сент-Луис, Миссури: Ежегодник Мосби; 1993. 128-9.
Кугельман А., Гангитано Э., Тащук Р. и др. Экстракорпоральная мембранная оксигенация у младенцев с синдромом аспирации мекония: десятилетний опыт вено-венозной ЭКМО. Дж. Педиатр Хирургия . 2005 июл. 40 (7): 1082-9. [Медлайн].
Lo KW, Роджерс М. Контролируемое испытание амниоинфузии: предотвращение аспирации мекония во время родов. Aust N Z J Obstet Gynaecol . 1993 Февраль 33 (1): 51-4. [Медлайн].
Ранзини А.С., Чан Л. Меконий и компромисс между плодами и новорожденными. В: Spitzer AR, ed. Интенсивная терапия плода и новорожденного . Сент-Луис, Миссури: Мосби; 1996. 297-303.
297-303.
Робертон NRC.Синдромы аспирации. В: Greenough A, Robertson NRC, Milner AD, eds. Заболевания дыхательных путей новорожденных . Лондон, Великобритания: Публикация Арнольда; 1996. 313-33.
Солл Р.Ф., Даргавиль П. Поверхностно-активное вещество при синдроме аспирации мекония у доношенных детей. Кокрановская база данных Syst Rev . 2000. CD002054. [Медлайн].
Уста И.М., Мерсер Б.М., Асвад Н.К., Сибай Б.М. Влияние политики амниоинфузии околоплодных вод, окрашенных меконием. Акушерский гинекол . 1995 Февраль 85 (2): 237-41. [Медлайн].
Whitsett JA, Pryhuber GS, Rice WR, Warner BB, Wert SE. Острые респираторные расстройства. В: Avery GB, Fletcher MA, MacDonald MG, eds. Неонатология: патофизиология и лечение новорожденных . 5-е изд. Филадельфия, Пенсильвания: Липпинкотт Уильямс и Уилкинс; 1999. 494-508.
5-е изд. Филадельфия, Пенсильвания: Липпинкотт Уильямс и Уилкинс; 1999. 494-508.
Wiswell TE, Gannon CM, Jacob J, et al. Ведение родильного отделения новорожденного с явно выраженным здоровьем, окрашенным меконием: результаты многоцентрового международного совместного исследования. Педиатрия . 2000 января 105 (1 п.1): 1-7. [Медлайн]. [Полный текст].
Да TF. Основные понятия: синдром аспирации мекония: патогенез и текущее лечение. Астраханьская область . Сентябрь 2010. 11 (9): e503-12. [Полный текст].
Young TE, Mangum OB. Neofax: Руководство по лекарствам, используемым при уходе за новорожденными . 11-е изд. Bethesda, M: Американское общество фармацевтов систем здравоохранения; 1998.
Boet A, Brat R, Aguilera SS, Tissieres P, De Luca D. Поверхностно-активное вещество от новорожденных до педиатрических отделений интенсивной терапии: лабораторные и прикроватные доказательства. Минерва Анестезиол . 2014 декабрь 80 (12): 1345-56. [Медлайн].
Поверхностно-активное вещество от новорожденных до педиатрических отделений интенсивной терапии: лабораторные и прикроватные доказательства. Минерва Анестезиол . 2014 декабрь 80 (12): 1345-56. [Медлайн].
Хермансен К.Л., Махаджан А. Дыхательная недостаточность новорожденного. Ам Фам Врач . 2015 г. 1. 92 (11): 994-1002. [Медлайн].
фон Бахр В., Халтман Дж., Эксборг С. и др. Долгосрочная выживаемость и причины поздней смерти детей, получавших экстракорпоральную мембранную оксигенацию. Педиатр Crit Care Med .2017 марта 18 (3): 272-80. [Медлайн].
Синдром аспирации мекония
Синдром аспирации мекония (MAS) — это потенциально опасное медицинское событие во время родов, которое происходит, когда ребенок вдыхает меконий и околоплодные воды во время родов.
Меконий — это, по сути, первая какашка ребенка. Это густое, темно-зеленое вязкое фекальное вещество, которое младенцы выделяют в течение первых нескольких дней после рождения. Иногда к концу беременности ребенок выделяет меконий внутри матки, где он смешивается с околоплодными водами.МАС возникает, когда меконий выделяется внутри матки. Ребенок вдыхает его в легкие еще до рождения. МАС может вызвать серьезный риск для здоровья и вызвать осложнения у ребенка. Если не лечить должным образом, ребенок может получить необратимую травму или умереть.
Иногда к концу беременности ребенок выделяет меконий внутри матки, где он смешивается с околоплодными водами.МАС возникает, когда меконий выделяется внутри матки. Ребенок вдыхает его в легкие еще до рождения. МАС может вызвать серьезный риск для здоровья и вызвать осложнения у ребенка. Если не лечить должным образом, ребенок может получить необратимую травму или умереть.
Что вызывает МАС?
МАС возникает, когда ребенок выделяет меконий внутри матки, а затем вдыхает его. Обычно у ребенка не выделяется меконий до тех пор, пока он не родится. Вопрос о том, что вызывает MAS, заключается в том, что вызывает выделение мекония внутри матки.Раннее выделение мекония внутри матки часто вызвано стрессом плода или аномалиями, связанными с плацентой. Поражение плода на поздних сроках беременности почти всегда связано с кислородным голоданием или снижением уровня кислорода у плода. Распространенные причины дистресса плода и / или перебоя в подаче кислорода, приводящие к MAS, включают:
- Переношенная беременность (более 40 недель)
- Длительные или травматические роды
- Проблемы со здоровьем матери, такие как преэклампсия или гестационный диабет
- Инфекция матери
Переношенная беременность, вероятно, имеет сильнейшую связь с повышенным риском МАС. Младенцы не начинают вырабатывать меконий до последних стадий беременности. Чем дольше срок беременности превышает установленный срок, тем больше вероятность того, что у ребенка будет выделяться меконий в утробе матери. Более того, по мере того, как беременность прогрессирует после положенного срока, уровень околоплодных вод снижается. Это делает любой выброс мекония более концентрированным.
Младенцы не начинают вырабатывать меконий до последних стадий беременности. Чем дольше срок беременности превышает установленный срок, тем больше вероятность того, что у ребенка будет выделяться меконий в утробе матери. Более того, по мере того, как беременность прогрессирует после положенного срока, уровень околоплодных вод снижается. Это делает любой выброс мекония более концентрированным.
Симптомы MAS
Наиболее заметным начальным симптомом MAS является респираторный дистресс после рождения. Новорожденные с МАС часто демонстрируют учащенное или ненормальное дыхание.Если вдыхать слишком много мекония, он может заблокировать дыхательные пути ребенка и помешать дыханию. Дополнительные симптомы, обычно связанные с MAS, включают:
- Цианоз (синий или фиолетовый цвет кожи)
- Низкий мышечный тонус или вялость
- Низкое кровяное давление
Диагностика MAS
MAS почти всегда сразу диагностируется врачи и / или медсестры в родильном отделении после родов. Когда меконий выделяется внутри матки, он обычно окрашивает околоплодные воды.Окрашивание меконием обычно легко обнаружить и часто является первым предупреждающим признаком MAS. Если околоплодные воды окрашены меконием, врачи обычно внимательно осматривают ребенка на предмет наличия дополнительных признаков МАС. Обычно это делается просто путем прослушивания грудной клетки, но также можно сделать рентген.
Когда меконий выделяется внутри матки, он обычно окрашивает околоплодные воды.Окрашивание меконием обычно легко обнаружить и часто является первым предупреждающим признаком MAS. Если околоплодные воды окрашены меконием, врачи обычно внимательно осматривают ребенка на предмет наличия дополнительных признаков МАС. Обычно это делается просто путем прослушивания грудной клетки, но также можно сделать рентген.
По причинам, которые до конца не изучены, новорожденные афроамериканцы страдают синдромом аспирации мекония на 50% чаще, чем белые новорожденные.
Лечение MAS
Младенцам с MAS требуется немедленное вмешательство и лечение.Лечение MAS обычно начинается с ручного удаления мекония и околоплодных вод из дыхательных путей ребенка. Сначала врач, вероятно, очистит жидкость вручную, а затем дополнительный объем жидкости будет удален с помощью аспирационной трубки. Отсасывающая ванна аккуратно вытесняет жидкость, окрашенную меконием, и высасывает ее из дыхательных путей.
После завершения первоначального отсасывания дыхательная функция ребенка будет повторно оценена. Если ребенок все еще испытывает затруднения с дыханием, следующий этап лечения обычно включает устройство вентиляции с мешком / маской, чтобы облегчить доставку кислорода ребенку.Ручная подача кислорода с помощью аппарата ИВЛ помогает доставить кислород к органам ребенка. Это также помогает раздуть легкие и вывести меконий и жидкость наружу.
Если после отсасывания и вентиляции у ребенка все еще возникают проблемы с дыханием, то следующий уровень лечения MAS включает хирургическое введение дыхательной трубки. Дыхательная трубка вставляется в дыхательное горло ребенка и присоединяется к некоторому типу аппарата искусственной вентиляции легких. Младенцы, которым требуется такой уровень вмешательства, будут помещены в отделение интенсивной терапии интенсивной терапии.
После того, как будет проведено экстренное вмешательство, младенцы с МАС часто будут получать последующее наблюдение и лечение, чтобы избежать возможных осложнений. Обычный последующий уход за MAS включает:
Обычный последующий уход за MAS включает:
- Кислородную терапию
- Помещение ребенка под лучистую грелку для поддержания температуры тела
- Антибиотики для защиты от инфекций, связанных с MAS
- Механические дыхательные устройства (при необходимости)
В некоторых случаях В наиболее тяжелых случаях MAS, когда ребенок не может дышать самостоятельно или имеет очень высокое кровяное давление в легких, может потребоваться экстракорпоральная мембранная оксигенация (ЭКМО).С помощью ЭКМО ребенок подключается к сложному дыхательному аппарату, который по сути выполняет функции легких и сердца.
Возможные осложнения от MAS
MAS обычно можно эффективно контролировать и лечить без каких-либо долгосрочных осложнений или травм. Примерно 10-15% беременностей осложняются околоплодными водами, окрашенными меконием. Только у 0,2% (2 из 1000) этих детей разовьется МАС.
Но риск по-прежнему велик, если MAS не лечить должным образом. Обычно проблемы с МАС являются респираторными, и МАС является основной причиной серьезных респираторных заболеваний. Выделение мекония часто вызывает воспаление и инфекцию в легких. Инфекция, вероятно, является наиболее частым осложнением, связанным с МАС.
Обычно проблемы с МАС являются респираторными, и МАС является основной причиной серьезных респираторных заболеваний. Выделение мекония часто вызывает воспаление и инфекцию в легких. Инфекция, вероятно, является наиболее частым осложнением, связанным с МАС.
Еще одно возможное осложнение — чрезмерное расширение легких. Когда дыхательные пути заблокированы MAS, воздушные карманы в легких часто чрезмерно расширяются, чтобы получить больше кислорода. Если легкие чрезмерно расширяются или слишком сильно раздуваются в ответ на МАС, они могут потенциально разорваться и даже разрушиться.При разрыве легкого воздух может выйти в грудную полость (состояние, называемое пневмотораксом), что затрудняет надувание и восстановление легкого. Разрыв или коллапс легкого, вероятно, является наиболее опасным осложнением, связанным с МАС.
MAS также увеличивает риск развития у ребенка состояния, называемого стойкой легочной гипертензией новорожденного (PPHN). PPHN — очень редкое, но потенциально опасное для жизни состояние, при котором высокое давление в кровеносных сосудах, окружающих легкие, ограничивает кровообращение, что затрудняет дыхание ребенка.
Медицинская литература по аспирации мекония
- Буздар Н. Факторы, приводящие к синдрому аспирации мекония у новорожденных. Журнал Медицинского колледжа Равалпинди. 2017 30 декабря; 21 (4): 371-5.
- Dargaville PA, Copnell B: Эпидемиология синдрома аспирации мекония: заболеваемость, факторы риска, методы лечения и исходы. Педиатрия 2006; 117: 1712-21.
- Walsh MC, Fanaroff JM: Жидкость, окрашенная меконием: Подойдите к матери и ребенку.ClinPerinatol. 2007; 34 (4): 653-65.
- Frey HA, et. al: Интерпретация результатов измерения ЧСС плода категории II: имеет ли значение меконий ?. Am J Obstet Gynecol. 2014; 211 (6): 644.e1-8.
Синдром аспирации мекония: проблемы и решения
Отделение неонатологии, Медицинский колледж леди Хардиндж и детская больница Калавати Саран, Шахид Бхагат Сингх Марг, Нью-Дели, Индия
Резюме: Синдром аспирации мекония (MAS) является важной причиной заболеваемости и смертности доношенных новорожденных. В результате дородовой или послеродовой аспирации околоплодных вод, окрашенных меконием (MSAF), MAS вызывает респираторный дистресс различной степени тяжести, часто осложняемый утечкой воздуха или стойкой легочной гипертензией (PPHN). За последние несколько десятилетий в концепциях патофизиологии и лечения МАС произошли огромные изменения. Обычное эндотрахеальное отсасывание больше не рекомендуется как у энергичных, так и у неторопливых новорожденных с MSAF. Поддерживающая терапия, наряду с новыми методами лечения, такими как сурфактант, вдыхание оксида азота и высокочастотная вентиляция, привела к заметному улучшению общего результата MAS.В настоящем обзоре освещены проблемы понимания сложной патофизиологии и оптимального подхода к лечению MAS. Также кратко обсуждаются потенциальные будущие методы лечения и исследуемые препараты.
В результате дородовой или послеродовой аспирации околоплодных вод, окрашенных меконием (MSAF), MAS вызывает респираторный дистресс различной степени тяжести, часто осложняемый утечкой воздуха или стойкой легочной гипертензией (PPHN). За последние несколько десятилетий в концепциях патофизиологии и лечения МАС произошли огромные изменения. Обычное эндотрахеальное отсасывание больше не рекомендуется как у энергичных, так и у неторопливых новорожденных с MSAF. Поддерживающая терапия, наряду с новыми методами лечения, такими как сурфактант, вдыхание оксида азота и высокочастотная вентиляция, привела к заметному улучшению общего результата MAS.В настоящем обзоре освещены проблемы понимания сложной патофизиологии и оптимального подхода к лечению MAS. Также кратко обсуждаются потенциальные будущие методы лечения и исследуемые препараты.
Ключевые слова: синдром аспирации мекония, эндотрахеальное отсасывание, сурфактант, ингаляционный оксид азота, высокочастотная вентиляция, стойкая легочная гипертензия
Введение
Синдром аспирации мекония (MAS) — это результат дородовой или послеродовой аспирации околоплодных вод, окрашенных меконием, у доношенных или недоношенных детей, что приводит к респираторным заболеваниям различной степени тяжести. 1 Несмотря на быстрый прогресс в диагностических и терапевтических методах за последние десятилетия, меконий и его воздействие на плод и новорожденных остаются причиной серьезного беспокойства как акушеров, так и неонатологов. До сих пор ведутся широкие споры с разными мнениями относительно оптимального акушерского подхода, реанимационных мероприятий при рождении и ведения тяжелобольных новорожденных с MAS. С признанием роли хронической внутриутробной гипоксии и связанной с ней перинатальной асфиксии в патогенезе МАС, обычное эндотрахеальное отсасывание больше не рекомендуется даже у неторопливых младенцев с МАС.Появление новых методов лечения, таких как ингаляционный NO, сурфактант, высокочастотная вентиляция и экстракорпоральная мембранная оксигенация (ЭКМО), привело к огромным улучшениям в выживаемости MAS. В этом обзоре подчеркивается текущее понимание патофизиологии MAS и проблем, с которыми приходится сталкиваться при оптимальном ведении таких пациентов.
Определение
MAS определяется как респираторный дистресс у новорожденного, рожденного из околоплодных вод, окрашенных меконием (MSAF), с характерными радиологическими признаками (гиперинфляция и пятнистые помутнения), симптомы которых нельзя объяснить иначе. 2 Это одна из наиболее частых причин респираторных заболеваний у доношенных новорожденных, которым требуется пребывание в отделении интенсивной терапии новорожденных (ОИТН). Традиционно степень тяжести МАС оценивалась на основе потребности в респираторной поддержке как: 1) легкая МАС, требующая <40% кислорода в течение <48 часов, 2) умеренная МАС, которая требует более 40% кислорода в течение более 48 часов с отсутствие утечки воздуха и 3) тяжелый MAS, который требует вспомогательной вентиляции в течение более 48 часов и часто связан со стойкой легочной гипертензией (PPHN). 3 Эта классификация, хотя и широко применяется, имеет недостаток, заключающийся в том, что не удается классифицировать новорожденных с MAS, которым требуется вентиляция в течение <48 часов. Следовательно, любое требование механической вентиляции и / или постоянного положительного давления в дыхательных путях (CPAP) использовалось в качестве критерия тяжелого MAS в нескольких эпидемиологических исследованиях (классифицируя их как MAS интубированный и MAS неинтубированный). 4
Эпидемиология
Перенос мекония через плод, ведущий к MSAF, осложняет примерно 7–20% всех беременностей во всем мире, причем заболеваемость выше у чернокожих и представителей южноазиатской национальности. 3,5 Заболеваемость также увеличивается по мере увеличения гестационного возраста с зарегистрированными частотами на 37, 40 и> 42 неделях, составляющих 3%, 13% и 18% соответственно. 6 Помимо созревания плода, различные факторы материнского стресса, такие как материнская гипертензия, маловодие, злоупотребление наркотиками (особенно табаком и кокаином), первородство, анемия, хориоамнионит, затяжные роды, дистресс плода, проблемы с пуповиной и задержка роста плода, способствуют прохождению беременности. меконий. 7
Аспирация мекония в дыхательные пути плода может происходить внутриутробно или во время родов, приводя к MAS в 2–9% случаев MSAF. 8 Из них почти половине требуется механическая вентиляция, у 15–20% возникает утечка воздуха, а 5–12% умирают. 9 По оценкам, в США ежегодно происходит от 25 000 до 30 000 случаев и 1000 смертей, связанных с MAS. 10 Обзор десяти отчетов, опубликованных с 1990 по 1998 год, показал, что общий уровень заболеваемости составляет 13,1% для MSAF, 4,2% MAS среди MSAF и 49,7% MAS, требующих искусственной вентиляции легких, с 4,6% летальностью. 11 Ретроспективное обследование населения, проведенное во Франции в период с 2000 по 2007 год, продемонстрировало глобальную распространенность MAS среди MSAF как 2.29% с 36,9% младенцев с MAS, имеющими тяжелую MAS (требующую искусственной вентиляции легких / назального CPAP). 8 В различных исследованиях сообщалось об этнической принадлежности (жители островов Тихого океана, африканцы и азиаты), преклонном сроке беременности, неутешительной частоте сердечных сокращений плода, густом меконии, родоразрешении путем кесарева сечения, необходимости эндотрахеальной интубации, наличии мекония под связками и APGAR. оценка ≤3 через 1 минуту как значительный фактор риска, связанный с развитием MAS у младенцев с MSAF. 4,8,12
В последнее время наблюдаются обнадеживающие тенденции к постепенному снижению заболеваемости МАС.В США Yoder et al. Зарегистрировали четырехкратное снижение частоты MAS с 5,8% до 1,5% в течение 1990–1997 гг., Что объясняется снижением частоты родов на 33% при сроке беременности> 41 недели. 13 Об аналогичном снижении заболеваемости сообщалось в результате многоцентрового исследования в Австралии и Новой Зеландии (0,43–0,37 на 1000 живорождений в период с 1995 по 2002 год). 4 Это снижение заболеваемости MAS было связано с улучшением акушерской практики, в частности, предотвращением переношенности и быстрыми родами, когда были отмечены патологические состояния плода.Напротив, развивающиеся страны, такие как Индия и Африка, с ограниченными ресурсами для наблюдения за плодами и ухода за родильными отделениями, по-прежнему несут основное бремя заболеваемости из-за MAS.
Патофизиология
Меконий представляет собой стерильный материал черновато-зеленого цвета без запаха, состоящий из секрета кишечника и поджелудочной железы, шелушащихся клеток, верникса казеоза, волос лануго, желчных пигментов, околоплодных вод и крови. Он впервые появляется в кишечнике плода примерно на 10-й неделе беременности и перемещается в толстую кишку к 16-й неделе. 2 В нормальных условиях переход мекония от плода в амнион предотвращается из-за отсутствия перистальтики кишечника из-за низкого уровня мотилина, тонического сокращения анального сфинктера и концевого колпачка вязкого мекония. 10 Преходящая парасимпатическая нервная стимуляция из-за сдавления головы или пуповины, более высоких уровней мотилина и усиления холинергической иннервации с увеличением гестационного возраста объясняет более высокую частоту MSAF в доношенных и после родовых сроках. 14 Помимо созревания плода, внутриутробный стресс, приводящий к гипоксии и ацидозу плода, вызывает расслабление анального сфинктера, что приводит к отхождению мекония. 10 В подтверждение механизма хронического стресса Manning et al сообщили, что MSAF встречается в два раза чаще, если оценка биофизического профиля составляла ≤6, по сравнению с ≥8. 15 Было обнаружено, что уровни эритропоэтина повышены у детей, рожденных через MSAF, что может указывать на хроническую гипоксию, способствующую прохождению мекония. 16 Однако в нескольких исследованиях задокументирована заболеваемость MSAF без предшествующего дистресса плода или ацидоза, что указывает на более надежные исследования для выяснения истинного механизма этой связи. 17
Меконий из околоплодных вод может быть аспирирован во время удушья плода или при первых вдохах после родов. Было высказано предположение, что хронический внутриутробный инсульт является причиной тяжелых случаев MAS, в отличие от острых послеродовых событий. 18 Некоторые исследования, касающиеся MAS, показали, что большинство случаев тяжелых MAS причинно не связаны с аспирацией мекония, а скорее вызваны другими патологическими процессами, происходящими в утробе матери, в первую очередь хронической асфиксией и инфекцией. 19
Несмотря на обширные исследования, патофизиология MAS сложна и до сих пор не полностью выяснена. Несколько механизмов вовлечены в патогенез гипоксемии и снижения эластичности легких, вызванного аспирацией мекония.
- Обструкция дыхательных путей: В зависимости от консистенции и количества меконий в виде твердых частиц может механически закупорить дыхательные пути, полностью приводя к ателектазу и несоответствию вентиляции и перфузии или частично вызывая синдромы захвата воздуха шаровым клапаном и утечки воздуха.
- Инактивация поверхностно-активного вещества: компоненты мекония (холестерин и желчные кислоты) инактивируют поверхностно-активное вещество легких, изменяя вязкость и ультраструктуру поверхностно-активного вещества, фрагментацию дипальмитоилфосфатидилхолина и ускоряя его превращение из крупных поверхностно-активных агрегатов в мелкие, менее активные формы. Он также снижает уровень сурфактантных белков A и B и непосредственно вредит пневмоцитам типа II, тем самым уменьшая выработку сурфактанта. 20
- Химическое раздражение: Меконий является хемоаттрактантом нейтрофилов и макрофагов, что приводит к их накоплению в альвеолах и дыхательных путях в течение нескольких часов после аспирации.Последующее высвобождение провоспалительных цитокинов, таких как фактор некроза опухоли-α, интерлейкин-1β и интерлейкин-8, может непосредственно повредить паренхиму легких или привести к утечке через сосуды, вызывая токсический пневмонит с геморрагическим отеком легких. 3 Апоптоз, клеточная инфильтрация, активация альвеолярных макрофагов с образованием супероксид-анионов, повышенная чувствительность дыхательных путей или повышенные концентрации цитокинов (IL6 и панкреатическая фосфолипаза A2) в бронхоальвеолярном лаваже легких животных, инстиллированных меконием, были продемонстрированы в многочисленных исследованиях. 21–23 Недавнее исследование Hofer et al. Продемонстрировало, что тяжелый MAS тесно связан с высокими значениями C-реактивного белка и низким общим количеством лейкоцитов и абсолютным количеством нейтрофилов, что указывает на роль воспаления в патогенезе MAS. 24
- Активация комплемента: недавняя гипотеза предполагает, что меконий активирует две основные системы распознавания врожденного иммунитета, толл-подобные рецепторы и систему комплемента, что приводит не только к дисфункции легких, но и к системной воспалительной реакции. 23,25 Несмотря на все большее внимание к воспалению легких при MAS, клеточные механизмы, запускающие этот воспалительный каскад, еще предстоит выяснить.
- Стойкая легочная гипертензия (PPHN): индуцированная гипоксией вазоконстрикция легочной артерии способствует развитию PPHN, которая является ведущей причиной смертности при тяжелой MAS. Кроме того, опосредованная вазоактивными воспалительными веществами легочная вазоконстрикция и опосредованная хронической гипоксией аномальная мускуляризация и архитектурные изменения легочных сосудов способствуют перинатальной дезадаптации легочного кровообращения, что приводит к легочной гипертензии. 26
- Инфекция: Предыдущие экспериментальные работы показали, что меконий усиливает рост бактерий in vitro, а риск интраамниотической инфекции (как клинически, так и посевной) увеличивается в присутствии MSAF. 27 Однако четкая связь между MAS и сепсисом до настоящего времени не была документально подтверждена.
Меконий также оказывает пагубное воздействие на ткани плаценты и пуповины, приводя к сужению сосудов, изъязвлениям и некрозу сосудов, потенциально нарушая оксигенацию плода. 26 Он подавляет реабсорбцию легочной жидкости плода при рождении посредством неизвестных механизмов, нарушая способность легких правильно адаптироваться к внематочной жизни. 28 Дальнейшие подробные исследования для выяснения меняющихся концепций патофизиологии MAS от механической обструкции до роли иммуно-воспалительных механизмов необходимы для изучения новых стратегий в управлении MAS.
Клинические особенности
Новорожденные с MAS часто демонстрируют классические признаки переношенности с шелушением кожи, длинными ногтями, потерей веса и уменьшением верникса.Смесь, ногти и кожа окрашиваются меконием в зависимости от времени воздействия; ногти окрашиваются через 6 часов, а гниль — через 12–14 часов воздействия. 2 Примерно у 20–33% из них при рождении наблюдается неврологическое и / или респираторное угнетение, как правило, из-за гипоксии или шока. 29
Респираторный дистресс с выраженным тахипноэ, втягиванием, хрюканьем, расширением носа и цианозом наступает вскоре после рождения. У пораженных младенцев грудная клетка обычно имеет бочкообразную форму с увеличенным передне-задним диаметром, вызванным чрезмерным надуванием.При аускультации в груди выявляются хрипы и хрипы. Пациенты с тяжелым заболеванием подвержены риску респираторной недостаточности, которая часто связана с ПРГН, шунтированием справа налево и утечками воздуха (пневмоторакс или пневмомедиастинум). У некоторых пациентов, у которых при рождении не было симптомов заболевания, симптомы респираторного дистресса развиваются позже, когда меконий перемещается из крупных дыхательных путей в нижнее трахеобронхиальное дерево. Следовательно, любой ребенок, рожденный в результате MSAF, должен находиться под наблюдением не менее 24 часов.
Диагностика
Несмотря на обширные исследования, диагностический критерий MAS четко не определен.Считается, что MAS возникает у любого новорожденного, рожденного в результате MSAF с респираторным дистресс-синдромом во время или вскоре после рождения. Первоначальный снимок грудной клетки может показывать полосатую линейную плотность (подобную преходящему тахипноэ у новорожденного), прогрессирующую до гиперинфляции с диффузной пятнистой плотностью. 30 Утечка воздуха происходит у 10–30% младенцев с МАС. Измерения газов артериальной крови обычно демонстрируют гипоксемию и гиперкарбию. Однако эти данные неспецифичны и используются не для диагностики МАС, а для оценки респираторного статуса младенца.
Дифференциальный диагноз MAS включает другие причины респираторного дистресса, которые встречаются в 4–9% случаев MSAF. Это преходящее тахипноэ у новорожденных (возникает на 34–37 неделе беременности и обычно проходит в течение 24 часов), отсроченный переход из состояния кровообращения плода, сепсис или пневмония, стойкая легочная гипертензия и врожденный цианотический порок сердца.
Менеджмент
Лечение MAS в первую очередь поддерживающее без однозначно доказанной терапии.В общих чертах его можно разделить на стратегии профилактики и ведения новорожденных.
Профилактика MAS
MAS часто ассоциируется с порочным кругом гипоксемии, шунтирования, ацидоза и легочной гипертензии. Большая часть заболеваний, связанных с MAS, является вторичной по отношению к связанным с ними проблемам, таким как асфиксия, сепсис и PPHN. Поэтому цель вмешательства в родильном зале должна быть направлена на снижение частоты и тяжести аспирации мекония и этих сопутствующих заболеваний.За последнее десятилетие такие вмешательства, как плановое сокращение числа родов после родов, агрессивное лечение дистресса плода и снижение частоты родовой асфиксии, привели к значительному снижению заболеваемости MAS. 31
Плановая стимуляция родов на 41 неделе беременности предотвращает прохождение мекония, вызванное созреванием, и возможную асфиксию из-за нарушения функции плаценты, приводящей к вторичному MAS. Недавний Кокрановский обзор 19 исследований показал, что плановая индукция на 41 неделе беременности снижает риск перинатальной смертности с более низкой частотой MAS в индуцированной группе (относительный риск: 0.29, 95% ДИ: 0,12–0,68). 32 Аналогичные результаты были предложены метаанализом 14 рандомизированных контролируемых испытаний (РКИ), подчеркивающих преимущества этого вмешательства. 33 Непрерывный или периодический мониторинг сердечного ритма плода во время родов был рекомендован в качестве стандарта лечения беременных с высоким риском. Дистресс плода предшествует MAS, и на это может указывать низкий pH пуповины и / или оценка APGAR через 5 мин. Пульсоксиметрию плода, одобренную Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA), можно проводить только после разрыва плодных оболочек с раскрытием шейки матки на 2–3 см.В случаях неутешительных измерений частоты сердечных сокращений плода была показана высокая корреляция между насыщением плода кислородом ниже 30% и значением pH кожи головы 7,2, хотя с помощью современных технологий адекватные сигналы могут быть получены только в 70% случаев. 34
Внутриродовая амниоинфузия с использованием изотонического стерильного раствора (физиологический раствор или лактат Рингера) была предложена для снижения частоты и тяжести MAS путем разбавления густого мекония, тем самым уменьшая его консистенцию и облегчая компрессию пуповины, олигогидрамнион и таким образом, дистресс плода.Мета-анализ 13 исследований продемонстрировал, что профилактическая амниоинфузия во время родов для умеренных или толстых MSAF значительно снижает частоту MAS, частоту кесарева сечения, меконий ниже голосовых связок и ацидемию новорожденных без увеличения хориоамнионита. 35 Однако было обнаружено, что преимущества этого вмешательства противоречат риску потенциальных осложнений, таких как хориоамнионит, преждевременный разрыв плодных оболочек, отслойка плаценты, преждевременные роды, кровотечение из пуповины, выпадение пуповины, эмболия околоплодными водами и смерть матери. . 36 Американский колледж гинекологии и акушерства заявил, что рутинное использование амниоинфузии для разведения MSAF не рекомендуется. 37 Обзор Кокрановского метаанализа предлагает рассмотреть возможность амниоинфузии у женщин с ликвором, окрашенным меконием, в отделениях с ограниченными возможностями для послеродового наблюдения и без явного снижения заболеваемости MAS в условиях стандартного перинатального наблюдения. 38
В настоящее время окрашивание мекония можно диагностировать только путем прямой визуализации околоплодных вод в момент разрыва плодных оболочек.В настоящее время проводится оценка диагностического процесса, который позволит использовать неинвазивные методы выявления окрашивания мекония при доношенной беременности. Это будет включать неинвазивное освещение амниона светом определенной длины волны и обнаружение флуоресценции определенных биологических пигментов, содержащихся в меконии. 39
Управление родильным отделением
Рекомендации по ведению родильного отделения новорожденных, окрашенных меконием, претерпели значительные изменения за последние четыре десятилетия на основе нескольких обсервационных исследований, РКИ и систематических обзоров.
Внутриродовое отсасывание из ротоглотки
Это считалось стандартной процедурой на протяжении более 25 лет на основании основополагающей работы Carson et al, которые пришли к выводу, что рутинное отсасывание из глотки во время родов у новорожденных, окрашенных меконием, значительно снижает частоту и тяжесть MAS . 40 Серия крупных проспективных рандомизированных контролируемых исследований, проведенных за последнее десятилетие, внесла существенные изменения в этот подход, продемонстрировав отсутствие пользы от такого вмешательства. Vain et al., Сравнивая аспирацию во время родов с отсутствием аспирации у новорожденных, окрашенных меконием, не показали различий в частоте MAS, смертности, потребности в искусственной вентиляции легких и продолжительности кислородной терапии. 41 Другое исследование Nangia et al, проведенное в условиях ограниченных ресурсов и ограниченных возможностей для наблюдения за плодом до и во время родов, также дало аналогичные результаты. 42 После этого рутинная ротоглоточная аспирация в родах у здоровых новорожденных, окрашенных меконием, была исключена из рекомендаций NRP 2005 и больше не практикуется. 43
Послеродовое эндотрахеальное отсасывание
Интубация и уборка трахеи до недавнего времени оставались предметом дискуссий.Традиционно проводимая для всех новорожденных с окрашиванием меконием, эта практика не дала никаких дополнительных преимуществ по сравнению с выжидательной тактикой в предотвращении MAS у энергичных детей без депрессии в большом многоцентровом РКИ. 29 Кокрановский метаанализ четырех РКИ также не показал различий в частоте возникновения MAS у интубированных и неинтубированных энергичных новорожденных, окрашенных меконием. 44 Впоследствии, согласно NRP 2010, эта практика была ограничена детьми, не имеющими активной жизненной силы и окрашенными меконием, из-за отсутствия доказательств какого-либо вреда или преимуществ этой процедуры в вышеупомянутой группе. 45
Недавние пилотные испытания, проведенные Nangia et al и Chettri et al, пришли к выводу, что эндотрахеальное отсасывание не влияет на частоту MAS / смерти даже у младенцев, не окрашенных меконием. 46,47 Кроме того, не было обнаружено различий между двумя группами по другим параметрам, таким как тяжесть и продолжительность респираторного дистресса, потребность в респираторной поддержке, частота гипоксической ишемической энцефалопатии, продолжительность кислородной терапии и продолжительность госпитализации.Таким образом, в самых последних рекомендациях ILCOR 2015 г. рекомендуется, чтобы новорожденным, не имеющим физической формы, с MSAF не требовалась рутинная интубация и отсасывание трахеи. 48
Институциональная политика, предусматривающая наличие хорошо скоординированной и обученной «группы быстрого реагирования», состоящей из акушеров, перинатальных медсестер и педиатров для родов, окрашенных меконием, вероятно, будет применять научно-обоснованный подход и эффективно управлять такими событиями , тем самым снижая частоту MAS и потребность в дорогостоящих и сложных вмешательствах. 5
Ведение новорожденных
Все новорожденные с риском МАС, у которых наблюдается респираторный дистресс-синдром, должны быть госпитализированы в отделение интенсивной терапии новорожденных и находиться под тщательным наблюдением. Лечение в основном поддерживающее и направлено на коррекцию гипоксемии и ацидоза с поддержанием оптимальной температуры и артериального давления.
Общее ведение
Все младенцы должны находиться под наблюдением с использованием неинвазивных мониторов и отбора проб газов крови через постоянный центральный артериальный катетер.Минимальное обращение, поддержание бесшумной среды, седация и обезболивание (с использованием опиоидов) часто используются для предотвращения гипоксии, вызванной болью и стрессом, а также шунтирования справа налево у пациентов с ИВЛ с МАС. Другие эффективные меры включают поддержание нормотермии, коррекцию метаболических нарушений (гипогликемия, гипокальциемия, ацидоз и полицитемия) и поддержание системного артериального давления, превышающего легочное артериальное давление, путем увеличения объема, переливания крови или вазопрессоров.
Назогастральная аспирация
Профилактический назогастральный лаваж перед первым кормлением рекомендуется для предотвращения непереносимости корма и вторичного MAS из-за послеродовой аспирации желудочного содержимого. Однако в большом РКИ, проведенном в нашем центре с участием энергичных детей с MSAF, не было обнаружено различий в частоте проблем с кормлением или вторичных MAS между группой лаважа и группой без лаважа. 49 Подобные результаты были продемонстрированы и в других испытаниях, но без явных очевидных преимуществ этой практики. 50,51 Большинство этих исследований включали только энергичных новорожденных, у которых, возможно, не было длительного воздействия мекония в утробе матери. В недавнем метаанализе Deshmukh et al. Пришли к выводу, что профилактическое промывание снижает риск непереносимости корма у детей, окрашенных меконием, на 30%. 52 Следовательно, доказательства использования этой процедуры у неторопливых новорожденных требуют дополнительных исследований.
Респираторная поддержка
Требование респираторной поддержки варьируется в зависимости от тяжести MAS, при этом большинство новорожденных реагируют только на дополнительное введение кислорода через капюшон или носовые канюли.Целевое насыщение кислородом поддерживается в пределах от 90% до 95%, учитывая высокую частоту шунтирования справа налево. Около 10% пациентов с тяжелым MAS лечатся только с помощью CPAP, вводимого с помощью биназальных или одиночных назальных канюль с давлением 5-8 см H 2 O. 8 Однако толерантность к устройству CPAP часто ограничена из-за относительная зрелость младенцев и вероятность того, что в результате возбуждение ухудшится, легочная гипертензия станет показателем интубации. 29
Примерно 40% новорожденных с MAS нуждаются в интубации и механической вентиляции.Показания для интубации включают высокую потребность в кислороде (фракция вдыхаемого кислорода [FiO 2 ]> 0 , 8), респираторный ацидоз (артериальный pH постоянно <7,25), легочная гипертензия и нарушение кровообращения. 53 Несмотря на более чем четыре десятилетия использования ИВЛ у младенцев с MAS, оптимальное лечение ИВЛ остается спорным с очень небольшим количеством клинических испытаний, на которых можно было бы основывать определенные рекомендации. Это происходит из-за сложной патофизиологии, затрагивающей области ателектаза, сосуществующей с гиперинфляцией, а также несоответствием вентиляции и перфузии и нарушением дыхательных путей.Целью вспомогательной вентиляции является достижение оптимального газообмена с минимальной баротравмой легких. Хотя испытания подходящего режима вентиляции отсутствуют, синхронизированная прерывистая принудительная вентиляция является наиболее часто используемым режимом традиционной вентиляции. Настройки вентилятора и целевой газ крови зависят от наличия или отсутствия PPHN и преобладающей патологии легких. В случаях с выраженным региональным или глобальным ателектазом высокое пиковое давление на вдохе (PIP) (максимум до 30 см) и высокое положительное давление в конце выдоха (ПДКВ) (4-7 см) с более длительным временем вдоха помогает рекрутированию альвеол. .Если есть очевидная задержка газа, ПДКВ следует снизить (3–4 см) с оптимальным временем выдоха (0,5–0,7) и высокой частотой вентиляции. 54 У младенцев с ассоциированным PPHN следует учитывать более высокие показатели (50–70) с более высоким FiO 2 (80–100%) для поддержания PaO 2 между 70 и 100 мм рт. Ст. И PaCO 2 между 35 и 45 мм рт. Ст. Вместе с увеличением объема, вазопрессорами и другими поддерживающими мерами. 53,54 Алкалоза, вызванного гипервентиляцией, следует избегать из-за риска неврологического повреждения, вызванного церебральной вазоконстрикцией, и нейросенсорной тугоухости.В таких ситуациях следует заранее рассмотреть другие методы, такие как вдыхание оксида азота и высокочастотная вентиляция.
Высокочастотная вентиляция
Несмотря на недостаток клинических данных, высокочастотная вентиляция (HFV) оказалась полезной при лечении пациентов с тяжелой формой MAS и неэффективностью традиционной вентиляции. Он обеспечивает эффективный газообмен при низком дыхательном объеме, уменьшая, таким образом, баротравму и утечку воздуха. Опубликованные серии из больших баз данных по новорожденным показывают, что 20–30% всех младенцев, нуждающихся в интубации и вентиляции с помощью MAS, получают высокочастотную вентиляцию. 55 Высокочастотная осцилляторная вентиляция является наиболее часто используемым режимом, особенно у пациентов со значительным ателектазом, когда было обнаружено, что применение более высоких средних давлений в дыхательных путях (около 25 см) с маневрами рекрутмента с умеренной частотой (6-8 Гц) выгодный. 54 Он также дает клиническое преимущество при MAS с сопутствующим тяжелым PPHN, поскольку реакция на вдыхаемый NO лучше при HFOV, чем при традиционной вентиляции, причем недавние данные свидетельствуют о неэффективности этой комбинации и необходимости ЭКМО только у 5% таких детей. 54 Высокочастотная струйная вентиляция также оказалась полезной для оптимизации оксигенации и предотвращения ЭКМО при тяжелом МАС, особенно при сочетании ателектаза и захвата газов. 56 Следовательно, высокочастотная вентиляция должна рассматриваться по сравнению с обычным пневмотораксом в условиях тяжелого MAS с трудноизлечимой гипоксемией, стойким респираторным ацидозом или высоким риском пневмоторакса.
Терапия сурфактантом
Пагубное влияние мекония на продукцию и функцию сурфактанта хорошо известно и лежит в основе использования экзогенного сурфактанта при тяжелом MAS.Канадское педиатрическое общество рекомендует экзогенный сурфактант для всех интубированных пациентов с МАС с требованием FiO 2 > 50%. Поверхностно-активное вещество можно вводить болюсно или в виде бронхоальвеолярного лаважа. В развитых странах болюсная терапия сурфактантом в настоящее время используется у 30–50% детей с МАС на ИВЛ. 8 Метаанализ четырех РКИ с участием 326 детей с MAS показал снижение тяжести респираторных заболеваний и потребности в ЭКМО с введением сурфактанта, но не оказало существенного влияния на общую смертность. 57 Клинические испытания лаважа легких сурфактантом показали, что лаваж может улучшить оксигенацию и сократить продолжительность вентиляции. 58 Однако метаанализ двух РКИ не показал значительного улучшения показателей смертности, пневмоторакса, продолжительности вентиляции или продолжительности госпитализации. 59 В другом РКИ авторы не продемонстрировали влияния промывания на легочные исходы, но обнаружили более высокий уровень выживаемости без ЭКМО в группе, получавшей лечение. 60 В недавнем систематическом обзоре, оценивающем эффект введения сурфактанта в виде болюса или лаважа, был сделан вывод, что и то, и другое снижает продолжительность пребывания в больнице, продолжительность ИВЛ и необходимость ЭКМО без снижения смертности. 61 Следовательно, сурфактантную терапию следует разумно использовать при МАС, выбирая младенцев с тяжелым заболеванием и начинающих лечить, а при необходимости, повторно, для достижения оптимальных результатов. Необходимы дальнейшие испытания для подтверждения лечебного эффекта, определения оптимальных доз и метода введения сурфактанта и сравнения лаважа с болюсным введением.
Кортикостероиды
Легочное и системное воспаление — ключевая особенность патофизиологии МАС, обеспечивающая обоснование использования стероидов в случаях тяжелого МАС для улучшения легочной функции.Согласно Кокрановскому метаанализу, использование стероидов не было связано с уменьшением смертности, продолжительности ИВЛ или продолжительности госпитализации, но показало увеличение продолжительности кислородной терапии. 62 Недавно испытания кортикостероидов показали сокращение продолжительности пребывания в стационаре и кислородную зависимость с улучшенным радиологическим клиренсом в группе, получавшей стероиды. 63,64 При отсутствии убедительных доказательств рутинная стероидная терапия не рекомендуется при МАС.В нескольких исследованиях на животных ингаляционный будесонид показал многообещающий ответ при интратрахеальном введении отдельно или с сурфактантом, что обеспечило многообещающую терапию в будущем. 65,66 Сейчас необходимо больше научно-обоснованных исследований для оценки потенциальных преимуществ и вреда стероидной терапии при МАС.
Антибиотиков ассоциация между меконием и сепсисом были оценены широко, но роль антибиотиков в рутинном управлении MAS до сих пор остается спорной.В рандомизированном контролируемом исследовании доношенных детей, рожденных в результате MSAF, проведенном автором, рутинная антибиотикопрофилактика не снизила частоту подтвержденного посевом сепсиса или MAS в группе вмешательства. 67 Мета-анализ трех РКИ показал, что использование антибиотиков для лечения MAS не привело к значительному снижению риска смертности, сепсиса или продолжительности пребывания в больнице. 61 Учитывая ограниченное количество исследований и небольшое количество новорожденных, роль антибиотиков необходимо переоценить в хорошо спланированных испытаниях.
Вдыхаемый оксид азота (iNO)
Крупные РКИ показали эффективность iNO у доношенных новорожденных с PPHN в снижении смертности и необходимости ЭКМО. 68 Каждое из этих испытаний включало большую подгруппу с МАС. В настоящее время около 20–30% всех младенцев с МАС на ИВЛ получают iNO, а около 40–60% демонстрируют устойчивый ответ. 69 Являясь селективным легочным вазодилататором, он является идеальным средством лечения умеренного и тяжелого ПРГН, сохраняющегося, несмотря на вентиляционные маневры.При тяжелом PPHN синергетическое улучшение оксигенации происходит при использовании HFV с iNO из-за уменьшения легочного шунтирования и увеличения доставки iNO к месту его действия. 70 Значительная часть новорожденных с PPHN не отвечает на iNO. Более того, высокая стоимость терапии препятствует ее рутинному использованию в развивающихся странах. Другие легочные вазодилататоры, такие как ингибиторы фосфодиэстеразы 5 (силденафил, дипиридамол и запринаст), были опробованы на новорожденных, но их мало, и на сегодняшний день нет крупных контрольных исследований. 71
Экстракорпоральная мембранная оксигенация (ЭКМО)
MAS является ведущим диагнозом новорожденных, направляемых на эту терапию, с обычным показанием к тяжелой гипоксемии (стойкий индекс оксигенации> 40), несмотря на оптимальную вентиляцию. 72 С появлением новых методов лечения количество младенцев, нуждающихся в ЭКМО, резко сократилось, но выживаемость в случаях MAS остается высокой (до 95%). 72 Последующие исследования пациентов, получавших ЭКМО, демонстрируют более низкие показатели тяжелой инвалидности через 1 год, что указывает на положительную роль терапии тяжелого MAS в качестве спасательной терапии. 73
Будущая терапия
Ведение MAS остается в основном поддерживающим без определенной терапии для повреждения легких, вызванного меконием. Лучшее понимание патологических механизмов, приводящих к повреждению паренхимы, вызванному меконием, расширило сферу потенциальных будущих методов лечения МАС. Последние данные предполагают, что по крайней мере некоторые случаи гибели клеток меконием происходят из-за апоптоза, который опосредуется ренин-ангиотензиновой системой. Предварительная обработка щенка кролика ингибитором ангиотензинпревращающего фермента каптоприлом перед интратрахеальной инстилляцией мекония уменьшала апоптоз эпителиальных клеток легких. 74 Аналогичным образом, было показано, что введение N-ацетилцистеина вместе с сурфактантом предотвращает миграцию нейтрофилов, отек легких и окислительное повреждение путем подавления образования IL-8 и IL-β. 75 Введение ингибитора циклооксигеназы II парекоксиба кроликам, получавшим меконий, снижает экспрессию миелопероксидазы и рецепторов СОХ II и ослабляет гистопатологические повреждения и острое повреждение легких, вызванное меконием, со значительным улучшением респираторных функций. 76 Спасательная терапия с использованием интратрахеального альбумина также улучшает функцию легких, связывая и блокируя активные вещества, такие как свободные жирные кислоты и желчные кислоты в меконии. 77 Комбинация ингибиторов протеазы предотвращает отложение клеток, вызванное меконием, что предполагает возможную роль пищеварительных ферментов поджелудочной железы плода в лечении MAS. 78 Жидкая вентиляция с перфторуглеродами оказалась полезной для улучшения выживаемости на животных моделях MAS, предлагая исследовательский потенциал для ее использования на людях. 79 Все эти методы лечения находятся на экспериментальной стадии, пока доступны только исследования на животных, и ожидают дальнейших испытаний на людях.
Результат
Усовершенствования в отделениях интенсивной терапии новорожденных и новые методы лечения, включая респираторную поддержку, привели к заметному улучшению общего результата MAS. Ретроспективный обзор доношенных детей с MAS в период с 1997 по 2007 год показал уровень смертности 1,2% по сравнению с 4,2%, о которых сообщалось ранее (с 1973 по 1987 год). В том же исследовании было обнаружено, что оценка APGAR <3, потребность в искусственной вентиляции легких в течение 48 часов, повторная доза вазопрессоров и использование цефотаксима являются независимыми факторами риска смертности. 80 В недавнем исследовании, проведенном в Индии, было обнаружено, что уровень смертности достигает 26%, при этом более низкая масса тела при рождении, наличие дисфункции миокарда и более высокая начальная потребность в кислороде являются независимыми предикторами смертности. 81 Примерно одна треть этих смертей при МАС напрямую связана с легочной причиной, а остальные приписываются сопутствующей гипоксической ишемической энцефалопатии.
Краткосрочные заболевания включают пневмоторакс и другие утечки воздуха у 10% пациентов, находящихся на ИВЛ. 8 Другие, такие как добавление кислорода в 28 дней (5%), судороги (4%) или легочное кровотечение возникают только у небольшой части младенцев. 8,80 Долговременная болезнь легких, особенно в форме реактивного заболевания дыхательных путей, является обычным явлением, при этом примерно у половины младенцев в младенчестве развиваются эпизоды кашля / хрипов. 82 Дети более старшего возраста, вероятно, будут иметь легкую обструкцию дыхательных путей, гиперинфляцию и гиперчувствительность дыхательных путей при нормальном тесте функции легких и рентгенографии грудной клетки. 83 Напротив, неврологический исход более мрачен: у 21% младенцев развивается церебральный паралич или общая задержка развития, несмотря на то, что они реагируют только на обычную вентиляцию легких. 84 Плохой неврологический исход (10–20% нарушение развития) независимо от способа родоразрешения, более легкого течения болезни или режима вентиляции свидетельствует о том, что предрасполагающие факторы и факторы, лежащие в основе, приводящие к MAS, являются фундаментальными для патогенеза развития нервной системы. инвалидность среди выживших. 84 По мере снижения смертности требуются более надежные последующие исследования для изучения этих факторов и долгосрочных результатов развития нервной системы у этих пациентов.
Заключение
Достижения в акушерской и неонатальной практике ведения пациентов привели к заметному снижению заболеваемости и смертности, связанной с МАС. Однако отсутствие новых терапевтических средств и протоколированных руководств по лечению по-прежнему является серьезной проблемой при лечении этого распространенного состояния в развивающихся странах.Поддерживающая терапия является краеугольным камнем ведения MAS, и с ее судебным применением, младенцы даже с тяжелой MAS выживают с приемлемым бременем краткосрочных и долгосрочных заболеваний. Необходимо провести дальнейшие исследования, чтобы глубже понять сложную патофизиологию этого заболевания и оценить новые методы лечения, с потенциальными преимуществами, документально подтвержденными в предварительных испытаниях на животных.
Раскрытие информации
Авторы сообщают об отсутствии конфликта интересов в этой работе.
Ссылки
1. | Antonowiez I, Schwachman H. Меконий в здоровье и болезнях. Адв. Педиатр . 1979; 26: 275–310. | |
2. | Fanaroff AA. Синдром аспирации мекония: исторические аспекты. Дж Перинатол . 2008; 28 (Приложение 3): S3 – S7. | |
3. | Клири GM, Wiswell TE. Окрашенные меконием околоплодные воды и синдром аспирации мекония: обновленная информация. Педиатрическая клиника North Am . 1998. 45 (3): 511–529. | |
4. | Фишер К., Рыбаковски С., Фердинус С., Сагот П., Гуйон Дж. Б.. Популяционное исследование синдрома аспирации мекония у новорожденных, родившихся на сроке от 37 до 43 недель беременности. Международный Педиатр . 2012; 321545. | |
5. | Бутани В.К. Разработка системного подхода к профилактике синдрома аспирации мекония: уроки, извлеченные из многонациональных исследований. Дж Перинатол . 2008; 28 (Приложение 3): S30 – S35. | |
6. | Погги Ш.Г., Гидини А. Патофизиология перехода мекония в околоплодные воды. Ранний Hum Dev . 2009. 85 (10): 607–610. | |
7. | Санкхян Н., Шарма В.М. Предикторы околоплодных вод, окрашенных меконием: возможная стратегия снижения неонатальной заболеваемости и смертности. J ObstetGynecol India .2006. 56 (6): 514–517. | |
8. | Даргавилль, Пенсильвания, Копнелл В; Сеть новорожденных Австралии и Новой Зеландии. Эпидемиология синдрома мекония: заболеваемость, факторы риска, методы лечения и исходы. Педиатрия . 2006. 117 (5): 1712–1721. | |
9. | Wiswell TE. Ведение родильного отделения новорожденного с меконием. Дж Перинатол . 2008; 28 (Дополнение 3): S19 – S26. | |
10. | Гельфанд С.Л., Фанарофф Дж. М., Уолш М.С. Жидкость, окрашенная меконием: подойти к матери и ребенку. Pediatr Clin North Am. 2004; 51 (3): 655–667. | |
11. | Лю В.Ф., Харрингтон Т. Факторы риска в родильном отделении для синдрома аспирации мекония. Am J Перинатол . 2002. 19 (7): 367–378. | |
12. | Уста И.М., Мерсер Б.М., Сибай Б.М.Факторы риска синдрома аспирации мекония. Акушерство . 1995. 86 (2): 230–234. | |
13. | Йодер Б.А., Кирш Э.А., Барт У.Х., Гордон М.С. Изменение акушерской практики, связанное со снижением заболеваемости синдромом аспирации мекония. Obstet Gynecol. 2002; 99 (5): 731–739. | |
14. | Баллард Р.А., Хансен Т.Н., Корбет А. Дыхательная недостаточность у доношенных детей.В: Taeusch HW, Ballard RA, Gleason CA, редакторы. Болезни новорожденных Эйвери . 8-е изд. Филадельфия: Elsevier Inc; 2005: 705–722. | |
15. | Manning FA, Harman CR, Morrison I., Menticoglou SM, Lange IR, Johnson JM. Оценка плода на основе оценки биофизического профиля плода. Am J Obstet Gynecol . 1990. 162 (3): 703–709. | |
16. | Richey SD, Ramin SM, Bawson RE et al.Маркеры острой и хронической асфиксии у младенцев с околоплодными водами, окрашенными меконием. Am J Obstet Gynecol . 1995; 172: 1212–1215. | |
17. | Ciftci AO, Tanyel FC, Karnak I, Büyükpamukçu N, Hiçsönmez A. Внутриутробная дефекация: факт или вымысел? Eur J Pediatr Surg . 1999. 9 (6): 376–380. | |
18. | Blackwell SC, Moldenhauer J, Hassan SS и др. Синдром аспирации мекония у доношенных новорожденных с нормальным кислотно-основным статусом при родах: чем отличается? Am J Obstet Gynecol .2001. 184 (7): 1422–1425. | |
19. | Ghidini A Spong CY. Синдром тяжелой аспирации мекония не вызван аспирацией мекония. Am J Obstet Gynecol. , 2001; 185 (4): 931–938. | |
20. | Копинкова Ю., Кальковска А. Мекониевое воспаление и инактивация сурфактанта: особенности молекулярных механизмов. Педиатр Рес . 2016; 79 (4): 514–521. | |
21. | Загария А., Бхат Р., Навале С., Видьясагар Д. Экспрессия цитокинов в легких, индуцированных меконием. Индийский Дж. Педиатр . 2004. 71 (3): 195–201. | |
22. | Кодзима Т., Хаттори К., Фудзивара Т., Сасай-Такедацу, М., Кобаяси Ю. Повреждение легких, вызванное меконием, опосредованное активацией альвеолярных макрофагов. Наука о жизни . 1994. 54 (21): 1559–1562. | |
23. | Lindenskov PH, Castellheim A, Saugstad OD, Mollnes TE. Синдром аспирации мекония: возможные патофизиологические механизмы и будущие потенциальные методы лечения. Неонатология . 2015; 107 (3): 225–230. | |
24. | Hofer N, Jank K, Strenger V, Pansy J, Resch B. Воспалительные показатели при синдроме аспирации мекония. Педиатр Пульмон . 2016; 51 (6): 601–606. | |
25. | Молнес Т.Э., Кастельхейм А., Линденсков PH, Сальвесен Б., Саугстад О. Роль комплемента при синдроме аспирации мекония. J Perinatol. 2008; 28 (Дополнение 3): S116 – S119. | |
26. | Аханя С.Н., Сурешбабу Н., Морган Б.Л., Росс М.Г. Переход мекония в утробе матери: механизмы, последствия и лечение. Наблюдение за акушерством и гинекологом . 2005. 60 (1): 45–56. | |
27. | Хаттон Е.К., Торп Дж.Последствия окрашивания околоплодных вод меконием: о чем говорят доказательства? Ранний Hum Dev . 2014. 90 (7): 333–339. | |
28. | Чуа Б.А., Чан Л., Киндлер П.М., Перкс А.М. Связь между меконием и производством и реабсорбцией легочной жидкости и потерей лактата легкими in vitro у морских свинок. Am J Obstet Gynecol. 2000; 183 (1): 235–244. | |
29. | Wiswell TE, Gannon CM, Jacob J, et al.Ведение родильного отделения новорожденного с явно выраженным здоровьем, окрашенным меконием: результаты многоцентрового международного совместного исследования. Педиатрия . 2000; 105 (1 Пет 1): 1–7. | |
30. | Гудинг, Калифорния, Грегори, Джорджия. Рентгенографический анализ аспирации мекония у новорожденного. Радиология . 1971; 100 (1): 131. | |
31. | Vain NE, Szyld EG, Prudent LM, Aguilar AM.Что (нельзя) делать во время и после родов? Профилактика и лечение синдрома аспирации мекония. Ранний Hum Dev . 2009. 85 (10): 621–626. | |
32. | Гульмезоглу AM, Crowther CA, Миддлтон П. Индукция родов для улучшения исходов родов у женщин в срок или после родов. Кокрановская база данных Syst Rev. 2006; (4): CD004945. | |
33. | Hussain AA, Yakoob MY, Imdad A, Bhutta ZA.Избирательная индукция беременностей на сроке 41 недели и более и ее влияние на мертворождение: систематический обзор с метаанализом. BMC Общественное здравоохранение . 2011; 11 (Приложение 3): S5. | |
34. | Kuhnert M, Seelbach-Goebel B, Butterwegge M. Прогностическое соответствие между насыщением артериальной крови плода кислородом и pH кожи головы плода: результаты многоцентрового исследования в Германии. Am J Obstet Gynecol . 1998. 178 (2): 330–335. | |
35. | Pierce J, Gaudier F, Sanchez-Ramos L. Внутриродовая амниоинфузия жидкости, окрашенной меконием: метаанализ проспективных клинических испытаний. Obstet Gynecol. 2000; 95 (6 Pt 2): 1051–1056. | |
36. | Велфи С., Видьясагар Д. Ведение младенцев, родившихся от матери с околоплодными водами, окрашенными меконием: рекомендации, основанные на фактах. Clin Perinatol. 2006; 33 (1): 29–42. | |
37. | Акушерская практика Комитета ACOG. Заключение комитета ACOG № 346, октябрь 2006 г .: амниоинфузия не предотвращает синдром аспирации мекония. Obstet Gynecol. 2006; 108 (4): 1053. | |
38. | Hofmeyr GJ, Xu H, Eke AC. Амниоинфузия ликвора, окрашенного меконием, в родах. Кокрановская база данных Syst Rev .2014; (1): CD000014. | |
39. | Дуди М.С., изобретатель; Дуди Майкл Си, правопреемник. Пренатальное обнаружение околоплодных вод, окрашенных меконием. Патент США US5172693. 1992 22 декабря. | |
40. | Carson B, Losey R, Bowes Jr WA, Simmons MA. Комбинированный акушерский и педиатрический подход для профилактики синдрома аспирации мекония. Am J Obstet Gynecol . 1976; 126 (6): 712–715. | |
41. | Vain NE, Szyld EG, Prudent LM, Wiswell TE, Aguilar AM, Vivas NI. Отсасывание из ротоглотки и носоглотки новорожденных, окрашенных меконием, до родов через плечи: многоцентровое рандомизированное контролируемое исследование. Ланцет . 2004. 364 (9434): 597–602. | |
42. | Nangia S, Pal MM, Saili A, Gupta U. Влияние внутриродовой аспирации (IP-OP) на синдром аспирации мекония в развивающихся странах: рандомизированное контролируемое исследование. Реанимация . 2015; 97: 83–87. | |
43. | Международный комитет связи по реанимации. Консенсус Международного комитета по связям по реанимации (ILCOR) в отношении научных данных с рекомендациями по лечению педиатрических и неонатальных пациентов: базовая и расширенная поддержка жизни в педиатрии. Педиатрия . 2006; 117 (5): e955 – e977. | |
44. | Halliday HL.Эндотрахеальная интубация при рождении для предотвращения заболеваемости и смертности у доношенных новорожденных, окрашенных меконием. Кокрановская база данных Syst Rev. 2001; (1): CD000500. | |
45. | Perlman JM, Wyllie J, Kattwinkel J, et al; Сотрудники отделения реанимации новорожденных. Часть 11: Реанимация новорожденных: 2010 Международный консенсус в области сердечно-легочной реанимации и неотложной сердечно-сосудистой помощи с рекомендациями по лечению. Тираж . 2010; 122 (16 Дополнение 2): S516–538. | |
46. | Nangia S, Sunder S, Biswas R, Saili A. Эндотрахеальная аспирация у доношенных новорожденных, не окрашенных меконием — пилотное исследование. Реанимация . 2016; 105: 79–84. | |
47. | Chettri S, Adhisivam B, Bhat BV. Эндотрахеальная аспирация у новорожденных, не являющихся здоровыми, рожденных из околоплодных вод, окрашенных меконием: рандомизированное контролируемое исследование. Дж. Педиатр . 2015. 166 (5): 1208–1213. | |
48. | Wyckoff MH, Aziz K, Escobedo MB, et al. Часть 13: Реанимация новорожденных: Обновление рекомендаций Американской кардиологической ассоциации 2015 г. по сердечно-легочной реанимации и неотложной сердечно-сосудистой помощи. Тираж . 2015; 132 (18 Приложение 2): S543 – S560. | |
49. | Sharma P, Nangia S, Tiwari S, Goel A, Singla B, Saili A.Промывание желудка для предотвращения проблем с кормлением новорожденных околоплодными водами, окрашенными меконием: рандомизированное контролируемое исследование. Педиатрический центр здоровья ребенка . 2014. 34 (2): 115–119. | |
50. | Гарг Дж., Масанд Р., Томар Б.С. Полезность промывания желудка у энергичных новорожденных, рожденных с ликвором, окрашенным меконием: рандомизированное контролируемое исследование. Международный Педиатр . 2014; 2014: 204807. | |
51. | Ameta G, Upadhyay A, Gothwal S, Singh K, Dubey K, Gupta A. Роль промывания желудка у здоровых новорожденных, рожденных с околоплодными водами, окрашенными меконием. Индийский Дж. Педиатр . 2013; 80 (3): 195–198. | |
52. | Дешмук М., Баласубраманиан Х., Рао С., Патоле С. Влияние промывания желудка на кормление новорожденных, рожденных через жидкость, окрашенную меконием: систематический обзор. Arch Dis Child Fetal Neonatal Ed .2015; 100 (5): F394 – F399. | |
53. | Goldsmith JP. Постоянное положительное давление в дыхательных путях и традиционная механическая вентиляция в лечении синдрома аспирации мекония. Дж Перинатол . 2008; 28 (Приложение 3): S49 – S55. | |
54. | Даргавилль, Пенсильвания. Респираторная поддержка при синдроме аспирации мекония: практическое руководство. Международный Педиатр . 2012; 2012: 965159. | |
55. | Tingay DG, Mills JF, Morley CJ, Pellicano A, Dargaville PA; Сеть новорожденных Австралии и Новой Зеландии. Тенденции использования и исходы лечения новорожденных с помощью высокочастотной вентиляции легких в Австралии и Новой Зеландии, 1996–2003 гг. J Детский педиатр . 2007. 43 (3): 160–166. | |
56. | Engle WA, Yoder MC, Andreoli SP, Darragh RK, Langefeld CD, Hui SL.Контролируемое проспективное рандомизированное сравнение высокочастотной струйной вентиляции и традиционной вентиляции у новорожденных с дыхательной недостаточностью и стойкой легочной гипертензией. Дж Перинатол . 1997. 17 (1): 3–9. | |
57. | El Shahed AI, Dargaville P, Ohlsson A, Soll RF. Поверхностно-активное вещество при синдроме аспирации мекония у доношенных / недоношенных детей. Кокрановская база данных Syst Rev. 2007; (3): CD002054. | |
58. | Wiswell TE, Knight GR, Finer NN и др. Многоцентровое рандомизированное контролируемое исследование, сравнивающее лаваж сурфаксина (луцинактанта) со стандартными методами лечения синдрома аспирации мекония. Педиатрия . 2002. 109 (6): 1081–1087. | |
59. | Hahn S, Choi HJ, Soll R, Dargaville PA. Промывание легких при синдроме аспирации мекония у новорожденных. Кокрановская база данных Syst Rev . 2013; (4): CD003486. | |
60. | Dargaville PA, Copnell B, Mills JF и др .; lessMAS Trial Study Group. Рандомизированное контролируемое исследование промывания легких разбавленным сурфактантом при синдроме аспирации мекония. Дж. Педиатр . 2011. 158 (3): 383–389. | |
61. | Натараджан К.К., Санкар М.Дж., Джайн К., Агарвал Р., Пол В.К. Сурфактант и антибиотикотерапия у новорожденных с синдромом аспирации мекония: систематический обзор и метаанализ. Дж Перинатол . 2016; 36 (Приложение 1): S48 – S53. | |
62. | Ward MC, Sinn J. Стероидная терапия синдрома аспирации мекония у новорожденных. Кокрановская база данных систематической редакции . 2003; (4): CD003485. | |
63. | Басу С., Кумар А., Бхатиа Б.Д., Сатья К., Сингх ТБ. Роль стероидов в клиническом течении и исходе синдрома аспирации мекония — рандомизированное контролируемое исследование. Дж. Троп Педиатр . 2007. 53 (5): 331–337. | |
64. | Tripathi S, Saili A. Влияние стероидов на клиническое течение и исходы новорожденных с синдромом аспирации мекония. J Trop Pediatr. 2007; 53 (1): 8–12. | |
65. | Mokra D, Mokry J, Drgova A, Petraskova M, Bulikova J, Calkovska A. Кортикостероиды, введенные интратрахеально, улучшили функции легких у кроликов, которым вводили меконий. Дж. Физиол Фармакол . 2007; 58 (Дополнение 5, часть 1): 389–398. | |
66. | Mikolka P, Mokra D, Kopinkova J, Tomčíková-Mikušiaková L, Calkovská A. Будесонид, добавленный к модифицированному свиному сурфактанту curosurf, может дополнительно улучшить функции легких у меня. Physiol Res . 2013; 62 (Приложение 1): S191 – S200. | |
67. | Goel A, Nangia S, Saili A, Garg A, Sharma S, Randhawa VS.Роль профилактических антибиотиков у новорожденных, рожденных из околоплодных вод, окрашенных меконием (MSAF) — рандомизированное контролируемое исследование. Eur J Педиатр . 2015. 174 (2): 237–243. | |
68. | Финер Н.Н., Баррингтон, штат Кентукки. Оксид азота при дыхательной недостаточности у младенцев, родившихся в срок или в ближайшее время. Кокрановская база данных Syst Rev . 2006; (4): CD000399. | |
69. | Гупта А., Растоги С., Сахни Р. и др.Вдыхание оксида азота и щадящая вентиляция в лечении легочной гипертензии у новорожденных — одноцентровый опыт 5 лет. Дж Перинатол . 2002. 22 (6): 435–441. | |
70. | Kinsella JP, Truog WE, Walsh WF и др. Рандомизированное многоцентровое исследование вдыхания оксида азота и высокочастотной осцилляторной вентиляции при тяжелой стойкой легочной гипертензии у новорожденных. Дж. Педиатр . 1997; 131 (1): 55–62. | |
71. | Асад А., Бхат Р. Фармакотерапия при аспирации мекония. Дж Перинатол . 2008; 28 (Приложение 3): S72 – S78. | |
72. | Короткий BL. Экстракорпоральная мембранная оксигенация: использование при синдроме аспирации мекония. J Perinatol. 2008: 28 (Дополнение 3): S79 – S83. | |
73. | Mugford M, Elbourne D, FieldD.Экстракорпоральная мембранная оксигенация при тяжелой дыхательной недостаточности у новорожденных. Кокрановская база данных Syst Rev . 2008; (3): CD001340. | |
74. | Ухал Б.Д., Абдул-Хафез А. Ангиотензин II при апоптотическом повреждении легких: потенциальная роль в синдроме аспирации мекония. Дж Перинатол . 2008: 28 (Приложение 3): S108 – S112. | |
75. | Kopincova J, Mokra D, Mikolka P, Kolomazník M, Čalkovská A.Развитие N-ацетилцистеина сурфактантной терапии при экспериментальном синдроме аспирации мекония: возможные механизмы. Physiol Res . 2014; 63 (Приложение 4): S629 – S642. | |
76. | Li A, Zhang L, Li W. Уменьшение острого повреждения легких, вызванного меконием, с помощью парекоксиба на модели кролика. Int J Clin Exp Med. 2015; 8 (5): 6804–6812. | |
77. | Saugstad OD, Tollofsrud P, Lindenskov P, Drevon CA.Токсические эффекты различных фракций мекония на функцию легких: новые терапевтические стратегии при синдроме аспирации мекония? Дж Перинатол . 2008; 28 (Приложение 3): S113 – S115. | |
78. | Иванов В.А., Геволб И.Х., Угал Б.Д. Новый взгляд на патогенез синдрома аспирации мекония: роль протеолитических ферментов поджелудочной железы плода в отслоении эпителиальных клеток. Pediatr Res .2010; 68 (3): 221–224. | |
79. | Дженг М.Дж., Сунг В.Дж., Ли Ю.С. и др. Влияние лечебного бронхоальвеолярного лаважа и частичной жидкостной вентиляции на новорожденных поросят, подвергшихся аспирации мекония. Crit Care Med. 2006; 34 (4): 1099–1105. | |
80. | Сингх Б.С., Кларк Р.Х., Пауэрс Р.Дж., Спитцер АР. Синдром аспирации мекония остается серьезной проблемой в отделении интенсивной терапии новорожденных: результаты и схемы лечения доношенных новорожденных, поступивших в реанимацию в течение десятилетнего периода. Дж Перинатол . 2009. 29 (7): 497–503. | |
81. | Луис Д., Сундарам В., Мукхопадхай К., Дутта С., Кумар П. Предикторы смертности новорожденных с синдромом аспирации мекония. Indian Pediatr. 2014; 51 (8): 637–640. | |
82. | Юксель Б., Гриноу А., Гамсу Х.Р. Синдром неонатальной аспирации мекония и респираторные заболевания в младенчестве. Педиатр Пульмонол .1993. 16 (6): 358–361. | |
83. | Swaminathan S, Quinn J, Stabile MW, Bader D, Platzker AC, Keens TG. Отдаленные легочные последствия синдрома аспирации мекония. Дж. Педиатр . 1989. 114 (3): 356–361. | |
84. | Белигере Н., Рао Р. Исход нервного развития младенцев с синдромом аспирации мекония: отчет об исследовании и обзор литературы. Дж Перинатол .2008; 28 (Приложение 3): S93 – S101. |
Синдром аспирации мекония: исторические аспекты
Меконий, фекальный материал, который накапливается в толстой кишке плода на протяжении всей беременности, — это термин, производный от греческого mekoni, , означающего маковый сок или опиум. Начиная с наблюдений Аристотеля о связи между окрашиванием меконием околоплодных вод и сонным состоянием или неонатальной депрессией, акушеры беспокоились о благополучии плода в присутствии околоплодных вод, окрашенных меконием (MSAF).Гипоксический стресс плода может стимулировать активность толстой кишки, что приводит к выходу мекония, а также может стимулировать судорожные движения плода, приводящие к аспирации мекония.
Меконий представляет собой стерильное, густое, черно-зеленое вещество без запаха, которое впервые обнаруживается в кишечнике плода на третьем месяце беременности. Меконий образуется в результате накопления инородных тел, в том числе слущенных клеток кишечника и кожи, муцина желудочно-кишечного тракта, лануго-волос, жировых отложений казеозной черве, околоплодных вод и кишечных секретов.Он содержит от 72 до 80% воды и содержит холестерин и его предшественники, липиды, ферменты, включая фосфолипазу А2 поджелудочной железы, мукополисахариды, белок, желчные кислоты и соли, а также метаболиты лекарств. Черно-зеленый цвет обусловлен желчными пигментами. При аспирации в легкие у плода или новорожденного ребенка меконий может стимулировать высвобождение цитокинов и других вазоактивных веществ, которые вызывают сердечно-сосудистые и воспалительные реакции.
У плода отхождение мекония происходит физиологически на ранних сроках беременности, когда он способствует выработке щелочной фосфатазы в околоплодных водах.Абрамович 1 отметил, что дефекация плода уменьшается через 16 недель и прекращается через 20 недель, одновременно с иннервацией анального сфинктера. В это время кажется, что прямая кишка заполнена меконием. Примерно с 20 до 34 недель меконий внутриутробно переносился нечасто. 2 Большинство новорожденных, у которых выделяется меконий, являются зрелыми (доношенными). Многие из них являются недоношенными, и у младенцев может быть шелушение кожи, длинные ногти и уменьшение верникса. Смазка, пуповина и ногти могут быть окрашены меконием, в зависимости от того, как долго ребенок подвергался воздействию in utero .Как правило, ногти окрашиваются через 6 часов, а гниль — через 12–14 часов воздействия.
Выделение мекония обычно происходит в течение первых 24–48 часов после рождения. Тем не менее, прохождение мекония плода, приводящее к MSAF, происходит примерно в 8–25% всех родов, в первую очередь в ситуациях позднего созревания плода или стресса плода. У большинства младенцев, родившихся с MSAF, срок беременности превышает 37 недель, и меконий редко появляется в околоплодных водах до 32 недель беременности.Недоношенному ребенку не хватает «мотилина», но он помогает меконию перемещаться по нижним отделам желудочно-кишечного тракта. Синдром аспирации мекония (MAS), связанный с аспирацией или, возможно, диффузией мекония в дыхательные пути плода, встречается примерно у 5% этих младенцев. 3, 4
Синдром аспирации мекония определяется как респираторный дистресс у ребенка, рожденного в результате MSAF, симптомы которого невозможно объяснить иначе. Аспирированный меконий может мешать нормальному дыханию по нескольким причинам.Они включают обструкцию дыхательных путей, химическое раздражение, инфекцию и инактивацию сурфактанта (см. Рисунок 1). При аспирации в легкие плода частицы мекония механически закупоривают мелкие дыхательные пути. Меконий или вызываемый им химический пневмонит подавляет функцию сурфактанта, а воспаление легочной ткани еще больше способствует небольшой обструкции дыхательных путей. Грудная клетка обычно имеет бочкообразную форму с увеличенным передне-задним диаметром, вызванным чрезмерным надуванием. При аускультации хрипы и хрипы.Эти признаки обычно видны сразу после рождения.
Рисунок 1
Патофизиология синдрома аспирации мекония. Из книги Фанароффа и Мартина «Неонатальная перинатальная медицина», «Заболевания плода и младенца» , 8-е издание, под редакцией Р. Мартина, А. Фанароффа и М. Уолша, Мосби Эльзевьер, 2006 г. захват вместе со снижением податливости легких. Клири и Висвелл 3 предложили критерии тяжести для определения MAS: (1) легкая MAS — это заболевание, при котором требуется менее 40% кислорода в течение менее 48 часов, (2) умеренное MAS — это заболевание, при котором требуется более 40% кислорода для более длительного более 48 часов без утечки воздуха и (3) тяжелый MAS — это заболевание, которое требует вспомогательной вентиляции более 48 часов и часто связано со стойкой легочной гипертензией.Из младенцев, у которых развивается МАС, умирают более 4%, что составляет 2% всех перинатальных смертей.
По оценкам, от 25 000 до 30 000 случаев и 1000 смертей, связанных с MAS, происходит ежегодно в Соединенных Штатах, и намного больше случаев в развивающихся странах. Однако Yoder et al. 5 документально подтвердили снижение заболеваемости MAS в Соединенных Штатах (с 5,8 до 1,5% — почти четырехкратное сокращение) в период с 1990 по 1997 год, что они приписали снижению частоты рождений на 33% в более позднем возрасте. срок беременности более 41 недели.Это, вероятно, можно объяснить сокращением числа младенцев, у которых меконий вырабатывается (в связи с преждевременной зрелостью), и снижением частоты внутриутробной гипоксии (риск которой увеличивается при переношенной беременности).
Острое внутрилегочное заражение меконием вызывает зависимую от концентрации реакцию легочной гипертензии, при этом у 15–20% младенцев с MAS наблюдается стойкая легочная гипертензия. Однако данные о длительном процессе мускуляризации дистальных легочных артериол у младенцев с MAS, которые умерли, позволяют предположить, что на легочные симптомы могут влиять другие факторы, помимо аспирации мекония (например, хроническая внутриутробная гипоксемия). 6
Аспирация мекония. О синдроме аспирации мекония
Синдром аспирации мекония (MAS) возникает, когда новорожденный вдыхает густые частицы мекония. Обычно это вторично по отношению к гипоксии плода, которая вызывает усиление перистальтики, расслабление анальных сфинктеров и рефлекторное дыхание. В большинстве случаев родоразрешение мекония связано с окрашиванием жидкости меконием, но дети остаются энергичными и не нуждаются в дальнейшем вмешательстве.
Окрашенные меконием околоплодные воды можно аспирировать до или во время родов.Поскольку меконий редко обнаруживается в околоплодных водах до 34 недель беременности, аспирация мекония обычно поражает доношенных и доношенных детей.
Есть несколько патомеханизмов, участвующих в MAS, в частности обструкция дыхательных путей, дисфункция сурфактанта, воспаление, отек легких, легочная вазоконстрикция и бронхоспазм [1] .
Исследования аспирата трахеи подтверждают воспалительную реакцию с увеличением количества воспалительных клеток и уровня провоспалительных цитокинов с соответствующим снижением функции легких.В большинстве случаев эти изменения начинают исчезать после первых шести часов жизни с последующим улучшением функции легких.
Одно исследование предполагает, что пищеварительные ферменты поджелудочной железы плода могут играть определенную роль в повреждении легких, наблюдаемом в MAS [2] .
Эпидемиология
Цифра, указанная для младенцев, рожденных с ликвором, окрашенным меконием, в промышленно развитых странах составляет 8-25% рождений после 34 недель беременности. МАС встречается примерно у 1-3% живорождений [3] .
Снижение заболеваемости MAS в течение десятилетия было связано с сокращением послеродовых родов, агрессивным контролем аномального мониторинга сердечного ритма и уменьшением числа младенцев с низким баллом по шкале Апгар [4] . Было показано, что плановая индукция родов при беременности на сроке 41 недели или позже ассоциируется со значительным снижением частоты MAS и меньшим числом перинатальных смертей по сравнению с выжидательной тактикой [5] .
В развивающихся странах частота MAS выше, и это связано с более высоким уровнем смертности.
Этиология
[6]
Такие факторы, как плацентарная недостаточность, материнская гипертензия, преэклампсия, маловодие или злоупотребление материнскими наркотиками (табак, кокаин), увеличивают проникновение мекония внутрь матки.
Аспирация мекония может происходить внутриутробно при задыхании плода или после рождения при первых вдохах жизни. МАС определяется как респираторный дистресс-синдром, развивающийся вскоре после рождения, с рентгенологическим подтверждением аспирационного пневмонита и наличием околоплодных вод, окрашенных меконием.
Дистресс плода и асфиксия связаны с тяжелой формой MAS [7] .
Презентация
- Явное присутствие мекония или темно-зеленого окрашивания околоплодных вод.
- Зеленое или синее окрашивание кожи при рождении.
- Ребенок выглядит вялым, с низкой оценкой по шкале Апгар.
- Дыхание частое, затрудненное или отсутствует.
- Признаки переношенности (например, шелушение кожи) присутствуют.
- Монитор плода может показать брадикардию.
Исследования
- Анализ газов крови показывает низкий pH крови, повышенное pCO 2 , пониженное pO 2 .
- Уровень электролитов в сыворотке следует измерять у детей с МАС, поскольку перинатальный стресс может привести к синдрому несоответствующей секреции антидиуретического гормона (АДГ) и острому повреждению почек.
- FBC может быть полезен для исключения инфекции или признаков, определяющих причину перинатального стресса (например, тромбофилия, указывающая на кровотечение, или полицитемию, связанную со снижением легочного кровотока).
- Рентгенография показывает пятнистые инфильтраты, грубые штрихи обоих легких, увеличенный диаметр АД и уплощение диафрагмы (из-за гиперинфляции).
- УЗИ легких — это быстрый, простой и дешевый метод визуализации, который все чаще используется в отделениях интенсивной терапии, в том числе для новорожденных [8] .
- Визуализация головного мозга может быть показана при наличии неврологических отклонений.
- ЭКГ следует выполнять для оценки структуры сердца и степени тяжести любой легочной гипертензии и шунтирования слева направо.
Ведение
Все младенцы из группы риска по МАС, у которых наблюдаются признаки респираторного дистресс-синдрома, должны быть помещены в отделения интенсивной терапии новорожденных.Тщательный мониторинг важен, поскольку они могут очень быстро испортиться. Поддержание адекватной оксигенации, оптимального артериального давления, коррекция ацидоза, гипогликемии и других метаболических нарушений является основой лечения [4] .
- Терапевтические вмешательства при тяжелом МАС включают отсасывание дыхательных путей, доставку кислорода или искусственную вентиляцию легких [9] .
- Отсасывание — Национальный институт здравоохранения и передового опыта (NICE) не рекомендует регулярно отсасывать носоглотку и ротоглотку до рождения плеча и туловища.Однако он рекомендует отсосать верхние дыхательные пути после родов из плеч, если в ротоглотке присутствует густой или вязкий меконий. Если после родов у ребенка ухудшились жизненно важные функции, ларингоскопию и аспирацию под контролем должен проводить медицинский работник, обученный продвинутым технологиям жизнеобеспечения новорожденных [10] .
- Кислород необходимо подавать для поддержания насыщения кислородом на уровне 95-98%. Может потребоваться вентиляция. При пневмотораксе потребуется установка дренажа грудной клетки.
- В некоторых случаях может применяться вентиляция с высокочастотными колебаниями [11] .
- Профилактическое назначение антибиотиков новорожденным, рожденным через околоплодные воды, окрашенные меконием, не снижает частоту MAS (или других осложнений) [12] .
- Поверхностно-активное вещество — меконий, попадающий в легкие, деактивирует активность сурфактанта, вызывает повышение поверхностного натяжения и предвещает начало респираторной недостаточности. Замещение сурфактанта может быть полезным для детей с МАС, так как оно может быстро улучшить оксигенацию [13] .
- Замена поверхностно-активного вещества болюсным или медленным вливанием у младенцев с тяжелым MAS также снижает потребность в экстракорпоральной мембранной оксигенации [14] .
- Разработка активных синтетических поверхностно-активных веществ очень сложна [15] .
- Противовоспалительные препараты могут быть назначены для уменьшения неблагоприятного действия продуктов вызванного меконием воспаления как на эндогенное, так и на экзогенно доставленное сурфактант [16] .
- Вдыхаемый оксид азота может быть полезен при лечении легочной гипертензии, связанной с MAS [4] .Считается, что он действует, расслабляя гладкие мышцы легочных сосудов, вызывая расширение сосудов, а также способствуя бронходилатации.
- Энтеральный силденафил может использоваться для лечения стойкой легочной гипертензии, вызванной MAS [17] .
- Экстракорпоральная мембранная оксигенация (ЭКМО) может потребоваться у детей, состояние которых ухудшается.
- Стероиды — ингаляционные или системные — были использованы с хорошим эффектом в некоторых исследованиях. Было показано, что будесонид улучшает эффекты экзогенного поверхностно-активного вещества в экспериментальном MAS [9] .
Осложнения и прогноз
В легких случаях респираторный дистресс обычно проходит через 2–4 дня, хотя тахипноэ может сохраняться дольше. В редких случаях может произойти более продолжительное поражение органов дыхания, которое может сохраняться в течение многих лет. Это более вероятно, если требовалась вентиляция.
Церебральная гипоксия может привести к длительному неврологическому повреждению.
Исследования показали широкий диапазон смертности младенцев с МАС от 5% до 40% [3] .Дисфункция миокарда, масса тела при рождении и исходная потребность в кислороде являются независимыми предикторами смертности. МАС ассоциируется с неонатальными припадками и хроническими судорожными расстройствами.
Было показано, что младенцы с высоким уровнем аспартатаминотрансферазы связаны с худшими исходами в области нервного развития [18] .
Синдром аспирации мекония — обзор
Синдром аспирации мекония
Синдром аспирации мекония (САМ) является одной из наиболее частых причин гипоксемической дыхательной недостаточности у доношенных новорожденных, нуждающихся в интенсивной терапии (рис. 47-1).По оценкам последних исследований, частота MAS у детей на сроке беременности более 37 недель колеблется от 0,4% до 1,8% (Dargaville and Copnell, 2006; Singh et al, 2009). Среди детей, рожденных после 39 недель беременности с заболеванием легких, требующим искусственной вентиляции легких, более половины страдают МАС (Gouyon et al, 2008).
Более того, MAS является основным диагнозом для значительной части новорожденных, которым требуется экстракорпоральная мембранная оксигенация (ЭКМО) в США (26%) и Великобритании (51%) (Brown et al, 2010).
Хотя значительный процент доношенных родов осложняется прохождением мекония до или во время родов, менее чем у 10% подвергшихся воздействию мекония развивается МАС. Считается, что среди этих 10% ацидемия плода приводит к усилению перистальтической активности кишечника, пассажу мекония и одышке плода, в результате чего частицы мекония попадают глубоко в легкие. Подтверждая эту теорию, исследования аутопсии младенцев, умерших от MAS, демонстрируют дистальную мускуляризацию малых легочных артериол, предполагая длительную гипоксемию (Murphy et al, 1984).Частицы мекония в дистальных отделах легких вызывают закупорку дыхательных путей обратным клапаном и приводят к региональной гиперинфляции и ателектазу. Кроме того, меконий инактивирует сурфактант, что приводит к вторичной недостаточности сурфактанта (Moses et al, 1991). Более того, дети с МАС подвержены высокому риску стойкой легочной гипертензии, что значительно увеличивает их заболеваемость и усложняет лечение.
Исторически профилактика MAS была направлена на снижение воздействия на легкие плода и новорожденного вредного воздействия внутрилегочных околоплодных вод, загрязненных меконием.Инфузия физиологического раствора в амниотическую полость (т.е. амниоинфузия) во время родов была изучена как средство разведения мекония и снятия давления на пуповину, потенциальную причину ацидемии плода. В крупнейшем исследовании этой практики Fraser et al (2005) не обнаружили снижения риска MAS. Альтернативной стратегией уменьшения воздействия мекония на легкие является всасывание через рот и носоглотку во время родов у плодов, рожденных через околоплодные воды, окрашенные меконием. Хотя эта практика была широко распространена в 1970-х годах, более поздние исследования не продемонстрировали положительных результатов (Vain et al, 2004), и эта практика больше не поддерживается Американским колледжем акушеров и гинекологов (ACOG) (Комитет по акушерской практике, 2007).Эффективность рутинной практики аспирации трахеи у младенцев, подвергшихся воздействию мекония, сразу после рождения, не была изучена должным образом. В недавних сообщениях сурфактантный лаваж легких продемонстрировал некоторые перспективы улучшения функции легких на животных моделях MAS (Dargaville et al, 2003), но небольшое клиническое испытание этой практики не показало никаких преимуществ (Gadzinowski et al, 2008). Отсутствие явной эффективности любой из этих профилактических стратегий, направленных на удаление мекония, вероятно, говорит о сложной и многофакторной природе патофизиологии MAS.
Клинические признаки MAS широко варьируются среди младенцев и могут быть связаны со степенью дородового компромисса; время, объем и консистенция аспирированного мекония; и наличие сопутствующих проблем. Клинические признаки MAS обычно проявляются сразу после рождения в виде тахипноэ, повышенной работы дыхания и цианоза. Другими часто встречающимися сопутствующими явлениями являются метаболический ацидоз, сердечная дисфункция и гипотензия, а также постпротоковая десатурация, указывающая на шунтирование крови в артериальном протоке справа налево, вызванное легочной гипертензией.Пневмоторакс может осложнить клиническую картину из-за возможности обструкции мелких дыхательных путей шаровым клапаном и невозможности опорожнения дистальных сегментов легкого. В недавних исследованиях риск пневмоторакса у детей, находящихся на ИВЛ с МАС, колебался от 10% до 24% (Dargaville and Copnell, 2006; Velaphi and Van Kwawegen, 2008). Как и степень клинических признаков, результаты рентгенограммы грудной клетки сильно различаются. Классический рентген грудной клетки показывает диффузные пушистые инфильтраты. Однако у некоторых младенцев первоначальные рентгенологические результаты более мягкие, и часто наблюдается прогрессирование видимого паренхиматозного заболевания с течением времени, вероятно, связанное с вторичной дисфункцией сурфактанта.
Примерно половине детей с МАС требуется искусственная вентиляция легких. Стратегия искусственной вентиляции легких должна быть индивидуальной для каждого ребенка и патологии, очевидной на рентгенограмме грудной клетки. В целом, из-за вероятности повышенного сопротивления дыхательных путей традиционная стратегия, использующая более медленные скорости с большим временем вдоха и выдоха, позволяет улучшить диспергирование газа и более адекватное опорожнение во время выдоха. Могут возникнуть газовые ловушки и региональная или общая гиперинфляция, особенно при использовании быстрых темпов с обычным режимом вентиляции.Некоторые младенцы лучше реагируют на вентиляцию с помощью высокочастотного устройства, хотя существует также высокий риск гиперинфляции. В тяжелых случаях гиперинфляция вызывает нарушение газообмена и гиперкарбию, ограничивает системный венозный возврат (отрицательно влияет на работу сердца), увеличивает риск пневмоторакса и может усугубить легочную гипертензию.
Помимо лечения паренхиматозных заболеваний легких при МАС, особое внимание следует уделять другим проблемам, особенно легочной гипертензии.Риск PPHN довольно высок, превышая 50% в некоторых сериях. Исследования показывают, что iNO улучшает оксигенацию при MAS и особенно эффективен в сочетании со стратегией вентиляции легких, направленной на улучшение рекрутирования легких, такой как высокочастотная осцилляторная вентиляция (HFOV) (Kinsella et al, 1997). У детей с ПРГН следует настоятельно рассмотреть возможность лечения системными антибиотиками по ряду причин. К ним относятся тот факт, что внутриутробная инфекция может быть провоцирующим фактором в начальном прохождении мекония, и что исследования in vitro показывают, что присутствие мекония может способствовать росту бактерий в легких.

 В наиболее тяжелых случаях мекониальная аспирация осложняется синдромом персистирующей легочной гипертензии (ПЛГ), при ИВЛ частым нередким осложнением является синдром «утечки воздуха». Через 24-48 часов большинство детей развивают клинику аспирационной пневмонии.
В наиболее тяжелых случаях мекониальная аспирация осложняется синдромом персистирующей легочной гипертензии (ПЛГ), при ИВЛ частым нередким осложнением является синдром «утечки воздуха». Через 24-48 часов большинство детей развивают клинику аспирационной пневмонии.