Энтеровирусная инфекция — Симптомы, лечение
Энтеровирусная инфекция – это кишечное заболевание, которое провоцируют энтеровирусы. Установлено более 60 разновидностей возбудителей этой патологии. Их можно разделить на четыре основные группы. Чаще всего развитие заболевания вызывают вирусы Коксаки и полиомиелита.
Стоит отметить, что энтеровирусная инфекция крайне опасна. Вирусы устойчивы к воздействию внешней среды, длительное время не гибнут, даже находясь в почве или воде.
Заражение происходит через загрязненную воду или немытые и термически не обработанные продукты питания.
Последняя крупная вспышка подобного заболевания произошла в Китае несколько лет назад. Тогда пострадало более 15 тысяч детей, а 20 малышей погибли. Болезнь провоцировал опасный энтеровирус EV71. С током крови он разносится по всему организму человека и поражает все органы, в том числе легкие и мозг. Поэтому при постановке диагноза энтеровирусная инфекция, к лечению стоит отнестись очень внимательно.
Вероятные пути заражения
Возбудители инфекции в организм попадают воздушно-капельным путем, через зараженную воду, грязные продукты или при контакте с больным и предметами его обихода.
Огромную роль в профилактике этого заболевания играет соблюдение санитарно-гигиенических правил: мытье рук, термическая обработка продуктов и фильтрация питьевой воды.
Симптомы энтеровирусной инфекции
Длительность скрытого периода заболевания зависит от разных факторов. Большую роль играет тип возбудителя и состояние защитных функций человека.
По окончании инкубационного периода могут проявиться следующие симптомы:
-
повышение температуры тела; -
боль в голове; -
болезненные ощущения в живете; -
тошнота; -
рвота.
До попадания возбудителей инфекции в кровь, симптомы патологии могут быть выражены слабо или вовсе никак не проявляться. Но когда вирус разносится по организму, симптомы интоксикации становятся сильно выражены:
Но когда вирус разносится по организму, симптомы интоксикации становятся сильно выражены:
-
гипертермия достигает значений 39-40; -
появляется сыпь на конечностях; -
наблюдаются отеки рук и ног; -
выступают язвы во рту.
Если человек игнорирует проявления заболевания и вовремя не начинает лечение патологии, энтеровирусная инфекция может стать причиной осложнений. К ним относятся:
-
воспаление оболочек мозга; -
энцефалит; -
сильный отек легочной ткани.
Эти грозные заболевания нередко приводят к поражению оболочек мозга и провоцируют паралич или смерть человека. Особенно они опасны для детей дошкольного и младшего школьного возраста.
В последнее время среди детского населения наиболее часто врачи стали диагностировать малую энтеровирусную инфекцию. Симптомы этого заболевания выражены слабо и проявляются небольшим подъемом температуры тела, болью в суставах. Как правило, эти проявления заболевания уже через несколько дней проходят самостоятельно и не требуют специфического лечения.
Как правило, эти проявления заболевания уже через несколько дней проходят самостоятельно и не требуют специфического лечения.
Как ставится диагноз?
Поставить диагноз энтеровирусная инфекция человеку можно только по результатам анализов. На срок их выполнения врачи рекомендуют изолировать заболевшего, чтобы он не заразил других.
Так как инфекция легко передается, профилактическое обследование проводят всем контактным лицам. Любой случай заражения требует регистрации.
Лечение энтеровирусной инфекции
Специфической терапии заболевания не существует. В основном практикуется симптоматическое лечение. В острый период врачи прописывают больному пастельный режим, витаминотерапию, усиленное питание.
Если у заболевшего человека наблюдается рвота или понос, требуется прием большого количества жидкости, чтобы избежать обезвоживания. Так же рекомендованы препараты типа Регидрон, восстанавливающие водно-солевой баланс.
При наличии высокой температуры тела и сильной боли в голове, показан прием жаропонижающих и обезболивающих препаратов.
Антибактериальные препараты при вирусной инфекции используют только для профилактики вторичных инфекций бактериального характера.
Что касается диеты, то из рациона болеющего энтеровирусной инфекцией убирают продукты, вызывающие брожение и усиленную перистальтику. К ним относятся сладкие блюда, газировки, копченые колбасы, хлебобулочные изделия, свежие фрукты и овощи. Так же стоит исключить любые молочные продукты.
Все перечисленные правила касаются как взрослых, так и малолетних детей.
Как избежать заражения?
Избежать заражения кишечной инфекцией можно строго соблюдая правила гигиены. Обязательно тщательно мыть руки перед едой, а продукты питания подвергать термической обработке и тщательной чистке перед употреблением.
Одной из мер профилактики так же является употребление только чистой и качественной питьевой воды из проверенных и обустроенных источников.
Смотрите также:
Памятка по энтеровирусной инфекции
Энтеровирусная инфекция — это группа острых инфекционных болезней, вызываемые кишечными вирусами (энтеровирусами), характеризующихся лихорадкой и полиморфизмом клинических симптомов, обусловленных поражением ЦНС, сердечно-сосудистой системы, ЖКТ, мышечной системы, легких, печени, почек и др. органов.
Основной путь передачи энтеровирусной инфекции считается фекально-оральный, контактно-бытовой, через предметы быта, загрязненные руки, при несоблюдении личной гигиены.
Воздушно-капельный, если возбудитель размножается в дыхательных путях, при кашле, чиханье.
Водный путь — заражение может происходить при поливе овощей и фруктов зараженными сточными водами, а также при купании в открытых зараженных водоемах, по некоторым данным даже вода в кулерах является источником энтеровирусной инфекции.
Если беременная женщина заражена энтеровирусной инфекцией, возможен и вертикальный путь передачи возбудителя ребенку.
Для энтеровирусной инфекции характерна летне-осенняя сезонность, у человека очень высокая естественная восприимчивость.
Условно можно выделить две группы заболеваний, вызываемых энтеровирусами:
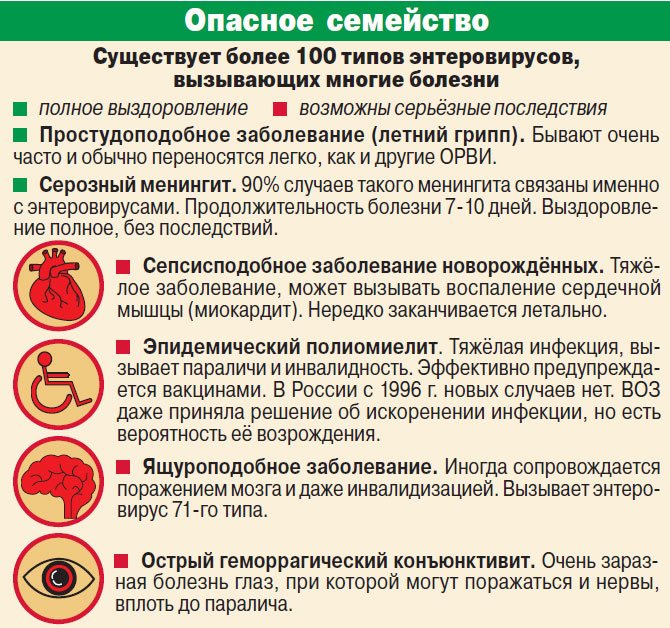
I. Потенциально тяжелые:
— серозный менингит;
— энцефалит;
— острый паралич;
— неонатальные септикоподобные заболевания;
— мио-(пери-)кардит;
— гепатит;
— хронические инфекции иммунодефицитных лиц.
II. Менее опасные:
— трехдневная лихорадка с сыпью или без;
— герпангина;
— плевродиния;
— везикулярный фарингит;
— конъюнктивит;
— увеит;
— гастроэнтерит.
1. Герпетическая ангина. В первые сутки заболевания появляются красные папулы, которые располагаются на умеренно гиперемированной слизистой небных дужек, язычка, мягком и твердом нёбе, быстро превращаются в везикулы размером 1–2 мм, числом от 3–5 до 15–18, не сливающиеся между собой. Через 1–2 дня пузырьки вскрываются с образованием эрозий либо бесследно рассасываются к 3–6 дню болезни. Боль при глотании отсутствует или незначительная, иногда появляется слюнотечение. Увеличение шейных и подчелюстных лимфоузлов небольшое, но пальпация их болезненна.
В первые сутки заболевания появляются красные папулы, которые располагаются на умеренно гиперемированной слизистой небных дужек, язычка, мягком и твердом нёбе, быстро превращаются в везикулы размером 1–2 мм, числом от 3–5 до 15–18, не сливающиеся между собой. Через 1–2 дня пузырьки вскрываются с образованием эрозий либо бесследно рассасываются к 3–6 дню болезни. Боль при глотании отсутствует или незначительная, иногда появляется слюнотечение. Увеличение шейных и подчелюстных лимфоузлов небольшое, но пальпация их болезненна.
2. Эпидемическая миалгия (болезнь Борнхольма, «чертова пляска», плевродиния). Характеризуется острыми болями с локализацией в мышцах передней брюшной стенки живота, нижней части грудной клетки, спине, конечностях. Боли носят приступообразный характер, продолжительностью от 30–40 секунд до 15–20 минут, повторяются на протяжении нескольких дней, могут носить рецидивирующий характер, но уже с меньшей интенсивностью и продолжительностью.
3. Менингеальный синдром сохраняется от 2–3 дней до 7-10 дней, санация ликвора происходит на 2-й — 3-й неделе. Возможны остаточные явления в виде астенического и гипертензионного синдромов.
Возможны остаточные явления в виде астенического и гипертензионного синдромов.
Из других неврологических симптомов при менингите энтеровирусной этиологии могут быть расстройства сознания, повышение сухожильных рефлексов, отсутствие брюшных рефлексов, нистагм, клонус стоп, кратковременные глазодвигательные расcтройства.
4. Паралитические формы энтеровирусной инфекции отличаются полиморфизмом: могут развиться спинальная, бульбоспинальная, понтинная, полирадикулоневрическая формы. Чаще других встречается спинальная форма, которая характеризуется развитием острых вялых параличей одной или обеих ног, реже – рук с выраженным болевым синдромом мышечного характера. Течение этих форм легкое, не оставляет стойких парезов и параличей.
5. Энтеровирусная лихорадка (малая болезнь, 3-х дневная лихорадка). Это наиболее частая форма энтеровирусной инфекции, но трудно диагностируемая при спорадической заболеваемости. Характеризуется кратковременной лихорадкой без выраженных симптомов локальных поражений. Протекает с умереными общеинфекционными симптомами, самочувствие нарушено мало, токсикоза нет, температура сохраняется 2–4 дня. Клинически может быть диагносцирована при наличии вспышки в коллективе, когда встречаются и другие формы энтеровирусной инфекции.
Протекает с умереными общеинфекционными симптомами, самочувствие нарушено мало, токсикоза нет, температура сохраняется 2–4 дня. Клинически может быть диагносцирована при наличии вспышки в коллективе, когда встречаются и другие формы энтеровирусной инфекции.
6. Энтеровирусная экзантема («бостонская лихорадка»). Характеризуется появлением с 1-го – 2 дня болезни на лице, туловище, конечностях высыпаний розового цвета, пятнисто- или пятнисто-папулезного характера, иногда могут быть геморрагические элементы. Сыпь держится 1–2 дня, реже – дольше и исчезает бесследно.
7. Кишечная (гастроэнтеритическая) форма. Протекает с водянистой диареей до 5–10 раз в сутки, болями в животе, метеоризмом, нечастой рвотой. Симптомы интоксикации умеренные. У детей до 2-х летнего возраста кишечный синдром часто сочетается с катаральными явлениями со стороны носоглотки. Продолжительность болезни у детей раннего возраста в течение 1–2-х недель, у детей старшего возраста 1–3 дня.
8. Респираторная (катаральная) форма проявляется слабо выраженными катаральными явлениями в виде заложенности носа, ринита, сухого редкого кашля. При осмотре выявляется гиперемия слизистой ротоглотки, мягкого нёба и задней стенки глотки. Могут отмечаться легкие диспепсические расстройства. Выздоровление наступает через 1–1,5 недели.
9. Миокардит, энцефаломиокардит новорожденных, гепатит, поражение почек, глаз (увеит) – эти формы энтеровирусной инфекции у детей встречаются редко. Клиническая диагностика их возможна только при наличии манифестных форм энтеровирусной инфекции или эпидемических вспышек заболевания. Чаще они диагносцируются при проведении вирусологических и серологических исследований.
Высокая тропность энтеровирусов к нервной системе характеризуется многообразием клинических форм наиболее часто встречающихся поражений нервной системы: серозных менингитов, энцефалитов, полирадикулоневритов, невритов лицевого нерва.
Диагностика энтеровирусной инфекции включает 4 основных метода:
1) серологический;
2) иммуногистохимический;
3) молекулярно-биологический;
4) культуральный.
Лечение энтеровирусной инфекции
Лечение направлено на облегчение симптомов болезни и на уничтожение вируса. Поскольку этиотропное лечение энтеровирусных инфекций не разработано, производится симптоматическая и дезинтоксикационная терапия, в зависимости от тяжести и локализации воспалительного процесса. Используются противовирусные препараты, такие как интерфероны, обезболивающие, жаропонижающие средства для детей, противорвотные, антигистаминные препараты, спазмолитики.
При присоединении бактериальной вторичной инфекции назначаются антибиотики.
При тяжелых формах инфекции, когда поражается нервная система, назначают кортикостероидные препараты, для коррекции кислотно-щелочного и водно-электролидного баланса — мочегонные средства. Если развиваются состояния, угрожающие жизни — требуются реанимационные меры и интенсивная терапия.
Профилактика
Для предупреждения распространения вирусной инфекции больной человек должен пользоваться личной посудой, полотенцем, часто мыть руки, помещение с больным должно часто проветриваться и должна производиться ежедневная влажная уборка. Соблюдение правил личной гигиены, правильная тщательная обработка пищевых продуктов, при купании в открытых водоемах избегать попадания воды в носоглотку — это лучшая профилактика энтеровирусной инфекции. Маленьким детям (до 3 лет), контактирующим с больным, обычно для профилактики назначают иммуноглобулин и интерферон интраназально в течение недели.
Соблюдение правил личной гигиены, правильная тщательная обработка пищевых продуктов, при купании в открытых водоемах избегать попадания воды в носоглотку — это лучшая профилактика энтеровирусной инфекции. Маленьким детям (до 3 лет), контактирующим с больным, обычно для профилактики назначают иммуноглобулин и интерферон интраназально в течение недели.
Памятка для населения по профилактике энтеровирусных инфекций
Среда,
22
Мая
2019
Энтеровирусные инфекции (ЭВИ) — группа острых заболеваний, вызываемых энтеровирусами, характеризующихся многообразием клинических проявлений от легких лихорадочных состояний до тяжелых менингитов. Энтеровирусы устойчивы во внешней среде и длительное время могут сохраняться в сточных водах, плавательных бассейнах, открытых водоемах, предметах обихода, продуктах питания (молоко, фрукты, овощи). Вирус быстро погибает при прогревании, кипячении. ЭВИ характеризуются быстрым распространением заболевания.
ЭВИ характеризуются быстрым распространением заболевания.
Сезонность – летне-осенняя, чаще май-август.
Возможные пути передачи инфекции: воздушно-капельный, контактно-бытовой, пищевой и водный. Серозный вирусный менингит является наиболее типичной и тяжелой формой энтеровирусной инфекции.
Источником инфекции являются больные и вирусоносители, в том числе больные бессимптомной формой.
Заболевание начинается остро, с подъема температуры тела до 39-40 градусов. Появляется сильная головная боль, головокружение, рвота, иногда боли в животе, спине, судорожный синдром, нередко выраженные катаральные проявления со стороны ротоглотки, верхних дыхательных путей. При появлении аналогичных жалоб необходимо срочно изолировать больного, т.к. он является источником заражения, для окружающих, и обратиться к врачу.
Учитывая возможные пути передачи, меры личной профилактики должны заключаться в соблюдении правил личной гигиены, соблюдении питьевого режима (кипяченая вода, бутилированная вода), тщательной обработки употребляемых фруктов, овощей и последующим ополаскиванием кипятком. Следует избегать посещения массовых мероприятий, мест с большим количеством людей (общественный транспорт, кинотеатры и т.д.). Рекомендуется влажная уборка жилых помещений не реже 2 раз в день, проветривание помещений.
Следует избегать посещения массовых мероприятий, мест с большим количеством людей (общественный транспорт, кинотеатры и т.д.). Рекомендуется влажная уборка жилых помещений не реже 2 раз в день, проветривание помещений.
Ни в коем случае не допускать посещения ребенком организованного детского коллектива (школа, детские дошкольные учреждения) с любыми проявлениями заболевания. При первых признаках заболевания необходимо немедленно обращаться за медицинской помощью, не заниматься самолечением!
Энтеровирусный менингит
Энтеровирусный менингит – вирусное инфекционное заболевание, характеризующееся лихорадкой, сильными головными болями, рвотой.
Инкубационный период при энтеровирусных серозных менингитах составляет в среднем около 1 недели. Чаще болеют городские жители, преимущественно дети до 7 лет, посещающие детские дошкольные учреждения. Менингеальный синдром протекает обычно доброкачественно, с улучшением в течение нескольких дней. Смертельные исходы редки.
Смертельные исходы редки.
Серозный менингит сопровождается лихорадкой, головными болями, фотофобией и менингеальными симптомами. Клиническая картина энтеровирусного менингита в значительной степени зависит от возраста пациентов. Новорожденные дети и дети раннего возраста (до 2 — 3 месяцев) входят в особую группу риска. Энтеровирусное поражение ЦНС в указанном возрасте обычно является частью тяжелого системного заболевания. При этом серозный менингит и/или менингоэнцефалит может быть диагностирован у 27 — 62% детей с энтеровирусной инфекцией. В случае прогрессирующего развития системных проявлений инфекции, таких как некроз печени, миокардит, некротизирующий энтероколит, внутрисосудистая коагуляция, заболевание напоминает бактериальный сепсис. Наблюдаемый у части детей летальный исход связан при этом не с поражением ЦНС, а является результатом острой печеночной недостаточности (вирусы ЕСНО) или миокардита (вирусы Коксаки). У детей более старшего возраста и у взрослых лиц заболевание энтеровирусным менингитом начинается остро, с внезапного повышения температуры до 38 – 40о C. Вслед за этим наблюдается развитие ригидности затылочных мышц, головные боли, светобоязнь. У части пациентов отмечены рвота, потеря аппетита, диарея, сыпь, фарингит, миалгии. Болезнь длится обычно менее одной недели. Многие пациенты чувствуют себя значительно лучше вскоре после люмбальной пункции. Неврологические симптомы, связанные с воспалением менингеальных оболочек у детей раннего возраста, включают ригидность затылочных мышц и выбухание родничка. Симптомы могут носить стертый характер. Развитию серозного менингита часто сопутствуют такие признаки болезни, как повышение температуры, беспокойство, плохой сон, высыпания на кожных покровах, ринит, диарея. В случае легкого течения энтеровирусной инфекции менингеальный синдром у детей протекает доброкачественно и, как правило, быстро, в течение 7 — 10 дней, заканчивается полным выздоровлением без остаточных явлений. Благотворное воздействие на течение серозного менингита оказывает спинальная пункция, ведущая к снижению внутримозгового давления и способствующая быстрому улучшению состояния ребенка.
Вслед за этим наблюдается развитие ригидности затылочных мышц, головные боли, светобоязнь. У части пациентов отмечены рвота, потеря аппетита, диарея, сыпь, фарингит, миалгии. Болезнь длится обычно менее одной недели. Многие пациенты чувствуют себя значительно лучше вскоре после люмбальной пункции. Неврологические симптомы, связанные с воспалением менингеальных оболочек у детей раннего возраста, включают ригидность затылочных мышц и выбухание родничка. Симптомы могут носить стертый характер. Развитию серозного менингита часто сопутствуют такие признаки болезни, как повышение температуры, беспокойство, плохой сон, высыпания на кожных покровах, ринит, диарея. В случае легкого течения энтеровирусной инфекции менингеальный синдром у детей протекает доброкачественно и, как правило, быстро, в течение 7 — 10 дней, заканчивается полным выздоровлением без остаточных явлений. Благотворное воздействие на течение серозного менингита оказывает спинальная пункция, ведущая к снижению внутримозгового давления и способствующая быстрому улучшению состояния ребенка.
Прогноз у детей и взрослых, перенесших энтеровирусный менингит, как правило, благоприятный. Есть, однако, указания, что отдельные дети, переболевшие энтеровирусным менингитом, страдают нарушениями речи и имеют трудности в школьном обучении. У взрослых лиц в течение нескольких недель после перенесенной инфекции могут сохраняться головные боли.
Энтеровирусные менингиты могут быть вызваны вирусами Коксаки А и Коксаки В, ECHO, энтеровирусами 68 и 71 серотипов, содержат РНК. Возможны эпидемические вспышки серозных менингитов с высокой контагиозностью. Преимущественно заболевают дети в возрасте 5-9 лет. Заболеваемость значительно повышается весной и летом.
Энтеровирусная инфекция у детей. Симптомы и лечение
Энтеровирусные инфекции – это группа заболеваний, в основе причин которых лежит несколько разновидностей вирусов. Вызывают заболевание вирусы Коксаки, полиовирусы и ЕСНО (экхо). Эти вирусы имеют в своем строении капсулу и ядро, содержащее РНК. Строение капсулы может очень сильно отличаться, поэтому выделяют так называемые серотипы (разновидности). У полиовирусов выделяют 3 серологических типа. Вирусы группы Коксаки делятся на Коксаки А и Коксаки В. У вирусов Коксаки А выделяют 24 серологических разновидности, у Коксаки В – 6. У вирусов ЕСНО выделяют 34 серологических типа. После перенесенной энтеровирусной инфекции образуется стойкий пожизненный иммунитет, однако, он сероспицефичен. Это значит, что иммунитет образуется только к тому серологическому типу вируса, которым переболел ребенок и не защищает его от других разновидностей этих вирусов. Поэтому энтеровирусной инфекцией ребенок может болеть несколько раз за свою жизнь. Так же эта особенность не позволяет разработать вакцину, чтобы защитить наших детей от данного заболевания. Заболевание имеет сезонность: вспышки заболевания чаще всего наблюдаются в летне-осенний период.
Строение капсулы может очень сильно отличаться, поэтому выделяют так называемые серотипы (разновидности). У полиовирусов выделяют 3 серологических типа. Вирусы группы Коксаки делятся на Коксаки А и Коксаки В. У вирусов Коксаки А выделяют 24 серологических разновидности, у Коксаки В – 6. У вирусов ЕСНО выделяют 34 серологических типа. После перенесенной энтеровирусной инфекции образуется стойкий пожизненный иммунитет, однако, он сероспицефичен. Это значит, что иммунитет образуется только к тому серологическому типу вируса, которым переболел ребенок и не защищает его от других разновидностей этих вирусов. Поэтому энтеровирусной инфекцией ребенок может болеть несколько раз за свою жизнь. Так же эта особенность не позволяет разработать вакцину, чтобы защитить наших детей от данного заболевания. Заболевание имеет сезонность: вспышки заболевания чаще всего наблюдаются в летне-осенний период.
Причины заражения энтеровирусной инфекцией
Заражение происходит несколькими путями. Вирусы в окружающую среду могут попадать от больного ребенка или от ребенка, который является вирусоносителем. У вирусоносителей нет никаких проявлений заболеваний, однако вирусы находятся в кишечнике и выделяются в окружающую среду с калом. Такое состояние может наблюдаться у переболевших детей после клинического выздоровления либо у детей, у которых вирус попал в организм, но не смог вызвать заболевание из-за сильного иммунитета ребенка. Вирусоносительство может сохраняться на протяжении 5 месяцев.
Вирусы в окружающую среду могут попадать от больного ребенка или от ребенка, который является вирусоносителем. У вирусоносителей нет никаких проявлений заболеваний, однако вирусы находятся в кишечнике и выделяются в окружающую среду с калом. Такое состояние может наблюдаться у переболевших детей после клинического выздоровления либо у детей, у которых вирус попал в организм, но не смог вызвать заболевание из-за сильного иммунитета ребенка. Вирусоносительство может сохраняться на протяжении 5 месяцев.
Попав в окружающую среду, вирусы могут сохраняться довольно долго, так как хорошо переносят неблагоприятное воздействие. Хорошо сохраняются вирусы в воде и почве, при замораживании могут выживать на протяжении нескольких лет, устойчивы к действию дезинфицирующих средств (при воздействии растворов высокой концентрации фенола, хлора, формалина вирусы начинают погибать только через три часа), однако восприимчивы к действию высоких температур (при нагревании до 45º С погибают через 45-60 секунд). Вирусы хорошо переносят перепады рН среды и отлично себя чувствуют в среде с рН от 2,3 до 9,4, поэтому кислая среда желудка не оказывает на них никакого воздействия и кислота не выполняет своей защитной функции.
Вирусы хорошо переносят перепады рН среды и отлично себя чувствуют в среде с рН от 2,3 до 9,4, поэтому кислая среда желудка не оказывает на них никакого воздействия и кислота не выполняет своей защитной функции.
Как передается энтеровирусная инфекция
Механизм передачи может быть воздушно-капельный (при чихании и кашле с капельками слюны от больного ребенка к здоровому) и фекально-оральный при не соблюдении правил личной гигиены. Чаще всего заражение происходит через воду, при употреблении сырой (не кипяченой) воды. Так же возможно заражение детей через игрушки, если дети их берут в рот. Болеют чаще всего дети в возрасте от 3 до 10 лет. У детей, находящихся на грудном вскармливании, в организме присутствует иммунитет, полученный от матери через грудное молоко, однако, этот иммунитет не стойкий и после прекращения грудного вскармливания быстро исчезает.
Симптомы энтеровирусной инфекции
В организм вирусы попадают через рот или верхние дыхательные пути. Попав в организм ребенка, вирусы мигрируют в лимфатические узлы, где они оседают и начинают размножаться. Дальнейшее развитие заболевания связано со многими факторами, такими как вирулентность (способность вируса противостоять защитным свойствам организма), тропизмом (склонностью поражать отдельные ткани и органы) вируса и состоянием иммунитета ребенка.
Попав в организм ребенка, вирусы мигрируют в лимфатические узлы, где они оседают и начинают размножаться. Дальнейшее развитие заболевания связано со многими факторами, такими как вирулентность (способность вируса противостоять защитным свойствам организма), тропизмом (склонностью поражать отдельные ткани и органы) вируса и состоянием иммунитета ребенка.
У энтеровирусных инфекций есть как схожие проявления, так и различные, в зависимости от вида и серотипа. Инкубационный период (период от попадания вируса в организм ребенка, до появления первых клинических признаков) у всех энтеровирусных инфекций одинаковый – от 2 до 10 дней (чаще 2-5 дней).
Заболевание начинается остро — с повышения температуры тела до 38-39º С. Температура чаще всего держится 3-5 дней, после чего снижается до нормальных цифр. Очень часто температура имеет волнообразное течение: 2-3 дня держится температура, после чего снижается и 2-3 дня находится на нормальных цифрах, затем снова поднимается на 1-2 дня и вновь нормализуется уже окончательно. При повышении температуры ребенок ощущает слабость, сонливость, может наблюдаться головная боль, тошнота, рвота. При снижении температуры тела все эти симптомы проходят, однако при повторном повышении могут вернуться. Также увеличиваются шейные и подчелюстные лимфоузлы, так как в них происходит размножение вирусов. В зависимости от того, какие органы больше всего поражаются, выделяют несколько форм энтеровирусной инфекции. Энтеровирусы могут поражать: центральную и периферическую нервные системы, слизистую ротоглотки, слизистую глаз, кожу, мышцы, сердце, слизистую кишечника, печень, у мальчиков возможно поражение яичек.
При повышении температуры ребенок ощущает слабость, сонливость, может наблюдаться головная боль, тошнота, рвота. При снижении температуры тела все эти симптомы проходят, однако при повторном повышении могут вернуться. Также увеличиваются шейные и подчелюстные лимфоузлы, так как в них происходит размножение вирусов. В зависимости от того, какие органы больше всего поражаются, выделяют несколько форм энтеровирусной инфекции. Энтеровирусы могут поражать: центральную и периферическую нервные системы, слизистую ротоглотки, слизистую глаз, кожу, мышцы, сердце, слизистую кишечника, печень, у мальчиков возможно поражение яичек.
При поражении слизистой ротоглотки происходит развитие энтеровирусной ангины. Она проявляется повышением температуры тела, общей интоксикацией (слабость, головная боль, сонливость) и наличие везикулярной сыпи в виде пузырьков, заполненных жидкостью, на слизистой ротоглотки и миндалинах. Пузырьки эти лопаются, и на их месте образуются язвочки, заполненные белым налетом. После выздоровления на месте язвочек не остается никаких следов.
После выздоровления на месте язвочек не остается никаких следов.
При поражении глаз развивается конъюнктивит. Он может быть одно- и двусторонним. Проявляется в виде светобоязни, слезотечения, покраснения и припухлости глаз. Возможно наличие кровоизлияний в конъюнктиву глаза.
При поражении мышц развивается миозит – боли в мышцах. Боли появляются на фоне повышения температуры. Болезненность наблюдается в грудной клетке, руках и ногах. Появление болей в мышцах, как и температуры, может носить волнообразный характер. При снижении температуры тела боли уменьшаются или исчезают совсем.
При поражении слизистой кишечника наблюдается наличие жидкого стула. Стул обычной окраски (желтый или коричневый), жидкий, без патологических (слизь, кровь) примесей. Появление жидкого стула может быть как на фоне повышение температуры, так, и изолировано (без повышения температуры тела).
Энтеровирусные инфекции могут поражать различные участки сердца. Так при поражении мышечного слоя развивается миокардит, при поражении внутреннего слоя с захватом клапанов сердца, развивается эндокардит, при поражении внешней оболочки сердца – перикардит. У ребенка может наблюдаться: повышенная утомляемость, слабость, учащенное сердцебиение, падение артериального давления, нарушения ритма (блокады, экстрасистолы), боли за грудиной.
Так при поражении мышечного слоя развивается миокардит, при поражении внутреннего слоя с захватом клапанов сердца, развивается эндокардит, при поражении внешней оболочки сердца – перикардит. У ребенка может наблюдаться: повышенная утомляемость, слабость, учащенное сердцебиение, падение артериального давления, нарушения ритма (блокады, экстрасистолы), боли за грудиной.
При поражении нервной системы могут развиваться энцефалиты, менингиты. У ребенка наблюдается: сильная головная боль, тошнота, рвота, повышение температуры тела, судороги, парезы и параличи, потеря сознания.
При поражении печени развивается острый гепатит. Он характеризуется увеличением печени, чувством тяжести в правом подреберье, болью в этом месте. Возможно появление тошноты, изжоги, слабости, повышения температуры тела.
При поражении кожи возможно появление экзантемы – гиперемия (красное окрашивание) кожи, чаще всего на верхней половине туловища (голова, грудь, руки), не приподнимается над уровнем кожи, появляется одномоментно.
Также наблюдается энтеровирусная инфекция с кожным проявлением в виде везикулярной сыпи на ладонях и стопах. Пузырьки через 5-6 дней сдуваются, не вскрываясь, и на их месте образовывается участок пигментации (коричневая точка), которая исчезает через 4-5 дней.
У мальчиков возможно наличие воспаления в яичках с развитием орхита. Чаще всего такое состояние развивается через 2-3 недели после начала заболевания с другими проявлениями (ангина, жидкий стул и другие). Заболевание довольно быстро проходит и не несет никаких последствий, однако, в редких случаях возможно развитие в половозрелом возрасте аспермии (отсутствие спермы).
Также существуют врожденные формы энтеровирусной инфекции, когда вирусы попадают в организм ребенка через плаценту от матери. Обычно такое состояние имеет доброкачественное течение и излечивается самостоятельно, однако в некоторых случаях энтеровирусная инфекция может вызвать прерывание беременности (выкидыш) и развитие у ребенка синдрома внезапной смерти (смерть ребенка наступает на фоне полного здоровья).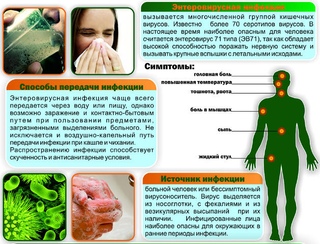
Очень редко возможно поражение почек, поджелудочной железы, легких. Поражение различных органов и систем может наблюдаться как изолированное, так и сочетанное.
Диагностика энтеровирусной инфекции
Диагноз энтеровирусной инфекции подтверждается только лабораторно – обнаружение энтеровирусов или их рибонуклеиновой кислоты (РНК) в стерильных типах клинического материала, а также выявление энтеровирусов или их РНК в двух пробах нестерильных клинических материалов разных типов.
Лечение энтеровирусной инфекции
Специфического лечения энтеровирусной инфекции не существует. Лечение проводят в домашних условиях, госпитализация показана при наличии поражения нервной системы, сердца, высокой температуры, которая долго не поддается снижению при использовании жаропонижающих средств. Ребенку показан постельный режим на весь период повышения температуры тела. Питание должно быть легким, богатым белками. Необходимо достаточное количество жидкости: кипяченая вода, минеральная вода без газов, компоты, соки, морсы.
Необходимо достаточное количество жидкости: кипяченая вода, минеральная вода без газов, компоты, соки, морсы.
Лечение проводят симптоматически в зависимости от проявлений инфекции – ангина, конъюнктивит, миозит, жидкий стул, поражения сердца, энцефалиты, менингиты, гепатит, экзантема, орхит. В некоторых случаях (ангина, понос, конъюнктивит и др.) проводят профилактику бактериальных осложнений.
Дети изолируются из организованного коллектива на весь период заболевания. В детском коллективе могут находиться после исчезновения всех симптомов заболевания.
Профилактика энтеровирусной инфекции
Для профилактики необходимо соблюдение правил личной гигиены: мыть руки после посещения туалета, прогулки на улице, пить только кипяченую воду или воду из заводской бутылки, недопустимо использование для питья ребенка воды из открытого источника (река, озеро).
Специфической вакцины против энтеровирусной инфекции не существует, так как в окружающей среде присутствует большое количество серотипов этих вирусов. Однако в Европе часто используют вакцины, содержащие наиболее часто встречающиеся энтеровирусные инфекции (Коксаки А-9, В-1, ЕСНО -6). Использование таких вакцин снижает риск заболеваемости у детей энтеровирусными инфекциями.
Однако в Европе часто используют вакцины, содержащие наиболее часто встречающиеся энтеровирусные инфекции (Коксаки А-9, В-1, ЕСНО -6). Использование таких вакцин снижает риск заболеваемости у детей энтеровирусными инфекциями.
Начинается сезон энтеровирусных инфекций, будьте внимательнее к своему здоровью и соблюдайте все рекомендованные правила профилактики энтеровирусных инфекций.
СОВРЕМЕННЫЕ ВОЗМОЖНОСТИ ДИАГНОСТИКИ, ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ ЭНТЕРОВИРУСНОЙ ИНФЕКЦИИ КОКСАКИ У ДЕТЕЙ | Ботвиньева
1. Сейбиль В. Б., Малышкина Л. П. Всемирная организация здравоохранения и проблема ликвидации инфекционных заболеваний в мире. Вопросы вирусологии. 2005; 50: 3.
2. Амвросьева Т. В., Богуш З. Ф. и др. Вспышка энтеровирусной инфекции в Витебске в условиях загрязнения питьевой воды. Вопросы вирусологии. 2004; 1: 7–9.
Вопросы вирусологии. 2004; 1: 7–9.
3. Ежлова Е. Б., Чернявская О. П., Михайлов М. И. Эпидемио логический надзор и профилактика энтеровирусной (неполио) инфекции. Методические указания 3.1.1.2363-08. Москва. 2008.
4. Кузнецова В. Г., Мечетина А. А. и др. Клинико-эпидемиологическая характеристика энтеровирусного менингита по данным вспышки 2004 года. Сборник материалов XV Научно-практической конференции врачей. Новосибирск. 2005. С. 415–416.
5. Лашкевич В. А., Дроздов С. Г., Грачев В. П. и др. Неполиомиелитные энтеровирусные инфекции: Эпидемиология, характеристика энтеровирусов, клиника, диагностика, профилактика. Методическое пособие. Федеральный центр Госсанэпиднадзора РФ. Москва. 2004.
6. Melnick J. L., Shaw E. W., Curnen E. C. A virus irom patients diagnosed as non-paralytic poliomyelitis or aseptic meningitis. Proc. Soc. Exp. Biol. 1949; 71: 344–349.
Melnick J. L., Shaw E. W., Curnen E. C. A virus irom patients diagnosed as non-paralytic poliomyelitis or aseptic meningitis. Proc. Soc. Exp. Biol. 1949; 71: 344–349.
7. Abubakar S., Chee H. Y., Shafee N. et al. Molecular detection of enteroviruses from an outbreak of hand, foot and mouth disease in Malaysia in 1997. Scand. J. Infect. Dis. 1999; 31 (4): 331–335.
8. Ang L. W., Koh B.K., Chan K. P. et al. Epidemiology and control of hand, foot and mouth disease in Singapore, 2001–2007. Ann. Acad. Med. Singapore. 2009; 38 (2): 106–112.
9. Энтеровирусные заболевания: клиника, лабораторная диагностика, эпидемиология, профилактика. Методические указания (МУ 3.1.1.2130-06). Москва. 2006.
10. Ding N. Z., Wang X. M., Sun S. W. et al. Appearance of mosaic enterovirus 71 in the 2008 outbreak of China. Virus Res. 2009; 45 (1): 157–161.
Ding N. Z., Wang X. M., Sun S. W. et al. Appearance of mosaic enterovirus 71 in the 2008 outbreak of China. Virus Res. 2009; 45 (1): 157–161.
11. Osterback R., Vuorinen T., Linna M. et al. Coxsackievirus A6 and hand, foot and mouth disease, Finland. Emerg. Infect. Dis. 2009; 15 (9): 1485–1488.
12. Yamashita T., Ito M., Taniguchi A., Sakae K. Prevalence of coxsackievirus A5, A6, and A10 in patients with herpangina in aichi prefecture. J. Infect. Dis. 2005; 58: 390–391.
13. Бочаров Е. Ф., Ерман Б. А., Фомин В. В. и др. Энтеровирусная инфекция: Новые аспекты. Новосибирск: Наука. Сибирское отделение РАМН. 1990. С. 224.
14. Лозовская Л. С. и др. Значение вертикальной передачи энтеровирусов в эпидемиологии врожденных вирусных инфекций. Акушерство и гинекология. 1995; 2: 26–30.
Акушерство и гинекология. 1995; 2: 26–30.
15. Mori M., Takagi K., Kuwabara S. et al. Guillain-Barre syndrome following hand-foot-and-mouth disease. Intern. Med. 2000; 39 (6).
16. Cabral L. A., Almeida J. D., de Oliveria M. L., Meza A. C. Hand, foot and mouth disease: a case report. Quintessence Int. 1998; 29: 194–196.
17. Злобин В. И. Энтеровирусные инфекции. Инфекционные болезни. 1999. С. 302–307.
18. Демина А. В., Маркович Н. А., Нетесов С.В. Энтеровирусы. Часть 1. История открытия, таксономия, строение генома, эпидемиология. Бюллетень СО РАМН. 2008; 1 (129): 92–100.
19. Демина А. В. и др. Энтеровирусы. Часть 2. Энтеровирусные инфекции: Многообразие клинических проявлений. Бюллетень СО РАМН. 2009; 6 (140): 116–125.
Часть 2. Энтеровирусные инфекции: Многообразие клинических проявлений. Бюллетень СО РАМН. 2009; 6 (140): 116–125.
20. Лобзин Ю. В., Пилипенко В. В., Громыко Ю. Н. Менингиты и энцефалиты. СПб.: Фолиант. 2001. С. 55–110.
21. Михайлов Е. В., Штейнберг А. В., Еремеева И. Г. Менингиты энтеровирусной этиологии у детей: Современные подходы к диагностике и особенности клинического течения. Инфекционные болезни. 2008; 6 (1): 31–34.
22. McMinn P., Stratov I., Nagarajan L., Davis S. Neurological manifestations of enterovirus 71 infection in children during an outbreak of hand, foot, and mouth disease in western australia. Clin. Infect. Dis. 2001; 32 (2): 236–242.
23. Nix W. A., Oberste M. S., Pallansch M. A. Sensitive, seminested PCR amplification of VP1 sequences for direct identification of all enterovirus serotypes from original clinical specimens. J. Clin. Microbiol. 2006; 44 (8): 2698–2704.
S., Pallansch M. A. Sensitive, seminested PCR amplification of VP1 sequences for direct identification of all enterovirus serotypes from original clinical specimens. J. Clin. Microbiol. 2006; 44 (8): 2698–2704.
24. Logotheti M., Pogka V., Horefti E. et al. Laboratory investigation and phylogenetic analysis of enteroviruses involved in an aseptic meningitis outbreak in greece during the summer of 2007. J. Clin. Virol. 2009; 46 (3): 270–274.
25. Sasidharan C. K., Sugathan P., Agarwal R. et al. Hand-foot-andmouth disease in calicut. Indian J. Pediatr. 2005; 72 (1): 17–21.
26. Tu P., Thao N., Perera D. et al. Epidemiologic and virologic investigation of hand, foot, and mouth disease, southern vietnam, 2005. Emerging Infectious Diseases. 2007; 13 (11).
27. Zhang Y., Nan L. J., Wu G. S. et al. The epidemiologic and virological analysis of an outbreak of hand, foot, and mouth disease in inner Mongolia in 2007. Bing Du Xue Bao. 2009; 25 (3): 159–165.
Zhang Y., Nan L. J., Wu G. S. et al. The epidemiologic and virological analysis of an outbreak of hand, foot, and mouth disease in inner Mongolia in 2007. Bing Du Xue Bao. 2009; 25 (3): 159–165.
Энтеровирусная инфекция у детей — признаки, причины, симптомы, лечение и профилактика
Причины
Возбудители энтеровирусной природы чувствительны к повышенной температуре, а также обработке перекисью водорода, и других антисептических растворов.
Передача болезнетворных организмов происходит воздушно-капельным путем и через отходы жизнедеятельности. Наиболее уязвимы перед болезнетворными бактериями дети от 2-х до 11 лет, в дальнейшем вырабатывается иммунная защита.
Возбудители проникают в организм через слизистые дыхательных и пищеварительных систем и размножаются на участках глотки и желудочно-кишечного тракта, потому первичные проявления симптомов схожи с ангиной, фарингитом либо поносом. В дальнейшем распространение происходит по кровяной системе и поражает большое количество органов.
В дальнейшем распространение происходит по кровяной системе и поражает большое количество органов.
Симптомы
Вызванные энтеровирусами патологии проявляют себя по-разному, однако существует и ряд общих признаков. Спустя 3–5 дней после проникновения и инкубации наступает острый период, который характеризуется высокой температурой (до 40-ка градусов), ослабленностью, головными болями, тошнотой и утратой аппетита. Пациента при этом знобит. Всегда отмечается опухание и покраснение сосудов на лице, глазном яблоке, на некоторых участках тела. Иногда наблюдается высыпания.
Существуют и специфические симптомы, разнящиеся в зависимости от типа патологии.
Лихорадка – быстрое, чаще трехдневное, протекание, кашель и першение в горле.
Кишечная разновидность – незначительные патологические изменения слизистой горла, заложенный нос, кашель, понос, тошнота, скопление газов в кишечнике, продолжительность – до двух недель.
Поражение дыхательных путей – клиническая картина ОРЗ, непродолжительный жар, ларингит.
Экзантема – сыпь на туловище и коже, иногда появляется пузырьковая сыпь во рту.
Миалгия – высокая температура, болезненность в мышцах, обильное выделение пота.
Менингит – повышенная температура, резкие головные боли, многократная рвота, состояние бреда, тревоги и возбужденности.
Паралитическая форма – парезы и параличи ног, хромота, утрата мышечной силы, в тяжелых случаях – смерть.
Энцефаломиокардит – наблюдается у новорожденных и сопровождается аритмией, тахикардией, одышкой, летальность составляет около 70 %.
Конъюнктивит – активное выделение слез, раздражительность к свету, ощущение постороннего объекта в зрительном аппарате.
Увеит – затрагивает младенцев и сопровождается жаром, кашлем, диареей, дефектами сосудов зрительного органа.
Энтеровирусная инфекция. Профилактика | Министерство здравоохранения Хабаровского края
В летне-осенний период обычно регистрируется подъем заболеваемости энтеровирусными инфекциями. Однако их повсеместное распространение, аналогичная ежегодная ситуация не позволяют в настоящий момент говорить об эпидемии.
Однако их повсеместное распространение, аналогичная ежегодная ситуация не позволяют в настоящий момент говорить об эпидемии.
Энтеровирусная инфекция встречается во всех возрастных группах, но чаще болеют дети раннего возраста. Заболеваемость значительно снижается после первого десятилетия жизни.
Летальный исход вследствие инфекции является редкостью (конкретных описаний случаев смерти от данной инфекции не обнаружено). У новорожденных и иммунокомпрометированных лиц имеется наибольший риск развития осложнений, вторичных по отношению ко всем энтеровирусным инфекциям.
Основные механизмы передачи энтеровирусов — фекально-оральный (посредством загрязненных рук и предметов) и воздушно-капельный. Возможно заражение водным и пищевым путем, а также трансплацентарная передача инфекции.
Инкубационный период при энтеровирусной инфекции продолжается от 2 до 14 (в среднем 7) суток. После заражения вирусы обнаруживаются в верхних дыхательных путях до 3 недель, в желудочно-кишечном тракте — до 8 недель. На протяжении этого периода инфицированные могут выделять их в окружающую среду. Дети наиболее заразны в конце инкубационного периода и в начале заболевания.
На протяжении этого периода инфицированные могут выделять их в окружающую среду. Дети наиболее заразны в конце инкубационного периода и в начале заболевания.
Энтеровирусы распространены повсеместно. Риск заражения выше в любых местах отдыха или скученности людей, независимо от страны пребывания. В тропическом климате заболеваемость круглогодичная, в отличие от умеренного, где прослеживается сезонность заболеваемости энтеровирусными инфекциями — летом и осенью. Ежегодно в летне-осенний период регистрируется подъем заболеваемости энтеровирусными инфекциями. Так, например, по данным Центра по контролю и профилактике заболеваний США (Centers for Disease Control and Prevention, CDC), ежегодно в стране регистрируется около 10 млн случаев энтеровирусных инфекций.
Вирусы первоначально реплицируются в клетках верхних дыхательных путей и дистальном отделе тонкой кишки, в подслизистой и лимфатической ткани. Затем они с кровотоком (первичная виремия) распространяются по тканям и органам. Поражение органов-мишеней происходит после вторичной виремии.
Поражение органов-мишеней происходит после вторичной виремии.
Во время болезни образуются специфические Ig класса M, циркулирующие в кровотоке до 6 месяцев, и IgG, сохраняющиеся на всю жизнь. Типоспецифические нейтрализующие антитела обеспечивают пожизненный иммунитет только к соответствующему серотипу вируса. Специфические IgA, содержащиеся в грудном молоке, защищают от энтеровирусных инфекций детей, находящихся на естественном вскармливании.
Клинические проявления
Энтеровирусы вызывают заболевания с различной симптоматикой, однако наиболее частыми (более 90 % случаев) являются энтеровирусная лихорадка, вирусная пузырчатка полости рта и конечностей, герпангина.
Энтеровирусная лихорадка («летний грипп»)
Это самая частая клиническая форма энтеровирусной инфекции.
Энтеровирусная экзантема. Кожные проявления характеризуются болезненными везикулярными элементами на дорсальных поверхностях кистей и стоп, часто распространяются также на ладони и подошвы, иногда элементы появляются на ногах, ягодицах, предплечьях. В отличие от ветряной оспы, элементы редко зудят. Обычно лихорадка купируется в течение 1–3 суток, высыпания проходят в течение 7–10 суток.
В отличие от ветряной оспы, элементы редко зудят. Обычно лихорадка купируется в течение 1–3 суток, высыпания проходят в течение 7–10 суток.
Контагиозность крайне высокая, заболевают практически 100 % детей раннего возраста. Подавляющее большинство случаев синдрома рот–кисть–стопа протекает легко. Беспокойство могут вызвать болезненные афтозные элементы сыпи во рту, затрудняющие прием пищи и жидкости, что может привести к обезвоживанию. Тяжелое течение болезни — редкость, может быть связано с появлением многочисленных буллезных элементов, возможно отслоение ногтей.
Герпангина (NB! Не имеет отношения к вирусу герпеса!)
Заболевание характеризуется повышением температуры тела до фебрильных значений, болью в горле, за счет чего возникает дисфагия, и энантемой на слизистой оболочке полости рта. Высыпания локализуются на передних нёбных дужках, маленьком язычке, мягком нёбе и представлены папулезно-везикулярными элементами серовато-белого цвета с гиперемированными очертаниями. Вскрываются с образованием болезненных эрозий. Чаще высыпания купируются в течение 7–10 суток, но иногда могут сохраняться и несколько недель.
Вскрываются с образованием болезненных эрозий. Чаще высыпания купируются в течение 7–10 суток, но иногда могут сохраняться и несколько недель.
Острый геморрагический конъюнктивит
Заболевание начинается с острой боли в области глаза, снижения четкости зрения, появления отделяемого из глаз, может присутствовать светобоязнь. При осмотре обнаруживают выраженный отек конъюнктивы, субконъюнктивальные кровоизлияния. Из остальных симптомов могут наблюдаться лихорадка, головная боль. Болезнь спонтанно разрешается в течение 7 суток. Осложнения в виде кератита, двигательного паралича редки. Болезнь крайне заразна.
Эпидемическая миалгия (плевродиния, борнхольмская болезнь)
Начинается остро, с лихорадки до 39–40 °C, в первые часы болезни возникают приступы резких схваткообразных болей в верхней части живота (более характерно для детей), боли в груди (чаще у взрослых). Длительность приступа составляет 15–30 минут, больной принимает вынужденное положение, отмечается тахикардия. Эти боли симулируют плеврит, перитонит.
Эти боли симулируют плеврит, перитонит.
Менингит, энцефалит
Энтеровирусы вызывают большинство серозных менингитов у детей и молодых людей, этиологию которых удается установить. Менингит развивается остро, с такими симптомами, как фебрильная лихорадка, фотофобия, головная боль, рвота, тошнота. При осмотре: ригидность затылочных мышц, положительные симптомы Кернига, Брудзинского. Очаговая неврологическая симптоматика отсутствует. В некоторых случаях симптомы менингита появляются в поздние сроки болезни. В спинно-мозговой жидкости всегда обнаруживается лейкоцитоз: в начале болезни — нередко нейтрофильный, который в дальнейшем меняется на лимфоцитарный. Концентрация глюкозы находится в пределах нормы, белка — или в пределах нормы, или незначительно повышена. В большинстве случаев исход энтеровирусного менингита благоприятный, неврологических отклонений в дальнейшем нет.
Гораздо реже возникает энтеровирусный энцефалит. При этом у больных нарастает сонливость, появляются дезориентация, неврологический дефицит (например, моторный, сенсорный, речевой), иногда судороги. Прогноз в большинстве случаев также благоприятный.
Прогноз в большинстве случаев также благоприятный.
Диагностика
В клинической практике дополнительных исследований для подтверждения энтеровирусной инфекции, как правило, не требуется. Диагноз основан на характерной клинической картине. Нерационально выделение вируса в мазках из зева, носоглотки и кала в связи с вероятностью вирусоносительства. Диагноз подтверждается при обнаружении вируса в крови, спинно-мозговой или плевральной жидкости, тканях. Используют метод полимеразной цепной реакции. Его чувствительность достигает 95 %, специфичность — до 100 %. Серологические методы в клинической практике не используют ввиду наличия множества серотипов с отсутствием общего антигена.
Дополнительные исследования необходимы при развитии осложнений. По показаниям выполняется люмбальная пункция с исследованием спинно-мозговой жидкости, компьютерная томография головного мозга для исключения кровоизлияний, электроэнцефалограмма (при менингите, энцефалите), ЭКГ, УЗИ сердца (при мио- и перикардите).
Лечение
В подавляющем большинстве случаев энтеровирусные инфекции переносятся легко и лечения не требуют. Специфической противовирусной терапии при данной инфекции не существует. Антибактериальные препараты не показаны (могут быть применены только при развитии бактериальных осложнений). Лечение симптоматическое.
Профилактика
Как и при других вирусных инфекциях, единственной мерой профилактики заболеваний, вызванных вирусами Коксаки, является предотвращение попадания их в организм через кожный покров и слизистые оболочки. Для этого необходимо применять несколько правил, полезных для предотвращения любых инфекций:
соблюдать общие правила личной гигиены: мытье рук с мылом перед едой, после гигиенических мероприятий, после возвращения с прогулки, из общественных мест;
употреблять только чистую питьевую воду;
тщательно мыть кипяченой водой фрукты, овощи, ягоды;
следить за свежестью употребляемых продуктов, сроками и условиями их хранения;
в период подъема заболеваемости избегать посещения мест массового скопления людей, контакта с заболевшими.

Главный внештатный специалист по инфекционным болезням у детей
министерства здравоохранения Хабаровского края,
заведующая кафедрой инфекционных болезней
КГБОУ ДПО ИПКСЗ, д.м.н. Татьяна Евгеньевна Макарова
Источник: КГБОУ ДПО ИПКСЗ
ЭНТЕРОВИРУСНАЯ ИНФЕКЦИЯ
Энтеровирусы – названы так, потому что после возникновения инфекции они размножаются первоначально в желудочно-кишечном тракте. Несмотря на это, они обычно не вызывают кишечных симптомов, чаще всего они активно распространяются и вызывают симптомы и заболевания таких органов как: сердце, кожа, легкие, головной и спинной мозг Энтеровирусы встречаются во всем мире, но инфицирование чаще всего происходит в районах с низким уровнем гигиены и высокой перенаселенностью. Вирус чаще всего передается фекально-оральным путем, а также через загрязненную пищу или воду. Попадание в организм некоторых штаммов вируса воздушно-капельным путем может привести к респираторным заболеваниям. Грудное молоко содержит антитела, которые могут защитить новорожденных. Инкубационный период для большинства энтеровирусов составляет от 2 до 14 дней. В районах с умеренным климатом инфекции возникают в основном летом и осенью.
Грудное молоко содержит антитела, которые могут защитить новорожденных. Инкубационный период для большинства энтеровирусов составляет от 2 до 14 дней. В районах с умеренным климатом инфекции возникают в основном летом и осенью.
Энтеровирус чаще всего попадает в организм человека через желудочно-кишечный тракт (ЖКТ) или дыхательные пути. Попадая в ЖКТ вирусы останавливаются в местных лимфатических узлах где они начинают первую стадию размножения. Примерно на третий день после инфицирования вирусы попадают в кровоток и начинают циркулировать по организму. На 3-7й день вирусы с кровью могут попасть в системы органов где может начаться вторая стадия размножения и как следствие вызвать различные заболевания. Производство антител к вирусу происходит в течении первых 7-10и дней.
Симптомы и признаки энтеровирусной инфекции
Энтеровирусы вызывают огромное количество случаев инфицирования в год. Более 90% этих случаев протекает либо бессимптомно, либо вызывает неспецифическое лихорадочное заболевание.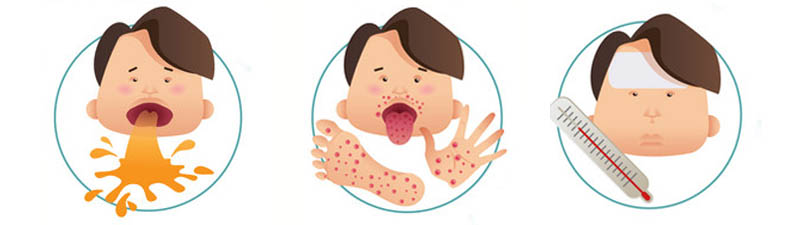 Обычно спектр симптомов очень большой, но в большинстве случаев он практически всегда включают: лихорадку (повышение температуры тела до 39-40°С), общая слабость, головная боль, мышечная боль и желудочно-кишечные симптомы.
Обычно спектр симптомов очень большой, но в большинстве случаев он практически всегда включают: лихорадку (повышение температуры тела до 39-40°С), общая слабость, головная боль, мышечная боль и желудочно-кишечные симптомы.
Энтеровирусы попадая в организм человека, могут вызывать несколько симптомов.
- Насморк и заложенность носа и его пазух, боль в носу, боль в горле, боль в ушах, затруднение глотания, потеря обоняния или вкуса.
- Тошнота, расстройство желудка, рефлюкс, вздутие живота, верхняя и нижняя боли в животе, судороги, запоры, чередующиеся с диареей.
- Стремительная потеря веса из-за нарушения пищеварения и уменьшенного потребления калорий или увеличение веса из-за неактивности.
- Онемение в конечностях, подергивание мышц и спазмы. Могут наблюдаться покалывание лица и онемение.
- Различные виды головной боли (острые, ноющие, пульсирующие).

- Боли в костях, мышцах и суставах. Боль в ногах является довольно распространенным явлением.
- Боль и стеснение в груди, сердцебиение.
- Кашель, одышка, свистящее дыхание.
- Нарушение сердечного ритма (аритмии) или тахикардия (учащенное сердцебиение)
- Перемежающаяся лихорадка — характеризующаяся быстрым, значительным повышением температуры (38-40°С), которая держится несколько часов, а затем сменяется быстрым её падением до нормальных значений), озноб и сильная ночная потливость.
- Затуманенное зрение, снижение остроты зрения.
- Пузырьки или изъязвления в ротовой полости, глотке и у женщин во влагалище/ шейке матки.
- Психологические проблемы – тревожные состояния или депрессии.
- Проблемы с концентрацией внимания. Когнитивные проблемы, краткосрочные проблемы с памятью.

- Нарушение сна.
- Судороги возникают редко, но случаются.
- Увеличение лимфатических узлов в области шеи и в подмышечных впадинах
- Сыпь
Нельзя говорить о каких-то специфических симптомах характерных для всей группы энтеровирусов помимо перечисленных выше, но можно сгруппировать симптомы проявляющиеся при осложнениях энтеровирусной инфекции:
Лечение энтеровирусной инфекции
В большинстве случаев Энтеровирусная инфекция протекает без осложнений и не требует какого-либо специфического лечения. Основой является симптоматическое и поддерживающее лечение. Постельный режим, обильное питье, витамины, в случае высокой температуры жаропонижающие. Не стоит забывать, что даже при появлении малейших и незначительных симптомов стоит немедленно обратиться к врачу, особенно если симптомы появились у ребенка! САМОЛЕЧЕНИЕ НЕДОПУСТИМО!
Профилактика
Общая гигиена и частое мытье рук эффективны в снижении распространения этих вирусов. Если мыло, и чистая вода не доступны, используйте «дезинфицирующее средство для рук» на спиртовой основе. Важно отметить, что грудное молоко содержит антитела, которые могут защитить малыша.
Если мыло, и чистая вода не доступны, используйте «дезинфицирующее средство для рук» на спиртовой основе. Важно отметить, что грудное молоко содержит антитела, которые могут защитить малыша.
Медицинское обслуживание, консультации, диета и деятельность
Автор
Дэниел Оуэнс, BM, MRCPCH (Великобритания) Научный сотрудник по клиническим исследованиям, Центр клинических исследований NIHR, Больница общего профиля Саутгемптона, Великобритания
Раскрытие: Ничего не разглашать.
Соавтор (ы)
Сол Н. Фауст, MA, MBBS, PhD, MRCPCH (Великобритания) Старший преподаватель педиатрической иммунологии и инфекционных заболеваний, Медицинский факультет Саутгемптонского университета; Директор Центра клинических исследований NIHR, Университетская больница Саутгемптона, NHS Foundation Trust, Великобритания
Сол Н. Фауст, магистр медицины, бакалавр медицины и биологии, доктор философии, MRCPCH (Великобритания) является членом следующих медицинских обществ: Британской педиатрической группы аллергии, иммунитета и инфекций, Европейской Общество детских инфекционных заболеваний, Международное общество инфекционных заболеваний, Королевский колледж педиатрии и здоровья детей
Раскрытие информации: выступать (d) в качестве докладчика или члена бюро докладчиков по вопросам: менингококковых вакцин Pfizer
Получен грант на исследования от : Учреждение Pfizer
(без личных гонораров) получало консультационные услуги от Pfizer, Sanofi, Seqrius, Merck, Medimmune, AstraZeneca.
Специальная редакционная коллегия
Мэри Л. Виндл, PharmD Адъюнкт-профессор, Фармацевтический колледж Медицинского центра Университета Небраски; Главный редактор Medscape Drug Reference
Раскрытие информации: нечего раскрывать.
Mark R Schleiss, MD Minnesota American Legion and A Additional Heart Research Foundation Кафедра педиатрии, профессор педиатрии, директор отделения, Отделение инфекционных болезней и иммунологии, Департамент педиатрии, Медицинская школа Университета Миннесоты
Mark R Schleiss, MD является членом следующих медицинских обществ: Американского педиатрического общества, Американского общества инфекционных заболеваний, Общества педиатрических инфекционных болезней, Общества педиатрических исследований
Раскрытие информации: не подлежит разглашению.
Главный редактор
Рассел Стил, доктор медицины Профессор-клиницист, Медицинский факультет Тулейнского университета; Врач, штатный врач, Ochsner Clinic Foundation
Рассел Стил, доктор медицинских наук, является членом следующих медицинских обществ: Американской академии педиатрии, Американской ассоциации иммунологов, Американского педиатрического общества, Американского общества микробиологии, Американского общества инфекционных болезней, Медицинского центра штата Луизиана. Общество, Общество детских инфекционных болезней, Общество педиатрических исследований, Южная медицинская ассоциация
Общество, Общество детских инфекционных болезней, Общество педиатрических исследований, Южная медицинская ассоциация
Раскрытие информации: нечего раскрывать.
Дополнительные участники
Джозеф Домачовске, доктор медицины Профессор педиатрии, микробиологии и иммунологии, кафедра педиатрии, отделение инфекционных заболеваний, Медицинский университет штата Нью-Йорк, Государственный университет штата Нью-Йорк
Джозеф Домачовске, доктор медицины, является членом следующих медицинских обществ: Alpha Omega Alpha , Американская академия педиатрии, Американское общество микробиологии, Общество инфекционных заболеваний Америки, Общество педиатрических инфекционных заболеваний, Phi Beta Kappa
Раскрытие: Получен грант на исследования от: Pfizer; GlaxoSmithKline; AstraZeneca; Merck; Американской академии педиатрии, Novavax, Regeneron , Diassess, Actelion
Полученный доход в размере 250 долларов США или более от: Sanofi Pasteur.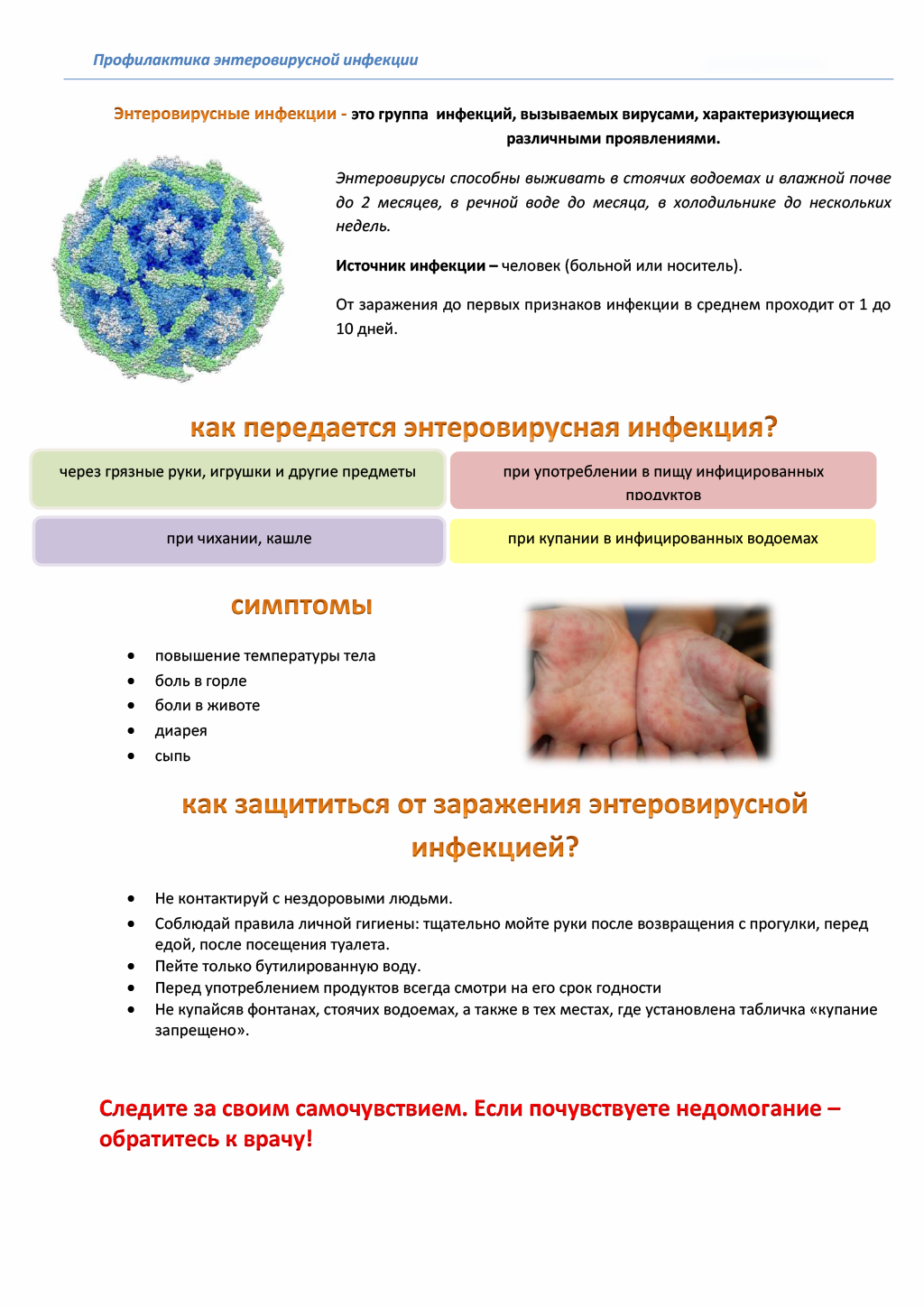
Леонард Р. Крылов, доктор медицины Заведующий отделением детских инфекционных болезней и международного усыновления, заместитель председателя педиатрического отделения больницы Уинтропского университета; Профессор педиатрии, Медицинский факультет Университета Стони Брук
Леонард Р. Крылов, доктор медицинских наук, является членом следующих медицинских обществ: Американской академии педиатрии, Американского педиатрического общества, Американского общества инфекционных болезней, Общества педиатрических инфекционных болезней, Общества педиатрических исследований.
Раскрытие информации: раскрывать нечего.
Mobeen H Rathore, MD, CPE, FAAP, FIDSA Начальник отдела детских инфекционных заболеваний / иммунологии, заместитель председателя педиатрического отделения Медицинского колледжа Университета Флориды в Джексонвилле; Эпидемиолог больницы и начальник отдела инфекционных болезней и иммунологии детской больницы Вольфсона; Директор Центра исследований, образования и обслуживания в области ВИЧ / СПИДа Университета Флориды (UF CARES)
Mobeen H Rathore, MD, CPE, FAAP, FIDSA является членом следующих медицинских обществ: Американской академии педиатрии, Американского общества микробиологов. , Медицинская ассоциация Флориды, Общество инфекционных болезней Америки, Общество педиатрических инфекционных болезней, Общество эпидемиологии здравоохранения Америки, Общество педиатрических исследований, Южная медицинская ассоциация, Южное общество педиатрических исследований, Флоридское отделение Американской академии педиатрии, Педиатрическое общество Флориды , Европейское общество детских инфекционных заболеваний
, Медицинская ассоциация Флориды, Общество инфекционных болезней Америки, Общество педиатрических инфекционных болезней, Общество эпидемиологии здравоохранения Америки, Общество педиатрических исследований, Южная медицинская ассоциация, Южное общество педиатрических исследований, Флоридское отделение Американской академии педиатрии, Педиатрическое общество Флориды , Европейское общество детских инфекционных заболеваний
Раскрытие информации: нечего раскрывать.
Николас Джон Беннетт, MBBCh, PhD, FAAP, MA (Cantab) Доцент педиатрии, содиректор отдела управления противомикробными препаратами, медицинский директор, Отделение детских инфекционных заболеваний и иммунологии Детского медицинского центра Коннектикута
Николас Джон Беннетт, MBBCh, PhD, FAAP, MA (Cantab) является членом следующих медицинских обществ: Alpha Omega Alpha, Американская академия педиатрии
Раскрытие информации: получил исследовательский грант от: Cubist
Полученный доход в размере не менее чем 250 долларов США от: Horizon Pharmaceuticals, Shire
Юридические консультации по вопросам Medico: Разн.
Благодарности
Авторы и редакторы eMedicine выражают признательность предыдущему автору Мишель Мовад, доктору медицины, за вклад в первоначальное написание и разработку этой статьи.
Рис. 5 представляет собой фотографию случая атипичной HFMD, которую видели д-р Генри Федер и д-р Николас Беннетт. Разрешение на использование фотографии было предоставлено семьей пациента. Изображение перепечатано из The Lancet Infectious Diseases, Vol.14 (1), Федер, Беннет и Модлин, Атипичное заболевание рук, ног и рта: пузырно-пузырчатая сыпь, вызванная вирусом Коксаки A6, страницы 83-86., Copyright (2014), с разрешения Elsevier.
Выявление, диагностика и лечение энтеровирусных инфекций у новорожденных
Неполиовирусные энтеровирусы обычно поражают новорожденных с последствиями от бессимптомной инфекции и доброкачественных заболеваний до тяжелых, опасных для жизни заболеваний. Часто возникающие симптомы включают жар, раздражительность, вялость, анорексию и сыпь. Хотя большинство заболеваний протекает в легкой форме, тяжелое заболевание развивается у части новорожденных, инфицированных в течение первых 2 недель жизни. Тяжелое заболевание может включать сепсис, менингоэнцефалит, миокардит, пневмонию, гепатит и / или коагулопатию. Сообщается о значительных показателях смертности, и среди выживших могут возникать долгосрочные последствия. Факторы риска и клинические признаки, связанные с тяжелым заболеванием, включают отсутствие нейтрализующих антител к инфекционному серотипу, материнское заболевание до или во время родов, недоношенность, начало заболевания в течение первых нескольких дней жизни, полиорганное заболевание, тяжелый гепатит, положительный результат вирусной культуры в сыворотке крови, и специфический инфекционный серотип (например,грамм. вирусы Коксаки и эховирус группы В 11). В то время как основой диагностики традиционно было выделение вируса в культуре ткани, полимеразная цепная реакция оказалась более чувствительной, чем культура, высокоспецифичной и быстрой.
Часто возникающие симптомы включают жар, раздражительность, вялость, анорексию и сыпь. Хотя большинство заболеваний протекает в легкой форме, тяжелое заболевание развивается у части новорожденных, инфицированных в течение первых 2 недель жизни. Тяжелое заболевание может включать сепсис, менингоэнцефалит, миокардит, пневмонию, гепатит и / или коагулопатию. Сообщается о значительных показателях смертности, и среди выживших могут возникать долгосрочные последствия. Факторы риска и клинические признаки, связанные с тяжелым заболеванием, включают отсутствие нейтрализующих антител к инфекционному серотипу, материнское заболевание до или во время родов, недоношенность, начало заболевания в течение первых нескольких дней жизни, полиорганное заболевание, тяжелый гепатит, положительный результат вирусной культуры в сыворотке крови, и специфический инфекционный серотип (например,грамм. вирусы Коксаки и эховирус группы В 11). В то время как основой диагностики традиционно было выделение вируса в культуре ткани, полимеразная цепная реакция оказалась более чувствительной, чем культура, высокоспецифичной и быстрой. Иммуноглобулин использовался в качестве терапевтического средства для новорожденных с энтеровирусным заболеванием; однако клиническая эффективность не доказана. Специфическая противовирусная терапия энтеровирусов находится в стадии разработки. Плеконарил — это исследуемый агент, который ингибирует прикрепление вируса к рецепторам клетки-хозяина и освобождает от оболочки вирусной нуклеиновой кислоты.Он обладает широкой и сильной антиэнтеровирусной активностью, отличной биодоступностью при пероральном приеме и хорошо переносится. Некоторые клинические испытания продемонстрировали пользу у детей и взрослых с энтеровирусным менингитом, а также у взрослых с инфекциями верхних дыхательных путей, вызванными пикорнавирусами (риновирусами или энтеровирусами). Данные, обобщающие данные о сострадательном использовании при тяжелых энтеровирусных заболеваниях (включая неонатальный сепсис), также предполагают возможную пользу. Ограниченные фармакокинетические данные доступны для младенцев и новорожденных.
Иммуноглобулин использовался в качестве терапевтического средства для новорожденных с энтеровирусным заболеванием; однако клиническая эффективность не доказана. Специфическая противовирусная терапия энтеровирусов находится в стадии разработки. Плеконарил — это исследуемый агент, который ингибирует прикрепление вируса к рецепторам клетки-хозяина и освобождает от оболочки вирусной нуклеиновой кислоты.Он обладает широкой и сильной антиэнтеровирусной активностью, отличной биодоступностью при пероральном приеме и хорошо переносится. Некоторые клинические испытания продемонстрировали пользу у детей и взрослых с энтеровирусным менингитом, а также у взрослых с инфекциями верхних дыхательных путей, вызванными пикорнавирусами (риновирусами или энтеровирусами). Данные, обобщающие данные о сострадательном использовании при тяжелых энтеровирусных заболеваниях (включая неонатальный сепсис), также предполагают возможную пользу. Ограниченные фармакокинетические данные доступны для младенцев и новорожденных. В настоящее время проводится многоцентровое плацебо-контролируемое рандомизированное исследование плеконарила у новорожденных с тяжелым гепатитом, коагулопатией и / или миокардитом.
В настоящее время проводится многоцентровое плацебо-контролируемое рандомизированное исследование плеконарила у новорожденных с тяжелым гепатитом, коагулопатией и / или миокардитом.
Лечение энтеровируса | Everyday Health
Простые домашние методы лечения могут помочь в лечении большинства случаев энтеровируса.
Не существует лекарств, специально предназначенных для лечения энтеровирусной инфекции.
В большинстве случаев энтеровирус проходит самостоятельно с помощью обычных поддерживающих мер в домашних условиях, таких как отдых, жидкости и использование безрецептурных препаратов для облегчения симптомов, таких как ибупрофен (Адвил / Мотрин) или ацетаминофен (Тайленол) для лечения симптомов. боль.
Антибиотики нельзя использовать, потому что они бесполезны против любых вирусных инфекций, включая энтеровирус.
Серьезные случаи
Однако следует обратиться за медицинской помощью, если болезнь станет серьезной.
Большинство тяжелых случаев встречается у младенцев, взрослых со слабой иммунной системой или у детей, у которых уже есть проблемы с легкими, такие как астма.
Людей, страдающих серьезными респираторными заболеваниями, может потребовать госпитализация.
Несмотря на то, что существуют противовирусные препараты, которые могут использоваться против вирусов, включая энтеровирус, ни один из них не оказался полезным против энтеровируса D68 (EV-D68) — штамма энтеровируса, вызвавшего вспышку 2014 года, — по данным Центров по контролю за заболеваниями и Профилактика (CDC).
Профилактика
Энтеровирусы, скорее всего, передаются от одного человека к другому, когда инфицированный человек кашляет, чихает или касается поверхности, к которой затем прикасаются другие.
Энтеровирусная инфекция начинается при проглатывании материала, зараженного вирусом.
Вирус размножается в пищеварительном тракте, а затем — если он не убит иммунной системой — попадает в кровоток и начинает вызывать симптомы.
Для передачи вируса новому хозяину требуется всего лишь мельчайший кусочек инфицированного материала — например, капля слюны, слишком маленькая, чтобы ее можно было увидеть невооруженным глазом.
Для предотвращения распространения энтеровирусов рекомендуется соблюдать те же правила гигиены, что и для предотвращения распространения простуды и гриппа:
- Часто и тщательно мойте руки, и пусть ваши дети поступают так же. Это особенно важно перед едой и когда вы впервые зашли в дом.
- Не прикасайтесь к глазам, носу или рту немытыми руками.
- Оставайтесь дома, если у вас есть симптомы инфекции верхних дыхательных путей.
- Не оставляйте детей дома, если у них есть симптомы инфекции верхних дыхательных путей.Не отправляйте их в школу или детский сад.
- Научите своих детей кашлять или чихать в плечо или локоть, чтобы защитить окружающих и избежать попадания заразных капель на руки.
- Не делитесь столовыми приборами, чашками, стаканами или бутылками с больным человеком.

- Продезинфицируйте твердые поверхности, к которым мог прикасаться больной, например игрушки, клавиатуры, телефоны, а также ручки дверей, смесители и туалеты со смывом.
Вакцины от энтеровирусной инфекции нет.
Вакцина против гриппа важна для защиты от вирусов гриппа, вызывающих грипп, но не защищает от энтеровирусов.
Энтеровирус и дети с астмой
Люди, страдающие астмой — состоянием, при котором определенные триггеры вызывают воспаление и сужение дыхательных путей — в целом более уязвимы к респираторным заболеваниям.
Вспышка EV-D68 в 2014 году вызвала особенно тяжелое респираторное заболевание у детей, страдающих астмой.
У CDC был особый совет для родителей детей с астмой, как подготовиться к возможности заражения EV-D68.
Совет важен даже в годы с менее серьезными вспышками энтеровируса:
- Обсудите и обновите план лечения астмы вашего ребенка с врачом.
- Следите за тем, как ваш ребенок использует прописанные вам лекарства от астмы, особенно лекарства длительного действия.

- Убедитесь, что ваш ребенок всегда имеет доступ к лекарствам от астмы (также известным как спасательные средства, такие как ингалятор с альбутеролом).
- Следуйте плану действий вашего ребенка при появлении новых или ухудшающихся симптомов астмы.
- Сделайте прививку вашему ребенку от гриппа.
- Обратитесь к врачу, если симптомы не исчезнут или не ухудшатся при соблюдении плана действий.
Лечение потенциально опасных для жизни энтеровирусных инфекций с помощью Плеконарила | Клинические инфекционные болезни
Аннотация
Энтеровирусы обычно вызывают самоограничивающееся заболевание, которое, хотя и связано с высокой заболеваемостью, редко заканчивается смертельным исходом. Однако у определенных групп пациентов энтеровирусы могут вызывать потенциально опасные для жизни инфекции.Плеконарил — это новое соединение, которое интегрируется в капсид пикорнавирусов, включая энтеровирусы и риновирусы, предотвращая прикрепление вируса к клеточным рецепторам и освобождая оболочку для высвобождения РНК в клетку. Плеконарил использовался для лечения пациентов с потенциально опасными для жизни энтеровирусными инфекциями, и для 38 из этих пациентов имелось достаточно данных последующего наблюдения для определения ответа на терапию. Ответ оценивался в 4 категориях: клиническая, вирусологическая, лабораторная и радиологическая.Большинство пациентов (28 [78%] из 36), в том числе 12 из 16 с хроническим энтеровирусным менингоэнцефалитом, имели клинический ответ, временно связанный с терапией плеконарилом. Аналогичным образом, почти все пациенты, чьи вирусологические ответы (12 [92%] из 13), лабораторные ответы (14 [88%] из 16) и радиологические ответы (3 [60%] из 5) могли быть оценены), были признаны ответившими на лечение. выгодно по сравнению с курсом лечения плеконарилом. Побочные эффекты были минимальными, и препарат в целом хорошо переносился.
Плеконарил использовался для лечения пациентов с потенциально опасными для жизни энтеровирусными инфекциями, и для 38 из этих пациентов имелось достаточно данных последующего наблюдения для определения ответа на терапию. Ответ оценивался в 4 категориях: клиническая, вирусологическая, лабораторная и радиологическая.Большинство пациентов (28 [78%] из 36), в том числе 12 из 16 с хроническим энтеровирусным менингоэнцефалитом, имели клинический ответ, временно связанный с терапией плеконарилом. Аналогичным образом, почти все пациенты, чьи вирусологические ответы (12 [92%] из 13), лабораторные ответы (14 [88%] из 16) и радиологические ответы (3 [60%] из 5) могли быть оценены), были признаны ответившими на лечение. выгодно по сравнению с курсом лечения плеконарилом. Побочные эффекты были минимальными, и препарат в целом хорошо переносился.
Энтеровирусы включают около 70 серотипов близкородственных патогенов, вызывающих широкий спектр заболеваний человека, от легкой неспецифической лихорадки до распространенных инфекций верхних дыхательных путей, асептического менингита, тяжелого миокардита, энцефалита и паралитического полиомиелита [1]. Подгруппы энтеровирусов включают полиовирусы, вирусы Коксаки А и В, эховирусы и энтеровирусы с новыми номерами. По оценкам, в США ежегодно регистрируется 10–30 миллионов энтеровирусных инфекций [2], вызывая значительную краткосрочную заболеваемость и экономические последствия [3–5].
Подгруппы энтеровирусов включают полиовирусы, вирусы Коксаки А и В, эховирусы и энтеровирусы с новыми номерами. По оценкам, в США ежегодно регистрируется 10–30 миллионов энтеровирусных инфекций [2], вызывая значительную краткосрочную заболеваемость и экономические последствия [3–5].
У некоторых пациентов развиваются потенциально опасные для жизни энтеровирусные инфекции, возможности лечения которых ограничены. У людей с дефицитом антител, инфицированных энтеровирусами, может развиться хронический менингит или менингоэнцефалит, длящийся много лет, часто со смертельным исходом [6, 7]. Недавно было обнаружено, что пациенты с трансплантацией костного мозга (ТКМ) как остро [8], так и хронически [9] инфицированы энтеровирусами, что приводит к потенциально сложным и тяжелым исходам.Новорожденные, также относительно иммунодефицитные, по-видимому, подвергаются наибольшему риску тяжелой заболеваемости и смертности, когда признаки и симптомы развиваются в первые дни жизни, что свидетельствует о трансплацентарном заражении с высокой вирусной нагрузкой [10–12].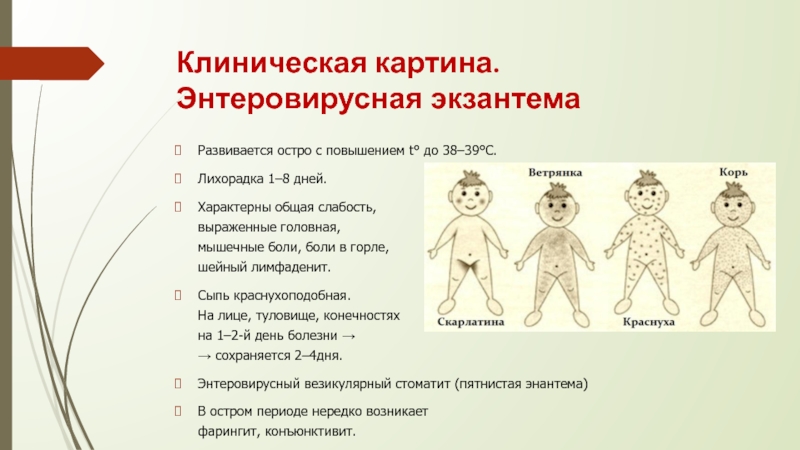 Энтеровирусы также входят в число наиболее часто определяемых этиологий миокардита [13]. У меньшинства пациентов с энтеровирусным миокардитом развиваются застойная сердечная недостаточность, хронический миокардит или дилатационная кардиомиопатия [13].
Энтеровирусы также входят в число наиболее часто определяемых этиологий миокардита [13]. У меньшинства пациентов с энтеровирусным миокардитом развиваются застойная сердечная недостаточность, хронический миокардит или дилатационная кардиомиопатия [13].
Энтеровирусы являются наиболее частой причиной менингита в США [14] и важной причиной энцефалита [15].Последний неврологический синдром может привести к значительным краткосрочным и долгосрочным осложнениям [15]. Недавно боковой амиотрофический склероз снова был связан с хронической энтеровирусной инфекцией, что вновь вызвало споры на протяжении многих лет [16].
Атомная структура полиовирусов, определенная компьютерными кристаллографическими исследованиями, включает икосаэдрическую архитектуру с 60 идентичными «сторонами», каждая из которых имеет глубокую центральную щель или каньон, в который помещается специфический клеточный рецептор энтеровируса, когда вирус встречает вирус. чувствительная клетка-хозяин [17].Под каньоном находится гидрофобный карман, в который могут проникать самые разные гидрофобные соединения [17]. Плеконарил (3- {3,5-диметил-4 — [[3-метил-5-изоксазолил} пропил] фенил] -5- [трифторметил] -1,2,4-оксадиазол; ViroPharma) интегрируется в этот гидрофобный карман и предотвращает репликацию вируса, подавляя расплетение вируса и блокируя прикрепление вируса к рецепторам клетки-хозяина [18, 19].
Плеконарил (3- {3,5-диметил-4 — [[3-метил-5-изоксазолил} пропил] фенил] -5- [трифторметил] -1,2,4-оксадиазол; ViroPharma) интегрируется в этот гидрофобный карман и предотвращает репликацию вируса, подавляя расплетение вируса и блокируя прикрепление вируса к рецепторам клетки-хозяина [18, 19].
Мы сообщаем о предварительных результатах лечения потенциально опасных для жизни энтеровирусных инфекций плеконарилом по протоколу сострадательного использования в течение 2 баллов.Пятилетний период с осени 1996 года.
Пациенты и методы
Осенью 1996 года ViroPharma, разработчик плеконарила, сделала этот препарат доступным для лечения пациентов с потенциально опасными для жизни энтеровирусными инфекциями. Подходящие пациенты включали пациентов с хроническим энтеровирусным менингоэнцефалитом и агаммаглобулинемией или гипогаммаглобулинемией (CEMA), энтеровирусным сепсисом новорожденных, миокардитом, вакциноассоциированной инфекцией или полиовирусной инфекцией дикого типа, синдромом постполиомышечной атрофии или энтеровирусным энцефалитом пациентов, инфицированных энтеровирусным энцефалитом. Пациенты были направлены на исследование врачами со всего мира, которые связались с одним из авторов (Х.А. Р. или А. Д. У.) или производителем лекарств.
Пациенты были направлены на исследование врачами со всего мира, которые связались с одним из авторов (Х.А. Р. или А. Д. У.) или производителем лекарств.
После первых 2,5 лет программы сострадательного использования было 38 пациентов с достаточной информацией о последующем наблюдении, доступной для предварительной оценки ответа на терапию. Ответы были разделены на «клинические», «вирусологические», «лабораторные» и «радиологические» и основывались на сравнении конкретных параметров, измеренных до и после терапии плеконарилом.Клинический ответ определялся как уменьшение ≥1 заметных имеющихся симптомов или признаков. Для целей этого анализа «отсутствие изменений» в состоянии пациента считалось отсутствием ответа, хотя стабилизация без прогрессирования заболевания может фактически представлять терапевтический ответ у некоторых из этих пациентов. Вирусологический ответ определяли как возврат от положительного результата на культуру энтеровируса к отрицательному результату на культуре энтеровируса и / или от положительного результата ПЦР на энтеровирус к отрицательному результату ПЦР на энтеровирус. Методики вирусологической идентификации энтеровирусов с помощью посева и ПЦР с обратной транскриптазой подробно описаны в другом месте [20]. Лабораторный ответ включал нормализацию или существенное улучшение ранее аномальных лабораторных характеристик для конкретного заболевания, которое лечили (например, функции печени, плеоцитоза). Наконец, несколько пациентов прошли МРТ или сканирование м-бисиката технеция-99 или рентгенографию грудной клетки до и после терапии; Объективные улучшения результатов этих исследований считались радиологическим свидетельством ответа.
Методики вирусологической идентификации энтеровирусов с помощью посева и ПЦР с обратной транскриптазой подробно описаны в другом месте [20]. Лабораторный ответ включал нормализацию или существенное улучшение ранее аномальных лабораторных характеристик для конкретного заболевания, которое лечили (например, функции печени, плеоцитоза). Наконец, несколько пациентов прошли МРТ или сканирование м-бисиката технеция-99 или рентгенографию грудной клетки до и после терапии; Объективные улучшения результатов этих исследований считались радиологическим свидетельством ответа.
Детей лечили в течение 7-10 дней 5,0 мг / кг на дозу 3 раза в день. Взрослые получали 200 мг или 400 мг на дозу 3 раза в день в течение 7–10 дней; более высокая доза была выбрана для большинства пациентов после того, как первые несколько пациентов без труда перенесли более низкую дозу. Пять пациентов прошли второй курс терапии из-за их реакции на первоначальный курс и либо последующего ухудшения состояния после терапии, либо желания еще больше усилить первоначальный ответ. Все лечение проводилось пероральным приемом суспензии плеконарила.
Все лечение проводилось пероральным приемом суспензии плеконарила.
Нежелательные явления были охарактеризованы в соответствии с их отношением к исследуемому препарату («не связаны», «возможно связаны», «вероятно связаны» или «определенно связаны»), интенсивности («легкие», «умеренные» или «тяжелые». »), Исход (« выздоровел »,« улучшился »или« без изменений ») и серьезность (« серьезный »или« несерьезный »).
Результаты
Общие показатели ответа приведены в таблице 1, а отдельные пациенты описаны в таблице 2.Среди 17 поддающихся оценке пациентов с CEMA (таблица 2) возрастной диапазон составлял 2–50 лет (медиана — 16 лет). Заголовок категории CEMA для целей данного обсуждения включал пациентов со всеми типами дефицита Ig. Всего у 9 из этих пациентов была врожденная агаммаглобулинемия, сцепленная с типом X Брутона, у 4 — общий вариабельный иммунодефицит, у 2 — синдром гипер-IgM, у 1 — дефицит IgA и подклассов IgG2 и IgG4, а у 1 — тяжелая комбинированная иммунодефицитная болезнь (SCID). . Еще 2 пациента (1 с Х-сцепленной агаммаглобулинемией Брутона и 1 с ТКИД) заболели вакциноассоциированной полиовирусной инфекцией и рассматривались отдельно (см. Ниже).В общей сложности 12 из 16 пациентов с CEMA, у которых можно было оценить клинические ответы, имели клинический ответ на терапию: 9 с улучшенным неврологическим статусом, 3 с ростом / увеличением веса, 2 с уменьшением миозита / фасциита, 1 с улучшенным зрением. , и 1 со сниженной гепатомегалией. Еще 4 пациента оставались стабильными (без улучшения или ухудшения их состояния) после терапии.
. Еще 2 пациента (1 с Х-сцепленной агаммаглобулинемией Брутона и 1 с ТКИД) заболели вакциноассоциированной полиовирусной инфекцией и рассматривались отдельно (см. Ниже).В общей сложности 12 из 16 пациентов с CEMA, у которых можно было оценить клинические ответы, имели клинический ответ на терапию: 9 с улучшенным неврологическим статусом, 3 с ростом / увеличением веса, 2 с уменьшением миозита / фасциита, 1 с улучшенным зрением. , и 1 со сниженной гепатомегалией. Еще 4 пациента оставались стабильными (без улучшения или ухудшения их состояния) после терапии.
Таблица 1
Резюме ответов на терапию плеконарилом потенциально опасных для жизни энтеровирусных инфекций.
Таблица 1
Резюме ответов на терапию плеконарилом потенциально опасных для жизни энтеровирусных инфекций.
Таблица 2
Обзор пациентов, получавших терапию плеконарилом по поводу потенциально опасных для жизни энтеровирусных инфекций.
Таблица 2
Обзор пациентов, получавших терапию плеконарилом по поводу потенциально опасных для жизни энтеровирусных инфекций.
Данных 7 пациентов с CEMA было достаточно для оценки вирусологического ответа.Считалось, что у шести из 7 был вирусологический ответ: у двоих после терапии статус посевов и ПЦР-положительный изменился на отрицательный статус посева и ПЦР; 2, оцененные только с помощью ПЦР, изменились с положительного на отрицательный; 1, оцененный только посевом, изменился с положительного на отрицательный после терапии; и у 1 человека, который оставался положительным по культуре после терапии, был снижен уровень вируса при количественном измерении. Два пациента (в том числе один, отмеченный выше, с уменьшенным количеством энтеровируса и один с отрицательным вирусологическим ответом) имели признаки смешанной инфекции 2 энтеровирусами.У одного пациента был подтвержден положительный результат посева на энтеровирус до начала терапии, но последующие посевы не проводились; еще 9 пациентов никогда не имели подтвержденной энтеровирусной инфекции, но имели типичные признаки CEMA.
У девяти пациентов с CEMA были измерены лабораторные параметры, достаточные для оценки лабораторного ответа; Такой ответ оказался у 8 пациентов. Большинство ответов были с уменьшением плеоцитоза или снижением уровня белка в спинномозговой жидкости после терапии плеконарилом.Один пациент умер от не связанных причин (случайное утопление), и мозг пациента был нормальным при вскрытии без признаков инфекции. Из 3 пациентов, которым проводились исследования ЦНС до и после терапии плеконарилом, улучшение их состояния было продемонстрировано для всех (сканирование м-бисиката технеция-99 для 3 и МРТ для 1).
Большинство ответов были с уменьшением плеоцитоза или снижением уровня белка в спинномозговой жидкости после терапии плеконарилом.Один пациент умер от не связанных причин (случайное утопление), и мозг пациента был нормальным при вскрытии без признаков инфекции. Из 3 пациентов, которым проводились исследования ЦНС до и после терапии плеконарилом, улучшение их состояния было продемонстрировано для всех (сканирование м-бисиката технеция-99 для 3 и МРТ для 1).
Шесть новорожденных с подавляющей энтеровирусной инфекцией получали лечение плеконарилом. Двое из младенцев, которые были близнецами (пациенты 57 и 58), получили лечение на 7-й день жизни (4-й день болезни).Оба полностью выздоровели. Двое других младенцев, также близнецов (пациенты 71 и 72; таблица 2), лечились на 4 и 5 дни болезни соответственно; они выздоровели с легкими последствиями. Двое других младенцев, не связанных родственниками, не получали лечения до 9-го дня болезни. Один из этих пациентов (пациент 16) выжил с остаточной задержкой в развитии от легкой до умеренной; другой пациент (пациент XX; этому пациенту не был присвоен номер) умер в возрасте 28 дней от стойкой сердечной недостаточности и респираторного дистресс-синдрома взрослого типа. У всех 5 выживших младенцев были доказательства лабораторного ответа, а у 4 пациентов (включая смертельный случай), для которых были проведены вирусологические исследования до- и постплеконарила, были отменены тесты с положительным посевом на энтеровирус до терапии на отрицательный посев после терапии.
У всех 5 выживших младенцев были доказательства лабораторного ответа, а у 4 пациентов (включая смертельный случай), для которых были проведены вирусологические исследования до- и постплеконарила, были отменены тесты с положительным посевом на энтеровирус до терапии на отрицательный посев после терапии.
Четыре пациента с миокардитом в возрасте от 3 месяцев до 42 лет лечились плеконарилом; 3 из 4 имели подтвержденную энтеровирусную инфекцию. У трех из 4 пациентов сердечная функция улучшилась после терапии (включая 1 пациента, у которого не удалось подтвердить энтеровирусную инфекцию).Двум пациентам были проведены вирусологические исследования до и после лечения плеконарилом; один (пациент 56) дал отрицательный результат на культуру и ПЦР после первоначального положительного теста на энтеровирусы обоими методами, тогда как второй (пациент 66) дал отрицательный результат на ПЦР после первоначального положительного результата.
Четыре пациента с пикорнавирусными инфекциями, связанными с BMT (3 из-за энтеровируса, 1 из-за риновируса), лечились плеконарилом. Пациенту 42, 15 лет с SCID из-за основного дефицита MHC класса II, который находился в ремиссии после предыдущего эпизода эховирусного энцефалита 16, профилактически давали плеконарил до, во время и после процедуры трансплантации для предотвращения осложнений, связанных с энтеровирусами. ; ни один не разработан.Поскольку в этом случае плеконарил вводили профилактически, этот пациент не был включен в анализ ответа. У двух других пациентов (пациенты 41 и 59) после ТКМ развилась симптоматическая вирусологически подтвержденная энтеровирусная инфекция. У обоих были клинические ответы (неврологическое улучшение и исчезновение диареи у одного и исчезновение плевральных и перикардиальных выпотов и сыпи в другом). Другой пациент (пациент 75), 15-месячный ребенок с лейкемией, после трансплантации заболел тяжелой риновирусной пневмонией, и его лечили плеконарилом; во время терапии у ребенка отмечалось заметное улучшение респираторного статуса, но он все еще нуждался в кислороде и имел рентгенологические аномалии грудной клетки.
Пациенту 42, 15 лет с SCID из-за основного дефицита MHC класса II, который находился в ремиссии после предыдущего эпизода эховирусного энцефалита 16, профилактически давали плеконарил до, во время и после процедуры трансплантации для предотвращения осложнений, связанных с энтеровирусами. ; ни один не разработан.Поскольку в этом случае плеконарил вводили профилактически, этот пациент не был включен в анализ ответа. У двух других пациентов (пациенты 41 и 59) после ТКМ развилась симптоматическая вирусологически подтвержденная энтеровирусная инфекция. У обоих были клинические ответы (неврологическое улучшение и исчезновение диареи у одного и исчезновение плевральных и перикардиальных выпотов и сыпи в другом). Другой пациент (пациент 75), 15-месячный ребенок с лейкемией, после трансплантации заболел тяжелой риновирусной пневмонией, и его лечили плеконарилом; во время терапии у ребенка отмечалось заметное улучшение респираторного статуса, но он все еще нуждался в кислороде и имел рентгенологические аномалии грудной клетки. Этот пациент включен в анализ из-за близкого родства риновирусов с энтеровирусами (оба являются представителями семейства Picornaviridae ) и известной чувствительности риновирусов к плеконарилу (см. Обсуждение).
Этот пациент включен в анализ из-за близкого родства риновирусов с энтеровирусами (оба являются представителями семейства Picornaviridae ) и известной чувствительности риновирусов к плеконарилу (см. Обсуждение).
У трех пациентов были острые полиовирусные инфекции, 2 из которых были вакциноассоциированными (у пациентов с ослабленным иммунитетом), а один — дикого типа (пациент 65, с Ближнего Востока). У двух из этих пациентов был клинический ответ (неврологическое улучшение у 2 пациентов и улучшение респираторного статуса и мышечной силы у 1 пациента).У одного пациента, у которого проводились вирусологические исследования до и после терапии спеконарилом, был получен отрицательный результат на полиовирус как при посеве ЦСЖ, так и в ЦСЖ-ПЦР после первоначального положительного результата обоих методов.
Наконец, несколько пациентов с различными заболеваниями, вызванными или предположительно вызванными энтеровирусами, получали лечение плеконарилом. У 76-летнего мужчины (пациент 34) с синдромом постполиомышечной атрофии улучшились показатели легочной функции после прохождения терапии. Энтеровирусная инфекция у этого человека не могла быть подтверждена, и впоследствии был подтвержден его диагноз — боковой амиотрофический склероз. Мы включаем его анализ в результаты из-за недавно сообщенной связи между боковым амиотрофическим склерозом и энтеровирусной инфекцией [16]. У 18-летнего ранее здорового пациента (пациент 67) с острым началом ПЦР-подтвержденного энтеровирусного поперечного миелита и энцефалита наблюдалось неврологическое и респираторное улучшение, временно связанное с терапией плеконарилом.Двое пациентов с энтеровирусным энцефалитом, подтвержденным культурой, получали лечение плеконарилом; один (пациент 68) клинически улучшился, а состояние другого (пациент 73) осталось неизменным во время и после терапии.
Энтеровирусная инфекция у этого человека не могла быть подтверждена, и впоследствии был подтвержден его диагноз — боковой амиотрофический склероз. Мы включаем его анализ в результаты из-за недавно сообщенной связи между боковым амиотрофическим склерозом и энтеровирусной инфекцией [16]. У 18-летнего ранее здорового пациента (пациент 67) с острым началом ПЦР-подтвержденного энтеровирусного поперечного миелита и энцефалита наблюдалось неврологическое и респираторное улучшение, временно связанное с терапией плеконарилом.Двое пациентов с энтеровирусным энцефалитом, подтвержденным культурой, получали лечение плеконарилом; один (пациент 68) клинически улучшился, а состояние другого (пациент 73) осталось неизменным во время и после терапии.
Данные о нежелательных явлениях были доступны для 32 из 38 пациентов. У 13 из 32 пациентов не было побочных эффектов. У остальных 19 пациентов было 56 нежелательных явлений: у 1 пациента было 5 нежелательных явлений, у 2 пациентов — по 6, а у 1 пациента — 9. Таким образом, среди 19 пациентов, на которые пришлось 56 нежелательных явлений, у 4 пациентов было 26 явлений, о которых сообщалось.
Таким образом, среди 19 пациентов, на которые пришлось 56 нежелательных явлений, у 4 пациентов было 26 явлений, о которых сообщалось.
Среди этих 32 пациентов было 8 смертей. Пациент 5 умер от случайного утопления через 1 год после терапии. Пациент 7 умер от криптоспоридиальной диареи через 7 месяцев после лечения плеконарилом. Пациент 12 умер от хронического заболевания легких через 1 неделю после терапии; у этого пациента была Х-сцепленная агаммаглобулинемия, диагностированная за 18 лет до терапии, о которой сообщалось ранее [21]. Пациент 17 умер от предполагаемого сепсиса из-за основного заболевания (ТКИД) через 4 месяца после терапии. Пациент 24 умер от аспергиллеза через 2 месяца после лечения.Пациент XX умер от прогрессирующей сердечной недостаточности и респираторного дистресс-синдрома взрослого человека через 2 недели после терапии плеконарилом. Пациент 34 умер от основного заболевания (боковой амиотрофический склероз) через 1 год после лечения. Пациент 59 умер на 6-е сутки терапии леконарилом легочного кровотечения, осложнившего острый миелолейкоз. Пациент 66 умер от кардита и диссеминированного внутрисосудистого свертывания крови через 21 день после лечения. Врачи 8 умерших пациентов не верили, что смерть была связана с терапией плеконарилом.
Пациент 66 умер от кардита и диссеминированного внутрисосудистого свертывания крови через 21 день после лечения. Врачи 8 умерших пациентов не верили, что смерть была связана с терапией плеконарилом.
Из оставшихся нежелательных явлений 7 были классифицированы как «тяжелые», 23 — как «умеренные» и 11 — как «легкие» по интенсивности. Восемь из нежелательных явлений, не связанных со смертью, были признаны серьезными, а остальные — несерьезными. Взаимосвязь нежелательных явлений, не связанных со смертельным исходом, и лечения была определена врачами пациентов следующим образом: не связанные ( n = 15), возможно связанные ( n = 23), вероятно связанные ( n = 7) , и определенно связанные ( n = 3).«Вероятно, связанные» побочные эффекты включали головную боль, боль в животе, утомляемость, анорексию, слабость, недержание мочи и обострение атаксии. «Определенно связанные» явления включали тошноту (2 пациента) и рвоту. Полный список побочных эффектов доступен по запросу.
Обсуждение
Энтеровирусы являются одной из наиболее частых причин острых вирусных заболеваний с широким спектром клинических проявлений [1]. Некоторые пациенты особенно восприимчивы к тяжелым, потенциально опасным для жизни энтеровирусным инфекциям.Осенью 1996 г. для этой группы пациентов из группы риска стал доступен специфический антипикорнавирусный агент — плеконарил. Предварительные результаты, представленные в этом отчете, позволяют предположить, что плеконарил оказывает положительное влияние на клинические, вирусологические, лабораторные и радиологические параметры.
Дети или взрослые с отсутствующим или недостаточным гуморальным иммунитетом демонстрируют важный «эксперимент природы» в отношении энтеровирусных инфекций ЦНС. В отличие от других вирусов, которые в значительной степени сдерживаются врожденным и родственным клеточным иммунитетом, энтеровирусы, по-видимому, выводятся из организма хозяина преимущественно с помощью механизмов, опосредованных антителами. Благодаря доступности внутривенных препаратов Ig и раннему распознаванию энтеровирусной инфекции, меньшее количество пациентов с гуморальным иммунодефицитом, по-видимому, прогрессируют до классического описания CEMA [6], и появились атипичные неврологические проявления [7]. Однако тот факт, что 17 пациентов с CEMA были включены в регистр лечения Pleconaril за 2,5-летний период этого исследования, демонстрирует, что энтеровирусное заболевание остается важным осложнением для этих пациентов.
Благодаря доступности внутривенных препаратов Ig и раннему распознаванию энтеровирусной инфекции, меньшее количество пациентов с гуморальным иммунодефицитом, по-видимому, прогрессируют до классического описания CEMA [6], и появились атипичные неврологические проявления [7]. Однако тот факт, что 17 пациентов с CEMA были включены в регистр лечения Pleconaril за 2,5-летний период этого исследования, демонстрирует, что энтеровирусное заболевание остается важным осложнением для этих пациентов.
Примерно у 50% этих инфицированных пациентов развивается ревматологический синдром, чаще всего с признаками, сходными с дерматомиозитом, который также считается прямым результатом энтеровирусной инфекции пораженных тканей [6].Лечение препаратами антител внутривенно, интратекально или внутрижелудочково привело к стабилизации состояния некоторых из этих пациентов; тем не менее, вирусная персистенция была документально подтверждена во время терапии [7], и очень немногие из этих пациентов пережили свои инфекции или осложнения. Среди 16 пациентов с CEMA-синдромом, получавших плеконарил, для которых были доступны последующие клинические данные, 12 (75%) продемонстрировали ответ, временно связанный с терапией. Ни у одного из 4 пациентов без клинического ответа не было подтверждено, что они инфицированы энтеровирусом; они составляли почти половину из 9 пациентов с синдромом CEMA, для которых подтверждение энтеровирусной инфекции было невозможным.Возможно, что некоторые или все эти пациенты были инфицированы другими патогенами, кроме энтеровирусов. В общей сложности 7 пациентов с синдромом CEMA, у которых была подтверждена энтеровирусная инфекция, продемонстрировали клинический ответ, как и 5 пациентов, у которых энтеровирусная инфекция не могла быть подтверждена.
Среди 16 пациентов с CEMA-синдромом, получавших плеконарил, для которых были доступны последующие клинические данные, 12 (75%) продемонстрировали ответ, временно связанный с терапией. Ни у одного из 4 пациентов без клинического ответа не было подтверждено, что они инфицированы энтеровирусом; они составляли почти половину из 9 пациентов с синдромом CEMA, для которых подтверждение энтеровирусной инфекции было невозможным.Возможно, что некоторые или все эти пациенты были инфицированы другими патогенами, кроме энтеровирусов. В общей сложности 7 пациентов с синдромом CEMA, у которых была подтверждена энтеровирусная инфекция, продемонстрировали клинический ответ, как и 5 пациентов, у которых энтеровирусная инфекция не могла быть подтверждена.
Столь же высокий процент пациентов, для которых были доступны вирусологические и лабораторные данные для последующего наблюдения, по-видимому, имели ответы в этих категориях. Хотя естественная история этого заболевания, без лечения или лечения только Ig, может включать периоды очевидного улучшения клинических, вирусологических и лабораторных параметров, частота ответа, наблюдаемая у наших пациентов, вероятно, превышает то, что можно было бы ожидать без плеконарила. Кроме того, некоторые пациенты в этом исследовании страдали неврологическими симптомами в течение многих месяцев или лет, после чего наблюдалось временное улучшение, связанное с лечением плеконарилом. Четыре пациента с CEMA умерли в течение периода наблюдения по причинам, не связанным с энтеровирусной инфекцией, что отражает тяжесть этих иммунодефицитных расстройств.
Кроме того, некоторые пациенты в этом исследовании страдали неврологическими симптомами в течение многих месяцев или лет, после чего наблюдалось временное улучшение, связанное с лечением плеконарилом. Четыре пациента с CEMA умерли в течение периода наблюдения по причинам, не связанным с энтеровирусной инфекцией, что отражает тяжесть этих иммунодефицитных расстройств.
У младенцев (в возрасте ≤ 6 месяцев), инфицированных энтеровирусами, обычно развиваются неспецифические лихорадочные заболевания, часто сопровождающиеся асептическим менингитом [5, 22]. Эти дети обычно выздоравливают без осложнений.Однако, когда у младенцев развивается энтеровирусная инфекция в течение первой недели жизни, часто наблюдается более тяжелое заболевание. Предполагается, что эти дети заражаются перинатально и, вероятно, получают более высокий вирусный инокулят, возможно, посредством трансплацентарной передачи через кровь [10–12]. Могут развиться серьезные системные проявления, такие как некроз печени, миокардит, энцефалит, пневмония, некротический энтероколит и диссеминированное внутрисосудистое свертывание крови, имитирующие подавляющую бактериальную инфекцию [10–12]. Смерть наступает обычно из-за печеночной недостаточности или миокардита. Среди 6 пациентов с подавляющей неонатальной энтеровирусной инфекцией в этом испытании плеконарила 5 выжили, включая всех 4, которые лечились в течение первой недели болезни. Последствия у выживших младенцев были в основном легкими. Число пролеченных пациентов в этом исследовании сострадательного использования слишком мало, чтобы определить, был ли результат значительно улучшен по сравнению с таковым для новорожденных, не получавших плеконарил.
Смерть наступает обычно из-за печеночной недостаточности или миокардита. Среди 6 пациентов с подавляющей неонатальной энтеровирусной инфекцией в этом испытании плеконарила 5 выжили, включая всех 4, которые лечились в течение первой недели болезни. Последствия у выживших младенцев были в основном легкими. Число пролеченных пациентов в этом исследовании сострадательного использования слишком мало, чтобы определить, был ли результат значительно улучшен по сравнению с таковым для новорожденных, не получавших плеконарил.
Энтеровирусы давно известны как важные причины острого миокардита. Истинная частота этого заболевания неизвестна, как и истинная частота энтеровирусной этиологии. Большинство случаев миокардита, вероятно, не диагностированы (неспецифически проявляются как вирусное заболевание без кардиологических исследований или, в другом крайнем случае, как внезапная смерть без вскрытия) или, в случае постановки диагноза, не имеют идентифицируемой причины. Энтеровирусы могут вызывать от 25% до 35% случаев миокардита, причина которого устанавливается на основании серологического исследования, гибридизации нуклеиновых кислот и исследований эндомиокардиальной биопсии и аутопсии на основе ПЦР [13]. Новорожденные и младенцы грудного возраста особенно восприимчивы к миокардиту, связанному с вирусом Коксаки B, который сопровождает системную инфекцию этих серотипов (см. Выше). Однако в большинстве случаев речь идет о молодых людях в возрасте 20–39 лет.
Новорожденные и младенцы грудного возраста особенно восприимчивы к миокардиту, связанному с вирусом Коксаки B, который сопровождает системную инфекцию этих серотипов (см. Выше). Однако в большинстве случаев речь идет о молодых людях в возрасте 20–39 лет.
В настоящем исследовании участвовали 4 пациента с миокардитом, у 3 из которых были клинические ответы с улучшением сердечной функции, временно связанное с терапией плеконарилом. Различная естественная история этого заболевания не позволяет сделать определенные выводы относительно эффективности плеконарила в случаях энтеровирусного миокардита до дальнейшего изучения пациентов.Действительно, состояние пациента 56 заметно улучшилось после приема 1 или 2 доз плеконарила, что может быть, а может и не быть биологически правдоподобным ожиданием терапии. Более того, лечению этого заболевания мешает постинфекционное аутоиммунное повреждение сердца, так что активная вирусная инфекция больше не может быть основным патогенетическим механизмом на момент постановки диагноза [13].
В заключение, это предварительное исследование убедительно свидетельствует о том, что плеконарил обладает как клинической, так и вирусологической эффективностью у пациентов с потенциально опасными для жизни энтеровирусными инфекциями.Давно признанный плохой прогноз, связанный с энтеровирусной инфекцией у пациентов с CEMA или подавляющей неонатальной инфекцией, резко контрастирует с 75% частотой клинического ответа, наблюдаемой у пациентов с CEMA, получавших плеконарил, и выживаемостью всех 4 новорожденных, получавших плеконарил в течение первая неделя болезни. Аналогичные многообещающие результаты, хотя и у небольшого числа пациентов, наблюдались в случаях миокардита, острого полиомиелита, энтеровирусных инфекций, осложняющих ТКМ, и других различных типов энтеровирусных инфекций.Плеконарил оказался безопасным и в целом хорошо переносимым препаратом.
Pleconaril был изучен в испытаниях с участием множества наиболее часто встречающихся пикорнавирусных инфекций здоровых хозяев, в том числе крупных испытаний препарата в случаях энтеровирусного менингита у взрослых [23] и детей [24], а также в случаях респираторных вирусных инфекций (прежде всего с риновирусы) у взрослых [25]. В этих исследованиях было обнаружено, что плеконарил обладает клиническими и вирусологическими преимуществами и имеет благоприятный профиль безопасности.
В этих исследованиях было обнаружено, что плеконарил обладает клиническими и вирусологическими преимуществами и имеет благоприятный профиль безопасности.
Из-за относительной редкости энтеровирусных инфекций типа, описанного в этой статье, будет сложно разработать плацебо-контролируемые испытания плеконарила в этих популяциях пациентов. Недавние крупные вспышки тяжелых инфекций энтеровируса 70 и энтеровируса 71 [26] дают дополнительную мотивацию для изучения плеконарила в случаях потенциально опасной для жизни энтеровирусной инфекции. Группа совместных антивирусных исследований Национального института здравоохранения недавно провела плацебо-контролируемое испытание плеконарила для лечения энтеровирусного сепсиса новорожденных (Dr.Дэвид Кимберлин, личное сообщение). Доступность плеконарила для сострадательного введения пациентам с потенциально опасными для жизни инфекциями должна побудить врачей, ухаживающих за такими пациентами, знать о возможной энтеровирусной этиологии этих заболеваний и рассмотреть возможность терапии плеконарилом на ранней стадии заболевания.
Группа регистрации лечения Плеконарилом
Членами группы являются: М. Абзуг, Э. Аддерсон, К. Альберти, К.Ансевин, Р. Аспалтер, К. Белани, Дж. Бернадини, М. Бьен, С. Бланш, Ф. Д. Буше, М. Каппелло, Дж. Карбоне, Х. Чапел, Дж. Чатавей, Б. Кри, Г. Дэвис, Э Доббинс, М. Элдер, Э. Фернандес-Крус, С. Фаулер, Дж. Герн, Х. Гонсалес, Г. Готтесман, Д. Гротиус, Т. Гунгор, Э. Харон, К. Хартман, С. Хассин-Бэр , S. Hedderwick, B. Herold, A. Huisoon, A. Jain, A. Jones, A. Johnston, C. Kennedy, T. Keyes, D. King, S. Kurachek, T. Kyriakides, J. Levy, M Меллон, Д. Меллор, Р. Мудгал, Б. О’Киф, Т. Обермиллер, С.Боггс, М. Олеастро, Т. Паркер, Р. Поусон, Дж. Пететт, М. Поттер, Х. Прентис, Ф. Раффи, Дж. Рахал, П. Ранкин, Дж. Ромеро, С. Росс, Л. Сандерс, F. Schmalsteig, R. Seger, B. Sullivan, J. Tarafder, E. Thilo, A. Thompson, R. Turner, G. Waring, L. Williams и J. Zaia.
Список литературы
1.,.
Энтеровирусы: вирусы Коксаки, эховирусы и полиовирусы
,
Учебник детских инфекционных болезней
,
1998
4-е изд.
Филадельфия
WB Saunders
(стр.
1787
—
838
) 2,,.
Временные и географические особенности изолятов неполиомиелитного энтеровируса в США, 1970–1983 гг.
,
J Infect Dis
,
1986
, vol.
153
(стр.
346
—
51
) 3« и др.
Энтеровирусный менингит у взрослых
,
Clin Infect Dis
,
1998
, vol.
27
(стр.
896
—
8
) 4« и др.
Клинико-экономическое значение неполиомиелитных энтеровирусных заболеваний в частной педиатрической практике
,
Педиатрия
,
1998
, т.
102
(стр.
1126
—
34
) 5« и др.
Клиническое значение энтеровирусов при тяжелых летних лихорадочных заболеваниях у детей
,
Pediatr Infect Dis J
,
1999
, vol.
18
(стр.
869
—
74
) 6,,.
Хронический энтеровирусный менингоэнцефалит у пациентов с агаммаглобулинемией
,
Rev Infect Dis
,
1987
, vol.
9
(стр.
334
—
56
) 7,,, et al.
Диагностика энтеровирусной болезни мозга у пациентов с гипогаммаглобулинемией методом полимеразной цепной реакции
,
Clin lnfect Dis
,
1993
, vol.
17
(стр.
657
—
61
) 8,,,.
Диссеминированная инфекция Коксаки A9, осложняющая трансплантацию костного мозга
,
Pediatr Infect Dis J
,
1996
, vol.
15
(стр.
1053
—
4
) 9,,,,.
Длительная энтеровирусная инфекция у пациента, у которого после трансплантации костного мозга развился перикардит и сердечная недостаточность
,
Clin Infect Dis
,
1996
, vol.
22
(стр.
1004
—
8
) 10,,.
Профиль энтеровирусного заболевания в первые две недели жизни
,
Pediatr Infect Dis J
,
1993
, vol.
12
(стр.
820
—
4
) 11« и др.
Инфекции, вызванные вирусом Коксаки группы B, у детей младше трех месяцев: серьезное детское заболевание
,
Rev Infect Dis
,
1983
, vol.
5
(стр.
1019
—
32
) 12.
Перинатальная эховирусная инфекция: выводы из обзора литературы, посвященного 61 случаю серьезной инфекции и 16 вспышкам в питомниках
,
Rev Infect Dis
,
1986
, vol.
8
(стр.
918
—
26
) 13,,,. .
Энтеровирусный миокардит и дилатационная кардиомиопатия: обзор клинических и экспериментальных исследований
,
Энтеровирусные инфекции человека
,
1995
Вашингтон, округ Колумбия
Американское общество микробиологии Press
14..
Менингит и энцефалит
,
Энтеровирусные инфекции человека
,
1995
Вашингтон, округ Колумбия
Американское общество микробиологии Press
(стр.
271
—
89
) 15,,, et al.
Заболевания, имитирующие энцефалит простого герпеса
,
JAMA
,
1989
, vol.
262
(стр.
234
—
9
) 16« и др.
Выявление и клеточная локализация последовательностей РНК энтеровирусов в спинном мозге пациентов с БАС
,
Neurology
,
2000
, vol.
54
(стр.
20
—
5
) 17,,.
Трехмерная структура полиовируса с разрешением 2,9 A
,
Science
,
1985
, vol.
229
(стр.
1358
—
65
) 18,,.
Лечение энтеровирусных инфекций человека
,
Antivir Res
,
1998
, vol.
38
(стр.
1
—
14
) 19.
Противовирусная терапия пикорнавирусных инфекций: плеконарил
,
Программа и выдержки из 15-го ежегодного симпозиума по клинической вирусологии (Клируотер, Флорида)
,
1999
Тампа, Флорида
University of South Florida Press
20.,,.
Энтеровирусы
,
Руководство по клинической микробиологии
,
1999
7-е изд.
Вашингтон, округ Колумбия
Американское общество микробиологии Press
(стр.
990
—
8
) 21« et al.
Стойкие и смертельные эховирусные инфекции центральной нервной системы у пациентов с агаммаглобулинемией
,
N Engl J Med
,
1977
, vol.
296
(стр.
1485
—
9
) 22.
Неполиомиелитные энтеровирусы и младенцы с лихорадкой: эпидемиологические, клинические и диагностические аспекты
,
Pediatr Infect Dis J
,
1996
, vol.
15
(стр.
67
—
71
) 23« и др.
Плеконарил эффективен при энтеровирусном менингите у подростков и взрослых: рандомизированное плацебо-контролируемое многоцентровое исследование
,
Программа и выдержки из 39-й Международной конференции по антимикробным препаратам и химиотерапии
,
1999
Вашингтон, округ Колумбия
Американское общество микробиологии
24« и др.
Пероральный плеконарил снижает продолжительность и тяжесть энтеровирусного менингита у детей
,
Программа и выдержки из Ежегодного собрания педиатрических академических обществ 1999 г.
,
1999
Вашингтон, округ Колумбия
Педиатрические исследования
25,,, et al.
Лечение Плеконарилом сокращает продолжительность респираторного заболевания пикорнавирусом у взрослых
,
Программа и выдержки из 39-й Международной конференции по антимикробным препаратам и химиотерапии
,
1999
Вашингтон, округ Колумбия
Американское общество микробиологии
26,,, et al.
Эпидемия энтеровирусной 71 инфекции на Тайване
,
N Engl J Med
,
1999
, vol.
341
(стр.
929
—
35
)
Рисунки и таблицы
Таблица 2
Таблица 2
Заметки автора
© 2001 Американское общество инфекционных болезней
Клиническая характеристика тяжелой неонатальной энтеровирусной инфекции: систематический обзор | BMC Pediatrics
В результате поиска в базе данных было выявлено 1647 исследований, и 243 из них были сохранены после просмотра названий и аннотаций.Впоследствии 177 исследований были исключены из полнотекстового обзора. Наконец, в анализ были включены 66 статей с 237 случаями тяжелой неонатальной энтеровирусной инфекции. На рисунке 1 показана блок-схема процесса выбора исследования. Таблицы s1, s2 и s3 в дополнительном материале показывают общие характеристики включенных новорожденных и оценку риска предвзятости. Клиническая характеристика новорожденных с тяжелой энтеровирусной инфекцией по основным осложнениям представлена в таблице 1.
Клиническая характеристика новорожденных с тяжелой энтеровирусной инфекцией по основным осложнениям представлена в таблице 1.
Рис. 1
Схема последовательности отбора исследований
Таблица 1 Клинические особенности новорожденных с тяжелыми энтеровирусными инфекциями (%)
В целом у 237 новорожденных развились тяжелые осложнения энтеровирусной инфекции, при соотношении мужчин и женщин 116/88 , а вес при рождении от 1730 до 4500 г. Всего с помощью кесарева сечения родилось 51,3% (101/197) недоношенных детей и 52,5% (95/181) новорожденных. В 70,5% (167 случаев) случаев возраст появления симптомов был менее 7 дней.Семьдесят случаев (29,5%) были связаны с материнскими заболеваниями до родов, в то время как в 16 случаях (6,8%) зарегистрированы родные братья и сестры или друзья с симптомами. Посев околоплодных вод матери выявил дефицитные Staphylococcus epidermidis при миокардите [7]. Также у матери диагностирован хориоамнионит [8], а у другой матери заподозрено амнионит [9]. Энтеровирус был идентифицирован в основном из ректальных образцов или стула (118, 49,8%), а затем из респираторных образцов (101, 42,6%). Кроме того, 82.7% (124 случая) новорожденных были инфицированы вирусом Коксаки B (CVB), 16,7% (25 случаев) имели инфекцию эховирусом и 0,7% (1 случай) имели инфекцию энтеровируса 71 (EV71). Клинические проявления включали отклонения температуры (127, 53,6%), сыпь (88, 37,1%), плохое питание (58, 24,5%), респираторные симптомы (45, 19,0%), летаргию (40, 16,9%), желтуху (38). , 16,0%), недостаточность кровообращения или шок (37, 15,6%), аритмии (29, 12,2%), тромбоцитопения (28, 11,8%), плохая перфузия (23, 9,7%), раздражительность (17, 7.2%), гипотония (9, 3,8%) и диарея (9, 3,8%). В общей сложности 127 (53,6%) новорожденных получали эмпирические антибиотики, а 97 (40,9%) новорожденных — внутривенный иммуноглобулин (ВВИГ). Противовирусные препараты включали покапавир (3, 1,3%) и плеконарил (14, 5,9%). Всего летальность составила 30,4% (72 случая).
Энтеровирус был идентифицирован в основном из ректальных образцов или стула (118, 49,8%), а затем из респираторных образцов (101, 42,6%). Кроме того, 82.7% (124 случая) новорожденных были инфицированы вирусом Коксаки B (CVB), 16,7% (25 случаев) имели инфекцию эховирусом и 0,7% (1 случай) имели инфекцию энтеровируса 71 (EV71). Клинические проявления включали отклонения температуры (127, 53,6%), сыпь (88, 37,1%), плохое питание (58, 24,5%), респираторные симптомы (45, 19,0%), летаргию (40, 16,9%), желтуху (38). , 16,0%), недостаточность кровообращения или шок (37, 15,6%), аритмии (29, 12,2%), тромбоцитопения (28, 11,8%), плохая перфузия (23, 9,7%), раздражительность (17, 7.2%), гипотония (9, 3,8%) и диарея (9, 3,8%). В общей сложности 127 (53,6%) новорожденных получали эмпирические антибиотики, а 97 (40,9%) новорожденных — внутривенный иммуноглобулин (ВВИГ). Противовирусные препараты включали покапавир (3, 1,3%) и плеконарил (14, 5,9%). Всего летальность составила 30,4% (72 случая).
Всего было включено 109 случаев гепатита или коагулопатии из 17 исследований [9,10,11,12,13,14,15,16,17,18,19,20,21,22,23,24] ( 57 мальчиков, 46 девочек). Заболевания матери в период от 2 месяцев до родов до 1 недели после родов зарегистрированы в 33 случаях (30.3%), в том числе лихорадка у 23, боль в животе у шести, гриппоподобный синдром у пяти и диарея в четырех случаях. В трех случаях у братьев и сестер были симптомы лихорадочного заболевания и боли в горле за несколько дней до родов. У новорожденных первые симптомы появились в период между днем рождения и 1 месяцем; 98 (89,9%) обратились в течение 7 дней после рождения. Было извлечено 87 записей серотипов энтеровирусов, включая 16 случаев эховирусной инфекции (эховирус 3 в одном, эховирус 21 в одном, эховирус 11 в четырех, эховирус 30 в двух, эховирус 7 в двух, эховирус 6 в двух, эховирус 5 в один) и 71 случай CVB (CVB1 в 22, CVB2 в одном, CVB3 в 46, CVB4 в одном, CVB5 в одном).Наиболее частым симптомом были температурные аномалии: 60 случаев нестабильности температуры, 17 случаев лихорадки и 5 случаев переохлаждения. Другими симптомами были сыпь (73, 67,0%), желтуха (32, 29,4%) и асцит (27, 24,8%). Осложнения, связанные с гепатитом, составили 23 случая миокардита, один случай гипертрофической кардиомиопатии, пять случаев внутричерепного кровоизлияния, пять случаев энцефалита, восемь случаев диссеминированного внутрисосудистого свертывания крови (ДВС-синдром), три случая почечной недостаточности и три случая пневмонита.Повышение уровня аспартатаминотрансферазы (AST) или аланинтрансаминазы (ALT) было зарегистрировано в 85 случаях. В общей сложности 95 (87,2%) новорожденных получали лечение антибиотиками, а 56 (51,4%) получали лечение ВВИГ. Использовались противовирусные препараты: покапавир (1, 0,9%) и плеконарил (9, 8,3%). Более того, 94 (86,2%) новорожденных потребовалось переливание компонентов крови, таких как свежезамороженная плазма, тромбоциты и концентрат эритроцитов. Другое систематическое поддерживающее лечение включало механическую вентиляцию легких (17, 15.6%), перитонеальный диализ (4, 3,7%), гемодиализ (1, 0,9%), обменное переливание крови (4, 3,7%) и непрерывная веновенозная гемофильтрация (1, 0,9%). Трем (2,8%) новорожденным была проведена трансплантация печени. Двадцать девять из 109 (26,6%) новорожденных умерли в возрасте от 8 дней до 2 месяцев.
Заболевания матери в период от 2 месяцев до родов до 1 недели после родов зарегистрированы в 33 случаях (30.3%), в том числе лихорадка у 23, боль в животе у шести, гриппоподобный синдром у пяти и диарея в четырех случаях. В трех случаях у братьев и сестер были симптомы лихорадочного заболевания и боли в горле за несколько дней до родов. У новорожденных первые симптомы появились в период между днем рождения и 1 месяцем; 98 (89,9%) обратились в течение 7 дней после рождения. Было извлечено 87 записей серотипов энтеровирусов, включая 16 случаев эховирусной инфекции (эховирус 3 в одном, эховирус 21 в одном, эховирус 11 в четырех, эховирус 30 в двух, эховирус 7 в двух, эховирус 6 в двух, эховирус 5 в один) и 71 случай CVB (CVB1 в 22, CVB2 в одном, CVB3 в 46, CVB4 в одном, CVB5 в одном).Наиболее частым симптомом были температурные аномалии: 60 случаев нестабильности температуры, 17 случаев лихорадки и 5 случаев переохлаждения. Другими симптомами были сыпь (73, 67,0%), желтуха (32, 29,4%) и асцит (27, 24,8%). Осложнения, связанные с гепатитом, составили 23 случая миокардита, один случай гипертрофической кардиомиопатии, пять случаев внутричерепного кровоизлияния, пять случаев энцефалита, восемь случаев диссеминированного внутрисосудистого свертывания крови (ДВС-синдром), три случая почечной недостаточности и три случая пневмонита.Повышение уровня аспартатаминотрансферазы (AST) или аланинтрансаминазы (ALT) было зарегистрировано в 85 случаях. В общей сложности 95 (87,2%) новорожденных получали лечение антибиотиками, а 56 (51,4%) получали лечение ВВИГ. Использовались противовирусные препараты: покапавир (1, 0,9%) и плеконарил (9, 8,3%). Более того, 94 (86,2%) новорожденных потребовалось переливание компонентов крови, таких как свежезамороженная плазма, тромбоциты и концентрат эритроцитов. Другое систематическое поддерживающее лечение включало механическую вентиляцию легких (17, 15.6%), перитонеальный диализ (4, 3,7%), гемодиализ (1, 0,9%), обменное переливание крови (4, 3,7%) и непрерывная веновенозная гемофильтрация (1, 0,9%). Трем (2,8%) новорожденным была проведена трансплантация печени. Двадцать девять из 109 (26,6%) новорожденных умерли в возрасте от 8 дней до 2 месяцев.
Всего 88 новорожденных в 31 исследовании [7, 9, 25,26,27,28,29,30,31,32,33,34,35,36,37,38,39,40,41,42 , 43,44,45,46,47,48,49,50,51,52,53] развилось основное осложнение миокардита с соотношением мужчин и женщин 42/29.В целом 54,7% (35/64) новорожденных были младше 7 дней на момент появления симптомов. У 20 новорожденных в анамнезе были материнские заболевания до родов, а в восьми случаях сообщалось о братьях, сестрах или друзьях с симптомами. У 39 новорожденных была инфекция CVB (CVB1 у 13, CVB2 у 2, CVB3 у 13, CVB4 у 5, CVB5 у 3 и CVB2 у 1). У одного новорожденного была инфекция, вызванная эховирусом 6. Клинические признаки температурных аномалий (восемь новорожденных с гипотермией, 15 с лихорадкой и один с температурной нестабильностью) наблюдались у 24 новорожденных.Признаки миокардита включали респираторные симптомы (24, 27,3%), аритмии (27, 30,7%), недостаточность кровообращения или шок (35, 39,8%) и плохую перфузию (11, 12,5%). Сообщалось, что миокардит сопровождался другими осложнениями, включая менингоэнцефалит (10 случаев), почечную недостаточность (3 случая), ДВС-синдром (6 случаев) и гепатит (7 случаев). Повышение уровня тропонина и натрийуретического пептида головного мозга (BNP) наблюдалось в 30 и 20 случаях соответственно. Другими первичными дополнительными обследованиями были электрокардиограмма (ЭКГ) для выявления признаков ишемии миокарда (30, 34.1%) и эхокардиография для признаков дилатации желудочков или угнетения функции (56, 63,6%). Механическая вентиляция была использована у 27 новорожденных, а сердечно-легочная реанимация потребовалась у пяти новорожденных. Кроме того, 43 новорожденных получили поддержку экстракорпоральной мембранной оксигенации (ЭКМО). Лекарства включали антибиотики (16, 18,2%), ВВИГ (31, 35,2%), покапавир (2, 2,3%) и плеконарил (5, 5,7%). Более того, четверо новорожденных выжили после трансплантации сердца и одному произведена замена митрального клапана.Летальность среди новорожденных с миокардитом составила 38,6% (34/88), а у 40,7% (22/54) выживших были осложнения или потребовалось сердечное лечение.
У 26 случаев в 10 исследованиях [8, 54,55,56,57,58,59,60,61,62] был диагностирован менингоэнцефалит с соотношением мужчин и женщин 11/10. Проявления менингоэнцефалита у матери и других членов семьи выявлены в пяти и трех случаях соответственно. Серотипы энтеровирусов включали четыре случая эховируса (эховирус 6 в одном, эховирус 30 в двух, эховирус 31 в одном), семь случаев CVB (CVB1 в четырех, CVB2 в двух, CVB3 в одном) и один случай EV71.Признаки поражения центральной нервной системы: судороги (10, 38,5%), летаргия (5, 19,2%), раздражительность (9, 34,6%), тонико-клонические движения верхних конечностей (1, 3,8%), правосторонний гемипарез. (1, 3,8%), слабый рвотный рефлекс (1, 3,8%) и полный родничок (1, 3,8%). Осложнения центрального несахарного диабета возникли у одного новорожденного. Повреждение белого вещества было обнаружено с помощью магнитно-резонансной томографии (МРТ) в 21 случае, в то время как в 16 случаях при УЗИ головного мозга наблюдалась обширная перивентрикулярная эхогенность.Четырем новорожденным была проведена искусственная вентиляция легких, а двоим — ВВИГ. В общей сложности 23 из 26 новорожденных выжили, а неврологические осложнения были зарегистрированы у шести.
Другие редкие осложнения показаны в таблице 2, включая гемофагоцитарный лимфогистиоцитоз (HLH) [63,64,65,66], легочное кровотечение [67], легочную гипоплазию [68], стойкую легочную гипертензию [69], недостаточность костного мозга [ 70] и врожденные поражения кожи [71]. Из шести новорожденных с HLH у четырех перед родами развились лихорадка, боли в животе и симптомы гриппа.У всех новорожденных заболевание развилось в течение 5 дней. Пятерым новорожденным была введена ВВИГ. В конце концов, один новорожденный умер, а другому сделали пересадку печени в возрасте 2 месяцев. В четырех случаях, состоящих из двух пар близнецов с легочным кровотечением, у обеих матерей в день родов развились лихорадка и другие симптомы. Первоначальный возраст двух пар близнецов составлял 7 и 5 дней соответственно. Только один новорожденный выжил с легкой болезнью. Отмечен единичный случай гипоплазии легких с полным нарушением развития терминальных отделов дыхания.Эховирус 11 был положительным в околоплодных водах. Новорожденный был доставлен на срок 38 недель и умер через час. Другой случай связан с внутриутробным инфицированием эховирусом 11 со стойкой легочной гипертензией и пневмонией. Новорожденный умер через 36 часов после рождения. Также был случай недостаточности костного мозга и сопутствующей энтеровирусной инфекции. При аспирации костного мозга и биопсии обнаружена гипоцеллюлярность. Новорожденный наконец поправился. Также сообщалось о мальчике с врожденной диссеминированной папуловезикулярной, узловатой, буллезной и некротической язвенной сыпью.Впоследствии у него развилась пневмония, кардит и гепатит. CVB3 был идентифицирован в сыворотке новорожденного. Мальчик выжил с осложнениями в возрасте 6 месяцев.
Таблица 2 Клинические особенности новорожденных тяжелых энтеровирусных инфекций с редкими осложнениями (%)
Frontiers | Долгосрочные результаты детской энтеровирусной инфекции на Тайване: популяционное когортное исследование
Введение
В последние десятилетия основное бремя болезней у детей и подростков сместилось с инфекционных болезней на хронические состояния здоровья (1, 2).Хотя уровень инфекционных заболеваний снизился, похоже, что хронические заболевания, вызванные инфекционными агентами, растут. Инфекции могут быть просто первым ошибочным шагом на пути от здоровья к длительной инвалидности и болезням (3).
Энтеровирусы являются одними из самых распространенных инфекционных патогенов у младенцев и детей. Они связаны с различными клиническими проявлениями от легкого до тяжелого заболевания, включая неспецифическое лихорадочное заболевание, слизисто-кожные проявления (герпангина, болезнь рук и ног, конъюнктивит и различные экзантемы), поражение ЦНС (асептический менингит, энцефалит, полиомиелит и др.) Синдром Гийена-Барре и др.), сердечная инфекция (миоперикардит), неонатальная инфекция и недавно выявленный клинический синдром (обострение астмы, вторичное по отношению к EV D68 и экземе Coxsackium) (4, 5). Энтеровирус 71 (EV71) вызывает ряд крупных эпидемий заболеваний рук, ног и рта у детей и в редких случаях может привести к серьезному осложнению, известному как неврологическое заболевание EV71 (6). Самая крупная и самая серьезная вспышка EV71 на Тайване произошла в 1998 г. (7). Смертность от энтеровирусной инфекции снизилась после введения в 2000 г. национальной программы поэтапного лечения (8).Однако долгосрочные последствия, особенно развитие нервной системы и когнитивные функции, остаются серьезной проблемой при лечении этого заболевания. Помимо неврологических последствий, энтеровирусная инфекция, как было показано, имеет другие долгосрочные последствия, приводящие к общим проблемам со здоровьем, таким как аллергические заболевания, аутоиммунные заболевания и заболевания, затрагивающие другие системы, и по этой причине энтеровирусная инфекция стала серьезной проблемой общественного здравоохранения в дети (5, 9).
В этом исследовании изучалась взаимосвязь между энтеровирусной инфекцией и общими проблемами со здоровьем у детей с популяционной точки зрения (10).
Метод
Источник данных
База данных долгосрочного медицинского страхования (LHID) — это поднабор данных Национальной базы данных исследований в области медицинского страхования (NHIRD), в которой хранятся данные анонимных заявлений из программы Тайваньского национального медицинского страхования (NHI). LHID 2000 содержит все продольные данные о претензиях 1 000 000 человек, выбранных случайным образом из регистрационных данных бенефициаров программы NHI за период 1996–2000 годов.
Данные о расходах на амбулаторную помощь по файлам посещений (CD) и стационарных расходах по файлам госпитализации (DD) были основным источником данных, использованных в анализе.База данных LHID 2000, использованная в этом исследовании, предоставила медицинскую информацию об этих 1 000 000 бенефициаров NHI до конца 2013 года.
Состав исследования и дизайн исследования
Блок-схема дизайна исследования и выбора субъектов исследования показана на рисунке 1. Поскольку количество случаев заражения ЭМ резко возросло из-за эндемической вспышки в 1998 г. на Тайване, мы решили проводить исследования с 1999 г. для более четкого определения статуса заболевания. Это исследование данных о претензиях. Основа диагностики — кодировка врачей.Международная классификация болезней, 9-й пересмотр, клиническая модификация (МКБ-9-CM) использовалась NHI Тайваня в течение периода исследования. Симптоматическая энтеровирусная инфекция (герпангина, кистозно-ягодичная инфекция, энтеровирусная инфекция с заболеваниями ЦНС) определялась как пациенты с кодами ICD-9-CM 047, 048, 049 или 074. За период 1999–2003 гг. Энтеровирусом было 49 236 пациентов. (EV) инфекции (ICD-9-CM 047-049, 074) были идентифицированы из LHID2000. Были отобраны дети в возрасте до 18 лет. Лица, у которых до диагностики энтеровируса были диагностированы дефицит внимания и гиперактивное расстройство (СДВГ), эпилепсия, атопические заболевания, ишемическая болезнь сердца (ИБС), инсульт, ревматоидный артрит (РА) или системная красная волчанка (СКВ).Также были исключены субъекты, у которых отсутствовали данные, касающиеся занятий родителей и урбанизации. Наконец, в исследование были включены в общей сложности 14 168 субъектов. Инфекция EV была далее классифицирована в соответствии с уровнем тяжести на основании поступления в больницу с диагнозом инфекции EV. Субъекты, которые не были госпитализированы по поводу инфекции EV, были классифицированы как пациенты с нетяжелой инфекцией EV. Субъекты, которые были госпитализированы с инфекцией EV, были классифицированы как пациенты с тяжелой инфекцией EV. Контрольную группу составили лица, у которых не была диагностирована инфекция ЭВ в течение 1999–2003 гг., В соотношении 1: 1 по возрасту и полу.Последующее наблюдение было прекращено в каждой когорте, когда: участники исследования вышли из программы NHI, имел место серьезный исход, такой как СДВГ, эпилепсия, астма, аллергический ринит или атопический дерматит, или был достигнут срок до 31 декабря 2013 г., поскольку это было конец учебного периода.
Рисунок 1 . Блок-схема дизайна исследования и отбора исследуемой популяции.
Наблюдалось пять основных результатов. События определялись по CD и DD кодами ICD-9-CM. РА и СКВ определялись по EV.Основные исходы были следующими: СДВГ (ICD-9-CM 314), эпилепсия (ICD-9-CM 345), астма (ICD-9-CM 493), аллергический ринит (ICD-9-CM 477) и атопический дерматит. (МКБ-9-СМ 691). Демографические переменные, включая возраст, пол, род занятий родителей и урбанизацию, были собраны в качестве контрольных переменных. Родительские занятия классифицировались как «белые воротнички» для тех, кто большую часть времени работает в помещении, «« синие воротнички »- для тех, кто большую часть времени работает на открытом воздухе или связан с промышленным трудом, и« прочие », в том числе пенсионеры и те, кто не работает.Урбанизация была разделена на четыре уровня: уровень 1 был определен как высшая степень урбанизации, а уровень 4 — как самый низкий (11).
Протокол исследования был одобрен институциональным наблюдательным советом больницы общего профиля для ветеранов Тайчжун (IRB TCVGH No. CE17178A-2).
Статистический анализ
SAS 9.4 (SAS Institute Inc. Кэри, Северная Каролина, США) использовался для поиска и анализа данных. Описательный статистический анализ EV и контрольной группы, среднего и стандартного отклонения был проведен для описания непрерывных переменных, таких как возраст, количество и процентное соотношение, которые использовались для описания категориальных переменных, таких как пол, место проживания и род занятий. .Сравнивались различия в распределении переменных между EV и контрольной группой. T -тест использовался для сравнения непрерывных переменных. Для сравнения категориальных переменных использовался критерий хи-квадрат. Заболеваемость каждым заболеванием рассчитывалась с использованием плотности заболеваемости. Для оценки риска основных исходов после инфицирования ЭВ использовались метод Каплана-Мейера и тест Log-Rank для анализа выживаемости. Для контроля вмешивающихся факторов использовались регрессионные модели Кокса.
Результаты
Исследуемая популяция состояла из 14 168 детей с диагнозом EV-инфекция и 14 168 детей без EV-инфекции. В таблице 1 представлены характеристики когорты и контрольной группы. Средний возраст составил 3,6 ( SD : 2,9) года в группе EV и 3,8 ( SD : 3,0) года в контрольной группе. Был значительно более высокий процент родителей, которые были « белыми воротничками » в когорте EV, по сравнению с контрольной группой (когорта vs.контроль: 64,3 против 59,1%, p <0,0001).
Таблица 1 . Демографические характеристики исследуемой популяции.
Таблица 2 показывает частоту возникновения и отношение рисков (ЧСС) 5 основных событий в когортной группе ЭМ и контрольной группе. Заболеваемость СДВГ составила 28,0 на 10 000 человеко-лет в группе ЭВ и 21,3 на 10 000 человеко-лет в контрольной группе. После поправки на возраст, пол, род занятий отца и уровень урбанизации проживания когортная группа EV имела 1.В 25 раз больший риск СДВГ по сравнению с контрольной группой (HR = 1,25, 95% CI-1,11–1,41). Заболеваемость эпилепсией составила 13,7 на 10 000 человеко-лет и 10,7 на 10 000 человеко-лет в когорте ЭВ и контрольной группе, соответственно. После поправки на смешивающие факторы риск эпилепсии в группе ЭВ был в 1,25 раза выше, чем в контрольной группе. В этом исследовании были проанализированы три основных аллергических заболевания: астма, аллергический ринит и атопический дерматит. Заболеваемость астмой составляла 150 на 10 000 человеко-лет в группе ЭВ и 93.0/10 000 человеко-лет в контрольной группе. Риск астмы был выше в когортной группе EV после поправки на вмешивающиеся факторы (HR = 1,49, 95% CI = 1,41–1,58). Заболеваемость аллергическим ринитом в группе ЭВ была в 1,37 раза выше, чем в контрольной группе (уровень заболеваемости = 462 на 10 000 человеко-лет против 316 на 10 000 человеко-лет, соответственно). После поправки на сопутствующие факторы риск аллергического ринита в группе ЭВ был в 1,37 раза выше (ОР = 1,37, 95% ДИ = 1.33–1,42). Заболеваемость атопическим дерматитом составила 45,6 и 39,3 на 10 000 человеко-лет соответственно. Однако после поправки на факторы, влияющие на факторы, не было значительной разницы в риске атопического дерматита между двумя группами (ОР = 1,09, 95% ДИ = 0,99–1,19). Сравнивались совокупные риски пяти основных событий в когортной группе ЭМ и контрольной группе (рисунки 2, 3).
Таблица 2 . Частота встречаемости и отношение рисков (HR) 5 основных событий в когорте ЭВ и контрольной группе.
Рисунок 2 . Совокупный риск аллергических заболеваний у детей с инфекцией ЭМ или без нее. (A) астма, (B) аллергический ринит, (C) атопический дерматит.
Рисунок 3 . Кумулятивный риск осложнений со стороны ЦНС для детей с инфекцией ЭВ или без нее. (A) ADHD, (B) Эпилепсия.
Сравнение рисков пяти основных событий у пациентов с тяжелой или нетяжелой инфекцией ЭВ было продемонстрировано в таблице 3.Что касается неврологических заболеваний, частота и риск СДВГ между пациентами с тяжелым и нетяжелым EV не различались (частота = 34,2 против 27,4 / 10 000 человеко-лет, соответственно) (HR = 1,12, 95% ДИ = 0,84–1,47). Заболеваемость эпилепсией составила 29,5 на 10 000 человеко-лет у пациентов с тяжелой инфекцией ЭВ и 12,1 на 10 000 человеко-лет у пациентов с нетяжелой инфекцией ЭВ. После поправки на возраст, пол, род занятий отца и урбанизацию проживания, по сравнению с пациентами с нетяжелой ЭВ, пациенты с тяжелой формой ЭВ имели 2.В 36 раз выше риск эпилепсии (ОР = 2,36, 95% ДИ = 1,62–3,24). При сравнении риска аллергических заболеваний между двумя группами не было различий в риске атопического дерматита (HR = 1,10, 95% CI = 0,88–1,38), но был более высокий риск астмы (HR = 1,33, 95% CI). = 1,18–1,50) и аллергического ринита (ОР = 1,17, 95% ДИ = 1,08–1,28) у пациентов с тяжелой инфекцией ЭВ. Совокупные риски пяти основных событий сравнивались между группами тяжелой ЭВ и нетяжелой инфекции (рисунки 4, 5).
Таблица 3 . Риск пяти основных событий для детей с тяжелой инфекцией ЭВ или без нее *.
Рисунок 4 . Кумулятивный риск аллергических заболеваний у детей с тяжелой и нетяжелой инфекцией ЭВ. (A) астма, (B) аллергический ринит, (C) атопический дерматит.
Рисунок 5 . Кумулятивный риск осложнений со стороны ЦНС для детей с тяжелой и нетяжелой инфекцией ЭВ. (A) ADHD, (B) Эпилепсия.
Обсуждение
Основное бремя состояний общественного здоровья, связанное с младенцами, детьми и подростками, резко изменилось за последние десятилетия (1, 2, 10). Последствия серьезных детских инфекционных заболеваний постепенно уменьшаются; однако частота хронических заболеваний неуклонно растет. Считается, что причины этих изменений связаны с улучшением питания и санитарии, реализацией программ иммунизации детей для предотвращения тяжелых патогенов, достижениями медицины как в лечении первичных заболеваний, так и в борьбе с серьезными осложнениями, а также с большей осведомленностью населения о хронических состояниях здоровья (1).В значительной степени рост хронических состояний здоровья можно объяснить четырьмя распространенными заболеваниями, а именно астмой, ожирением, расстройствами психического здоровья и нарушениями развития нервной системы. Растет понимание того, что некоторые хронические заболевания возникают в результате инфекционных заболеваний. Последние достижения в диагностических методах позволили исследователям доказать причинную связь между различными инфекционными агентами и хроническими заболеваниями (3).
Согласно долгосрочным данным, собранным Тайваньским CDC, количество амбулаторных пациентов и обращений за неотложной помощью из-за энтеровируса, т.е.например, герпангина или болезнь рук-ящура, увеличивается в конце марта, достигает пика примерно в середине июня, а затем постепенно снижается. Дети в возрасте до 5 лет более подвержены энтеровирусной инфекции с тяжелыми осложнениями, в результате чего летальность составляет от 1,3 до 33,3%. В предыдущем исследовании также сообщалось, что более 93% случаев тяжелой энтеровирусной инфекции были обнаружены у детей младше 4 лет, а эпидемии энтеровируса происходят каждые 2–3 года из-за накопления новой популяции восприимчивых людей (7 ).Энтеровирус 71 (EV71) является основным этиологическим патогеном, ответственным за ряд тяжелых заболеваний и осложнений (6). Помимо болезни ладони-ящура (HFMD) и герпангины, этот вирус может быть потенциально осложнен тяжелыми неврологическими осложнениями, приводящими к смертности детей младшего возраста. На Тайване самая крупная и самая тяжелая эпидемия энтеровируса 71 на сегодняшний день произошла в 1998 г., и почти все пациенты с сердечно-легочной недостаточностью умерли (7, 12, 13). В 2000 г. была разработана национальная поэтапная программа лечения для улучшения выживаемости, и в последующие годы уровень летальности значительно улучшился (8, 14).Однако, несмотря на высокий уровень поддержки ОИТН, энтеровирус все еще может вызывать значительную смертность, заболеваемость и долгосрочные последствия (15). Благодаря увеличению выживаемости после внедрения национальной программы поэтапных руководств (8), выжило больше пациентов, инфицированных энтеровирусом; однако долгосрочные последствия, особенно развитие нервной системы и когнитивные функции, остаются серьезной проблемой при лечении этого заболевания (8, 16). Считается, что помимо неврологических последствий энтеровирусная инфекция оказывает долгосрочное влияние на различные общие проблемы со здоровьем, такие как аллергические заболевания и заболевания, связанные с другими системами, и, таким образом, энтеровирусная инфекция становится серьезной проблемой общественного здравоохранения у детей (5, 9).
В этом исследовании мы сравнивали детей с инфекцией ЭВ и без нее и обнаружили более высокий риск ЦНС и аллергических последствий в первой группе. У детей с тяжелой инфекцией EV был более высокий риск СДВГ, эпилепсии, астмы и аллергического ринита по сравнению с детьми с нетяжелой инфекцией EV. Кумулятивные риски СДВГ, эпилепсии, астмы, аллергического ринита и атопического дерматита были значительно увеличены у детей с инфекцией EV, особенно у детей с тяжелой инфекцией EV, в период последующего наблюдения.
Было документально подтверждено, что вирусные инфекции ЦНС в детстве связаны с более поздним развитием долгосрочных неврологических последствий, таких как слабость конечностей, паралич черепных нервов, церебральный паралич, неаффективное психотическое заболевание, когнитивные нарушения, синдром дефицита внимания и гиперактивности (СДВГ). , нарушение обучаемости и эпилепсия (16–20). Сообщается, что энтеровирус является одной из основных причин вирусной инфекции ЦНС (21, 22). В нескольких исследованиях оценивали долгосрочные неврологические последствия, вторичные по отношению к энтеровирусным поражениям ЦНС (16, 23-25).Даже когда проявления ЦНС полностью исчезнут, при поступлении детей в школу могут наблюдаться психиатрические проблемы (23). В нашем исследовании риски СДВГ и эпилепсии были увеличены, особенно у детей с тяжелой инфекцией ЭВ. Это означает, что раннее распознавание психических и когнитивных проблем и раннее вмешательство имеют решающее значение, особенно для детей, инфицированных энтеровирусом в раннем возрасте. В этом отношении особую озабоченность вызывают пациенты с тяжелой инфекцией ЭВ. В настоящем исследовании тяжелая инфекция ЭМ, выявленная при госпитализации по поводу инфекции ЭМ, является серьезной проблемой общественного здравоохранения, которую необходимо срочно решить.
Заболеваемость аллергическими заболеваниями среди населения в целом растет, и их симптомы могут сохраняться в течение длительного времени, оказывая негативное влияние на качество жизни (26, 27). Более того, аллергические заболевания являются серьезным социальным бременем из-за отсутствия в школе и приводят к значительным расходам на медицину во всем мире (28–31). Множественные факторы окружающей среды также увеличивают риск аллергических заболеваний, включая более широкое использование антибиотиков, улучшение гигиены, уменьшение размеров семьи, использование летучих продуктов (32, 33) и личные факторы (34) (ожирение и резидентный микробиом легких).Сообщалось, что врожденный иммунный ответ на вирусные инфекции является важным фактором, вызывающим аллергические заболевания в детстве. Было показано, что респираторная инфекция, вызванная риновирусом и респираторно-синцитиальным вирусом, достоверно коррелирует с увеличением частоты случаев астмы (35–38). Сообщается, что энтеровирус человека коррелирует с развитием аллергических заболеваний (39–41). Энтеровирус D68 (EV-D68) был идентифицирован в 1962 году, но ранее был редкостью до вспышки в США в 2014 году.EV-D68 может вызывать тяжелое респираторное заболевание, подобное риновирусу человека, и усугубляет тяжесть симптомов у детей, страдающих астмой и хрипом (5, 42). Кроме того, в предыдущих исследованиях сообщалось о повышении серологической распространенности антител IgE к энтеровирусу 71 и снижении уровня антител против эховируса у детей-астматиков с HFMD (43, 44). Сообщалось также о повышенном уровне циркулирующих фолликулярных хелперных Т-клеток у детей с HFMD (45). Разумно предположить, что энтеровирусы влияют на последующие риски аллергических заболеваний у детей через иммунную систему.Недавно Ли и др. наблюдали повышенный риск последующего развития аллергического дерматита и аллергического ринита у детей, которые ранее были инфицированы герпангиной, и снижение риска последующего возникновения астмы у детей с предшествующим диагнозом HFMD по сравнению с населением в целом, на основе анализа большая популяционная база данных (40). Однако в нашем исследовании повышенный риск астмы и аллергического ринита был отмечен у детей, ранее перенесших энтеровирусную инфекцию, по сравнению с населением в целом.Мы также обнаружили повышенный риск астмы и аллергического ринита у детей, госпитализированных с тяжелой энтеровирусной инфекцией, по сравнению с детьми с нетяжелой энтеровирусной инфекцией. Тем не менее, значимая разница в риске атопического дерматита между когортой EV и контрольной группой была лишь пограничной. Наблюдался значительно повышенный кумулятивный риск атопического дерматита в период наблюдения. Разница между нашим результатом и выводом вышеупомянутого исследования может быть связана с используемыми определениями болезни.
Энтеровирусы исследуются несколько десятилетий. В предыдущем исследовании изучались ассоциации между генотипами энтеровируса и клиническим спектром, но результаты показали значительное разнообразие причинных генотипов в каждой клинической картине (15). Некоторые хронические заболевания, такие как СД I типа (46), лейкемия (47), тики (48), аутоиммунные заболевания (49, 50) и сердечно-сосудистые заболевания, могут быть связаны с энтеровирусными инфекциями (9). Хотя сообщалось, что некоторые из этих расстройств и заболеваний имеют сильную причинно-следственную связь с энтеровирусом, например, сахарный диабет I типа, в литературе имеются противоречивые данные по другим.Таким образом, совокупность имеющихся данных указывает на то, что энтеровирус тесно связан с многочисленными хроническими заболеваниями и что для детей этот патоген может стать серьезным долгосрочным бременем для здоровья, которое распространяется и во взрослую жизнь.
Основная сила этого исследования заключается в том, что это первое эпидемиологическое исследование, демонстрирующее связь общих педиатрических заболеваний с энтеровирусной инфекцией с использованием данных национальной репрезентативной когорты с длительным периодом наблюдения.Хотя данные, использованные в этом исследовании, были получены из Тайваньской национальной исследовательской базы данных по медицинскому страхованию (NHIRD), которая представляет собой большую популяционную базу данных с высоконадежными диагнозами благодаря строгому процессу экспертной оценки квалифицированными специалистами, существуют определенные ограничения. Он не содержит данных, относящихся к лабораторным тестам, включая выделение вируса из ткани, титр вирусной сыворотки или полимеразную цепную реакцию с обратной транскрипцией (ОТ-ПЦР). Более того, причинно-следственная связь не может быть дополнительно исследована в этом исследовании.
В заключение, хронические заболевания, такие как СДВГ, эпилепсия и аллергические заболевания, были связаны с энтеровирусной инфекцией в детстве. Инфекция ЭМ в раннем детстве может иметь долгосрочные последствия для общественного здравоохранения, поэтому необходимо разработать профилактические программы.
Заявление о доступности данных
Наборы данных, представленные в этой статье, недоступны, потому что выпуск данных не разрешен Национальной исследовательской базой данных по медицинскому страхованию.Запросы на доступ к наборам данных следует направлять доктору Chien-Heng Lin/[email protected].
Заявление об этике
Исследования с участием людей были рассмотрены и одобрены институциональным наблюдательным советом больницы для ветеранов Тайчжун. Письменное информированное согласие законного опекуна / ближайшего родственника участников не требовалось для участия в этом исследовании в соответствии с национальным законодательством и институциональными требованиями.
Авторские взносы
M-CL и C-HL разработали модель и вычислительную основу.C-HL проанализировал данные и выполнил расчеты. J-JT написал рукопись при участии всех авторов. M-CL разработала исследование и отвечала за общее руководство и планирование.
Финансирование
Это исследование поддержано Фондом исследований больницы для ветеранов Тайчжун (регистрационный номер TCVGH-NHRI10901, TCVGH-1097306C и TCVGH-1097328D).
Конфликт интересов
Авторы заявляют, что исследование проводилось при отсутствии каких-либо коммерческих или финансовых отношений, которые могут быть истолкованы как потенциальный конфликт интересов.
Список литературы
1. Перрин Дж. М., Андерсон Л. Е., ван Клив Дж. Рост хронических заболеваний среди младенцев, детей и молодежи можно встретить с помощью постоянных инноваций в системе здравоохранения. Закон о здоровье . (2014) 33: 2099–105. DOI: 10.1377 / hlthaff.2014.0832
PubMed Аннотация | CrossRef Полный текст | Google Scholar
2. Бернс К. Х., Кейси PH, Лайл Р. Э., Берд TM, Фасселл Дж. Дж., Роббинс Дж. М.. Растет распространенность детей со сложными соматическими заболеваниями в больницах США. Педиатрия .(2010) 126: 638–46. DOI: 10.1542 / педс.2009-1658
PubMed Аннотация | CrossRef Полный текст | Google Scholar
7. Chen KT, Chang HL, Wang ST, Cheng YT, Yang JY. Эпидемиологические особенности заболевания ладонно-ягодичной полости и герпангины, вызванной энтеровирусом 71, на Тайване, 1998-2005 гг. Педиатрия . (2007) 120: e244–52. DOI: 10.1542 / педс.2006-3331
PubMed Аннотация | CrossRef Полный текст | Google Scholar
8. Чанг Л.Ю., Ся Ш., Ву К.Т., Хуанг Ю.К., Линь К.Л., Фанг Т.Й. и др.Исход энтеровирусной инфекции 71 с поэтапным ведением или без такового: с 1998 по 2002 год. Pediatric Infect Dis J . (2004) 23: 327–32. DOI: 10.1097 / 00006454-200404000-00010
CrossRef Полный текст | Google Scholar
10. Wijlaars LP, Gilbert R, Hardelid P. Хронические состояния у детей и молодых людей: обучение на основе административных данных. Арка Дис Детский . (2016) 101: 881–5. DOI: 10.1136 / archdischild-2016-310716
PubMed Аннотация | CrossRef Полный текст | Google Scholar
12.Хо М., Чен Э.Р., Хсу К.Х., Тву С.Дж., Чен К.Т., Цай С.Ф. и др. Эпидемия энтеровирусной 71 инфекции на Тайване. Тайваньская рабочая группа по эпидемии энтеровируса. Новый английский J Med . (1999) 341: 929–35. DOI: 10.1056 / NEJM199
3411301
PubMed Аннотация | CrossRef Полный текст | Google Scholar
13. Chang LY, Lin TY, Hsu KH, Huang YC, Lin KL, Hsueh C и др. Клинические особенности и факторы риска отека легких после энтеровируса-71 заболевания рук, ног и рта. Ланцет .(1999) 354: 1682–6. DOI: 10.1016 / S0140-6736 (99) 04434-7
PubMed Аннотация | CrossRef Полный текст | Google Scholar
14. Lin TY, Chang LY, Hsia SH, Huang YC, Chiu CH, Hsueh C, et al. Вспышка энтеровируса 71 в 1998 г. на Тайване: патогенез и лечение. Clin Infect Dis . (2002) 34 (Дополнение 2): S52–7. DOI: 10.1086 / 338819
PubMed Аннотация | CrossRef Полный текст | Google Scholar
15. де Грааф Х., Пелоси Э., Купер А., Паппачан Дж., Сайкс К., Макинтош И. и др.Тяжелые энтеровирусные инфекции у госпитализированных детей на юге Англии: клинические фенотипы и причинные генотипы. Детский инфекционный диск J . (2016) 35: 723–7. DOI: 10.1097 / INF.0000000000001093
PubMed Аннотация | CrossRef Полный текст | Google Scholar
16. Ли Х.Ф., Чи К.С. Острый вялый паралич, связанный с инфекцией Enterovirus 71: серия случаев длительного неврологического наблюдения. J Детский Neurol . (2014) 29: 1283–90. DOI: 10.1177 / 0883073813516193
PubMed Аннотация | CrossRef Полный текст | Google Scholar
17.Ян Т.Т., Хуанг Л.М., Лу Сиай, Као К.Л., Ли В.Т., Ли П.И. и др. Клинические особенности и факторы неблагоприятных исходов неполиомиелитной энтеровирусной инфекции центральной нервной системы на севере Тайваня, 1994-2003 гг. J Microbiol Immunol Infect . (2005) 38: 417–24.
PubMed Аннотация | Google Scholar
18. Далман К., Аллебек П., Ганнелл Д., Харрисон Г., Кристенссон К., Льюис Г. и др. Инфекции ЦНС в детстве и риск последующего психотического заболевания: когортное исследование с участием более одного миллиона шведских субъектов. Am J Psychiatry . (2008) 165: 59–65. DOI: 10.1176 / appi.ajp.2007.07050740
PubMed Аннотация | CrossRef Полный текст | Google Scholar
19. Михаэли О., Кассис И., Шахор-Мейухас Ю., Шахар Э., Равид С. Долгосрочные моторные и когнитивные исходы острого энцефалита. Педиатрия . (2014) 133: e546–52. DOI: 10.1542 / пед.2013-3010
PubMed Аннотация | CrossRef Полный текст | Google Scholar
21. Michos AG, Syriopoulou VP, Hadjichristodoulou C, Daikos GL, Lagona E, Douridas P, et al.Асептический менингит у детей: анализ 506 случаев. PLoS ONE . (2007) 2: e674. DOI: 10.1371 / journal.pone.0000674
PubMed Аннотация | CrossRef Полный текст | Google Scholar
22. Фаулкс А.Л., Хонарманд С., Глейзер С., Яги С., Шнурр Д., Оберсте М.С. и др. Энтеровирус-ассоциированный энцефалит в проекте Калифорнийского энцефалита, 1998-2005 гг. J Заразить Dis . (2008) 198: 1685–91. DOI: 10.1086 / 592988
PubMed Аннотация | CrossRef Полный текст | Google Scholar
23.Чанг Л.Й., Хуанг Л.М., Гау С.С., Ву Й.Ю., Ся Ш., Фань Т.Ю. и др. Нейроразвитие и когнитивные способности у детей после инфицирования энтеровирусом 71. N England J Med . (2007) 356: 1226–34. DOI: 10.1056 / NEJMoa065954
PubMed Аннотация | CrossRef Полный текст | Google Scholar
24. Гау СС, Чанг Л.Й., Хуанг Л.М., Фань Т.Ю., Ву Ю.Ю., Линь Т.Ю. Симптомы, связанные с дефицитом внимания / гиперактивностью, у детей с энтеровирусной инфекцией центральной нервной системы. Педиатрия .(2008) 122: e452–8. DOI: 10.1542 / педс.2007-3799
PubMed Аннотация | CrossRef Полный текст | Google Scholar
25. Chou IC, Lin CC, Kao CH. Энтеровирусный энцефалит увеличивает риск синдрома дефицита внимания с гиперактивностью: тайваньское популяционное исследование случай-контроль. Медицина . (2015) 94: e707. DOI: 10.1097 / MD.0000000000000707
PubMed Аннотация | CrossRef Полный текст | Google Scholar
26. Токунага Т., Ниномия Т., Осава И., Имото Ю., Ито И., Такабаяси Т. и др.Факторы, связанные с развитием и ремиссией аллергических заболеваний, в эпидемиологическом обследовании старшеклассников в Японии. Am J Rhinol Allergy . (2015) 29: 94–9. DOI: 10.2500 / ajra.2015.29.4135
PubMed Аннотация | CrossRef Полный текст | Google Scholar
27. Ozdemir C. Моноклональные антитела при аллергии; обновленные приложения и перспективные испытания. Recent Pat Inflamm Allergy Drug Discov. (2015) 9: 54–65. DOI: 10.2174 / 1872213X09666150223115303
PubMed Аннотация | CrossRef Полный текст | Google Scholar
28.Сильверстайн, доктор медицины, Майр Дж. Э., Katusic SK, Воллан ПК, О’Коннелл, Э. Дж., Юнгингер, Д. Посещаемость школы и успеваемость в школе: популяционное исследование детей с астмой. J Педиатр . (2001) 139: 278–83. DOI: 10.1067 / mpd.2001.115573
PubMed Аннотация | CrossRef Полный текст | Google Scholar
29. Шпее-ван дер Векке Дж., Меулмеестер Дж. Ф., Раддер Дж. Дж., Верлов-Ванхорик СП. Отсутствие в школе и лечение школьников с респираторными симптомами в Нидерландах: данные системы мониторинга здоровья детей. J Epidemiol Commun Health . (1998) 52: 359–63. DOI: 10.1136 / jech.52.6.359
PubMed Аннотация | CrossRef Полный текст | Google Scholar
31. Maziak W, Behrens T, Brasky TM, Duhme H, Rzehak P, Weiland SK, et al. Увеличиваются ли астма и аллергия у детей и подростков? Результаты исследований ISAAC фазы I и фазы III в Мюнстере, Германия. Аллергия . (2003) 58: 572–9. DOI: 10.1034 / j.1398-9995.2003.00161.x
PubMed Аннотация | CrossRef Полный текст | Google Scholar
32.Woon PY, Chang WC, Liang CC, Hsu CH, Klahan S, Huang YH и др. Повышенный риск атопического дерматита у детей дошкольного возраста с болезнью Кавасаки: популяционное исследование на тайване. Альтернативная медицина на основе доказательств . (2013) 2013: 605123. DOI: 10.1155 / 2013/605123
PubMed Аннотация | CrossRef Полный текст | Google Scholar
33. Тагиева Н., Шейх А. Бытовое воздействие летучих органических соединений в связи с астмой и аллергией у детей и взрослых. Эксперт Рев Клин Иммунол .(2014) 10: 1611–39. DOI: 10.1586 / 1744666X.2014.972943
PubMed Аннотация | CrossRef Полный текст | Google Scholar
35. Турунен Р., Койстинен А., Вуоринен Т., Арку Б., Седерлунд-Венермо М., Руусканен О. и др. Первый эпизод свистящего дыхания: этиология респираторного вируса, атопические характеристики и тяжесть заболевания. Pediatr Allergy Immunol. . (2014) 25: 796–803. DOI: 10.1111 / pai.12318
PubMed Аннотация | CrossRef Полный текст | Google Scholar
36. Кумар Р.К., Фостер П.С., Розенберг Х.Ф.Респираторно-вирусная инфекция, эпителиальные цитокины и врожденные лимфоидные клетки при обострениях астмы. J Leukocyte Biol . (2014) 96: 391–6. DOI: 10.1189 / jlb.3RI0314-129R
PubMed Аннотация | CrossRef Полный текст | Google Scholar
37. Аджамян Ф., Ву Й., Эбелинг С., Иларраза Р., Одемуива С.О., Мокбель Р. и др. Респираторно-синцитиальный вирус индуцирует активность индоламин-2,3-диоксигеназы: потенциально новая роль в развитии аллергических заболеваний. Clin Exp Allergy .(2015) 45: 644–59. DOI: 10.1111 / cea.12498
PubMed Аннотация | CrossRef Полный текст | Google Scholar
38. Feldman AS, He Y, Moore ML, Hershenson MB, Hartert TV. К первичной профилактике астмы. Обзор доказательств того, что респираторные вирусные инфекции в раннем возрасте являются изменяемыми факторами риска для предотвращения детской астмы. Am J Respir Crit Care Med . (2015) 191: 34–44. DOI: 10.1164 / rccm.201405-0901PP
PubMed Аннотация | CrossRef Полный текст | Google Scholar
39.Цукагоши Х., Ишиока Т., Нода М., Козава К., Кимура Х. Молекулярная эпидемиология респираторных вирусов при вирус-индуцированной астме. Передний микробиол . (2013) 4: 278. DOI: 10.3389 / fmicb.2013.00278
PubMed Аннотация | CrossRef Полный текст | Google Scholar
40. Ли З.М., Хуан Ю.Х., Хо С.К., Куо Х.С. Корреляция симптоматической энтеровирусной инфекции и последующего риска аллергических заболеваний посредством популяционного когортного исследования. Медицина . (2017) 96: e5827. DOI: 10,1097 / MD.0000000000005827
PubMed Аннотация | CrossRef Полный текст | Google Scholar
43. Смит-Норовиц Т.А., Карвахал-Рага С., Видон Дж., Джокс Р., Норовиц К.Б., Уивер Д. и др. Повышенная распространенность антител IgE к энтеровирусу 71 у астматиков по сравнению с детьми, не страдающими астмой. Ирландский журнал медицинских наук . (2017) 186: 495–503. DOI: 10.1007 / s11845-016-1480-0
PubMed Аннотация | CrossRef Полный текст | Google Scholar
44. Ивасаки Дж., Чай Л.Й., Кху С.К., Биззинтино Дж., Лейнг И.А., Ле Суеф П.Н. и др.Снижение реакции антител против эховируса у детей, поступающих в больницу с обострениями астмы. Clin Exp Allergy . (2015) 45: 1523–30. DOI: 10.1111 / cea.12501
PubMed Аннотация | CrossRef Полный текст | Google Scholar
45. Wu J, Cui D, Yang X, Lou J, Lin J, Ye X, et al. Повышенная частота циркулирующих фолликулярных хелперных Т-клеток у детей с заболеваниями рук, ног и рта, вызванными энтеровирусной инфекцией 71. Дж. Иммунол Рес . (2014) 2014: 651872.DOI: 10.1155 / 2014/651872
PubMed Аннотация | CrossRef Полный текст | Google Scholar
46. Лин Х. К., Ван Ч., Цай Ф. Дж., Хван К. П., Чен В., Лин С. К. и др. Энтеровирусная инфекция связана с повышенным риском развития диабета 1 типа у детей на Тайване: общенациональное популяционное когортное исследование. Диабетология . (2015) 58: 79–86. DOI: 10.1007 / s00125-014-3400-z
PubMed Аннотация | CrossRef Полный текст | Google Scholar
47. Lin JN, Lin CL, Lin MC, Lai CH, Lin HH, Yang CH, et al.Риск лейкемии у детей, инфицированных энтеровирусом: общенациональное ретроспективное популяционное исследование тайваньского регистра, когортное исследование. Ланцет Онкол . (2015) 16: 1335–43. DOI: 10.1016 / S1470-2045 (15) 00060-1
PubMed Аннотация | CrossRef Полный текст | Google Scholar
48. Цай К.С., Ян Ю.Х., Хуанг К.Ю., Ли Ю., Макинтайр Р.С., Чен В.К. Ассоциация тиковых расстройств и энтеровирусной инфекции: общенациональное популяционное исследование. Медицина . (2016) 95: e3347. DOI: 10.1097 / MD.0000000000003347
PubMed Аннотация | CrossRef Полный текст | Google Scholar
49. Кристенсен М.Л., Пахман Л.М., Шнайдерман Р., Патель, округ Колумбия, Фридман Дж. М.. Распространенность антител к вирусу Коксаки B у пациентов с ювенильным дерматомиозитом. Rheum артрита . (1986) 29: 1365–70. DOI: 10.1002 / art.1780291109
PubMed Аннотация | CrossRef Полный текст | Google Scholar
50. Triantafyllopoulou A, Tapinos N, Moutsopoulos HM. Доказательства инфекции вируса Коксаки при первичном синдроме Шегрена. Rheum артрита . (2004) 50: 2897–902. DOI: 10.1002 / art.20463
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Обзор, диагностика, лечение и профилактика
Введение в энтеровирус:
Часто, когда родители приводят больного ребенка к врачу и слышат: «Это просто вирус», у ребенка энтеровирус.
Что такое энтеровирус?
Энтеровирусы — это большое семейство вирусов, вызывающих многие инфекции у детей.Эти вирусы живут в кишечном тракте, но могут вызывать самые разные заболевания.
Существует более 70 различных штаммов, в том числе вирусы Коксаки группы А и В, эховирусы, полиовирусы, вирус гепатита А и несколько штаммов, которые просто называются энтеровирусом. Несмотря на то, что существует множество штаммов, большинство болезней вызывается примерно дюжиной из них. У большинства детей вырабатывается иммунитет к ним, и они не получают напряжения более одного раза.
Эти вирусы могут жить несколько дней при комнатной температуре.Охлаждение и замораживание не деактивируют их. Однако их легко убить теплом и дезинфицирующими средствами.
Кто заражается энтеровирусом?
Неполиомиелитные энтеровирусные инфекции очень распространены, особенно среди детей раннего возраста и в семьях с маленькими детьми. Летние лагеря и детские сады также являются обычным местом для этих инфекций.
Энтеровирусные инфекции могут возникать в любое время года, но лето и ранняя осень являются основными сезонами энтеровирусов.
Тяжелые инфекции чаще встречаются среди лиц с ослабленным иммунитетом.
Каковы симптомы энтеровируса?
Наиболее частым заболеванием, связанным с энтеровирусами, является «неспецифическое лихорадочное заболевание». У детей с этим типом заболевания повышается температура и они плохо себя чувствуют около 3 дней. Иногда у них поднимается температура в течение нескольких дней, они чувствуют себя лучше, а затем в течение нескольких дней снова поднимается температура. Иногда бывает довольно высокая температура. Может быть жидкий стул, боли в животе, боли в горле, головные боли, боли в мышцах, рвота — или только лихорадка.
В сезон энтеровирусов эти вирусы являются основной причиной сыпей у детей.
Энтеровирусы могут также вызывать респираторные инфекции, в том числе простуду, боль в горле и пневмонию.
Энтеровирусы могут вызывать инфекции ЖКТ, включая тошноту, рвоту, боли в животе и гепатит.
Энтеровирусы могут вызывать неврологические инфекции, включая менингит, энцефалит и заболевания, вызывающие паралич. Недавнее исследование показало, что некоторые дети, заразившиеся определенным видом энтеровирусной инфекции центральной нервной системы, имеют более высокий риск развития СДВГ.
Они могут вызывать артрит, боль в груди, мышечные инфекции, сердечные инфекции, инфекции яичек, инфекции новорожденных и глазные инфекции.
Болезни рук, ног и рта, герпангина и острый геморрагический конъюнктивит являются специфическими заболеваниями, вызываемыми энтеровирусами.
У подавляющего большинства детей с энтеровирусными инфекциями симптомы отсутствуют.
Энтеровирус заразен?
Да. Эти вирусы очень заразны. Они переходят от стула к коже и ко рту.Они также могут передаваться респираторным путем. Поскольку они могут так долго жить на поверхности, они часто передаются через инфицированные объекты (фомиты).
Сколько длится энтеровирус?
Продолжительность заражения зависит от конкретного вируса и типа инфекции.
Как диагностируется энтеровирус?
Энтеровирусные инфекции обычно подозреваются на основании анамнеза и физического осмотра. Энтеровирусные инфекции легко спутать с другими инфекциями, такими как розеола или пятая болезнь.Иногда для подтверждения болезни необходимы анализы горла, стула или крови.
Как лечится энтеровирус?
Большинству детей лечение не требуется, кроме как для облегчения надоедливых симптомов.
Людям с серьезными инфекциями могут потребоваться противовирусные препараты или внутривенное лечение. Антибиотики бесполезны для лечения энтеровирусов или других вирусных инфекций.
Как предотвратить энтеровирус?
Тщательное мытье рук, особенно после туалета, пеленания и перед едой, может предотвратить некоторые случаи энтеровируса.





