Сделать прививку для профилактики коклюша, дифтерии и столбняка вакциной Инфанрикс в Москве
Инфанрикс — вакцина для профилактики коклюша, дифтерии и столбняка у детей от 2 месяцев до 7 лет.
В отличие от российской цельноклеточной вакцины АКДС импортная вакцина Инфанрикс содержит бесклеточный коклюшный компонент и в медицинских документах отмечается как АаКДС (буква «а» строчная означает «ацеллюлярный») или DTaP. За счет бесклеточного коклюшного компонента Инфанрикс переносится значительно легче, чем АКДС.
Вакцина АаКДС входит в Национальный календарь профилактических прививок и вводится четыре раза в первые полтора года жизни. Обычно для этого используются комбинированные вакцины Пентаксим или Инфанрикс Гекса, которые содержат в себе все компоненты Инфанрикса и полиовакцину, ХИБ-вакцину и (в Инфанрикс Гекса) вакцину от гепатита В. Таким образом для ребенка значительно снижается количество болезненных инъекций. Однако при нарушенных графиках вакцинации иногда требуется ввести только АаКДС, без других компонентов. Для этого и нужна вакцина Инфанрикс.
Таким образом для ребенка значительно снижается количество болезненных инъекций. Однако при нарушенных графиках вакцинации иногда требуется ввести только АаКДС, без других компонентов. Для этого и нужна вакцина Инфанрикс.
Инфанрикс разрешена до 7 лет, поэтому ей можно ревакцинировать и перед школой; НКПП рекомендует вводить пятую дозу (вторую ревакцинацию) против столбняка и дифтерии перед школой (в 6,5 лет) вакциной АДС-м. Однако в западных странах рекомендуется в этом возрасте вводить еще и вакцину против коклюша, продлевая защиту от него на первые классы школы. Для этого используется Tdap (Адасель) либо DTaP (Инфанрикс).
Переносимость вакцины Инфанрикс средняя, примерно у каждого десятого привитого возникнет припухлость, краснота и болезненность в месте введения, появится недомогание и повысится температура до 38 °C или чуть выше. Эта реакция пройдет сама за 1–3 дня. Чтобы облегчить состояние, можно принимать ибупрофен или парацетамол. Вакцина неживая, поэтому отсроченных нежелательных реакций на нее не бывает.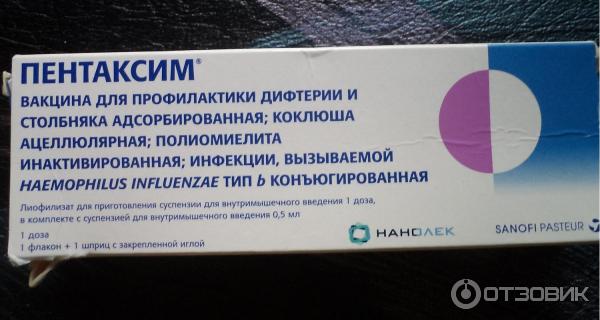
Детям старше 7 лет подходит вакцина Адасель (Tdap) с тем же набором антигенов, но их меньшей дозой. Это обусловлено тем, что старшие дети и взрослые имеют более эффективный иммунитет, способны вырабатывать защиту и на меньшие дозы, а высокие «детские» дозы дают у них более высокую частоту и выраженность нежелательных реакций.
Календарь вакцинации детей от 0 до 7 лет
Графический календарь прививок для детей от рождения и до 7-летнего возраста с обозначением сроков введения вакцин согласно российским правилам.
Источник: календарь CDC
Редакция: педиатр Сергей Бутрий
Прививка АКДС в Одинцово и Звенигороде, сделать прививку АКДС детям и взрослым
Чем опасны болезни?
Столбняк поражает нервную систему, вызывает напряжение в мышцах и судороги. Это острое инфекционное заболевание передается через раны, порезы, повреждения тканей и является смертельно опасным для человека.
Коклюшем можно заразиться воздушно-капельным путем. Основным симптомом является спазматический мучительный кашель, а также катаральные симптомы. Коклюшем болеют и взрослые, и дети, но у детей он протекает значительно тяжелее (в раннем возрасте приступ кашля может сопровождаться остановкой дыхания).
Основным симптомом является спазматический мучительный кашель, а также катаральные симптомы. Коклюшем болеют и взрослые, и дети, но у детей он протекает значительно тяжелее (в раннем возрасте приступ кашля может сопровождаться остановкой дыхания).
Дифтерия – инфекционное заболевание, которое наносит удар по дыхательным путям, поражая слизистую, провоцируя образование плотных фиброзных пленок, способных вызвать удушье и смерть. Высока опасность паралича и асфиксии гортани, почечной недостаточности, поражения сердечной мышцы. Заболеть могут как дети, так и взрослые.
Схема вакцинации АКДС
Первая прививка АКДС детям рекомендована по достижении трех месяцев, две последующие делают через каждые полтора месяца (в 4,5 месяцев и 6 месяцев). В полтора года вакцинация ребенка завершается ещё одной прививкой (если нарушены сроки прививок, то через 12-13 месяцев после последней вакцинации АКДС вакциной). Если интервалы между прививками нужно увеличить (по медицинским показаниям или иным причинам), то очередную прививку следует проводить в ближайший срок, определяемый состоянием здоровья ребёнка.
Прививка АКДС в «ВЕРАМЕД»
Если вам нужно сделать прививку АКДС, вы можете обратиться в наши медицинские центры в Одинцово или Звенигороде, где компетентные специалисты помогут вам спланировать график прививок и подберут нужную вакцину.
В МЦ «ВЕРАМЕД» представлены препараты «Пентаксим», «Инфанрикс», «Инфанрикс Гекса», признанные высококачественными импортными разновидностями отечественной вакцины АКДС. Чтобы понять, какая вакцина предпочтительнее для вашего ребенка, нужно проконсультироваться с врачом.
Сертифицированные препараты помогут достичь необходимой напряженности иммунитета к возбудителям опасных заболеваний. И что немаловажно – для этого не нужно ждать в очередях и опасаться, что цена вакцины ударит по семейному бюджету. Постоянно повышая качество медицинских услуг, мы сохраняем приемлемые цены и предоставляем скидки социально незащищенной категории граждан.
Вакцинация ИНФАНРИКС в Звенигороде
Инфанрикс – это импортная вакцина, являющаяся отечественным аналогом АКДС. Данную прививку делают малышам и детям для профилактики дифтерии, столбняка и коклюша.
Данную прививку делают малышам и детям для профилактики дифтерии, столбняка и коклюша.
Чтобы обезопасить ребёнка от трёх главных инфекций, специалисты Клиники Здоровья Исток рекомендуют своевременно посещать медицинское учреждение для вакцинации: процедура пройдёт быстро и без усилий, а организм малютки получит активную выработку иммунитета, необходимую для укрепления здоровья.
- Вакцина Инфанрикс полностью отвечает требованиям Всемирной Организации Здравоохранения.
- Состав вакцины не содержит консервантов и абсолютно безопасна.
- Инфанрикс является одной из самых распространённых вакцин.
Записаться на приём Задать вопрос в WHATSAPP
Когда необходимо делать прививку Инфанрикс?
Согласно Национальному календарю профилактических прививок, вакцинация проводится курсом из четырёх процедур:
- первая прививка – в 3 месяца
- вторая прививка – в 4,5 месяцев
- третья прививка – в 6 месяцев
- первая ревакцинация – в 18 месяцев
Как подготовиться к прививке Инфанрикс?
- Перед тем как провести вакцинацию, следует провести тщательный осмотр ребёнка и изучить его анамнез.

- За день до вакцинации не следует вводить в рацион ребёнка новые продукты питания.
- За 1 час до процедуры желудок должен оставаться пустым.
- В день вакцинации следует дать ребенку 0,25 таблетки Супрастина.
- Если ребёнок болеет ОРВИ, его температура тела не соответствует норме или имеются другие заболевания как в лёгкой, так и в острой форме, вакцинацию следует перенести на другую дату, чтобы избежать возможных осложнений.
Дополнительные рекомендации после проведения вакцинации вы можете получить у специалиста на приёме.
Есть ли у прививки Инфанрикс побочные действия?
У некоторых детей может наблюдаться отёк в месте инъекции и повышение температур теда. Однако не стоит беспокоиться раньше времени: эти симптомы проходят в течение 2-4 дней.
Специалисты Клиники Здоровья Исток ответственно подходят к подготовке перед вакцинацией и контролируют состояние ребенка в последующие дни.
Детская вакцинопрофилактика в Новосибирске | ЦНМТ
Вакцинация — это процесс, обеспечивающий биологическую устойчивость организма к определенным инфекционным заболеваниям. Искусственная активная иммунизация — стимуляция иммунной системы организма человека путем введения вакцины. В результате искусственной иммунизации у человека вырабатывается высокоспецифичный иммунитет, организм вырабатывает частичную или полную устойчивость к данному заболеванию. Вакцины длительно защищают организм.
Возможны два пути искусственной активной иммунизации:
- введение живых, но ослабленных микроорганизмов;
- введение убитых микроорганизмов или их токсинов.
В обоих случаях человеку вводят вакцину или токсин, которые сами по себе не вызывают заболевания, но стимулируют иммунную систему, делая ее способной распознать определенный микроорганизм.
По данным Всемирной Организации Здравоохранения ежегодно около 12 млн. детей погибают от инфекционных заболеваний во всем мире. Наиболее подвержены инфекционным заболеваниям дети, особенно раннего возраста, у которых эти болезни отличаются развитием осложнений, приводящим к необратимым последствиям.
детей погибают от инфекционных заболеваний во всем мире. Наиболее подвержены инфекционным заболеваниям дети, особенно раннего возраста, у которых эти болезни отличаются развитием осложнений, приводящим к необратимым последствиям.
В нашем Центре проводится вакцинация по следующим направлениям:
1. Вакцинация детей в рамках «Национального календаря профилактических прививок»:
- профилактика дифтерии, столбняка, коклюша ( АДС-М, Инфанрикс, Инфанрикс Гекса, Пентаксим)
- профилактика полиомиелита (Имовакс Полио,Пентаксим, вакцина полиомиелитная оральная)
- профилактика гепатита В (Энджерикс В 0,5)
- профилактика кори, эпидемического паротита, краснухи (Приорикс, вакцина коревая живая)
- Проба Манту (Туберкулин)
2. Рекомендуемая вакцинация детей вне «Календаря профилактических прививок»
- профилактика гемофильной инфекции (Хиберикс, Пентаксим)
- профилактика ветряной оспы (Варилрикс)
- профилактика гепатита А (Хаврикс)
- профилактика менингоккоковой инфекции (Менактра)
- профилактика пневмокковой инфекции (Пневмо 23, Превенар)
3. Планирование беременности
Планирование беременности
- профилактика краснухи ( Приорикс)
- профилактика гепатита В ( Энджерикс В 1,0)
- профилактика дифтерии (АДС-М, Инфанрикс, Пентаксим)
- профилактика столбняка (АДС-М, Инфанрикс, Пентаксим)
4. Вакцинация от рака
- профилактика вируса папилломы человека (рака шейки матки) (Гардасил, Церварикс)
5.Вакцинация, выезжающих за рубеж
- профилактика желтой лихорадки (Желтая лихорадка)
- профилактика брюшного тифа (Вианвак)
- профилактика гепатита А (Хаврикс)
- профилактика гепатита В (Энджерикс В 1,0, п/гепатитная вакцина взрослая Россия)
- профилактика дифтерии (АДС-М, Инфанрикс, Пентаксим)
- профилактика столбняка (АДС-М, Инфанрикс, Пентаксим)
6.Сезонная вакцинация
- профилактика гриппа (Ваксигрип, Инфлювак)
- профилактика клещевого энцефалита (ФСМЕ-Иммун Джуниор, ФСМЕ-Иммун ЭнцеВир, Энцепур, Клещ-Э-Вак)
- при укусе клеща (Иммуноглобулин (противоклещевой) (ставят в ЦНМТ на Коптюга)
8. Корпоративная вакцинация (вакцинация организаций)
Корпоративная вакцинация (вакцинация организаций)
9.Вакцинация охотников и рыболовов
- профилактика клещевого энцефалита (ФСМЕ-Иммун Инжект, ЭнцеВир, Энцепур, ФСМЕ-Иммун, Клещ-Э-Вак)
- при укусе клеща (Иммуноглобулин (противоклещевой) (ставят в ЦНМТ на Коптюга)
- профилактика столбняка (АДС-М, Инфанрикс, Пентаксим)
- профилактика дифтерии ( АДС-М, Инфанрикс, Пентаксим)
- профилактика гепатита А (Хаврикс 1440)
Вакцинация детей и взрослых, вакцины нового поколения – сеть клиник МЕДСИ
Вакцинация в клиниках МЕДСИ проводится под контролем квалифицированного специалиста в соответствии с Национальным календарем прививок. Кроме того, осуществляется вакцинация против некоторых инфекций, не входящих в список обязательных прививок, в том числе от гепатита А, вируса папилломы человека, клещевого энцефалита, ротавирусной инфекции, менингококковой инфекции, ветряной оспы.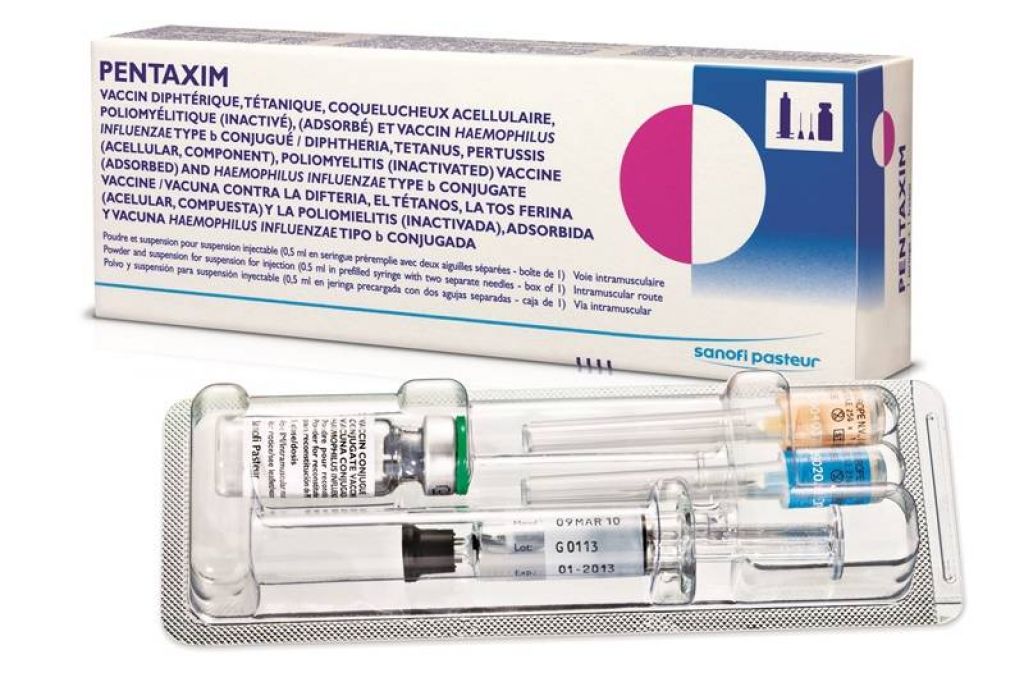
В клиниках используются только качественные отечественные и импортные вакцины. Специалисты МЕДСИ пристально следят за тенденциями фармацевтического рынка и оперативно приобретают в арсенал клиник вакцины нового поколения, то есть более эффективные и безопасные.
Вакцинация проводится в клиниках МЕДСИ по предварительной записи на удобное для вас время при наличии вакцины и после осмотра врача. Записаться на приём и уточнить информацию о наличии нужной Вам вакцины в клиниках «МЕДСИ» можно по телефону круглосуточного контактного центра +7 (495) 7-800-500.
Ежегодная вакцинации против гриппа – защита взрослых и детей
Грипп – острая инфекция, вызывающая ежегодные эпидемии. Протекает с высокой температурой в течение 3-5 дней, с резкой интоксикацией в виде головной боли, болей в мышцах. Грипп обостряет хронические воспалительные процессы в организме, тем самым обусловливая высокую летальность от осложнений.
Возбудители – пневмотропные РНК-содержащие вирусы 3-х серотипов (А,В,С).
Распространение гриппа в наше время в значительной степени связано с быстротой перемещения населения.
Вакцинация – наиболее эффективный метод снижения заболеваемости не только гриппом, но и ОРЗ, вызванных другими респираторными вирусами, как среди взрослых, так и среди детей, в том числе больных бронхиальной астмой и респираторными аллергозами.
Иммунитет вырабатывается через 14 дней после вакцинации.
Постоянная мутация штаммов вируса гриппа, а также непродолжительность поствакцинального периода (6-12 месяцев) требуют ежегодного повторения прививок, даже если ее штаммовый состав, по сравнению с предыдущим сезоном, не изменился. При заражении штаммами гриппозного вируса, отличающимся от вакцинных, заболевание у вакцинированных протекает легче. Живые вакцины слабореактогенны, температура выше 37, 5 в первые 3 дня допускается не более чем у 2% привитых. Субъединичные вакцины дают слабые кратковременные (48-72 часа) реакции не более чем у 3%. Наименее реактогенными по данным международных независимых исследований являются субъединичные вакцины.
Наименее реактогенными по данным международных независимых исследований являются субъединичные вакцины.
Противопоказания для всех вакцин – аллергия к белкам куриного яйца, аллергические реакции на введение любой гриппозной вакцины. Все гриппозные вакцины готовятся из актуальных штаммов вирусов А/h2N1, A/h4N2, В, рекомендуемых ежегодно BОЗ.
Вакцинация в Санкт-Петербурге в клинике «Скандинавия»
Детский неокрепший иммунитет является вечной головной болью родителей. На помощь приходит наука иммунология, которая занимается изучением и развитием защитных реакций организма. Иммунопрофилактика детей – широко распространенная практика в современном мире. Детские прививки делаются в соответствии с определенными нормативами и графиками, в первую очередь, – в соответствии с Детским календарем прививок.
Прививки новорожденным – основа здоровья ребенка на долгие годы. Как правило, в этот период усилия врачей направлены на развитие у ребенка иммунитета против таких заболеваний как коклюш, дифтерия, столбняк (для этого может быть использована вакцинация АКДС, а также прививки с использованием вакцин Пентаксим и Инфанрикс) и некоторых других опасных заболеваний.
В старшем детском возрасте проводится вакцинация от кори, прививки от свинки, прививки от ветряной оспы и прививки против краснухи (эта прививка особенно актуальна девочкам) и другие.
Часть прививок относится к категории обязательной вакцинации, так как направлена на избежание массовых эпидемий инфекционных заболеваний. От некоторых прививок можно отказаться, но прежде чем принять такое решение стоит детально изучить всю информацию, связанную с данной вакцинацией, и здраво взвесить все риски.
Если вас беспокоит, как ваш малыш перенесет вакцинацию, и насколько тяжелыми будут побочные эффекты от прививки, – то при обращении в центр вакцинации вам стоит дополнительно проконсультироваться о возможных вариантах вакцин. Медицинские клиники, предоставляющие услуги платной вакцинации, как правило, используют импортные вакцины. В отличие от отечественных аналогов, зарубежные вакцины, в большинстве случаев, имеют менее выраженные побочные эффекты и легче переносятся детьми.
В отличие от отечественных аналогов, зарубежные вакцины, в большинстве случаев, имеют менее выраженные побочные эффекты и легче переносятся детьми.
Мы создали объединенный календарь вакцинации, чтобы наши пациенты и их дети не пропускали прививки и были защищены.
Сделать прививку ребенку можно в любом отделении клиники «Скандинавия».
Все услуги в этом же направлении
| Наименование услуги | Цена, руб |
| Инфанрикс. Вакцинация в процедурном кабинете клиники | 2300 |
| Инфанрикс. Выездная вакцинация | 3300 |
| Пентаксим. Вакцинация в процедурном кабинете клиники | 2900 |
| Пентаксим. Выездная вакцинация | 3900 |
| Приорикс. Вакцинация в процедурном кабинете клиники | 1000 |
Приорикс. Выездная вакцинация Выездная вакцинация | 2000 |
| Энджерикс В. Вакцинация в процедурном кабинете клиники | 850 |
| Энджерикс В. Выездная вакцинация | 1850 |
| Инфлювак. Вакцинация в процедурном кабинете клиники | 1000 |
| Инфлювак. Выездная вакцинация | 2000 |
| Ваксигрип. Вакцинация в процедурном кабинете клиники | 1000 |
| Ваксигрип. Выездная вакцинация | 2000 |
| Совигрипп. Вакцинация в процедурном кабинете клиники | 800 |
| Совигрипп. Выездная вакцинация | 1800 |
| Ультрикс. Вакцинация в процедурном кабинете клиники | 800 |
| Ультрикс. Выездная вакцинация | 1800 |
| Варилрикс. Вакцинация в процедурном кабинете клиники | 3500 |
| Варилрикс. Выездная вакцинация | 4500 |
| Превенар-13. Вакцинация в процедурном кабинете клиники | 2800 |
Превенар-13. Выездная вакцинация Выездная вакцинация | 3800 |
| Пневмо-23. Вакцинация в процедурном кабинете клиники | 4300 |
| Пневмо-23. Выездная вакцинация | 5300 |
| Хаврикс. Вакцинация в процедурном кабинете клиники | 1500 |
| Хаврикс. Выездная вакцинация | 2500 |
| Хиберикс. Вакцинация в процедурном кабинете клиники | 1300 |
| Хиберикс. Выездная вакцинация | 2300 |
| Бивак ОПВ. Вакцинация в процедурном кабинете клиники | 1000 |
| Бивак ОПВ. Выездная вакцинация | 2000 |
| АДС-М. Вакцинация в процедурном кабинете клиники | 1150 |
| АДС-М. Выездная вакцинация | 2150 |
| АКДС. Вакцинация в процедурном кабинете клиники | 1000 |
| АКДС. Выездная вакцинация | 2000 |
| Полимилекс. Вакцинация в процедурном кабинете клиники | 1500 |
Полимилекс. Выездная вакцинация Выездная вакцинация | 2500 |
| Менингококковая вакцина. Вакцинация в процедурном кабинете клиники | 1400 |
| Менингококковая вакцина. Выездная вакцинация | 2400 |
| Инфанрикс ГЕКСА. Вакцинация в процедурном кабинете клиники | 3500 |
| Инфанрикс ГЕКСА. Выездная вакцинация | 4500 |
| Коревая вакцина. Вакцинация в процедурном кабинете клиники | 600 |
| Коревая вакцина. Выездная вакцинация | 1600 |
| М-М-Р II. Вакцинация в процедурном кабинете клиники | 1800 |
| М-М-Р II. Выездная вакцинация | 2800 |
| Альгавак-М детская. Вакцинация в процедурном кабинете клиники | 1100 |
| Альгавак-М детская. Выездная вакцинация | 2100 |
| Альгавак-М взрослая. Вакцинация в процедурном кабинете клиники | 2000 |
| Альгавак-М взрослая. Выездная вакцинация | 3000 |
Клещ-Э-Вак детская. Вакцинация в процедурном кабинете клиники Вакцинация в процедурном кабинете клиники | 1525 |
| Клещ-Э-Вак детская. Выездная вакцинация | 2525 |
| Клещ-Э-Вак взрослая. Вакцинация в процедурном кабинете клиники | 1600 |
| Клещ-Э-Вак взрослая. Выездная вакцинация | 2600 |
| Услуга вакцинации на выезде | 1000 |
Растущее количество данных свидетельствует о том, что вакцина Sputnik от COVID безопасна и эффективна
флаконов вакцины Sputnik V COVID-19 проходят по производственной линии на производственном предприятии недалеко от Санкт-Петербурга, Россия Фото: Ольга Мальцева / AFP / Getty
Российская вакцина против COVID-19, Sputnik, была предметом восхищения и споров с тех пор, как правительство России разрешило ее использование в прошлом году, еще до того, как были опубликованы результаты ранних испытаний. Данные из России и многих других стран теперь показывают, что это безопасно и эффективно, но остаются вопросы о качестве наблюдения за возможными редкими побочными эффектами.
Sputnik V — также известный как Gam-COVID-Vac — была первой вакциной против COVID-19, зарегистрированной для использования в любой стране, и с тех пор она была одобрена в 67 странах, включая Бразилию, Венгрию, Индию и Филиппины. Но вакцина — и ее однократный брат Sputnik Light — еще не получили одобрения для экстренного использования от Европейского агентства по лекарственным средствам (EMA) или Всемирной организации здравоохранения (ВОЗ). Одобрение ВОЗ имеет решающее значение для широкого распространения в рамках инициативы глобального доступа к вакцинам от COVID-19 (COVAX), которая обеспечивает дозы для стран с низкими доходами.
Вакцина, разработанная учеными из Национального исследовательского центра эпидемиологии и микробиологии «Гамалея» в Москве, была разрешена к применению Минздравом России 11 августа 2020 года, более чем за месяц до публикации результатов испытаний фазы I и II, и еще до того, как началось испытание фазы III.
Научное сообщество с возмущением восприняло объявление президента России Владимира Путина о регистрации вакцины. «Если правительство собирается одобрить вакцину до того, как станет известно о результатах испытания, это не укрепит доверия», — сказал эпидемиолог Майкл Тул из Института Бернета в Мельбурне, Австралия.
«Если правительство собирается одобрить вакцину до того, как станет известно о результатах испытания, это не укрепит доверия», — сказал эпидемиолог Майкл Тул из Института Бернета в Мельбурне, Австралия.
Доступ к полным данным
Некоторые из этих опасений были развеяны, когда результаты испытаний фазы III 1 , опубликованные в феврале разработчиками вакцины, показали, что она на 91,6% эффективна в предотвращении симптоматической инфекции COVID-19 и на 100% эффективна. для предотвращения тяжелой инфекции. Тем не менее, некоторые ученые раскритиковали авторов за то, что они не предоставили доступ к полным необработанным данным ранних испытаний, а также выразили обеспокоенность по поводу изменений в протоколе введения вакцины и несоответствий в данных.
Авторы ответили, что они предоставили регулирующим органам все данные, необходимые для получения разрешения, и что данных, включенных в документ 2 , было достаточно для читателей, чтобы подтвердить заявленную эффективность вакцины. Они также рассмотрели запросы протокола и заявили, что числовые несоответствия были «простыми опечатками, которые были формально исправлены».
Они также рассмотрели запросы протокола и заявили, что числовые несоответствия были «простыми опечатками, которые были формально исправлены».
Несмотря на отсутствие одобрения EMA или ВОЗ, несколько стран, включая Южную Корею, Аргентину и Индию, уже производят Sputnik V.А Индия планирует выпустить не менее 850 миллионов доз, чтобы ускорить вакцинацию населения, находящегося в боевых условиях. Многие другие страны, такие как Венгрия и Иран, импортируют Sputnik V, и он стал ключевым элементом их кампаний вакцинации.
Но не все шло гладко. Регулирующий орган Бразилии отклонил заявку на импорт Sputnik V в апреле из-за опасений по поводу отсутствия данных о безопасности, качестве и эффективности. Это решение было отменено в июне, но вакцина была одобрена только для здоровых взрослых.
Пожилой мужчина получает дозу вакцины Sputnik V в Каракасе, Венесуэла Фото: Федерико Парра / AFP / Getty
Два вирусных вектора лучше одного?
Sputnik V — это вакцина против аденовируса, что означает, что он использует сконструированный аденовирус — семейство вирусов, которые обычно вызывают только легкие заболевания, — в качестве механизма доставки для вставки генетического кода белка шипа SARS-CoV-2 в клетки человека. .
.
Аналогичен вакцинам Oxford – AstraZeneca и Johnson & Johnson.Но вместо использования одного сконструированного аденовируса, как эти две вакцины, Sputnik V использует разные аденовирусы, называемые rAd26 и rAd5, для первой и второй доз соответственно.
Дмитрий Кулиш, исследователь биотехнологии из Сколковского института науки и технологий в Москве, который не участвует в разработке Sputnik V, говорит, что научное обоснование должно было заключаться в повышении эффективности. По его словам, у двух аденовирусов есть несколько разные методы введения своего генетического материала в клетку-хозяина, что теоретически повысит вероятность успешной доставки вирусного генетического материала туда, где он должен быть.
В двух предварительных исследованиях разработчиков вакцины, опубликованных в сентябре 2020 г. Все участники вырабатывали антитела к белку шипа SARS-CoV-2, и сообщалось о побочных эффектах, в основном, в виде легкой боли в месте инъекции, лихорадки, головной боли, усталости и мышечных болей — побочных эффектов, типичных для других вакцин против SARS-CoV-2.
В рандомизированном исследовании фазы III, опубликованном в промежуточной форме в феврале, 14 964 взрослых получили двухдозовую вакцину и 4902 человека получили две дозы плацебо.Только у 16 субъектов в группе вакцины развился симптоматический COVID-19 по сравнению с 62 в группе плацебо, что составляет эффективность вакцины 91,6%. Кроме того, в группе вакцинированных не было случаев заболевания средней и тяжелой степени тяжести, а в группе плацебо — 20.
Неопубликованные данные о 3,8 миллионах россиян, вакцинированных двумя дозами, также указывают на эффективность 97,6%, говорится в апрельском пресс-релизе Института Гамалеи. По данным Министерства здравоохранения Объединенных Арабских Эмиратов о 81000 человек, получивших две дозы вакцины, предполагается 97.Эффективность 8% в предотвращении симптоматического COVID-19 и 100% эффективность в предотвращении тяжелого заболевания.
Российское исследование III фазы также показало, что даже одна доза на 73,6% эффективна в профилактике умеренных и тяжелых заболеваний. Это привело к тому, что российские органы здравоохранения одобрили однократную дозу Sputnik Light, в которой используется вектор rAd26, в мае на основе данных собственной программы вакцинации страны, которые показали, что ее эффективность в предотвращении симптоматических заболеваний составляет 79,4%.
Это привело к тому, что российские органы здравоохранения одобрили однократную дозу Sputnik Light, в которой используется вектор rAd26, в мае на основе данных собственной программы вакцинации страны, которые показали, что ее эффективность в предотвращении симптоматических заболеваний составляет 79,4%.
С тех пор, пока еще неопубликованное исследование министерства здравоохранения Буэнос-Айреса в Аргентине с участием 40 387 вакцинированных и 146 194 невакцинированных людей в возрасте 60–79 лет показало, что однократная доза Sputnik Light уменьшила симптоматические инфекции на 78.6%, госпитализации на 87,6% и смерти на 84,7%.
Вопросы о побочных эффектах
Побочные эффекты Sputnik также становятся яснее; исследования, проведенные на данный момент, предполагают, что они аналогичны вакцинам против других аденовирусов, за исключением редких случаев свертывания крови. В отличие от вакцин Oxford – AstraZeneca и Johnson & Johnson, никаких сообщений об этих заболеваниях от органов здравоохранения России или других стран, использующих Sputnik V.
A препринт 3 из итальянской больницы Буэнос-Айреса в Аргентине, не поступало. не сообщали о случаях нарушения свертываемости крови или нежелательных явлений, представляющих особый интерес, среди 683 медицинских работников, вакцинированных Sputnik V.А анализ 2,8 миллиона доз Sputnik V, введенных в Аргентину, показал отсутствие смертей, связанных с вакцинацией, и в основном умеренные побочные эффекты. Кроме того, исследование, опубликованное в качестве препринта в мае в республике Сан-Марино, не обнаружило серьезных побочных эффектов у 2558 взрослых, получивших одну дозу Sputnik V, и у 1288 человек, получивших две дозы 4 .
Вирусолог Элисон Кельвин из Университета Далхаузи в Галифаксе, Канада, говорит, что существует теория о том, что нарушение свертывания крови связано с вирусно-векторными вакцинами, но добавляет: «Я не думаю, что у нас есть точная причина того, какой компонент этих вакцин вызывая это », или может ли это повлиять на Sputnik.Она отмечает, что хотя в исследовании III фазы Sputnik V участвовало всего 21 977 человек, и поэтому вакцина была слишком маленькой, чтобы выявить редкие побочные эффекты, вакцина теперь широко используется во всем мире, а это означает, что отчеты должны появляться, «если появится сигнал безопасности. ».
».
палестинских медицинских работника выгружают коробки с вакциной Sputnik V из грузовика в секторе Газа Фото: Саид Хатиб / AFP / Getty
Неясно, в состоянии ли Россия обнаруживать такие редкие события. Те, кто связан с вакциной Oxford – AstraZeneca, впервые были выявлены в результате мониторинга побочных эффектов в Австрии, что побудило EMA провести анализ безопасности вакцины.
Но мониторинг побочных эффектов в России может быть менее эффективным, утверждает Кулиш, отчасти из-за культурного сопротивления обращению за медицинской помощью. «Большинство россиян вызовут [к] доктору только тогда, когда они больше не могут дышать», — шутит он. Кроме того, врачи в отдаленных регионах России могут не связать инсульт, вызванный, например, тромбами, с недавней вакцинацией, говорит он.
Аргентина не сообщала о каких-либо случаях свертывания крови, несмотря на получение более четырех миллионов доз вакцины, отмечает Кулиш.Сербия, которая также широко использует Sputnik V, до сих пор не сообщала о случаях нарушения свертываемости крови, зарегистрированных при применении других аденовирусных вакцин.
ВОЗ и EMA ждут разрешения на использование Sputnik
Ученые говорят, что опасения по поводу мониторинга побочных эффектов могут быть причиной того, что ВОЗ и EMA еще не выдали разрешение на использование в чрезвычайных ситуациях. ВОЗ запросила дополнительные данные у Института Гамалеи, и агентство продолжает инспекции российских предприятий по производству вакцин и клинических испытаний.К настоящему времени проинспектировано девять объектов, и ВОЗ выявила озабоченность по поводу одного производственного объекта. Точно так же EMA перечисляет разрешение на вакцину как находящееся на «непрерывном пересмотре».
Разработчики Sputnik обвинили Европейский Союз в предвзятости, сославшись на комментарий комиссара ЕС по внутреннему рынку Тьерри Бретона в марте о том, что ЕС «абсолютно не нужен Sputnik V».
Кулиш предполагает, что в EMA также существует позиция «про-Pfizer», которая мешает Sputnik получить разрешение — ссылка на вакцину Pfizer-BioNTech, совместно разработанную Pfizer в Нью-Йорке и BioNTech в Майнце, Германия. Представитель EMA ответил на это предложение, указав, что «одинаковые стандарты» применяются ко всем заявителям на вакцину COVID-19, «независимо от того, в какой части мира они находятся».
Представитель EMA ответил на это предложение, указав, что «одинаковые стандарты» применяются ко всем заявителям на вакцину COVID-19, «независимо от того, в какой части мира они находятся».
Тул говорит, что он подозревает, что главное беспокойство EMA вызывает то, что «они не очень довольны» российским надзором за нежелательными явлениями.
Есть также опасения по поводу Sputnik в России, где высокий уровень нерешительности в отношении вакцины против COVID. Мартовский опрос показал, что 62% россиян не планировали вакцинироваться, и в настоящее время Россия вводит обязательную вакцинацию для некоторых государственных и других работников, чтобы повысить уровень вакцинации.По состоянию на 28 июня только около 15% населения России, насчитывающего более 140 миллионов человек, получили одну дозу вакцины.
Несколько других исследований в настоящее время проводятся в странах, которые одобрили Sputnik, в том числе в Аргентине, Венесуэле, России и Турции, которые должны помочь построить более точную картину безопасности и эффективности вакцины.
Как действует вакцина Sinovac Covid-19
Частная китайская компания Sinovac разработала вакцину от коронавируса под названием CoronaVac .Вакцина одобрена для использования в Китае и разрешена для использования в экстренных случаях более чем в десятке других стран. В ходе испытания, проведенного в Бразилии, исследователи обнаружили, что его эффективность против инфекций с симптомами или без них составляет 50,65%. В ходе испытания, проведенного в Турции, исследователи обнаружили, что его эффективность против Covid-19 с симптомами составляет 91,25%.
Вакцина из коронавирусов
CoronaVac работает, обучая иммунную систему вырабатывать антитела против коронавируса SARS-CoV-2.Антитела прикрепляются к вирусным белкам, таким как так называемые белки-шипы, изучающие его поверхность.
Чтобы создать CoronaVac, исследователи Sinovac начали с получения образцов коронавируса у пациентов в Китае, Великобритании, Италии, Испании и Швейцарии. Один образец из Китая в конечном итоге послужил основой для вакцины.
Один образец из Китая в конечном итоге послужил основой для вакцины.
Убить вирус
Исследователи вырастили большие запасы коронавируса в клетках почек обезьян.Затем они обработали вирусы химическим веществом под названием бета-пропиолактон. Соединение отключило коронавирусы, связавшись с их генами. Инактивированные коронавирусы больше не могли размножаться. Но их белки, в том числе шипованные, остались нетронутыми.
Затем исследователи извлекли инактивированные вирусы и смешали их с небольшим количеством соединения на основе алюминия, называемого адъювантом. Адъюванты стимулируют иммунную систему, чтобы усилить ее ответ на вакцину.
Инактивированные вирусы используются более века. Джонас Солк использовал их для создания своей вакцины против полиомиелита в 1950-х годах, и они стали основой для вакцин против других болезней, включая бешенство и гепатит А.
Вызов иммунного ответа
Поскольку коронавирусы в CoronaVac мертвы, их можно ввести в руку, не вызывая Covid-19. Попав внутрь организма, некоторые из инактивированных вирусов поглощаются иммунной клеткой, называемой антигенпрезентирующей клеткой.
Попав внутрь организма, некоторые из инактивированных вирусов поглощаются иммунной клеткой, называемой антигенпрезентирующей клеткой.
Представляя
вирусный белок
фрагментов
Представляя
вирусный белок
фрагментов
Представляя
вирусный белок
фрагментов
Антигенпредставляющая клетка разрывает коронавирус и отображает некоторые его фрагменты на своей поверхности.Так называемая вспомогательная Т-клетка может обнаружить фрагмент. Если фрагмент входит в состав одного из его поверхностных белков, Т-клетка активируется и может помочь рекрутировать другие иммунные клетки для ответа на вакцину.
Изготовление антител
Другой тип иммунных клеток, называемых В-клетками, также может столкнуться с инактивированным коронавирусом. В-клетки имеют поверхностные белки самых разных форм, и некоторые из них могут иметь правильную форму, чтобы зацепиться за коронавирус. Когда В-клетка блокируется, она может втягивать часть или весь вирус внутрь и представлять фрагменты коронавируса на своей поверхности.
Когда В-клетка блокируется, она может втягивать часть или весь вирус внутрь и представлять фрагменты коронавируса на своей поверхности.
Вспомогательная Т-клетка, активированная против коронавируса, может прикрепляться к одному и тому же фрагменту. Когда это происходит, активируется и В-клетка. Он размножается и выделяет антитела, которые имеют ту же форму, что и их поверхностные белки.
Соответствие
поверхностные белки
Соответствие
поверхностных белков
Соответствие
поверхностных белков
Соответствие
поверхностные белки
Соответствие
поверхностные белки
Соответствие
поверхностные белки
Соответствие
поверхность
белков
Соответствие
поверхность
белков
Соответствие
поверхность
белков
Соответствие
поверхностные белки
Соответствие
поверхностные белки
Соответствие
поверхностных белков
Остановка вируса
После вакцинации CoronaVac иммунная система может реагировать на заражение живыми коронавирусами. В-клетки вырабатывают антитела, которые прилипают к захватчикам. Антитела, нацеленные на спайковый белок, могут предотвратить проникновение вируса в клетки. Другие виды антител могут блокировать вирус другими способами.
В-клетки вырабатывают антитела, которые прилипают к захватчикам. Антитела, нацеленные на спайковый белок, могут предотвратить проникновение вируса в клетки. Другие виды антител могут блокировать вирус другими способами.
Вспоминая вирус
Хотя CoronaVac может предложить некоторую защиту от Covid-19, никто пока не может сказать, как долго длится эта защита. Не исключено, что уровень антител снизится в течение нескольких месяцев. Но иммунная система также содержит специальные клетки, называемые В-клетками памяти, которые могут сохранять информацию о коронавирусе годами или даже десятилетиями.
Хронология вакцины
Январь, 2020 Sinovac начинает разработку инактивированной вакцины против коронавируса.
Инженеры Sinovac, работающие с клетками почек обезьян. Николас Асфури / Agence France-Presse
июнь Испытания фазы 1/2 на 743 добровольцах не выявили серьезных побочных эффектов.
июль Sinovac начинает испытание фазы 3 в Бразилии, за ним следуют другие испытания в Индонезии и Турции.Reuters сообщает, что правительство Китая дало разрешение на экстренное использование вакцины Sinovac для ограниченного использования.
Доза CoronaVac в Турции, Эмра Гурель / Associated Press
Октябрь Власти в городе Цзясин на востоке Китая объявляют, что они предоставляют CoronaVac людям, выполняющим работу с относительно высоким уровнем риска, включая медицинских работников, портовых инспекторов и персонал государственной службы.
Октябрь.19 Официальные лица в Бразилии говорят, что Sinovac — самая безопасная из пяти вакцин, которые они тестируют в рамках третьей фазы испытаний.
Ноябрь Sinovac публикует подробности своего исследования фазы 1/2 в медицинском журнале, показывая сравнительно скромное производство антител. Только испытание фазы 3 покажет, достаточно ли этого для защиты людей от Covid-19.
Только испытание фазы 3 покажет, достаточно ли этого для защиты людей от Covid-19.
19 ноября Правительство Бразилии объявляет о приостановке в прошлом месяце испытания Синовака в стране из-за неблагоприятного события.Детали паузы были туманными, вызывая подозрения в причастности к политике. Через два дня после объявления суд разрешили возобновить. Бразильское испытание зарегистрировало достаточно случаев Covid-19, чтобы исследователи могли определить эффективность Sinovac. Они рассчитывают опубликовать свои результаты к 23 декабря.
Власти Бразилии держат коробки с партией вакцины. Александр Шнайдер / Getty Images
Декабрь Sinovac заявляет, что планирует произвести 300 миллионов доз в 2020 году и увеличить мощность до 600 миллионов доз в год.
23 декабря Бразильские исследователи объявляют, что эффективность CoronaVac превышает 50 процентов.
24 декабря. Турецкие официальные лица заявляют, что эффективность вакцины составляет 91,25 процента.
7 января 2021 г. Исследователи из Бразилии объявляют, что эффективность CoronaVac составляет 78 процентов. Ни у одного из вакцинированных добровольцев в их испытании фазы 3 не развились тяжелые или умеренные случаи Covid-19. Но оценка эффективности была основана на эффективности вакцины в подгруппе добровольцев.Общая эффективность официально не опубликована.
11 января Индонезия разрешает вакцину для экстренного использования.
13 января Исследователи из Бразилии объявляют, что общая эффективность CoronaVac составляет чуть более 50 процентов. Турция разрешает вакцину для экстренного использования.
6 фев. Sinovac объявляет, что Китай предоставил CoronaVac условное одобрение.
13 марта Китай просит соискателей визы сделать прививки от коронавируса китайского производства.
Апрель 1 Sinovac объявляет, что его мощность увеличилась до 2 миллиардов доз после завершения третьей производственной линии.
Источники: Национальный центр биотехнологической информации; Наука; Ланцет; Линда Кофлан, медицинский факультет Мэрилендского университета; Дженна Гатмиллер, Чикагский университет.
Отслеживание коронавируса
Как действует вакцина Sinopharm Covid-19
В начале 2020 года Пекинский институт биологических продуктов создал инактивированную вакцину против коронавируса под названием BBIBP-CorV .Клинические испытания, проведенные государственной компанией Sinopharm, показали, что его эффективность составляет 79 процентов. Китай одобрил вакцину и вскоре начал экспортировать ее в другие страны. 7 мая Всемирная организация здравоохранения объявила аналогичную оценку эффективности в 78,1 процента.
Вакцина из коронавирусов
BBIBP-CorV работает, обучая иммунную систему вырабатывать антитела против коронавируса SARS-CoV-2. Антитела прикрепляются к вирусным белкам, таким как так называемые белки-шипы, изучающие его поверхность.
Антитела прикрепляются к вирусным белкам, таким как так называемые белки-шипы, изучающие его поверхность.
Для создания BBIBP-CorV исследователи Пекинского института получили три варианта коронавируса от пациентов в китайских больницах. Они выбрали один из вариантов, потому что он мог быстро размножаться в клетках почек обезьяны, выращенных в резервуарах биореактора.
Убить вирус
После того, как исследователи собрали большие запасы коронавирусов, они залили их химическим веществом под названием бета-пропиолактон.Соединение отключило коронавирусы, связавшись с их генами. Инактивированные коронавирусы больше не могли размножаться. Но их белки, в том числе шипованные, остались нетронутыми.
Затем исследователи извлекли инактивированные вирусы и смешали их с небольшим количеством соединения на основе алюминия, называемого адъювантом. Адъюванты стимулируют иммунную систему, чтобы усилить ее ответ на вакцину.
Инактивированные вирусы используются более века.Джонас Солк использовал их для создания своей вакцины против полиомиелита в 1950-х годах, и они стали основой для вакцин против других болезней, включая бешенство и гепатит А.
Вызов иммунного ответа
Поскольку коронавирусы в BBIBP-CorV мертвы, их можно вводить в руку, не вызывая Covid-19. Попав внутрь организма, некоторые из инактивированных вирусов поглощаются иммунной клеткой, называемой антигенпрезентирующей клеткой.
Представляя
вирусный белок
фрагментов
Представляя
вирусный белок
фрагментов
Представляя
вирусный белок
фрагментов
Антигенпредставляющая клетка разрывает коронавирус и отображает некоторые его фрагменты на своей поверхности.Так называемая вспомогательная Т-клетка может обнаружить фрагмент. Если фрагмент входит в состав одного из его поверхностных белков, Т-клетка активируется и может помочь рекрутировать другие иммунные клетки для ответа на вакцину.
Изготовление антител
Другой тип иммунных клеток, называемых В-клетками, также может столкнуться с инактивированным коронавирусом. В-клетки имеют поверхностные белки самых разных форм, и некоторые из них могут иметь правильную форму, чтобы зацепиться за коронавирус. Когда В-клетка блокируется, она может втягивать часть или весь вирус внутрь и представлять фрагменты коронавируса на своей поверхности.
Вспомогательная Т-клетка, активированная против коронавируса, может прикрепляться к одному и тому же фрагменту. Когда это происходит, активируется и В-клетка. Он размножается и выделяет антитела, которые имеют ту же форму, что и их поверхностные белки.
Соответствие
поверхностных белков
Соответствие
поверхностных белков
Соответствие
поверхностных белков
Соответствие
поверхностных белков
Соответствие
поверхностных белков
Соответствие
поверхностных белков
Соответствие
поверхность
белков
Соответствие
поверхность
белков
Соответствие
поверхность
белков
Соответствие
поверхностных белков
Соответствие
поверхностных белков
Соответствие
поверхностных белков
Остановка вируса
После вакцинации BBIBP-CorV иммунная система может реагировать на заражение живыми коронавирусами.В-клетки вырабатывают антитела, которые прилипают к захватчикам. Антитела, нацеленные на спайковый белок, могут предотвратить проникновение вируса в клетки. Другие виды антител могут блокировать вирус другими способами.
Вспоминая вирус
Клинические испытания Sinopharm продемонстрировали, что BBIBP-CorV может защитить людей от Covid-19. Но пока никто не может сказать, как долго продлится эта защита. Не исключено, что уровень антител снизится в течение нескольких месяцев. Но иммунная система также содержит специальные клетки, называемые В-клетками памяти, которые могут сохранять информацию о коронавирусе годами или даже десятилетиями.
Хронология вакцины
Январь, 2020 Sinopharm начинает разработку инактивированной вакцины против коронавируса.
июнь Исследователи сообщают, что вакцина дает многообещающие результаты на обезьянах. Испытания фазы 1/2 показывают, что вакцина не вызывает серьезных побочных эффектов и позволяет людям вырабатывать антитела против коронавируса.
Завод Sinopharm в Пекине.Чжан Ювэй / Синьхуа, через Associated Press
июль г. В Объединенных Арабских Эмиратах начинается третья фаза испытаний.
август г. Начало третьей фазы испытаний в Марокко и Перу.
Приготовление дозы Sinopharm в Лиме, Перу, Эрнесто Бенавидес / Agence France-Presse
14 сентября ОАЭ дает экстренное разрешение на использование вакцины Sinopharm для медицинских работников.Правительственные чиновники и другие люди начинают это получать.
Ноябрь Председатель Sinopharm говорит, что почти миллион человек в Китае получили вакцины Sinopharm.
3 ноября Правитель Дубая шейх Мохаммед бин Рашид аль-Мактум объявляет, что получил вакцину.
Шейх Мохаммед до вакцинации Агентство Франс Пресс
9 декабря г.A.E. полностью одобряет BBIBP-CorV, заявляя, что его эффективность составляет 86 процентов. Но правительство не сообщило никаких подробностей в своем заявлении, оставив неясным, как они пришли к своим выводам.
13 декабря Бахрейн также одобрил вакцину.
Флаконы с вакциной Sinopharm на заводе по упаковке. Чжан Ювэй / Синьхуа, через Associated Press
30 декабря Sinopharm объявляет об эффективности вакцины 79.34 процента, что побудило китайское правительство одобрить его. Компания еще не опубликовала подробные результаты исследования фазы 3.
3 января 2021 г. Египет разрешает вакцину для экстренного использования.
12 марта Венгрия соглашается платить около 36 долларов за дозу вакцины Sinopharm, что делает ее одной из самых дорогих в мире.
7 мая По оценкам Всемирной организации здравоохранения, эффективность вакцины Sinopharm составляет 78.1 процент и разрешает вакцину для экстренного использования.
июль Sinopharm планирует производить 5 миллиардов доз в год.
20 июля Китай разрешает вакцину Sinopharm для экстренного применения у детей и подростков.
3 августа Объединенные Арабские Эмираты вслед за Китаем разрешили вакцину Sinopharm для экстренного применения у детей и подростков.
Источники: Национальный центр биотехнологической информации; Наука; Ланцет; Линда Кофлан, медицинский факультет Мэрилендского университета; Дженна Гатмиллер, Чикагский университет.
Отслеживание коронавируса
FDA и CDC рекомендуют приостановить использование вакцины против COVID-19 компании Johnson & Johnson (Janssen) после тщательного анализа безопасности
- Для немедленного выпуска:
Español
После тщательного анализа безопасности, включая два заседания Консультативного комитета CDC по практике иммунизации, U.Управление по санитарному надзору за качеством пищевых продуктов и медикаментов и Центры США по контролю и профилактике заболеваний определили, что рекомендуемая пауза в отношении использования вакцины Johnson & Johnson (Janssen) COVID-19 в США должна быть отменена и использование вакцины должно быть возобновлено.
Пауза была рекомендована после сообщений о шести случаях редкого и тяжелого типа тромбов у людей после введения вакцины Janssen COVID-19. Во время паузы медицинские и научные группы из FDA и CDC изучили доступные данные для оценки риска тромбоза венозных синусов головного мозга или CVST (крупных кровеносных сосудов в головном мозге) и других участков тела (включая, но не ограничиваясь, к крупным кровеносным сосудам живота и венам ног) вместе с тромбоцитопенией или низким количеством тромбоцитов в крови.Команды FDA и CDC также провели обширную информационную работу с поставщиками медицинских услуг и клиницистами, чтобы убедиться, что они осведомлены о потенциале этих нежелательных явлений и могут правильно управлять и распознавать эти события благодаря уникальному лечению, необходимому для этих тромбов и низкого уровня тромбоцитов, а также известный как синдром тромбоз-тромбоцитопении (СТС).
Два агентства определили следующее:
- В США следует возобновить использование вакцины Janssen COVID-19.
- FDA и CDC уверены, что эта вакцина безопасна и эффективна для предотвращения COVID-19.
- FDA установило, что имеющиеся данные показывают, что известные и потенциальные преимущества вакцины перевешивают известные и потенциальные риски для людей в возрасте 18 лет и старше.
- В настоящее время имеющиеся данные предполагают, что вероятность возникновения TTS очень мала, но FDA и CDC будут продолжать изучать этот риск.
- Поставщики медицинских услуг, вводящие вакцину и получателей вакцины, или лица, осуществляющие уход, должны ознакомиться с Информационным бюллетенем о вакцине Janssen COVID-19 для медицинских работников, вводящих вакцину (поставщиками вакцинации) и Информационным бюллетенем для реципиентов и лиц, осуществляющих уход, которые были пересмотрены с целью включения информации о риске заражения. этот синдром, который возник у очень небольшого числа людей, получивших вакцину Janssen от COVID-19.
Независимый консультативный комитет CDC по практике иммунизации собрался сегодня, чтобы обсудить последние данные о TTS, заслушать сообщение производителя вакцины Janssen и Подгруппы технической безопасности вакцины COVID-19 (VaST), а также провести анализ риска и пользы. ACIP обязуется проявлять бдительность и реагировать на дополнительную информацию, которая может повлиять на анализ риска и пользы любой из этих вакцин. Мониторинг безопасности вакцин будет продолжен, и любая новая информация о TTS будет передаваться в ACIP по мере необходимости.
«Безопасность — наш главный приоритет. Эта пауза была примером нашей обширной работы по мониторингу безопасности, поскольку они были разработаны для работы — выявляя даже такое небольшое количество случаев. Мы сняли паузу на основании анализа всех доступных данных FDA и CDC, консультаций с медицинскими экспертами и рекомендаций Консультативного комитета CDC по практике иммунизации. Мы пришли к выводу, что известные и потенциальные преимущества вакцины Janssen COVID-19 перевешивают известные и потенциальные риски для людей в возрасте 18 лет и старше.Мы уверены, что эта вакцина продолжает соответствовать нашим стандартам безопасности, эффективности и качества. Мы рекомендуем людям, у которых есть вопросы о том, какая вакцина им подходит, обсудить это со своим лечащим врачом », — сказала Джанет Вудкок, доктор медицины, исполняющая обязанности комиссара FDA.
«Прежде всего, здоровье и безопасность находятся на переднем крае наших решений», — сказала директор CDC д-р Рошель П. Валенски. «Наши системы безопасности вакцин работают. Мы выявили исключительно редкие события — из миллионов введенных доз Janssen COVID-19 — и сделали паузу, чтобы изучить их более внимательно.Как и всегда, мы продолжим внимательно следить за всеми сигналами по мере того, как все больше американцев будут вакцинированы. Меня по-прежнему воодушевляет растущее количество реальных доказательств того, что разрешенные вакцины против COVID-19 безопасны и эффективны и защищают людей от болезней, госпитализации и смерти. Я призываю всех, у кого есть вопросы о вакцинах от COVID-19, поговорить со своим врачом или местным отделом здравоохранения ».
Оценка имеющихся данных
Медицинские и научные группы FDA и CDC изучили несколько источников информации и данных, связанных с вакциной Janssen COVID-19, чтобы принять сегодняшнее решение.
В частности, агентства оценили отчеты, представленные в Систему сообщений о побочных эффектах вакцин (VAERS), изучили медицинскую литературу и рассмотрели информацию от партнеров по глобальному регулированию о тромбозе с тромбоцитопенией, которые были зарегистрированы после использования аналогичного, но не идентичного COVID. -19 с использованием вируса из семейства аденовирусов, который был модифицирован, чтобы содержать ген для создания белка из SARS-CoV-2.
Обновленная информация о нежелательных явлениях
13 апреля FDA и CDC объявили об этом из более чем шести.Введено 8 миллионов доз, в VAERS поступило шесть сообщений о редком и тяжелом типе тромбов в сочетании с низким уровнем тромбоцитов у людей после вакцинации Janssen COVID-19. В этих случаях тип сгустка крови, называемый тромбозом венозного синуса головного мозга (CVST), наблюдался в сочетании с низким уровнем тромбоцитов (тромбоцитопения).
Сегодня агентства могут подтвердить, что всего в VAERS было сообщено о 15 случаях TTS, включая шесть первоначальных зарегистрированных случаев.Все эти случаи произошли у женщин в возрасте от 18 до 59 лет, средний возраст — 37 лет. В сообщениях указывалось, что симптомы проявляются через 6-15 дней после вакцинации.
Мониторинг безопасности будет продолжен
Действующие системы эпиднадзора за безопасностью вакцин против COVID-19, разрешенных для использования в экстренных случаях, работают, о чем свидетельствует быстрая работа обоих агентств по выявлению и расследованию этих редких, но серьезных побочных эффектов. FDA и CDC продолжат эти усилия по тщательному мониторингу безопасности этих вакцин.
Сообщения о побочных эффектах после вакцинации можно направлять в Систему сообщений о побочных эффектах вакцин.
Связанная информация
###
Заготовка
FDA, агентство в составе Министерства здравоохранения и социальных служб США, защищает общественное здоровье, обеспечивая безопасность, эффективность и безопасность лекарственных и ветеринарных препаратов, вакцин и других биологических продуктов для использования человеком, а также медицинских устройств.Агентство также отвечает за безопасность и сохранность продуктов питания, косметики, пищевых добавок, продуктов, излучающих электронное излучение, а также за регулирование табачных изделий.
Консультативный комитет по вакцинам и родственным биологическим продуктам Объявление о заседании от 26 февраля 2021 г. — 26.02.2021 — 26.02.2021
На этой странице
Обратите внимание, что из-за воздействия этой пандемии COVID-19 все участники встречи присоединятся к этому совещанию консультативного комитета через платформу онлайн-телеконференций.
Встреча онлайн-конференции будет доступна по следующему телефону:
Повестка дня
Презентации собрания будут слышны, просматриваются, подписываются и записываются с помощью онлайн-платформы для проведения телеконференций. Комитет встретится на открытом заседании, чтобы обсудить EUA компании Janssen Biotech Inc. Вакцина COVID-19 для активной иммунизации с целью предотвращения COVID-19, вызванного SARS-CoV-2, у лиц 18 лет и старше.
Материалы собрания
FDA намерено сделать справочные материалы доступными для общественности не позднее, чем за 2 рабочих дня до собрания.Если FDA не сможет разместить справочные материалы на своем веб-сайте до собрания, любые справочные материалы будут опубликованы во время заседания консультативного комитета, а дополнительные материалы будут размещены на веб-сайте FDA после заседания.
Материалы для этого собрания будут доступны на главной странице заседаний Консультативного комитета по вакцинам и родственным биологическим продуктам. . .
Встреча будет включать в себя слайд-презентации с аудиокомпонентами, которые позволят представить материалы в манере, максимально напоминающей личное заседание консультативного комитета.
Информация об участии общественности
Заинтересованные лица могут представить данные, информацию или мнения, устно или письменно, по вопросам, находящимся на рассмотрении комитета.
FDA составляет список для общественного обсуждения этой встречи. Номер дела: FDA-2021-N-0173
Досье закрывается 25 февраля 2021 года. Обратите внимание, что поздно поданные несвоевременные комментарии не рассматриваются. В электронной системе регистрации https://www.regulations.gov комментарии принимаются до 11:59 p.м. По восточному времени в конце 25 февраля 2021 года. Комментарии, полученные почтой / ручной доставкой / курьером (для письменных / бумажных представлений), будут считаться своевременными, если они проштампованы по почте или квитанция о принятии службы доставки пришла на эту дату или раньше.
Комментарии, полученные до 18 февраля 2021 г., будут переданы в комитет. Комментарии, полученные после 18 февраля 2021 г. и до 25 февраля 2021 г., будут приняты во внимание FDA. В случае отмены собрания FDA продолжит оценку любых соответствующих заявок, представленных материалов или информации и при необходимости рассмотрит любые комментарии, внесенные в список.
Вы можете отправлять следующие комментарии:
Электронные документы
- Федеральный портал электронного регулирования: https://www.regulations.gov. Следуйте инструкциям по отправке комментариев. Комментарии, отправленные в электронном виде, включая вложения, на https://www.regulations.gov, будут помещены в список без изменений. Поскольку ваш комментарий будет обнародован, вы несете единоличную ответственность за то, чтобы ваш комментарий не содержал никакой конфиденциальной информации, которую вы или третье лицо не желаете публиковать, например, медицинскую информацию, ваш или чей-либо номер социального страхования или конфиденциальная бизнес-информация, например производственный процесс.Обратите внимание, что если вы включите свое имя, контактную информацию или другую информацию, которая идентифицирует вас в тексте своих комментариев, эта информация будет размещена на https://www.regulations.gov
- Если вы хотите отправить комментарий с конфиденциальной информацией, которую вы не хотите делать общедоступной, отправьте комментарий в письменном / бумажном виде и в подробном порядке (см. «Письменные / бумажные материалы» и «Инструкции» ).
Письменные / бумажные документы
- Почта / Доставка вручную / Курьер (для письменных / бумажных представлений): Персонал управления документами (HFA-305), Управление по санитарному надзору за качеством пищевых продуктов и медикаментов, 5630 Fishers Lane, Rm.1061, Роквилл, Мэриленд 20852.
- Для письменных / бумажных комментариев, представленных персоналу управления документами, FDA опубликует ваш комментарий, а также любые приложения, за исключением предоставленной информации, помеченной и идентифицированной как конфиденциальная, если она представлена в соответствии с подробным описанием в «Инструкциях».
Инструкции: Все полученные материалы должны включать номер дела FDA-2021-N-0173. для «Вакцины и родственные биологические продукты»; Уведомление о собрании; Создание публичного реестра; Запрос комментариев.»Полученные комментарии, которые были поданы своевременно (см. АДРЕСА), будут помещены в список и, за исключением тех, которые представлены как« Конфиденциальные материалы », доступны для всеобщего просмотра на https://www.regulations.gov или в Управлении списками документов. Персонал с 9:00 до 16:00 с понедельника по пятницу, 240-402-7500.
- Конфиденциальные материалы — Чтобы отправить комментарий с конфиденциальной информацией, которую вы не хотите делать общедоступной, отправляйте свои комментарии только в письменном / бумажном виде.Вы должны предоставить всего две копии. Одна копия будет включать информацию, которую вы считаете конфиденциальной, с пометкой в заголовке или на обложке, в которой говорится: «ДАННЫЙ ДОКУМЕНТ СОДЕРЖИТ КОНФИДЕНЦИАЛЬНУЮ ИНФОРМАЦИЮ». FDA рассмотрит эту копию, включая заявленную конфиденциальную информацию, при рассмотрении комментариев. Вторая копия, в которой заявленная конфиденциальная информация будет отредактирована / затемнена, будет доступна для всеобщего просмотра и размещена на https://www.regulations.gov. Отправьте обе копии в отдел управления досье.Если вы не хотите, чтобы ваше имя и контактная информация были общедоступными, вы можете указать эту информацию на титульном листе, а не в тексте комментариев, и вы должны указать эту информацию как «конфиденциальную». Любая информация, помеченная как «конфиденциальная», не будет раскрыта, кроме как в соответствии с 21 CFR 10.20 и другими применимыми законами о раскрытии информации. Для получения дополнительной информации о том, как FDA размещает комментарии в публичных списках, см. 80 FR 56469, 18 сентября 2015 г. или доступ к информации по адресу: https: // www.govinfo.gov/content/pkg/FR-2015-09-18/pdf/2015-23389.pdf.
Досье: Для доступа к досье для чтения справочных документов или полученных электронных и письменных / бумажных комментариев перейдите на https://www.regulations.gov и вставьте номер досье, указанный в скобках в заголовке. этого документа, в поле «Поиск» и следуйте подсказкам и / или перейдите к сотрудникам службы управления документами, 5630 Fishers Lane, Rm. 1061, Роквилл, Мэриленд 20852, 240-402-7500.
ДЛЯ ДОПОЛНИТЕЛЬНОЙ ИНФОРМАЦИИ ОБРАЩАЙТЕСЬ: Прабхакара Атрейя или Кэтлин Хейс, Центр оценки и исследований биологических препаратов, Управление по санитарному надзору за качеством пищевых продуктов и медикаментов, 10903 New Hampshire Ave., Корп. 71, ком. 6306, Silver Spring, MD 20993-0002, по электронной почте [email protected] ; или информационная линия Консультативного комитета FDA, 1-800-741-8138 (301-443-0572 в районе Вашингтона, округ Колумбия). Уведомление в Федеральном реестре об изменениях в последнюю минуту, влияющих на ранее объявленное заседание консультативного комитета, не всегда может быть опубликовано достаточно быстро, чтобы своевременно уведомить об этом. Поэтому вам всегда следует проверять веб-сайт Агентства по адресу https://www.fda.gov/advisory-committees и прокручивать вниз до соответствующей ссылки на совещание консультативного комитета или звонить на информационную линию консультативного комитета, чтобы узнать о возможных изменениях, прежде чем присоединиться к совещанию. .
26 февраля 2021 г. устные выступления общественности будут запланированы примерно на 13:10. Восточное время и 14:10. По восточному времени.
Лица, заинтересованные в проведении официальных устных презентаций, должны уведомить [email protected] и представить краткое изложение общего характера доказательств или аргументов, которые они хотят представить, имена и адреса предполагаемых участников, а также указание приблизительное время, требуемое для проведения презентации не позднее 17 февраля 2021 г.
Время, отведенное для каждой презентации, может быть ограничено. Если количество зарегистрированных лиц, желающих выступить, больше, чем может быть разумно размещено во время запланированных открытых публичных слушаний, FDA может провести лотерею для определения выступающих на запланированных открытых публичных слушаниях. Контактное лицо уведомит заинтересованных лиц об их просьбе выступить до 18 февраля 2021 года .
Информация о веб-трансляции
CBER планирует организовать бесплатную прямую веб-трансляцию заседания Консультативного комитета по вакцинам и связанным с ними биологическим продуктам.Если есть случаи, когда трансляция интернет-трансляции не удалась; Персонал постарается восстановить передачу как можно скорее.
Встреча онлайн-конференции будет доступна по следующим ссылкам:
Контактная информация
- Прабхакара Атрейя или Кэтлин Хейс: [email protected]
- Информационная линия Консультативного комитета FDA: 1-800-741-8138 (301-443-0572 в районе Вашингтона, округ Колумбия) Пожалуйста, позвоните на информационную линию для получения последней информации об этой встрече.
- По вопросам прессы обращайтесь в Управление по связям со СМИ по телефону [email protected] или 301-796-4540.
Уведомление в Федеральном реестре об изменениях в последнюю минуту, влияющих на ранее объявленное заседание консультативного комитета, не всегда может быть опубликовано достаточно быстро, чтобы своевременно уведомить об этом. Поэтому вам всегда следует проверять главную страницу собрания или звонить на горячую линию / телефонную линию соответствующего консультативного комитета, чтобы узнать о возможных изменениях, прежде чем приходить на собрание.
FDA стремится к упорядоченному проведению заседаний консультативного комитета. Посетите наш веб-сайт, чтобы узнать о процедурах общественного поведения во время заседаний консультативного комитета.
Уведомление об этом собрании дается в соответствии с Законом о Федеральном консультативном комитете (5 U.S.C. app. 2).
Официальное уведомление FR
Уведомление в Федеральном реестре об изменениях в последнюю минуту, влияющих на ранее объявленное заседание консультативного комитета, не всегда может быть опубликовано достаточно быстро, чтобы своевременно уведомить об этом.Поэтому вам всегда следует проверять веб-сайт агентства или звонить уполномоченному федеральному должностному лицу комитета (см. Контактную информацию), чтобы узнать о возможных изменениях, прежде чем приходить на собрание.
Сообщаем лицам, посещающим заседания консультативного комитета FDA, что агентство не несет ответственности за обеспечение доступа к электрическим розеткам. FDA приветствует присутствие общественности на заседаниях консультативного комитета и приложит все усилия для размещения людей с ограниченными возможностями.Если вам требуется приспособление из-за инвалидности, пожалуйста, свяжитесь с уполномоченным федеральным должностным лицом комитета (см. Контактную информацию) как минимум за 7 дней до встречи.
Ответы на часто задаваемые вопросы, включая информацию о специальных приспособлениях из-за инвалидности, можно найти по адресу: Общие вопросы и ответы о заседаниях Консультативного комитета FDA.
FDA стремится к упорядоченному проведению заседаний консультативного комитета. Пожалуйста, посетите наш веб-сайт в разделе «Общественное поведение во время заседаний консультативного комитета FDA», чтобы узнать о процедурах общественного поведения во время заседаний консультативного комитета.
Уведомление об этом собрании дается в соответствии с Законом о Федеральном консультативном комитете (5 U.S.C. app.2).
Материалы для мероприятий
| Название | Тип / размер файла | Организация-источник |
|---|---|---|
| Консультативный комитет по вакцинам и родственным биологическим продуктам 26 февраля 2021 г. Встреча с подтверждением финансовых интересов | pdf (68.51 КБ) | Не в соответствии с FDA |
| Консультативный комитет по вакцинам и связанным с ними биологическим продуктам 26 февраля 2021 г. Отказ от права участия | pdf (133,50 КБ) | FDA |
| Консультативный комитет по вакцинам и родственным биологическим продуктам 26 февраля 2021 г. Информационный документ совещания — FDA | pdf (979.68 КБ) | FDA |
| Консультативный комитет по вакцинам и родственным биологическим продуктам 26 февраля 2021 г. Информационный документ совещания — Приложение — Спонсор | pdf (111,43 КБ) | Не в соответствии с FDA |
| Консультативный комитет по вакцинам и родственным биологическим продуктам 26 февраля 2021 г. Информационный документ совещания — Спонсор | pdf (2.28 МБ) | Не в соответствии с FDA |
| Консультативный комитет по вакцинам и родственным биологическим продуктам 26 февраля 2021 г. Проект повестки дня заседания | pdf (69,53 КБ) | FDA |
| Консультативный комитет по вакцинам и связанным с ними биологическим продуктам 26 февраля 2021 г. Заседание Проект реестра | pdf (194,36 КБ) | FDA |
| Консультативный комитет по вакцинам и родственным биологическим продуктам 26 февраля 2021 г. Презентация совещания — Эпидемиология вариантов SARS-CoV-2 | pdf (2.08 МБ) | Не в соответствии с FDA |
| Консультативный комитет по вакцинам и родственным биологическим продуктам 26 февраля 2021 г. Презентация — Заявление на выдачу разрешения на использование в чрезвычайных ситуациях (EUA) для Ad26.COV2.S | pdf (2,55 МБ) | Не в соответствии с FDA |
| Консультативный комитет по вакцинам и связанным с ними биологическим продуктам 26 февраля 2021 г. Презентация на заседании — Обзор разрешения на экстренное использование COVID-19 и рекомендации по вакцинам COVID-19 | pdf (248.16 КБ) | FDA |
| Консультативный комитет по вакцинам и связанным с ними биологическим продуктам 26 февраля 2021 г. Презентация встречи — COVID-19 FDA Обзор эффективности и безопасности вакцины Janssen COVID-19 на разрешение на экстренное использование | pdf (812,07 КБ) | FDA |
| Консультативный комитет по вакцинам и связанным с ними биологическим продуктам 26 февраля 2021 г. Презентация на заседании — COVID-19 Обновленная информация о мониторинге FDA безопасности и эффективности вакцины против COVID-19 | pdf (323.19 КБ) | FDA |
| Консультативный комитет по вакцинам и родственным биологическим продуктам 26 февраля 2021 г. Презентация совещания — Обновление безопасности вакцины COVID-19 | pdf (1,43 МБ) | Не в соответствии с FDA |
| Консультативный комитет по вакцинам и связанным с ними биологическим продуктам 26 февраля 2021 г. Презентация на заседании — Вопрос для голосования по COVID-19 | pdf (83.56 КБ) | FDA |
| Консультативный комитет по вакцинам и родственным биологическим продуктам 26 февраля 2021 г. | pdf (75,83 КБ) | FDA |
| Консультативный комитет по вакцинам и родственным биологическим продуктам, 26 февраля, 2021 г. Заседание, окончательная повестка дня | pdf (51,74 КБ) | FDA |
| Консультативный комитет по вакцинам и родственным биологическим продуктам 26 февраля 2021 г. Сводный протокол заседания | pdf (164.08 КБ) | FDA |
| Консультативный комитет по вакцинам и родственным биологическим продуктам 26 февраля 2021 г. Стенограмма заседания | pdf (2,86 МБ) | FDA |
доз вакцины COVID-19, отправленных центром COVAX в Гану, знаменуя начало глобального развертывания
- COVAX объявляет, что 600 000 доз вакцины AstraZeneca / Oxford, лицензированной для Института сыворотки Индии, прибыли в Аккру, Гана; на этой неделе ожидаются дальнейшие поставки в Абиджан, Кот-д’Ивуар.
- Окончательный первый раунд распределения доз вакцин AstraZeneca / Oxford и Pfizer-BioNTech для большинства стран и экономик, участвующих в программе COVAX, будет опубликован в ближайшие дни.
- Начало глобального внедрения означает, что по мере выполнения критериев готовности и производства доз вакцины будут отправляться участникам Объекта на постоянной основе.
Сегодня Гана стала первой страной за пределами Индии, которая получила дозы вакцины COVID-19, отправленные через центр COVAX.Это исторический шаг к нашей цели по обеспечению справедливого распределения вакцин против COVID-19 во всем мире, в том месте, которое будет самым крупным.
история закупок и поставок вакцин. Доставка является частью первой волны прибытий, которая продолжится в ближайшие дни и недели.
23 февраля COVAX доставил 600 000 доз вакцины AstraZeneca / Oxford из Индийского института сывороток (SII) из Пуны, Индия, в Аккра, Гана, и прибыл утром 24 февраля.Прибытие в Аккра — это первая отгруженная и доставленная партия.
в Африке Центром COVAX в рамках беспрецедентных усилий по доставке не менее 2 миллиардов доз вакцины COVID-19 к концу 2021 года.
COVAX проводится совместно с Гави, Альянсом по вакцинам, Всемирной организацией здравоохранения ( ВОЗ) и Коалиция за инновации в обеспечении готовности к эпидемиям (CEPI), работающие в партнерстве с ЮНИСЕФ, а также Всемирным банком, организациями гражданского общества, производителями,
и другие.
«Миссия COVAX — помочь остановить острую фазу пандемии как можно быстрее, обеспечив глобальный равноправный доступ к вакцинам против COVID-19. Сегодняшняя доставка делает нас еще на один шаг ближе к этой цели, и это то, что делает весь мир.
можно гордиться. В ближайшие недели COVAX должен доставить вакцины во все страны-участницы, чтобы гарантировать защиту наиболее подверженным риску, где бы они ни жили. Сейчас нам нужно, чтобы правительства и бизнес подтвердили свою поддержку COVAX и
помогите нам победить этот вирус как можно быстрее », — сказал д-р Сет Беркли, генеральный директор Gavi, Vaccine Alliance.
«Мы не остановим пандемию где бы то ни было, если не остановим ее повсюду», — сказал д-р Тедрос Адханом Гебрейесус, Генеральный директор ВОЗ. «Сегодняшний день — важный первый шаг к реализации нашего общего видения справедливости вакцин, но это только начало.
предстоит проделать большую работу с правительствами и производителями, чтобы обеспечить вакцинацию медицинских работников и пожилых людей во всех странах в течение первых 100 дней этого года ».
Д-р Ричард Хэтчетт, генеральный директор CEPI, сказал:« Это знаменательный момент в наших усилиях по распространению жизненно важной вакцины.Тот факт, что теперь у нас есть несколько безопасных и эффективных вакцин против COVID-19, разработанных в рекордно короткие сроки, свидетельствует о том, что
научное сообщество и промышленность принимают вызов этой пандемии. Этой поставкой мы также видим, как мировое сообщество с помощью COVAX решает задачу доставки этих вакцин тем, кто в них больше всего нуждается. Давайте праздновать
это как момент глобальной солидарности в борьбе с пандемией. Но еще многое предстоит сделать. С увеличением распространения вариантов COVID-19 мы вступили в новую и менее предсказуемую фазу пандемии.Очень важно, чтобы вакцины
мы разработали и используются во всем мире в срочном порядке, чтобы снизить распространенность болезней, замедлить вирусные мутации и положить конец пандемии ».
«Сегодняшний день знаменует собой исторический момент, который мы так долго планировали и работали. Получив первую партию доз, мы можем выполнить обещание центра COVAX, чтобы гарантировать, что люди из менее богатых стран не останутся без внимания.
гонка за жизненно важными вакцинами », — сказала Генриетта Фор, исполнительный директор ЮНИСЕФ.«В предстоящие дни рабочие начнут получать вакцины, и может начаться следующий этап борьбы с этой болезнью — наращивание
крупнейшей кампании иммунизации в истории. Каждый шаг на этом пути продвигает нас дальше по пути выздоровления для миллиардов детей и семей, пострадавших во всем мире ».
Вакцины прибыли рейсом из Мумбаи через Дубай, где также была доставлена партия шприцев из запасов, хранящихся в региональном центре снабжения ЮНИСЕФ, финансируемых Гави.
В течение последних нескольких месяцев партнеры COVAX поддерживали правительства и партнеров, особенно участников, имеющих право на AMC, в усилиях по обеспечению готовности к этому моменту. Это включает в себя помощь в разработке вакцинации на национальном уровне.
планы, поддержка инфраструктуры холодовой цепи, а также складирование полумиллиарда шприцев и безопасных ящиков для их утилизации, масок, перчаток и другого оборудования, чтобы обеспечить наличие достаточного количества оборудования для медицинских работников для начала вакцинации
приоритетные группы как можно скорее.
Для того, чтобы дозы были доставлены участникам Учреждения в рамках этого первого раунда распределения, необходимо наличие нескольких важных элементов, включая подтверждение национальных регулирующих критериев авторизации, относящихся к поставленным вакцинам, компенсация
соглашения, национальные планы вакцинации от участников AMC, а также другие логистические факторы, такие как экспортные и импортные лицензии.
По мере того, как участники удовлетворяют вышеуказанным критериям и завершают подготовку к готовности, COVAX будет выдавать производителю заказы на закупку и отправлять и доставлять дозы в итеративном процессе.Это означает, что поставки для этого первого раунда распределения займут
размещать на скользящей основе и траншами.
Основываясь на промежуточном прогнозе распределения, опубликованном ранее в этом месяце, ожидается, что окончательная информация о выделении средств в первом раунде, охватывающая большинство участников Механизма, будет сообщена в ближайшие дни.
Компания COVAX создала разнообразный портфель вакцин, подходящих для различных условий и групп населения, и находится на пути к достижению своей цели по доставке не менее 2 миллиардов доз вакцины в участвующие страны по всему миру в 2021 году, включая как минимум
1.3 миллиарда доз, финансируемых донорами, для 92 участников Фонда с низким доходом при поддержке Gavi COVAX AMC.
Цитаты партнеров и доноров
Президент Еврокомиссии Урсула фон дер Ляйен сказала : «Я очень рад, что сегодня у нас есть первая поставка вакцины COVAX в Аккре, Гана. Настал момент, когда долгие дни и ночи тяжелой работы наконец
показать с ощутимыми результатами на местах. Я хочу воздать должное неустанным усилиям наших партнеров, Гави, ВОЗ и ЮНИСЕФ.Команда Европы продолжит поддерживать народ Африки ».
Премьер-министр Джасинда Ардерн, Новая Зеландия сказала: : «Работа над широким глобальным охватом вакцинами против Covid-19 — это и правильный поступок, и путь к прекращению пандемии. Новая Зеландия признает замечательные
работа ГАВИ, CEPI, ВОЗ и фонда COVAX для достижения этой цели ».
Президент Педро Санчес, Испания сказал : «Испания с самого начала была ядром ACT Accelerator и других международных инициатив по борьбе с вирусом, потому что только шаг за шагом
вверх можем ли мы добиться успеха.Никто не будет в безопасности, пока все не будут в безопасности ».
Сенатор Достопочтенная Мариз Пейн, министр иностранных дел, министр иностранных дел Австралии сказала: : «В этой пандемии мы знаем, что никто не в безопасности, пока мы все а также
эффективные вакцины против COVID 19. Распространяя первые дозы, Австралия с гордостью поддерживает рыночные обязательства COVAX Advance, поскольку они обеспечивают доступ к вакцинам, которые защитят наиболее уязвимых людей в мире.
Бельгийский министр по сотрудничеству в целях развития Мерьям Китир приветствует поставку первых доз вакцины с помощью Центра Covax в Африке: «Это отличная новость. Бельгия поддерживает COVAX AMC, потому что это позволяет
ряд стран получить доступ к вакцинам от COVID-19. Я надеюсь, что это начало быстрого развертывания для достижения цели — в этом году доставить 2 миллиарда доз в страны-участницы по всему миру ».
Карина Гулд, министр международного развития правительства Канады и сопредседатель Gavi COVAX AMC сказала: : «Канада поддерживала механизм COVAX с самого начала.Он объединит страны, независимо от того,
уровень доходов, чтобы ускорить разработку, производство и распространение вакцин против COVID-19. Сегодня мы празднуем начало доставки COVAX в Гану первых вакцин. Это приближает нас на один шаг к достижению покрытия для
все группы высокого риска, включая медицинских работников, во всем мире. Это действительно веха для всех нас ».
Французский министр по делам Европы и иностранных дел Жан-Ив Ле Дриан сказал: «Франция приветствует первые поставки доз вакцины против Covid-19 в Африку благодаря центру COVAX, сегодня в Гане и в пятницу на Кот-д’И. Ивуар.Этот
является первым конкретным результатом, подтверждающим центральную важность ACT-A, ключевой международной платформы для равноправного и всеобщего доступа к вакцинам против Covid-19, которую Франция помогла запустить вместе с Европейской комиссией и ВОЗ весной.
2020 г., чтобы координировать глобальные ответные меры на пандемию. Мы должны продолжить эти усилия международной солидарности, создав, как это было предложено Президентом Республики, механизмы разделения доз, которые могли бы ускорить распространение
вакцины в Африке.
Ретно Марсуди, министр иностранных дел Индонезии и сопредседатель Gavi COVAX AMC сказал: : «Я воодушевлен значительным прогрессом, достигнутым Фондом COVAX в обеспечении равного доступа к вакцинам. Это первое прибытие
вакцины показывают, что глобальная солидарность и многосторонность работают и приносят результаты. Как один из сопредседателей AMC Group, я приветствую это важное достижение. Я настоятельно призываю все страны обеспечить больший доступ и убедиться, что никто не останется позади.»
Алессандро Ривера, генеральный директор казначейства Министерства экономики и финансов Италии сказал: «Италия рада видеть, что COVAX в ближайшие дни начнет внедрение вакцины в странах, отвечающих критериям AMC. Это ориентир
событие, поскольку мы успешно позволили беднейшим странам получить доступ к безопасной и эффективной вакцине в течение нескольких месяцев после их утверждения в странах с высоким уровнем дохода. Италия поддерживает COVAX AMC с момента его создания в июне 2020 года и обещает на сегодняшний день
более 100 миллионов долларов США.Наша цель — продолжать инвестировать в многосторонность, международное сотрудничество и солидарность, и в качестве нынешнего председательства в «Группе двадцати» мы гарантируем, что эти темы останутся в центре глобальных дебатов ».
Кейити ОНО, посол Японии по глобальным вопросам сказал: : «Мы приветствуем начало доставки вакцин через механизм COVAX как важный первый шаг. С момента запуска объекта COVAX последний
Июнь, Япония вносит свой вклад в разработку беспрецедентного механизма и финансирование AMC.Япония привержена поддержке обеспечения равного доступа к безопасным, эффективным вакцинам гарантированного качества ».
Пер Ольссон Фрид, министр международного сотрудничества Швеции, Швеция сказал: «Сегодня обнадеживающий день в борьбе с разрушительной пандемией и многообещающий день для многостороннего сотрудничества. Швеция остается твердо
привержены справедливому глобальному доступу к безопасным и эффективным вакцинам ».
Министр иностранных дел Доминик Рааб, Соединенное Королевство сказал: : «Сегодняшнее развертывание вакцин в наиболее уязвимых странах мира — огромный шаг вперед в прекращении этой пандемии.Как один из крупнейших доноров
для COVAX Великобритания гарантирует, что более одного миллиарда доз вакцины будет отправлено в 92 страны, чтобы никто не остался позади в этой глобальной борьбе. Мы спасем жизни и снизим риск заражения в будущем, только если предотвратим распространение вируса.
в развивающихся странах мира ».
Д-р Джон Нкенгасонг, директор Африканских центров по контролю и профилактике заболеваний сказал: : «Эти первые поставки вакцины COVID-19 через COVAX являются критическим моментом в борьбе Африки с вирусом.Благодаря этому
Благодаря глобальному сотрудничеству дополнительные члены ключевых групп, такие как медицинские работники и другие уязвимые группы, получат доступ к вакцинам против COVID-19 в ближайшие недели. Это важный шаг на пути к нашей континентальной цели — иммунизации не менее 60%.
населения Африки безопасными и эффективными вакцинами против COVID-19, чтобы снизить нагрузку на наши системы здравоохранения и экономику и продолжить нашу работу в направлении нашей повестки дня континентального развития ».
Томас Куени, генеральный директор, Международная фармацевтическая федерация Производители и ассоциации (IFPMA) заявили: : «Впервые в истории пандемий у вас будут вакцины.
скоординировано внедрено в СНСУД менее чем за три месяца после того, как ВОЗ получила разрешение на реализацию самой первой вакцины против Covid.Подобно тому, как увеличение производства с нуля до миллионов за считанные месяцы является историческим
достижения, переход к последней миле — важная веха, которую следует отметить. Производители были среди партнеров-учредителей ACT-A и COVAX. Мы в полной мере сыграли свою роль не только в увеличении масштабов производства благодаря удивительному количеству сотрудничества.
но также и в достижении общей цели справедливого и равноправного доступа к вакцинам. Но будут проблемы, будь то производство или доставка.Мы должны работать вместе, чтобы найти решения. Вот как мы дошли до такого
короткое время. Указывать пальцем и выделять производителей, которые не выполняют поставку, будет контрпродуктивным ».
Примечания для редакторов
Список пожертвований Gavi COVAX AMC доступен здесь.
О COVAX
COVAX, основа вакцины в ускорителе доступа к инструментам COVID-19 (ACT), возглавляется
Коалиция за инновации в обеспечении готовности к эпидемиям (CEPI), Гави, Альянс вакцин Гави) и Всемирная организация здравоохранения (ВОЗ) — работая в партнерстве с производителями вакцин в развитых и развивающихся странах, ЮНИСЕФ, Всемирным банком,
и другие.Это единственная глобальная инициатива, которая работает с правительствами и производителями для обеспечения доступности вакцин против COVID-19 во всем мире как для стран с более высоким, так и для стран с низким уровнем доходов.
CEPI фокусируется на портфеле исследований и разработок вакцины COVAX: инвестирование в исследования и разработки различных многообещающих кандидатов с целью поддержки разработок
трех безопасных и эффективных вакцин, которые могут быть предоставлены странам, участвующим в программе COVAX. В рамках этой работы CEPI заручился первым правом отказа от потенциально более одного миллиарда доз для установки COVAX ряду
кандидатов и осуществили стратегические инвестиции в производство вакцин, включая резервирование мощностей для производства доз вакцины COVAX в сети предприятий и обеспечение стеклянных флаконов для хранения 2 миллиардов доз вакцины.CEPI также
инвестирование в вакцины-кандидаты «следующего поколения», которые предоставят миру дополнительные возможности для борьбы с COVID-19 в будущем.
Гави занимается закупками и доставкой для COVAX: координирует проектирование, внедрение и администрирование объектов COVAX и Gavi.
COVAX AMC и работа со своими партнерами по Альянсу — ЮНИСЕФ и ВОЗ, а также правительствами над готовностью и доставкой в странах. Объект COVAX — это
глобальный механизм объединенных закупок вакцин против COVID-19, с помощью которого COVAX обеспечит справедливый и равноправный доступ к вакцинам для всех 190 стран-участниц, используя структуру распределения, сформулированную ВОЗ.Центр COVAX сделает это
путем объединения покупательной способности стран-участниц и предоставления гарантий объемов для ряда перспективных вакцин-кандидатов. Gavi COVAX AMC — это механизм финансирования, который поддержит участие 92 стран с низким и средним уровнем дохода.
в Учреждении, обеспечивая доступ к дозам безопасных и эффективных вакцин, финансируемых донорами. Гави занимается сбором средств для COVAX AMC и финансирует закупку вакцин ЮНИСЕФ, а также работу партнеров и правительств по обеспечению готовности и доставке, в том числе
поддержка оборудования холодовой цепи, технической помощи, шприцев, транспортных средств и других аспектов чрезвычайно сложной логистической операции по доставке.ЮНИСЕФ и Панамериканская организация здравоохранения (ПАОЗ) будут действовать в качестве координаторов закупок для
COVAX Facility, помогая доставлять вакцины участникам COVAX AMC и другим лицам.
ВОЗ выполняет несколько функций в рамках COVAX: она обеспечивает нормативное руководство по политике в отношении вакцин, регулированию, безопасности, НИОКР, распределению, а также готовности страны и доставке. Его Стратегическая консультативная группа экспертов (SAGE) по иммунизации разрабатывает научно обоснованные рекомендации по политике иммунизации. Перечень использования в чрезвычайных ситуациях (EUL) / программы предварительной квалификации обеспечивают:
согласованный обзор и авторизация в государствах-членах.Он обеспечивает глобальную координацию и поддержку государств-членов в области мониторинга безопасности вакцин. Он разработал профили целевых продуктов для вакцин COVID-19 и обеспечивает техническую координацию исследований и разработок. КТО
вместе с ЮНИСЕФ возглавляет направление работы по обеспечению готовности и доставки в стране, которое оказывает поддержку странам в их подготовке к получению и введению вакцин. Вместе с Гави и множеством других партнеров, работающих на глобальном, региональном и национальном уровнях,
рабочий поток CRD предоставляет инструменты, руководство, мониторинг и техническую помощь на местах для планирования и внедрения вакцин.Вместе с партнерами COVAX ВОЗ разработала схему компенсации без сбоев, поскольку
часть обязательств по возмещению убытков и ответственности с ограниченным сроком действия.
ЮНИСЕФ использует свой опыт в качестве крупнейшего единственного покупателя вакцин в мире и работает с производителями и партнерами в вопросах закупки доз вакцины COVID-19, а также транспортировки, логистики и хранения. ЮНИСЕФ уже закупил более
2 миллиарда доз вакцин ежегодно для плановой иммунизации и реагирования на вспышки болезней почти в 100 странах.В сотрудничестве с Оборотным фондом ПАОЗ,
ЮНИСЕФ возглавляет усилия по закупке и поставке доз вакцины COVID-19 от COVAX.
Кроме того, ЮНИСЕФ, Гави и ВОЗ круглосуточно работают с правительствами, чтобы обеспечить готовность стран к получению вакцин, наличие соответствующего оборудования холодовой цепи и обученных медицинских работников для их выдачи. ЮНИСЕФ также
играть ведущую роль в усилиях по укреплению доверия к вакцинам, распространению информации о доверии к вакцинам, отслеживанию и устранению дезинформации по всему миру.
О CEPI
CEPI — это инновационное партнерство между государственными, частными, благотворительными и гражданскими организациями, начатое в Давосе в 2017 году с целью разработки вакцин для остановки будущих эпидемий. CEPI начал действовать в срочном порядке и в координации с ВОЗ в ответ на
появление COVID-19. CEPI инициировал десять партнерств для разработки вакцин против нового коронавируса. В программах используются платформы быстрого реагирования, уже поддерживаемые CEPI, а также новые партнерства.
До появления COVID-19 приоритетными заболеваниями CEPI были вирус Эбола, вирус Ласса, коронавирус ближневосточного респираторного синдрома, вирус Нипах, лихорадка Рифт-Валли и вирус Чикунгунья. CEPI также инвестировала в платформенные технологии, которые могут
использоваться для быстрой разработки вакцины и иммунопрофилактики против неизвестных патогенов (болезнь X).
О Гави
Гави, Vaccine Alliance — это государственно-частное партнерство, которое помогает вакцинировать половину детей в мире от некоторых из самых смертоносных болезней в мире.С момента своего создания в 2000 году Гави помог иммунизировать целое поколение — более
822 миллиона детей — и предотвращено более 14 миллионов смертей, что помогло снизить вдвое детскую смертность в 73 развивающихся странах. Гави также играет ключевую роль в повышении безопасности глобального здравоохранения, поддерживая системы здравоохранения, а также финансируя глобальные
запасы вакцин против Эболы, холеры, менингита и желтой лихорадки. После двух десятилетий прогресса Гави теперь сосредоточен на защите следующего поколения и охвате невакцинированных детей, которые все еще остаются позади, с использованием инновационных финансовых средств.
и новейшие технологии — от дронов до биометрии — чтобы спасти еще миллионы жизней, предотвратить вспышки до того, как они распространятся, и помочь странам на пути к самоокупаемости.Узнайте больше на www.gavi.org и свяжитесь с нами в Facebook и Twitter.
Vaccine Alliance объединяет правительства развивающихся стран и стран-доноров, Всемирную организацию здравоохранения, ЮНИСЕФ, Всемирный банк, индустрию вакцин, технические агентства, гражданское общество, Фонд Билла и Мелинды Гейтс и другие частные лица.
отраслевые партнеры. Посмотреть полный список правительств-доноров и других ведущих организаций, финансирующих работу Гави, можно здесь.
О ВОЗ
Всемирная организация здравоохранения обеспечивает глобальное лидерство в области общественного здравоохранения в рамках системы Организации Объединенных Наций.Основанная в 1948 году, ВОЗ работает с 194 государствами-членами в шести регионах и из более чем 150 офисов в целях укрепления здоровья, обеспечения безопасности во всем мире и
служить уязвимым. Наша цель на 2019–2023 годы — обеспечить всеобщий охват услугами здравоохранения еще на миллиард человек, защитить еще один миллиард людей от чрезвычайных ситуаций в области здравоохранения и улучшить здоровье и благополучие еще одного миллиарда человек.
Для получения обновленной информации о COVID-19 и рекомендаций по защите здоровья от коронавируса посетите веб-сайт www.who.int и
подписывайтесь на ВОЗ в Twitter, Facebook, Instagram, LinkedIn, TikTok, Pinterest, Snapchat, YouTube
О ЮНИСЕФ
ЮНИСЕФ работает в некоторых из самых сложных уголков мира, чтобы охватить самых обездоленных детей. В 190 странах и территориях мы работаем для каждого ребенка и повсюду, чтобы построить лучший мир для всех. Для большего
информацию о ЮНИСЕФ и его работе для детей посетите www.unicef.org. Для получения дополнительной информации о COVID-19 посетите www.unicef.org/coronavirus. Узнайте больше о работе ЮНИСЕФ над вакцинами COVID-19 здесь или о работе ЮНИСЕФ по иммунизации здесь.
Следите за сообщениями ЮНИСЕФ в Twitter и Facebook.
О ACT-Accelerator
Доступ к инструментам COVID-19 ACT-Accelerator — это новое революционное глобальное сотрудничество для ускорения разработки, производства и равноправного доступа к тестам и лечению COVID-19 , и вакцины. Создан в ответ на призыв лидеров G20.
в марте и запущен ВОЗ, Европейской комиссией, Франция и Фондом Билла и Мелинды Гейтс в апреле 2020 года.
ACT-Accelerator не является органом, принимающим решения, или новой организацией, но работает для ускорения совместных усилий существующих организаций по прекращению пандемии. Это структура для сотрудничества, которая была разработана, чтобы объединить ключевых игроков
таблица с целью как можно быстрее положить конец пандемии за счет ускоренной разработки, справедливого распределения и увеличения масштабов предоставления тестов, лечения и вакцин, тем самым защищая системы здравоохранения и восстанавливая общества и
экономики в ближайшей перспективе.Он основан на опыте ведущих мировых организаций здравоохранения, которые решают самые сложные мировые проблемы в области здравоохранения и которые, работая вместе, могут достичь новых и более амбициозных результатов в борьбе с ними.
COVID-19. Его члены разделяют обязательство обеспечить всем людям доступ ко всем инструментам, необходимым для победы над COVID-19, и работать с беспрецедентным уровнем партнерства для его достижения.
ACT-Accelerator имеет четыре области работы: диагностика, лечение, вакцины и соединитель системы здравоохранения.Все это пересекается с рабочим потоком по доступу и размещению.
Пакистан одобрил китайскую вакцину CanSinoBIO COVID для экстренного использования
ИСЛАМАБАД (Рейтер) — Пакистан в пятницу одобрил китайскую вакцину CanSino Biologics Inc (CanSinoBIO) COVID-19 для экстренного использования, заявил министр здравоохранения Фейсал Султан, четвертый кандидат, утвержденный в Южноазиатская страна с 220 миллионами жителей.
ФОТОГРАФИЯ: Логотип китайского специалиста по вакцинам CanSino Biologics Inc изображен в Тяньцзине, Китай, 17 августа 2020 года.REUTERS / Thomas Peter / File Photo
Пакистан, в значительной степени полагающийся на инициативу ГАВИ / ВОЗ COVAX для бедных стран, также разрешил частным компаниям импортировать вакцины против коронавируса и согласился освободить такой импорт от ценовых ограничений.
«Да, правильно», — написал Султан Рейтер, когда его спросили, одобрило ли Управление по регулированию лекарственных средств вакцину.
Китайские Sinopharm, AstraZeneca и российский Sputnik V также получили разрешение.
Пакистан — вторая страна, одобрившая CanSinoBio после Мексики.
Мексика подписала соглашение с CanSino на поставку не менее 8 миллионов доз. Пакистан, по словам Султана, может получить «десятки миллионов» доз.
CanSinoBIO на прошлой неделе опубликовал промежуточные результаты исследования эффективности в многострановых испытаниях, в которых участвовал Пакистан, которые показали эффективность 65,7% в предотвращении симптоматических случаев коронавируса и 90,98% успеха в остановке тяжелых инфекций.
В пакистанской подгруппе эффективность вакцины CanSinoBIO в предотвращении симптоматических случаев составила 74.8% и 100% при предотвращении тяжелого заболевания.
Решение разрешить коммерческий импорт вакцины с освобождением от верхнего предела цен вызвало критику.
«Этот шаг усугубит неравенство в обществе в то время, когда существует потребность в широком охвате», — сказал Рейтер бывший министр здравоохранения Зафар Мирза.

