Асфиксия новорожденного: особенности заболевания и лечение
Асфиксия новорожденного – патологическое, угрожающее жизни ребенка состояние, характеризующееся ослабленным дыханием или его полным отсутствием при сохраненной сердечной деятельности. Возникает как следствие расстройства газообмена.
Такую патологию диагностируют у 5 – 6 % всех новорожденных детей.
Асфиксия новорожденных: причины
Это патологическое состояние является синдромом, который развивается из-за наличия проблем и болезней во время беременности.
Существует 2 вида асфиксии:
- Первичная – возникает сразу после появления ребенка на свет. Ее причиной является кислородное голодание плода еще во время внутриутробного развития. Оно может быть острым и хроническим. Также причиной может быть наличие инфекционного заболевания плода (герпетическая инфекция, краснуха, хламидиоз и другие), резус – несовместимость матери и плода, аспирация слизью или околоплодными водами.
 Это приводит к тому, что легкие младенца или не раскрыты полностью, или не раскрыты вообще.
Это приводит к тому, что легкие младенца или не раскрыты полностью, или не раскрыты вообще. - Вторичная — развивается через несколько дней после рождения. Развивается, как правило, из-за нарушения мозгового кровообращения плода. К этому могут привести заболевания матери, протекающие во время беременности (анемия, болезни сердца, сахарный диабет, инфекционные заболевания) и тяжелый акушерский анамнез (токсикоз, преждевременное отслоение плаценты, осложнения во время родов).
Патогенез асфиксии лежит в нарушении метаболизма и гемодинамики. Степень тяжести асфиксии зависит от длительности и интенсивности кислородного голодания. Недостаток кислорода приводит к развитию метаболического ацидоза, гипогликемии и гипокалиемии. Острая форма асфиксии приводит к увеличению объема циркулирующей крови, хроническая – к уменьшению. Эти состояния приводят к сгущению крови, и в дальнейшем – проблемам с почками, сердцем, работой головного мозга, печенью, надпочечниками. Все эти последствия развивают огромное количество последствий.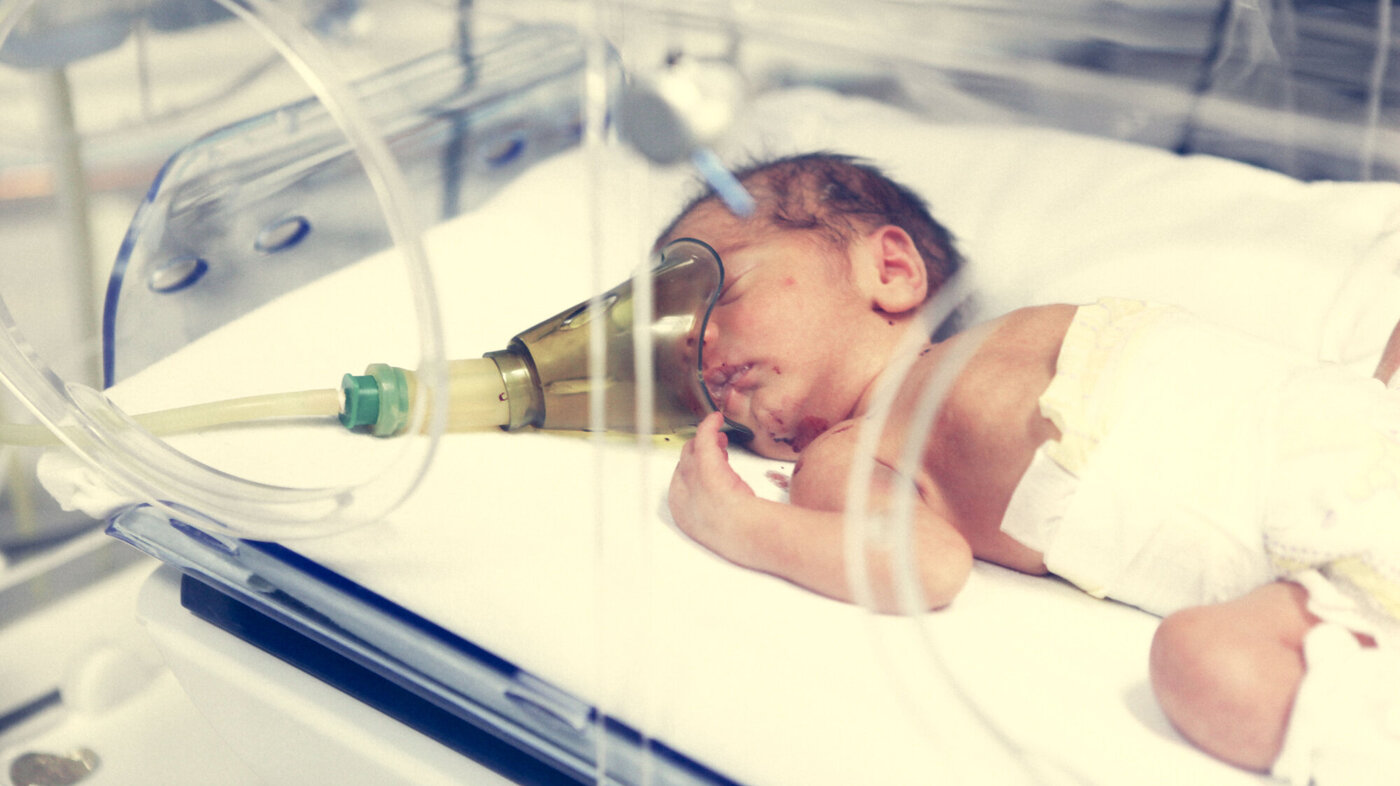
Симптомы
Основные клинические проявления асфиксии новорожденного оцениваются по шкале Апгар. Она включает в себя оценку цвета кожных покровов, частоту сердечных сокращений, рефлексы, мышечный тонус и дыхание. Оценка данных критериев происходит в первые минуты жизни новорожденного ребенка при помощи 10- балльной шкалы. В зависимости от количества набранных баллов существует 3 стадии асфиксии:
- Легкая асфиксия – 10 – 7 баллов по шкале Апгар: ослабленное дыхание, присутствует цианоз носогубного треугольника, мышцы в сниженном тонусе, кожные покровы не изменены.
- Асфиксия средней тяжести – 5 – 7 баллов по шкале Апгар: регулярное и нерегулярное дыхание ослабленное, крик слабый, брадикардия, мышечный тонус и рефлексы ослаблены, кожные покровы покрыты легкой синюшностью.
- Тяжеля асфиксия – 4 – 1 балл по шкале Апгар: крик отсутствует, дыхание нерегулярное или вообще отсутствует (апноэ), сердцебиение редкое, гипотония мышц, рефлексы отсутствуют. Это считается состоянием клинической смерти новорожденного.
 Эта угрожающая жизни стадия может привести к нарушению функций головного мозга или к летальному исходу.
Эта угрожающая жизни стадия может привести к нарушению функций головного мозга или к летальному исходу.
Диагностика
Проводится быстрый и точный осмотр ребенка, измерение уровня кислорода в крови при помощи пульсоксиметрии, оценка его состояния по шкале Апгар. Проводится исследование кислотно – основного состояния крови, которое покажет ацидоз, что и будет подтверждением асфиксии.
После этого дополнительно проводятся исследования, которые покажут, к каким нарушениям привела имеющая место асфиксия: неврологический осмотр, УЗД головного мозга на наличие изменений ткани мозга и кровоизлияний.
Обследованием ребенка занимается неонатолог или детский реаниматолог. Они могут быстро оценить состояние ребенка и принять меры для устранения проблемы.
Асфиксия новорожденных: неотложная помощь
Экстренная медицинская помощь заключается в восстановлении самостоятельного дыхания, нормализации сердечной деятельности, устранении метаболизма и коррекции гемодинамических показателей.
Комплекс реанимационных мероприятий состоит из:
- Отсасывание слизи из верхних дыхательных путей.
- Если дыхание не восстановилось – тактильная стимуляция: хлопанье по пяткам или вдоль спины. Это может рефлекторно, воздействием на нервные корешки спинного мозга, восстановить спонтанное дыхание.
- Если эффект не наступил — ребенку проводят 5 спасательных вдохов при помощи кислородной маски и мешка Амбу. Их суть состоит в том, что кислород, попавший в легкие при таких вдохах, действует на рецепторы в легких, которые посылают импульсы в центр дыхания о том, то есть кислород. Центр дыхательной деятельности начинает посылать импульсы в легкие. Это также может привести к возвращению дыхания.
- Если и это безуспешно – ребенка интубируют и подключают к аппарату ИВЛ.
- Далее проводится оценка сердечной деятельности и подключение ребенка к мониторам. Если ЧСС 60 – 70 ударов в минуту (при норме 140 – 160) – проводится закрытый массаж сердца со скоростью 100 – 120 ударов в минуту (при подключенном аппарате ИВЛ; если он не подключен – проводится 30 компрессий грудной клетки и 2 вдоха (это также должно составлять 100 – 120 компрессий в минуту).

- Лекарственные препараты новорожденным детям вводят в пупочную вену – Адреналин, Натрия Гидрокарбонат, Глюкоза. Препараты рассчитывают на 1 кг массы тела.
Реанимационные мероприятия проводятся прямо в родильном зале. Они проводятся при тяжелом состоянии ребенка и малом количестве баллов по шкале Апгар. Реанимация продолжается 30 минут до появления признаков самостоятельного дыхания и улучшения состояния и показателей монитора или признаков биологической смерти. Если реанимация успешная — ребенок переводится в палату интенсивной терапии под наблюдение врачей.
Если асфиксия легкой или средней степени тяжести — ребенок через маску получает кислород, или его помещают в кислородную камеру.
Асфиксия новорожденных: лечение
В палате интенсивной терапии ребенку назначаются антибиотики, витамины, парентеральное кормление, проводится инфузионная терапия, обеспечивается покой до полного выздоровления. После этого проводится неврологический осмотр, который покажет изменения со стороны центральной нервной системы, нанесенные ребенку асфиксией.
Асфиксия новорожденных: последствия
Ранние осложнения:
- Отек головного мозга.
- Кровоизлияния в мозг или оболочки.
- Некрозы отдельных участков головного мозга.
Поздние последствия:
- Гидроцефалия – наличие лишней воды в головном мозге.
- Энцефалопатия – невоспалительные процессы в головном мозге.
- Инфекционные осложнения – энцефалит, менингит, пневмония, сепсис.
Кислородное голодание может привести к отставанию в развитии, судорожным припадкам, гибели ребенка. Это развивается в первый год жизни ребенка.
Асфиксия новорожденного — причины, симптомы, диагностика и лечение
Асфиксия новорожденного – это патология раннего неонатального периода, обусловленная нарушением дыхания и развитием гипоксии у родившегося ребенка. Асфиксия новорожденного клинически проявляется отсутствием самостоятельного дыхания ребенка в первую минуту после рождения либо наличием отдельных, поверхностных или судорожных нерегулярных дыхательных движений при сохранной сердечной деятельности. Новорожденные с асфиксией нуждаются в проведении реанимационных мероприятий. Прогноз при асфиксии новорожденного зависит от тяжести патологии, своевременности и полноты оказания лечебных мероприятий.
Новорожденные с асфиксией нуждаются в проведении реанимационных мероприятий. Прогноз при асфиксии новорожденного зависит от тяжести патологии, своевременности и полноты оказания лечебных мероприятий.
Общие сведения
Из общего количества новорожденных асфиксия диагностируется у 4-6% детей. Тяжесть асфиксии обусловлена степенью нарушения газообмена: накопления углекислоты и недостатка кислорода в тканях и крови новорожденного. По времени развития асфиксия новорожденных бывает первичной (внутриутробной) и вторичной (внеутробной), возникшей в первые сутки после рождения. Асфиксия новорожденных является грозным состоянием и служит одной из частых предпосылок мертворождения или неонатальной смертности.
Асфиксия новорожденного
Причины
Асфиксия новорожденных является синдромом, развивающимся вследствие нарушения течения беременности, заболеваний матери и плода. Первичная асфиксия новорожденного обычно связана с хронической или острой внутриутробной недостаточностью кислорода, обусловленной внутричерепными травмами, внутриутробными инфекциями (краснуха, цитомегаловирус, сифилис, токсоплазмоз, хламидиоз, герпес и др. ), иммунологической несовместимостью крови матери и плода, пороками развития плода, частичной или полной обтурацией дыхательных путей новорожденного околоплодными водами или слизью (асфиксия аспирационная).
), иммунологической несовместимостью крови матери и плода, пороками развития плода, частичной или полной обтурацией дыхательных путей новорожденного околоплодными водами или слизью (асфиксия аспирационная).
Развитию асфиксии новорожденного способствует наличие экстрагенитальной патологии у беременной (анемии, пороков сердца, заболеваний легких, тиреотоксикоза, сахарного диабета, инфекций), а также отягощенного акушерского анамнеза (позднего токсикоза, преждевременной отслойки плаценты, перенашивания беременности, осложненных родов), вредных привычек у матери. Причинами вторичной асфиксии новорожденного, как правило, служат нарушения мозгового кровообращения ребенка или пневмопатии. Пневмопатии являются перинатальными неинфекционными заболеваниями легких, обусловленными неполным расправлением легочной ткани; проявляются ателектазами, отечно-геморрагическим синдромом, болезнью гиалиновых мембран.
Патогенез
Независимо от этиологии дыхательных расстройств при асфиксии новорожденного, в его организме развиваются патогенетически одинаковые нарушения метаболизма, микроциркуляции и гемодинамики. Степень тяжести асфиксии новорожденного определяется длительностью и интенсивностью гипоксии. При недостатке кислорода происходит развитие респираторно-метаболического ацидоза, характеризующегося азотемией, гипогликемией, гиперкалиемией (затем гипокалиемией). При дисбалансе электролитов нарастает клеточная гипергидратация.
Степень тяжести асфиксии новорожденного определяется длительностью и интенсивностью гипоксии. При недостатке кислорода происходит развитие респираторно-метаболического ацидоза, характеризующегося азотемией, гипогликемией, гиперкалиемией (затем гипокалиемией). При дисбалансе электролитов нарастает клеточная гипергидратация.
Острая асфиксия новорожденных характеризуется возрастанием объема циркулирующей крови за счет эритроцитов; асфиксия, протекающая на фоне хронической гипоксии – гиповолемией. Это приводит к сгущению крови, увеличению ее вязкости, повышению агрегации тромбоцитов и эритроцитов. При таких микроциркуляторных сдвигах у новорожденного страдают головной мозг, почки, сердце, надпочечники, печень, в тканях которых развиваются отек, ишемия, кровоизлияния, гипоксия. В итоге возникают нарушения центральной и периферической гемодинамики, снижается ударный и минутный объем выброса, падает АД.
Клиника асфиксии новорожденного
Определяющими критериями асфиксии новорожденного являются дыхательные расстройства, ведущие к нарушению гемодинамики, сердечной деятельности, мышечного тонуса и рефлексов. По тяжести проявлений в акушерстве и гинекологии различают 3 степени асфиксии новорожденных с оценкой в баллах по 10-балльной шкале (методике) Апгар в течение первой минуты после рождения: 6-7 баллов – легкая асфиксия, 4-5 баллов – средняя и 1-3 балла – тяжелая асфиксия. Оценка по шкале Апгар 0 баллов расценивается как клиническая смерть. Критериями оценки тяжести асфиксии новорожденных служат сердцебиение, дыхание, окраска кожи, выраженность тонуса мышц и рефлекторной возбудимости (пяточного рефлекса).
По тяжести проявлений в акушерстве и гинекологии различают 3 степени асфиксии новорожденных с оценкой в баллах по 10-балльной шкале (методике) Апгар в течение первой минуты после рождения: 6-7 баллов – легкая асфиксия, 4-5 баллов – средняя и 1-3 балла – тяжелая асфиксия. Оценка по шкале Апгар 0 баллов расценивается как клиническая смерть. Критериями оценки тяжести асфиксии новорожденных служат сердцебиение, дыхание, окраска кожи, выраженность тонуса мышц и рефлекторной возбудимости (пяточного рефлекса).
При легкой степени асфиксии первый вдох новорожденный делает на первой минуте после рождения, у ребенка выслушивается ослабленное дыхание, выявляется акроцианоз, цианоз носогубной области, сниженный мышечный тонус. Асфиксия новорожденного средней тяжести характеризуется вдохом на первой минуте, ослабленным регулярным или нерегулярным дыханием, слабым криком, брадикардией, сниженным мышечным тонусом и рефлексами, синюшностью кожи лица, стоп и кистей, пульсацией пуповины.
Тяжелой асфиксии новорожденных соответствует нерегулярное дыхание либо апноэ, отсутствие крика, редкое сердцебиение, арефлексия, атония или выраженная гипотония мышц, бледность кожи, отсутствие пульсации пуповины, развитие надпочечниковой недостаточности. В первые сутки жизни у новорожденных с асфиксией может развиваться постгипоксический синдром, проявляющийся поражением ЦНС — нарушением мозгового кровообращения и ликвородинамики.
Диагностика
Асфиксия диагностируется в первую минуту жизни новорожденного с учетом наличия, частоты и адекватности дыхания, показателей сердцебиения, мышечного тонуса, рефлекторной возбудимости, окраски кожи. Кроме внешнего осмотра и оценки тяжести состояния новорожденного по шкале Апгар, диагноз асфиксии подтверждается исследованием кислотно-основного состояния крови.
Методы неврологического обследования и УЗИ головного мозга (ультрасонография) направлены на дифференцирование гипоксического и травматического повреждения ЦНС (обширных субдуральных, субарахноидальных, внутрижелудочковых кровоизлияний и др. ). Для новорожденных с гипоксическим поражением ЦНС характерно отсутствие очаговой симптоматики и повышенная нервно-рефлекторная возбудимость (при тяжелой асфиксии — угнетение ЦНС).
). Для новорожденных с гипоксическим поражением ЦНС характерно отсутствие очаговой симптоматики и повышенная нервно-рефлекторная возбудимость (при тяжелой асфиксии — угнетение ЦНС).
Лечение
Новорожденные с асфиксией нуждаются в экстренном реанимационном пособии, направленном на восстановление дыхательной функции и сердечной деятельности, коррекции расстройств гемодинамики, метаболизма, электролитного обмена.
При асфиксии новорожденного легкой и средней тяжести производится аспирация содержимого из носоглотки, полости рта и желудка; вспомогательная вентиляция легких масочным способом; введение в пуповинную вену 20% раствора глюкозы и кокарбоксилазы по весу. Если при асфиксии новорожденного средней тяжести спонтанное дыхание после проведенных мероприятий не восстановилось, производится интубация трахеи, аспирация содержимого из дыхательных путей, налаживается аппаратная ИВЛ. Дополнительно внутривенно вводится раствор натрия гидрокарбоната.
Тяжелая асфиксия новорожденных также требует проведения ИВЛ, при брадикардии или асистолии – непрямого массажа сердца, введения глюкозы, кокарбоксилазы, преднизолона (гидрокортизона), адреналина, глюконата кальция. Реанимация недоношенных новорожденных с асфиксией несколько отличается от схемы реанимационных мероприятий у доношенных детей.
В дальнейшем новорожденные, перенесшие асфиксию, требуют интенсивного наблюдения и терапии: кислородной поддержки, краниоцеребральной гипотермии, инфузии растворов, витаминов, симптоматического лечения. Новорожденные с легкой асфиксией помещаются в кислородную палатку; со средней и тяжелой – в кувез. Вопрос о кормлении и его методах решается, исходя из состояния новорожденного. После выписки из роддома ребенку, перенесшему асфиксию, требуется наблюдение невролога.
Прогноз при асфиксии
Ближайший и отдаленный прогноз определяется тяжестью асфиксии новорожденного, полнотой и своевременностью лечебного пособия. Для оценки прогноза первичной асфиксии производится оценка состояния новорожденного по показателям шкалы Апгар через 5 минут после рождения. При возросшей оценке прогноз для жизни рассматривается как благоприятный. На первом году жизни у детей, родившихся в асфиксии, нередко отмечаются синдромы гипер- и гиповозбудимости, гипертензионно-гидроцефальная или судорожная перинатальная энцефалопатия, диэнцефальные (гипоталамические) нарушения. У части детей возможен летальный исход от последствий асфиксии.
Для оценки прогноза первичной асфиксии производится оценка состояния новорожденного по показателям шкалы Апгар через 5 минут после рождения. При возросшей оценке прогноз для жизни рассматривается как благоприятный. На первом году жизни у детей, родившихся в асфиксии, нередко отмечаются синдромы гипер- и гиповозбудимости, гипертензионно-гидроцефальная или судорожная перинатальная энцефалопатия, диэнцефальные (гипоталамические) нарушения. У части детей возможен летальный исход от последствий асфиксии.
Профилактика
В наше время акушерство и гинекология уделяют большое внимание осуществлению эффективных мер профилактики патологии новорожденных, в том числе и асфиксии новорожденных. Меры по предупреждению развития асфиксии новорожденного включают своевременную терапию экстрагенитальных заболеваний у беременной, ведение беременности с учетом имеющихся факторов риска, проведение внутриутробного мониторинга состояния плаценты и плода (допплерографии маточно-плацентарного кровотока, акушерского УЗИ).
Профилактикой должна заниматься и сама женщина, отказавшись от вредных привычек, соблюдая рациональный режим, выполняя предписания акушера-гинеколога. Профилактика асфиксии новорожденного во время родов требует оказания грамотного акушерского пособия, предупреждения гипоксии плода в родах, освобождения верхних дыхательных путей ребенка сразу после его рождения.
Профилактика асфиксии новорожденных
Будьте бдительны! Профилактика удушья у новорожденных
С пугающей периодичностью в СМИ проявляются сообщения о неосторожном удушении грудных детей. Чаще всего причиной трагедии является перекрытие дыхательных путей телом мамы, как правило, во сне при несоблюдении правил безопасности. Зафиксированы такие случаи и в Нягани. Впрочем, несчастный случай (асфиксия) возможен и при неправильно кормлении ребенка или недогляде при играх с мелкими предметами. НАДО ЗНАТЬ, что новорожденные дети не умеют дышать ртом в течение первых шести месяцев. Потому так важно следит за тем, чтобы его носик всегда находился «в свободном доступе»
Потому так важно следит за тем, чтобы его носик всегда находился «в свободном доступе»
Причины асфиксии:
1. Частые срыгивания и поперхивание, приводящие к попаданию молока (пищи) не в пищевод ребенка, а в гортань, бронхи;
2. Прикрытие дыхательных путей ребенка мягким предметом (подушкой, игрушкой)
3. Прикрытие дыхательных путей грудью матери во время кормления;
4. Попадание инородных тел в дыхательные пути (мелкие игрушки, пуговицы, кольца, монетки и т.д.)
5. Сдавление области шеи цепочками с крестиками (талисманами), тесьмой с соской, завязками одежды, пеленкой.
6. Малыши, достигшие определенного уровня активности, иногда играя, натягивают на голову полиэтиленовые мешочки, которые во время дыхания малыша плотно облегают лицо, препятствуя проникновению воздуха, что также приводит к асфиксии.
Профилактика асфиксии:
— После каждого кормления ребенка следует подержать вертикально и дать ему возможность отрыгнуть воздух;
— Ни в коем случае не класть его в кроватку сразу после кормления;
— Укладывая младенца в кроватку после кормления, всегда поворачивайте его голову набок;
— Выбирая детское постельное белье и одежду, отдавайте предпочтение товарам баз завязок и тесемок;
— Не используйте слишком большие «взрослые» одеяла;
— Не оставляйте надолго старших детей одних около младенцев, не кладите их спать в одну кровать;
Будьте бдительны!
М. Артанова, заведующая КДО № 1
Артанова, заведующая КДО № 1
как врачи перинатального центра «ДАР» выхаживают новорожденных малышей, рожденных в состоянии асфиксии – резкого кислородного голодания клеток головного мозга.
Метод терапевтической гипотермии, суть которого в воздействии низкой температуры на головной мозг ребенка, сегодня считают прорывом в лечении новорожденных, которые появились на свет в состоянии удушья. В «ДАРе» его впервые применили 2 года назад. С тех пор новаторскую терапию прошли 26 малышей.
Эти дети получили при рождении низкую оценку по шкале Апгар (3 балла и менее) и не восстановили к 10-й минуте рефлексы, мышечный тонус, сердцебиение и самостоятельное дыхание. При условии, что малыш весит не менее 1800 г, врачи принимают решение о сеансе гипотермии.
На малыша надевают специальный многослойный костюм, либо используют систему охлаждения (первые фото). В полость подается вода и охлаждается специальным аппаратом. В течение нескольких часов после рождения происходит охлаждение до 33,5-34 градусов. Длится сеанс 72 часа. Таким образом врачи снижают интенсивность метаболических процессов в головном мозге и предотвращают гибель клеток центральной нервной системы на фоне перенесенной гипоксии. Губительный эффект кислородного голодания нивелируется.
В течение нескольких часов после рождения происходит охлаждение до 33,5-34 градусов. Длится сеанс 72 часа. Таким образом врачи снижают интенсивность метаболических процессов в головном мозге и предотвращают гибель клеток центральной нервной системы на фоне перенесенной гипоксии. Губительный эффект кислородного голодания нивелируется.
Еще недавно специфического лечения такого поражения ЦНС не существовало. Это вызывало целый каскад необратимых патологических процессов, а стандартная помощь такому крохе предусматривала только поддержку функционирования жизненно важных органов – ребенок с большой долей вероятности оставался с тяжелыми нарушениями ЦНС.
Впервые данную методику применил советский акушер-гинеколог Сергей Копшев. В 1985 году он опубликовал исследования, результаты которых тогда никто не принял всерьез. Его методика краниоцеребральной гипотермии была довольно примитивной (малышам надевалась только охлаждающая шапочка), но и она показала, что рациональное зерно в идее есть. Ученый исследовал 197 детей: из них 168 прошли процедуру – только треть их них в итоге имели неврологические аномалии. В то время как у тех, кто через процедуру не прошел, отклонения зафиксированы в 70% случаев.
Ученый исследовал 197 детей: из них 168 прошли процедуру – только треть их них в итоге имели неврологические аномалии. В то время как у тех, кто через процедуру не прошел, отклонения зафиксированы в 70% случаев.
Заместитель главного врача по педиатрической помощи Олег Зуйков рассказывает: «В центре «ДАР» через процедуру гипотермии прошли уже 26 новорожденных. Малыши, которые были направлены на процедуру сразу же после рождения, сейчас ничем не отличаются от сверстников. Из центра они были выписаны в удовлетворительном состоянии.
Сложнее ситуация с малышами, которых привезли в «ДАР» из районов края. Чтобы не допустить необратимых процессов в ЦНС, важно начать сеанс в первые 6 часов после рождения – время, которое врачи называют «золотым часом». Полгода назад у нас появился второй – мобильный – аппарат для гипотермии (это он на первых фото). За малышом выезжает бригада дистанционно-консультативного центра и начинает охлаждать малыша уже во время транспортировки обратно в «ДАР». Замечу, что наших врачей уже ждут коллеги на местах и начинают охлаждать кроху налитыми в резиновые перчатки холодной водой. Самой дальней точкой края, откуда мы доставляли такого пациента, был Славгород – туда мы направляли вертолёт, чтобы не терять 6 часов на дорогу. Вертолёт долетает до Славгорода за полтора-два часа.
Замечу, что наших врачей уже ждут коллеги на местах и начинают охлаждать кроху налитыми в резиновые перчатки холодной водой. Самой дальней точкой края, откуда мы доставляли такого пациента, был Славгород – туда мы направляли вертолёт, чтобы не терять 6 часов на дорогу. Вертолёт долетает до Славгорода за полтора-два часа.
Асфиксия, сравнимая с кратковременным удушением, во время родов может возникнуть в силу разных причин. В первую очередь это затяжной второй период родов, когда акушер-гинеколог имеет минимум возможностей вмешаться в процесс: родовая деятельность приостановилась – проводить стимуляцию поздно, и избежать асфиксии может только своевременная вакуум-экстракция. Также причиной асфиксии может стать короткая пуповина, которая, натягиваясь, нарушает кровоснабжение малыша в родах.
Кроме того серьезным фактором риска могут стать хронические заболевания матери: сахарный диабет, артериальная гипертензия, нарушение маточно-плацентарного кровотока, инфекции. Рождение малыша в тяжелом состоянии прогнозируется (женщине объясняют необходимость рожать в учреждении родовспоможения третьего уровня) – и реанимационная бригада готова к оказанию неотложной помощи сразу после рождения.
После того, как малыш проведет три дня в «скафандре», дальнейшую тактику мы определяем в зависимости от его состояния: если он требует респираторной поддержки, мы подключаем его к аппарату ИВЛ. Когда малыш начинает дышать сам, из отделения реанимации он переводится в отделение патологии новорожденных и недоношенных детей. Если же драгоценное время упущено и произошли необратимые изменения в ЦНС, малыш еще долго будет требовать замещающей респираторной поддержки.
Добавлю, что метод терапевтической гипотермии применяется и во «взрослой медицине», к примеру, в нейрохирургии: два таких аппарата есть в краевой больнице скорой медицинской помощи. Мы гордимся, что современные технологии доступны теперь и для самых маленьких пациентов. Эти новорожденные до трех лет состоят на учете в кабинете катамнестического наблюдения центра «ДАР. Если такие малыши вовремя прошли через сеанс гипотермии, никто и не догадается, что они испытали в момент рождения, появившись на свет в состоянии тяжелейшей асфиксии».
«Замороженные дети»: как врачи перинатального центра «ДАР» выхаживают новорожденных малышей, рожденных в состоянии асфиксии – резкого кислородного голодания клеток головного мозга.
«Замороженные дети»: как врачи перинатального центра «ДАР» выхаживают новорожденных малышей, рожденных в состоянии асфиксии – резкого кислородного голодания клеток головного мозга.
«Замороженные дети»: как врачи перинатального центра «ДАР» выхаживают новорожденных малышей, рожденных в состоянии асфиксии – резкого кислородного голодания клеток головного мозга.
«Замороженные дети»: как врачи перинатального центра «ДАР» выхаживают новорожденных малышей, рожденных в состоянии асфиксии – резкого кислородного голодания клеток головного мозга.
«Замороженные дети»: как врачи перинатального центра «ДАР» выхаживают новорожденных малышей, рожденных в состоянии асфиксии – резкого кислородного голодания клеток головного мозга.
| Все будущие родители с нетерпением ждут рождения их малыша, беспокоятся о нем. И, увы, порой этим оправдания оправдываются. Одной из достаточно часто встречающихся патологий является асфиксия новорожденных. Слыша этот диагноз, почти все родители пугаются и впадают в панику. Конечно же, асфиксия – это повод для тревоги, однако зачастую беспокойство родителей зачастую бывает излишне сильным. И чаще всего это происходит из-за непонимания того, что происходит с ребенком при асфиксии. Асфиксия новорожденных – это такое состояние новорожденных, при котором, вследствие нарушения процесса дыхания, развивается кислородная недостаточность. Существует два типа асфиксии: первичная, возникающая в момент рождения, и вторичная – развивающаяся в первые сутки после рождения. |
Механическая асфиксия у детей до 1 года — Брянская городская администрация
С появлением в семье новорождённой крохи забот у родителей прибавляется. Помимо правильного питания и ухода крайне необходимо обеспечить безопасность малыша. К сожалению, нередко причиной трагедии может стать механическая асфиксия. Ежегодно на территории Брянской области от асфиксии погибают дети до 1 года.
Асфиксия — удушье, вызванное сдавлением дыхательных путей, закрытием их просвета слизью, пищей, сдавлением шеи, грудной клетки и живота, которое может привести к смерти ребёнка. У новорождённого это состояние может быть вызвано в основном следующими причинами:
- Прикрытие дыхательных путей ребёнка мягким предметом (подушкой, игрушкой, одеялом)
- Прикрытие дыхательных путей грудью матери во время кормления
- Попадание инородных тел в дыхательные пути (мелкие игрушки, пуговицы, кольца, монеты и т.д.).
- Поперхивание и попадание молока не в пищевод ребёнка, в гортань, иногда бронхи.
- Частые срыгивания.
- Сдавление области шеи цепочками с крестиками (талисманами), тесьмой с соской.
- Сном в одной кровати с родителями, другими детьми.
Признаки механической асфиксии:
- Отсутствие дыхания более 20 секунд
- Вялость, необычная слабость мышц
- Кожа малыша приобретает бледный, синюшный оттенок
ВНИМАНИЕ, РОДИТЕЛИ! Если вы заметили эти признаки, то обязательно вызовите скорую медицинскую помощь. Не теряйте самообладания, ребёнку нужна ваша дальнейшая помощь!
Профилактика асфиксии:
- После каждого кормления ребёнку следует дать возможность отрыгнуть воздух, заглоченный с пищей. Для этого его нужно подержать некоторое время вертикально и ни в коем случае не класть сразу после кормления. Некоторые дети (особенно недоношенные или ослабленные) могут срыгивать повторно, уже находясь в кроватке. Для предотвращения вдыхания содержимого поворачивайте голову младенца всегда набок. Если срыгивания частые и обильные, то это является поводом для обращения к врачу.
- Выбирая детское постельное белье и одежду, предпочтение следует отдавать товарам без всевозможных завязочек, тесемочек и т.п. Вместо детского одеяла можно пользоваться специальным конвертом для сна, не использовать слишком большие “взрослые” одеяла.
- Детский матрас должен быть полужестким. Не укладывайте ребёнка на мягкую перину, подушку, не используйте их для поддержания ребёнка на боку.
- Не надевайте на шею ребёнка цепочки, тесёмки с сосками.
- Исключите из зоны досягаемости ребёнка мелкие предметы, они могут быть проглочены и попасть в дыхательные пути.
- Не оставляйте надолго старших детей одних около новорождённого, надеясь на их взрослость и рассудительность.
- Совместный сон в одной кровати с родителями (и с другими детьми) небезопасен — он может стать причиной удушения малыша. Оптимальным все же будет сон в родительской спальне, но не в родительской кровати. С одной стороны, это обеспечит безопасность малыша, с другой — вы будете в непосредственной близости от своего ребёнка.
Уважаемые родители, не оставляйте малыша без присмотра!
Памятка для родителей «Профилактика механической асфиксии у детей до 1 года»
Асфиксия — удушье, вызванное сдавлением дыхательных путей, закрытием их просвета слизью, пищей, сдавлением шеи, грудной клетки и живота, которое может привести к смерти ребенка.
У новорожденного это состояние может быть вызвано в основном следующими причинами:
Прикрытие дыхательных путей ребенка мягким предметом (подушкой, игрушкой).
Прикрытие дыхательных путей грудью матери во время кормления.
Попадание инородных тел в дыхательные пути (мелкие игрушки, пуговицы, кольца, монеты и т.д.).
Поперхивание и попадание молока не в пищевод ребенка, в гортань, иногда бронхи.
Частые срыгивания.
Сдавление области шеи цепочками с крестиками (талисманами), тесьмой с соской.
Профилактика асфиксии
- После каждого кормления ребенку следует дать возможность отрыгнуть воздух, заглоченный с пищей. Для этого его нужно подержать некоторое время вертикально и ни в коем случае не класть сразу после кормления. Некоторые дети (особенно недоношенные или ослабленные) могут срыгивать повторно, уже находясь в кроватке. Для предотвращения вдыхания содержимого поворачивайте голову младенца всегда набок. Если срыгивания частые и обильные, то это является поводом для обращения к врачу.
- Выбирая детское постельное белье и одежду, предпочтение следует отдавать товарам без всевозможных завязочек, тесемочек и т.п. Вместо детского одеяла можно пользоваться специальным конвертом для сна, не использовать слишком большие «взрослые» одеяла. Можно использовать специальные сетчатые одеяла для младенцев.
- Не следует оставлять надолго старших детей одних около новорожденного, надеясь на их взрослость и рассудительность, а также класть спать младенца в одну кровать с ними. Да и совместный сон в одной кровати с родителями с точки зрения возможной асфиксии не безопасен.
- Совместный сон также может быть фактором риска удушения малыша. Хотя многие молодые мамы кладут с собой в постель малышей, оптимальным все же будет сон в родительской спальне, но не в родительской кровати. Поставьте детскую кроватку впритык к своей, опустите боковую решетку. С одной стороны, это обеспечит безопасность малыша, с другой — вы будете в непосредственной близости от своего ребенка и вам не придется вскакивать ночью по несколько раз. Вам будет удобно ночью кормить кроху, а затем, не вставая, перекладывать его в кроватку.
Адвокатов по рождению асфиксии в Индиане | Бесплатные консультации
Мозгу ребенка необходимо постоянное снабжение кислородом и кровью. Узнайте о признаках нарушения кровоснабжения и о том, как врач должен реагировать.
Асфиксия — это медицинский термин, означающий, что мозг не получает достаточно богатой кислородом крови, в которой он нуждается. Когда асфиксия случается с ребенком во время беременности, родов, родов или вскоре после рождения, это называется асфиксией при рождении.
Асфиксия при рождении опасна. В зависимости от степени кислородного голодания и того, как долго оно длится, асфиксия при рождении может вызвать серьезное повреждение органов, повреждение головного мозга, необратимую инвалидность или даже смерть.
Если вы беременная мать, важно, чтобы ваша медицинская бригада полностью понимала асфиксию при рождении: симптомы, методы лечения, осложнения и передовые методы профилактики.
К сожалению, многие случаи асфиксии при рождении вызваны халатностью врача, либо из-за того, что врач или медсестра совершают критическую ошибку во время беременности или родов, либо из-за отсутствия надлежащего наблюдения или незнания симптомов и методов лечения.
Симптомы асфиксии при рождении
Врачи должны постоянно контролировать жизненные показатели вашего ребенка — даже после родов — на предмет признаков асфиксии.Любые признаки того, что мозг вашего ребенка не получает достаточного кровоснабжения, следует рассматривать как неотложную медицинскую помощь, и врачи должны реагировать соответствующим образом.
Симптомы асфиксии при рождении включают:
- Голубоватый, серый или бледный цвет кожи
- Слабое дыхание / респираторный дистресс (или затрудненное дыхание)
- Медленное сердцебиение или слабый пульс
- Слабые рефлексы
- Слабые мышцы тон
- Ацидоз (опасно высокий уровень кислоты в крови)
- Меконий (т.е.е. фекалий или «пятно стула») в околоплодных водах
- Судороги
Лечение асфиксии при рождении
Соответствующее лечение зависит от степени тяжести асфиксии и жизненно важных функций ребенка.
Прежде всего, медицинские работники должны предпринять немедленные шаги для устранения причины асфиксии и восстановления нормального кровоснабжения.
В случаях легкой асфиксии наиболее распространенным лечением является поддержка дыхания, которую следует поддерживать до тех пор, пока ребенок снова не сможет самостоятельно дышать.Большинство младенцев полностью выздоравливают от легкой асфиксии со временем, хотя врачи должны продолжать внимательно следить за развитием осложнений (см. Ниже).
В случае более обширной асфиксии соответствующее лечение может включать:
- Охлаждение тела
- Поддержание жизни: сердечный насос или сердечно-легочный насос
- Диализ
- Лекарства (например, лекарства от кровяного давления или противосудорожные препараты)
- Внутривенные жидкости и питание (IV)
- Поддержка дыхания, которая может включать использование оксида азота и / или специально разработанного дыхательного аппарата или оборудования
Осложнения при родовой асфиксии
Осложнения при родовой асфиксии могут включать:
- Церебральные паралич
- СДВГ
- Потеря зрения или слуха (или другие проблемы со зрением / слухом)
- Дистресс плода
- Задержка развития
- Судорожные расстройства
- Гипоксико-ишемическая энцефалопатия (ГИЭ)
- Перивентрикулярная лейкомаляция
- Физическая инвалидность, которая может быть постоянным
- Паралич
- Смерть
Поговорите с адвокатом по асфиксии при рождении в Индианаполисе в Doehrman Buba Ring
Если ваш новорожденный получил травму из-за асфиксии при рождении, важно, чтобы вы понимали возможные осложнения для вашего ребенка, а также сложный юридический процесс, который может последовать.Вы и ваша семья можете иметь право на финансовую компенсацию за травмы вашего ребенка и ваши финансовые потери, а также на будущую стоимость ухода. Мы рекомендуем вам связаться с нашим офисом и поговорить с опытным юристом по травмам из Индианаполиса о ваших возможностях.
Мы не будем взимать с вас плату, если нам не удастся получить компенсацию по вашему иску. Чтобы узнать больше, свяжитесь с Doehrman Buba Ring и назначьте бесплатную консультацию сегодня.
Как управлять охлаждением в Великобритании вне клинических испытаний
, описанных в рандомизированных испытаниях терапевтической гипотермии,
предполагают, что младенцы в исследовании страдали асфиксией
той же степени тяжести.Младенцы в исследовании имели такой же балл энцефалопатии на уровне
24 часа, что и группа с аномальным исходом, о которой сообщали Thompson et
al.
9
Однако, в то время как оценка энцефалопатии в группе аномальных исходов
, сообщенная Томпсоном впоследствии
, ухудшилась, у младенцев, участвовавших в исследовании, оценка энцефалопатии
снизилась в течение следующих 3 дней и приблизилась к норме
. группа результатов, представленная в исследовании Томпсона (рис. 4).В
экспериментальных исследованиях было показано, что умеренная гипотермия
предотвращает начало вторичной энергетической недостаточности, вторичный
цитотоксический отек и повышение эпилептической активности и
апоптоз
20–24
; мы предполагаем, что лечение умеренной гипотермией
могло изменить процессы, приводящие к вторичному отказу энергии
и замедленной гибели клеток, таким образом предотвращая
ухудшение энцефалопатии.
В заключение, это исследование показывает, что в Великобритании терапевтическая гипотермия
все чаще предоставляется после завершения
включения в исследование гипотермии всего тела TOBY,
младенцев, получавших лечение, имеют такую же степень асфиксии, как и
, о которых было сообщено в рандомизированных исследованиях умеренной гипотермии,
целевая температура тела была успешно достигнута, а наблюдаемые клинические осложнения
в основном можно отнести к
асфиксии или другим состояниям.Национальный институт здравоохранения
и Clinical Excellence в настоящее время оценивает лечение с помощью
умеренной гипотермии у новорожденных после асфиксии, но
важно, чтобы даже если терапевтическая гипотермия стала стандартом лечения
, надзор за ее использованием в клинической практике
продолжается, чтобы выявить осложнения, которые могут возникнуть при более широком использовании терапевтической гипотермии
и введении нового
в неонатальные отделения.
Выражение признательности: следующие центры предоставили данные, использованные для этой статьи
(в порядке количества зарегистрированных случаев): профессор Марианна Торесен и доктор
Джеймс Тули, больница Святого Михаила, Бристоль (13), доктор Эндрю Карри и Мари
Хаббард, Королевский лазарет Лестера (12), профессор Эндрю Уайтлоу, Саутмид
больница (10), доктор Денис Аззопарди и профессор Дэвид Эдвардс, госпиталь Королевы Шарлотты
и
Челси (9), профессор Майкл Вайндлинг и Эндрю Берк, Ливерпуль
Женская больница (8), профессор Нил Марлоу и Тим Стич, Королевский медицинский центр
Ноттингем (8), доктор Фил Амесс, Королевская больница графства Сассекс, Брайтон (8), доктор Шобха
Чериан, Университетская больница Уэльса, Кардифф (8), д-р Элия Маалуф и Клаудия Харрис,
Больница Хомертон (7), д-р Джулиан Исон, больница Деррифорд, Плимут (5), д-р Майкл
Смит, крыло Джессопа, Шеффилд (5), д-р Пол Кларк, Университет Норфолка и Норвича
Госпиталь
(4), доктор Сара Скиннер и Ивонн Миллар, больница Лутон и Данстейбл (3), доктор
Бов Яни и Карина Вандертак, Морская больница Медуэй (3), доктор Джанет Беррингтон,
Больница Royal Victoria, Ньюкасл (3), доктор Саймон Митчелл и доктор Рут Готтштейн, St
Госпиталь Мэри, Манчестер (3), доктор Лесли Джексон, Королевский родильный дом принцессы
Госпиталь
, Глазго (2), доктор Джин Маттес, Госпиталь Синглтона (2), доктор Стивен Роуз и
Чармейн Мабор, больница Бирмингем Хартлендс (1), доктор Сью Чатфилд, Брэдфорд
Королевский лазарет (1), профессор Сунил Синха и Ян Гавей, Университет Джеймса Кука
Госпиталь
(1), Д-р Бэби Кумараратне и Линдола Грейг, больница Нью-Кросс (1), д-р Пол
Муньярд, Королевская больница Корнуолла, Труро (1), профессор Генри Холлидей и д-р Дэвид
Свит, родильный дом Королевского юбилея, Белфаст (1), д-р Никки Робертсон и доктор Судин 900 05
Thayyil, Госпиталь Университетского колледжа, Лондон (1).
Финансирование: В этом документе содержится отчет о независимом исследовании, которое частично финансируется Программой исследования политики
Министерства здравоохранения. Выраженные мнения не обязательно совпадают с мнениями Департамента. В британский регистр TOBY Cooling Register в настоящее время ведется учет
в рамках финансируемого MRC исследования TOBY (охлаждение всего тела в качестве лечения перинатальной асфиксической энцефалопатии
).
Конкурирующие интересы: Нет.
Члены руководящей группы: D Azzopardi, P Brocklehurst, S Ayers, U Bowler, A Currie,
AD Эдвардс, H Halliday, M Levene, E. Maalouf, N Marlow, E Juszczak, N Robertson, B
Strohm, M Торесен, М. Вайндлинг, Вайтлоу.
СПИСОК ЛИТЕРАТУРЫ
1. Глюкман П.Д., Вятт Дж. С., Аззопарди Д. и др. Избирательное охлаждение головы с легкой
системной гипотермией после неонатальной энцефалопатии: многоцентровое рандомизированное исследование.
Ланцет 2005; 365: 663–70.
2. Шанкаран С., Лапток А.Р., Эренкранц Р.А. и др. Гипотермия всего тела для
новорожденных с гипоксически-ишемической энцефалопатией. N Engl J Med 2005; 353: 1574–84.
3. Eicher DJ, Wagner CL, Katikaneni LP, et al. Умеренная гипотермия при неонатальной энцефалопатии
: результаты безопасности.Pediatr Neurol 2005; 32: 18–24.
4. Eicher DJ, Wagner CL, Katikaneni LP, et al. Умеренная гипотермия при неонатальной энцефалопатии
: результаты эффективности. Pediatr Neurol 2005; 32: 11–17.
5. Джейкобс С., Хант Р., Тарнов-Морди В. и др. Охлаждение новорожденных с гипоксической
ишемической энцефалопатией. Кокрановская база данных Syst Rev 2007; (4): CD003311.
6. Шах П.С., Олссон А., Перлман М. Гипотермия для лечения неонатальной гипоксической ишемии
энцефалопатия: систематический обзор.Arch Pediatr Adolesc Med 2007; 161: 951–8.
7. Ивата О., Ивата С., Торнтон Дж. С. и др. Продолжительность «терапевтического временного окна» уменьшается на
с увеличением тяжести церебральной гипоксии-ишемии при нормотермии и на
отсроченной гипотермии у новорожденных поросят. Brain Res 2007; 1154: 173–80.
8. Тейлор Д.Л., Мехмет Х., Кэди Э.Б. и др. Улучшенная нейрозащита при гипотермии
с задержкой на 6 часов после церебральной гипоксии-ишемии у 14-дневных крыс. Pediatr
Res 2002; 51: 13–19.
9. Томпсон С.М., Путерман А.С., Линли Л.Л. и др. Значение балльной системы для
гипоксической ишемической энцефалопатии в прогнозировании исходов нервного развития. Acta
Paediatr 1997; 86: 757–61.
10. Дебийон Т., Дауд П., Дюран П. и др. Охлаждение всего тела после перинатальной асфиксии: пилотное исследование
у доношенных новорожденных. Дев Мед Чайлд Нейрол 2003; 45: 17–23.
11. Gunn TR, Wilson NJ, Aftimos S, et al. Переохлаждение мозга и интервал QT. Педиатрия
1999; 103: 1079.
12. Аззопарди Д., Робертсон Н.Дж., Коуэн Ф.М. и др. Пилотное исследование лечения неонатальной энцефалопатии с помощью гипотермии всего тела
. Педиатрия 2000; 106: 684–94.
13. Торесен М., Уайтлоу А. Сердечно-сосудистые изменения во время легкой терапевтической гипотермии
и согревания у младенцев с гипоксически-ишемической энцефалопатией.
Педиатрия 2000; 106: 92–9.
14. Олдерсон П., Гардкари С., Синьорини Д.Ф. Лечебное переохлаждение при черепно-мозговой травме.
Кокрановская база данных Syst Rev 2004; (4): CD001048.
15. Wiswell TE, Robertson CF, Jones TA, et al. Некротический энтероколит у доношенных
новорожденных. Исследование случай-контроль. Ам Дж. Дис Чайлд 1988; 142: 532–5.
16. Ганн А.Дж., Беннет Л., Ганнинг М.И. и др. Церебральная гипотермия не оказывает нейропротекторного действия
, если оно началось после постишемических судорог у плодов овцы. Pediatr Res 1999; 46: 274–
80.
17. Shankaran S, Laptook A, Wright LL, et al. Гипотермия всего тела при неонатальной энцефалопатии
: наблюдения за животными как основа для рандомизированного контролируемого пилотного исследования
у доношенных детей.Педиатрия 2002; 110: 377–85.
18. Сарнат HB, Sarnat MS. Неонатальная энцефалопатия, вызванная дистрессом плода. Клиническое
и электроэнцефалографическое исследование. Arch Neurol 1976; 33: 696–705.
19. Volpe JJ. Неврология новорожденного. Филадельфия, Пенсильвания: WB Saunders, 2001.
20. Amess PN, Penrice J, Cady EB, et al. Легкая гипотермия после тяжелой преходящей гипоксии-ишемии
снижает замедленное повышение церебрального лактата у новорожденных поросят.
Pediatr Res 1997; 41: 803–8.
21. Эдвардс А.Д., Юэ Х, Сквайер М.В. и др. Специфическое ингибирование апоптоза после церебральной гипоксии-ишемии
путем умеренной постинсультной гипотермии. Biochem Biophys Res
Commun 1995; 217: 1193–9.
22. Торесен М., Пенрис Дж., Лорек А. и др. Легкая гипотермия после тяжелой преходящей гипоксии-ишемии
улучшает отсроченную церебральную энергетическую недостаточность у новорожденного поросенка.
Pediatr Res 1995; 37: 667–70.
23. Ганн А.Дж., Ганн Т.Р., Ганнинг М.И. и др.Нейропротекция с длительным охлаждением головы
начата перед постишемическими припадками у плодов овцы. Педиатрия 1998; 102: 1098–1106.
24. Gunn AJ, Gunn TR, de Haan HH, et al. Драматическое спасение нейронов с длительным избирательным охлаждением головы
после ишемии у плодов ягнят. Дж. Клин Инвест 1997; 99: 248–56.
Таблица 3 Диагнозы, зарегистрированные при поступлении
Диагноз
Аспирация мекония, n (%) 13 (10,8%)
Легочная гипертензия, n (%) 7 * (5.8%)
Утечка воздуха, n (%) 4 * (3,3%)
Поздний сепсис, n (%) 4 (3,3%)
Легочное кровотечение, n (%) 3 (2,5%)
NEC, n (%) 2 (1,7%)
Пневмония, n (%) 1 (0,8%)
NEC, некротизирующий энтероколит.
* Четверо детей с легочной гипертензией и двое из детей
с утечкой воздуха также прошли аспирацию мекония.
Определения всех элементов можно найти в дополнительном приложении
и в Справочнике врача (www.npeu.ox.ac.uk/tobyregister).
Оригинальная статья
F264 Arch Dis Child Fetal Neonatal Ed 2009; 94: F260 – F264. doi: 10.1136 / adc.2008.146977
group.bmj.com 12 ноября 2013 г. — Опубликовано fn.bmj.comЗагружено с сайта
Frontiers | Глобальный взгляд на асфиксию новорожденных и реанимацию
Фон
По оценкам, во всем мире ежегодно происходит 2,5 миллиона случаев смерти новорожденных, что составляет ~ 47% детской смертности в возрасте до 5 лет (1, 2). Асфиксия при рождении (БА), связанная с гипоксией-ишемией во время родов, составляет от 30 до 35 процентов неонатальных смертей (3).Это означает, что ежегодно во всем мире умирает около миллиона новорожденных (1–3). Кроме того, согласно оценкам, 1,3 миллиона новорожденных являются «свежими мертворожденными» (FSB), что свидетельствует о смерти во время родов незадолго до родов (4, 5). Первый день и особенно первый час имеют решающее значение для выживания новорожденных с самым высоким риском. неонатальных смертей, связанных с родами (60–70%), произошедших в течение 24 часов после рождения (1–3). Этот обзор будет сосредоточен на определении БА в условиях ограниченных ресурсов и сравнении его с диагнозом в условиях исчерпания ресурсов, подчеркивая важность прерывания плацентарного кровотока.В условиях ограниченных ресурсов выявление тяжелого ацидемического состояния может помочь дифференцировать случаи БА, действительно связанные с беременностью, приводящие к летальному исходу, от тех случаев, когда смертность связана с отсроченной или неэффективной базовой реанимацией.
Определение асфиксии при рождении
BA в условиях ограниченных ресурсов обычно определяется как неспособность инициировать или поддерживать самостоятельное дыхание при рождении и в некоторых случаях включает 1-минутную оценку по шкале Апгар <7,00 (3). Сравните это с настройкой изобилия ресурсов, где БА - это биохимическое определение, связанное с нарушением газообмена из-за прерывания плацентарного кровотока (PBF), с прогрессирующей гипоксемией, гиперкапнией и ацидозом.БА идентифицируют по наличию ацидоза плода в пуповинной артериальной крови после родов. Однако значение pH пупочной артерии, которое лучше всего определяет это состояние, остается неясным. Традиционно асфиксия определялась как рН пуповинной артерии <7,20 (6). Используя это определение, риск смерти или осложнений, связанных с развитием нервной системы, был чрезвычайно низким (7). Долгое время считалось, что pH пупочной артерии <7,00 отражает степень ацидоза, часто называемого тяжелой ацидемией плода, при которой повышается риск неблагоприятных неврологических последствий (8, 9).PH пуповины <7,00 усложняет ~ 0,3% всех родов, т. Е. 3 на 1000 срочных родов (8). Однако даже при тяжелой ацидемии плода вероятность последующего повреждения головного мозга или летального исхода невысока. Более того, было показано, что большинство младенцев, то есть> 60 процентов с pH пуповины <7,00, имеют нормальное течение родов и родов, начинают дышать вскоре после родов, направляются в обычные ясли и выписываются домой в течение 24 часов ( 10). Даже у младенцев с тяжелой ацидемией плода, поступающих в реанимацию (часто из-за затрудненного дыхания), в большинстве случаев наблюдается доброкачественное неврологическое течение.Лишь у небольшого процента пациентов наблюдается энцефалопатия от умеренной до тяжелой степени с неблагоприятным исходом, например, смерть или последующий церебральный паралич (11–13). Это наблюдение указывает на внутреннюю устойчивость мозга к тяжелой асфиксии.
Физиология асфиксии
Ответы кровообращения на прерывание плацентарного кровотока для сохранения мозгового кровотока
Когда плацентарный кровоток (PBF) нарушен, плод перераспределяет сердечный выброс для защиты жизненно важных органов, таких как мозг, сердце и надпочечники, за счет кровотока в почках, кишечнике и коже.Этому ответу способствуют несколько факторов, включая гипоксемию, которая вызывает сужение сосудов легких. Это приводит к снижению легочного кровотока, возврату крови из левого предсердия и снижению давления в левом предсердии (14, 15). Увеличивается шунтирование справа налево через овальное отверстие, что приводит к доставке более насыщенной кислородом крови в левое сердце, которое предпочтительно направляется в мозг и сердце. Внутри головного мозга гипоксемия приводит к снижению сопротивления сосудов головного мозга.В экспериментальных исследованиях было показано, что это сопротивление может снизиться на 50%, что приведет к увеличению церебрального кровотока. Это компенсирует пониженное содержание кислорода в крови, наблюдаемое в начальной фазе асфиксии. Когда асфиксический процесс является продолжительным и / или тяжелым, системное артериальное давление падает до точки, при которой компенсаторные механизмы перестают работать и наступает коллапс кровообращения. Этот критический порог варьируется среди плодов и представляет собой точку, ниже которой мозговое кровообращение больше не может расширяться для поддержания кровотока (16–18).В этот момент доставка кислорода в мозг недостаточна для удовлетворения клеточной потребности, и происходит повреждение головного мозга.
Респираторные реакции на асфиксию
В дополнение к сердечно-сосудистым изменениям, описанным выше, связанным с асфиксией, происходят характерные изменения в паттернах дыхания. Эти сердечно-респираторные изменения с асфиксией изящно описаны Dawes et al. (19) (Рисунок 1). При использовании макаки-резуса асфиксию вызывали путем перевязки пуповины и покрытия головы небольшим мешком с теплым физиологическим раствором.Сразу наблюдалась характерная серия изменений. В течение 30 с наступил короткий период быстрого ритмичного дыхательного усилия. Это приводило к апноэ (первичному) и брадикардии (частота сердечных сокращений (ЧСС)> 60 ударов в минуту (уд / мин) в большинстве случаев. Если асфиксический процесс прерывался (обычно в пределах от 30 до 90 с), частота сердечных сокращений неизменно реагировала на базовые вмешательства. в том числе сушку, стимуляцию и / или вентиляцию мешком-маской, если она была осуществлена своевременно (19). Если асфиксию позволяли продолжаться, животное начинало задыхаться.Если процесс асфиксии был прерван, спонтанное регулярное дыхание все же можно было вызвать с помощью быстрой физической стимуляции. Без вмешательства дыхание длилось ~ 4 мин, постепенно ослабевая, пока не произошел окончательный «последний вздох». Это считалось вторичным апноэ с ЧСС неизменно <60 ударов в минуту и pH <7,00. Без реанимации последовала смерть. Примечательно, что на каждую 1-минутную задержку начала реанимации на этой стадии асфиксии требовалось ~ 2 минуты, прежде чем наблюдалось удушье, и 4 минуты, пока дыхание не стало очевидным (19).
Рисунок 1 . Взаимосвязь между дыханием, частотой сердечных сокращений, артериальным давлением и ацидозом у макак-резусов во время асфиксии и реанимации [Адаптировано из Dawes et al. (19)].
Переходные изменения кровообращения при рождении
С переходом от in utero к ex-utero life, значительные изменения кровообращения тесно переплетаются с сопутствующими респираторными изменениями. При плаче при рождении легкие быстро расширяются, и сопротивление легочных сосудов падает.Соответственно, ЧСС быстро увеличивается примерно со 120 до 150 ударов в минуту в течение 10-25 секунд после начала дыхания (20). Это приводит к значительному увеличению легочного кровотока, уменьшению, а затем обращению вспять протокового шунтирования справа налево, поскольку давление в легочной артерии падает ниже системного кровяного давления. Увеличивается возврат легочных вен в левое предсердие с повышением давления, которое превышает давление в правом предсердии. Это приводит к функциональному закрытию овального отверстия.После пережатия пуповины и удаления плаценты с низким сопротивлением системное сосудистое сопротивление увеличивается с одновременным повышением системного артериального давления.
Влияние прерывания PBF на кардиореспираторную адаптацию
При pH пуповинной артерии <7,00 ребенок может родиться вялым с минимальным или минимальным дыхательным усилием, отсутствием расширения легких, продолжающимся повышенным легочным давлением и повышением систематического сосудистого сопротивления после отделения плаценты.Гипоксия, гиперкарбия и ацидоз будут быстро ухудшаться, если немедленно не начать реанимацию. Выполнение основных этапов вмешательства, изложенных в алгоритме помощи младенцам в дыхании (HBB) (21), с последующей эффективной вентиляцией с положительным давлением (PPV), в большинстве случаев приводит к расширению легких с обращением респираторного ацидоза и возникновению спонтанного дыхания. .
Другие причины прерывистой кардиореспираторной адаптации
Важно отметить, что диагноз БА, основанный на отсутствии спонтанного дыхания при рождении, может не отражать прерывание ФОР или быть связанным с ним (см. Выше).Задержка дыхания может быть связана со многими причинами, включая состояния матери, такие как лихорадка (22) или прием лекарств, принимаемых матерью, неонатальные факторы, такие как незрелость или аномалии. Эти младенцы, вероятно, будут находиться в состоянии первичного апноэ и будут реагировать на сушку, поддержание тепла и стимуляцию с появлением спонтанного дыхания. Если реанимация отложена и PPV не начата своевременно, могут быстро развиться гипоксия, гиперкарбия и ацидоз, и ребенок может перейти в «состояние удушья» (pH <7.00) или даже в «ФСБ».
Причины перинатальной асфиксии — важность прерывания PBF
При прерывании родов ПБФ приводит к БА. В этом отношении решающее значение имеют два элемента, а именно продолжительность и серьезность перерыва. Снижение плацентарного кровотока может быть вторичным по отношению к материнским состояниям, таким как гипертония или преэклампсия, вторичным по отношению к измененной сосудистой сети плаценты. Гипотония у матери, вторичная по отношению к действию лекарств или спинномозговой анестезии, может нарушить PBF.Действительно, в одном отчете спинальная анестезия была наиболее частой причиной непредвиденного значения pH артерии пуповины <7,00, вероятно, связанной с гипотензией у матери и снижением ФП (10). Плацентарные состояния, такие как отслойка и кровотечение у плода и матери, также могут нарушить PBF. Хориоамнионит и фунизит связаны с нарушением функции плаценты и асфиксией (10). Наконец, пуповина может быть сдавлена извне, что может привести к возникновению таких состояний, как затылочная пуповина или выпадение пуповины. Таким образом, методы последовательного обнаружения аномалий частоты сердечных сокращений плода (FHR) являются критически важным первым шагом к идентификации плода с высоким риском, и их можно значительно улучшить с помощью непрерывного мониторинга FHR.
Согласование глобальных различий в BA
Несколько факторов могут играть роль в объяснении этого поразительного несоответствия в диагнозе, а также исходе (черепно-мозговая травма или смертность) от БА. Во-первых, как отмечалось выше, отсутствие дыхательного усилия при рождении может проявляться при наличии или отсутствии пуповины pH <7,00. На физиологическом или клиническом уровне вопрос заключается в том, страдает ли младенец первичным или вторичным апноэ (19). Частично это можно определить по событиям, происходящим во время родов, т.е.е., аномалии ЧСС (важны как продолжительность, так и тяжесть) или острые события, например отслойка плаценты. Действительно, в качестве фундаментальной предпосылки мы предполагаем, что большинство младенцев находятся в состоянии первичного апноэ и будут реагировать на основные шаги реанимации (сушка, согревание и стимуляция) с началом спонтанного дыхания. Это было основной гипотезой после запуска учебной программы HBB в Танзании. Действительно, было продемонстрировано 47% снижение 24-часовой неонатальной смертности (21). Кроме того, было отмечено снижение ставок ФСБ на 24% (21).Значительное снижение смертности от БА и ФСБ отчасти связано с увеличением частоты стимуляции при рождении (с 47 до 87%) с последующим инициированием самостоятельного дыхания. Кроме того, было отмечено сопутствующее значительное снижение потребности в PPV. Интересно, что в этом отчете среди умерших младенцев не было различий в количестве стимуляции, предоставленной до и после тренировки HBB, то есть 93 и 97%, а также в обеспечении PPV, то есть 87 vs.97% соответственно (21).
Во-вторых, ранее также было продемонстрировано в условиях ограниченных ресурсов, что время до начала, а также продолжительность PPV значительно больше у умерших младенцев по сравнению с младенцами с нормальным исходом. В частности, риск смерти увеличивался на 16 процентов за каждые 30 секунд задержки начала PPV до 6 минут и на 6 процентов за каждую минуту примененного BMV (23). В-третьих, неспособность вводить эффективную и устойчивую PPV из-за частых перерывов в доставке PPV, чтобы установить неэффективную герметизацию маски и / или невозможность интубации во многих условиях, вероятно, являются дополнительными способствующими факторами.
Клиническое исследование, в котором изучалась взаимосвязь между наличием тяжелой ацидемии плода, началом дыхания в родильном зале и последующим неврологическим состоянием, подтверждает вышеуказанные наблюдения (24). Описаны клинические данные двух групп, доставленных в присутствии тяжелой ацидемии плода (pH пупочной артерии ≤ 7,00, дефицит оснований ≥12 мЭкв / л). Первая, группа I ( n = 17), требовала минимальной реанимации в родильном зале (DR), не требовала респираторной поддержки и имела нормальный неврологический исход.Вторая, группа II ( n = 7), требовала интубации и искусственной вентиляции легких в DR. У всех семи младенцев развился синдром гипоксически-ишемической энцефалопатии (ГИЭ), включая судороги, которые развились в течение первых 6–12 часов после рождения. Газы пуповинной артериальной крови отличались следующим: во-первых, более низким pH пуповины, т. Е. 6,75 ± 0,18 против 6,90 ± 0,09 ( P <0,005) и более высоким PaCO 2 пуповины, т.е. 37 по сравнению с 94 ± 22 мм рт. Ст. ( P <0.005) в группе II по сравнению с младенцами в группе I соответственно. Среднее начальное послеродовое значение pH было ниже, т. Е. 7,06 ± 0,15 против 7,25 ± 0,09, а PaCO 2 оставалось выше у младенцев группы II по сравнению с группой 1, т. Е. 45 ± 14 мм рт. Ст. И 30 ± 6 мм рт. Ст. Соответственно ( P <0,005). Эти наблюдения указывают на основную трудность определения БА на основании отсутствия дыхательного усилия при рождении, особенно без анализа пуповинной артериальной крови. Отсутствие дыхательного усилия при нормальном pH пуповинной артерии указывает на первичное апноэ (рис. 1).Смерть в этих обстоятельствах, вероятно, связана с задержкой или неэффективной вентиляцией (см. Выше). Напротив, отсутствие респираторного усилия при тяжелой ацидемии плода предполагает вторичное апноэ с повышенным риском смерти. Задержка в начале или предоставлении неэффективной респираторной поддержки быстро усугубит и без того ацидемическое состояние и приведет к быстрой смерти. Наконец, нормальная респираторная адаптация при рождении может происходить при тяжелой ацидемии плода (см. Выше). Эти наблюдения могут частично объяснить поразительные различия в смертности, связанной с БА, в условиях с низким и высоким уровнем ресурсов.
Выявление ребенка с высоким риском прерывания плацентарного кровотока во время родов
Периодическая аускультация с помощью фетального стетоскопа в значительной степени была основным методом мониторинга плода, доступным во многих странах с ограниченными ресурсами. Недавняя разработка нового ремешка для непрерывного монитора ЧСС под названием Мойо (Laerdal Global) способствовала более быстрой идентификации аномальной ЧСС и может стать прорывом в выявлении плодов с высоким риском гипоксии-ишемии во время родов.В недавнем исследовании в популяции с низким уровнем риска было показано, что осуществление непрерывного мониторинга ЧСС с помощью устройства Moyo было связано с 6,90-кратным увеличением выявления аномальной ЧСС, то есть ее отсутствия, ЧСС <120 или ЧСС> 160 ударов в минуту. и более короткий интервал времени от последней оценки ЧСС до родов (25). Роды кесарева сечения (CS) были в 5,7 раза, а роды с вакуумной экстракцией в 3,8 раза более вероятны после введения Moyo в результате обнаружения аномальной ЧСС.В целом потребность в реанимационных вмешательствах после внедрения была меньше. Перинатальные исходы, то есть новые мертворождения и ранняя неонатальная смерть, были схожими в разные периоды времени, что, вероятно, отражает низкую частоту этих заболеваний в этой популяции с низким уровнем риска. В то время как метод непрерывного допплера обнаруживает аномалии FHR более легко, чем метод прерывистой аускультации, время до введения CS не различается между группами мониторинга (26). Это означает, что это не только своевременная возможность выявления опасности для плода во время родов, но и ресурсы, т.е.е. должны быть доступны недостаточная вместимость операционной и компетентные поставщики. Кроме того, важно взвесить преимущества непрерывного мониторинга FHR (раннее выявление аномалий FHR, одновременное ведение нескольких пациентов) по сравнению с недостатками (больше родов CS) при отсутствии пользы для новорожденных. Поскольку популяции пациентов, изученные в этих отчетах, относились к группе низкого риска, необходимы будущие рандомизированные исследования с участием пациентов с высоким риском
Наконец, было бы полезно иметь возможность измерять газы пуповинной артериальной пуповинной крови после родов и / или раннего постнатального pH и дефицита оснований, чтобы обеспечить объективное измерение кислотно-основного статуса и, по умолчанию, степень прерывания PBF примерно на момент рождения.
Реанимация в родильном отделении
Подавляющее большинство новорожденных (85%) инициируют спонтанное дыхательное усилие в течение 15 секунд после рождения, еще 10 процентов будут реагировать на стимуляцию и / или отсасывание (23). Еще от 3 до 5 процентов потребуют PPV ± интубация, и только 0,1 процента (1 из 1000 младенцев) потребуются сердечно-легочная реанимация (СЛР), компрессионные сжатия грудной клетки ± лекарства, например, адреналин (27). Последнее подчеркивает важность эффективного PPV для восстановления спонтанного кровообращения.Примечательно, что программа HBB не включает проведение сердечно-легочной реанимации (21, 28).
Ключевым подходом к реанимации независимо от обстановки является ожидание рождения ребенка с высоким риском, например, аномалий ЧСС, выпадения пуповины, недоношенности. По возможности в доставке должны быть два врача, способные своевременно инициировать базовую стабилизацию / реанимацию. Первым шагом должен быть предварительный отчет, в котором следует обсудить возможность получения ребенка с депрессией и подготовку к началу HBB или руководящие принципы программы реанимации новорожденных (NRP), включая внедрение PPV (28, 29).Как отмечалось выше, большинство младенцев находятся в состоянии первичного апноэ и реагируют на высыхание, обеспечивая тепло и стимуляцию с началом самостоятельного дыхания. Внедрение раннего PPV должно способствовать коррекции респираторного ацидоза и возникновения спонтанного дыхания у большинства младенцев, у которых сохраняется депрессия. Следует отметить два важных момента. Во-первых, раннее определение частоты сердечных сокращений является критическим маркером эффективной вентиляции с быстрым увеличением частоты сердечных сокращений, отмечаемым в течение 30 секунд.Во-вторых, для недышащих новорожденных со стойкой брадикардией (ЧСС <100 ударов в минуту) шаги коррекции, указанные в мнемоническом MRSOPA (29) (см. Таблицу 1), или способность интубировать (если возможно) и обеспечить PPV должны привести к большему количеству эффективная вентиляция.
Таблица 1 . Мнемоника используется для напоминания поставщикам об оптимизации вентиляции.
Недавно были описаны потенциальные пути к смертности, связанной с БА, у доношенных детей в условиях ограниченных ресурсов (30).Большинству младенцев (92%) требовалась PPV в DR, и серьезность респираторного нарушения была очевидна тем фактом, что у большинства умерших младенцев была тяжелая гипоксия (насыщение <80%), а также умеренная или тяжелая гипотермия (температура <36 ° C) отмечены при поступлении в неонатальное отделение. Более того, у этих новорожденных с гораздо большей вероятностью развилась энцефалопатия от умеренной до тяжелой с припадками, отмеченными в 30% случаев. Даже без доказательств тяжелого ацидоза плода совокупность этих клинических данных убедительно свидетельствует о БА как о пути к ранней смерти у большинства этих младенцев.
Последствия
Несмотря на трудности определения БА в условиях ограниченных ресурсов, существуют потенциальные возможности для снижения смертности, связанной с БА. Более половины новорожденных, умерших от БА, имели нормальную ЧСС во время родов, периодически определяемую с помощью фетоскопа. Непрерывный мониторинг ЧСС может облегчить идентификацию таких младенцев и ускорить роды находящихся под угрозой плодов (25). Послеродовая, более эффективная реанимация, включая раннюю и непрерывную PPV, поддержание герметичности, CPAP и / или интубацию (при наличии), минимизацию гипоксии и поддержание нормальной температуры — это стратегии, потенциально способные снизить смертность (28).Необходимы дополнительные базовые шаги, включая доступное оборудование, обученный персонал, квалифицированного специалиста при каждом родах. Наконец, выявление тяжелого ацидемического состояния у новорожденного может помочь дифференцировать случаи действительно асфиксии во время родов, приводящие к летальности, от тех случаев, когда смертность связана с отсроченной или неэффективной базовой реанимацией.
Авторские взносы
Все перечисленные авторы внесли существенный, прямой и интеллектуальный вклад в работу и одобрили ее к публикации.
Конфликт интересов
Авторы заявляют, что исследование проводилось при отсутствии каких-либо коммерческих или финансовых отношений, которые могут быть истолкованы как потенциальный конфликт интересов.
Рецензент SN заявил редактору о прошлом соавторстве с одним из авторов JP.
Список литературы
1. Wang H, Liddell CA, Coates MM, Mooney MD, Levitz CE, Schumacher AE, et al. Глобальный, региональный и национальный уровни неонатальной, младенческой и детской смертности в период 1990-2013 гг .: систематический анализ для глобального исследования бремени болезней 2013 г. Ланцет . (2014) 384: 957–79. DOI: 10.1016 / S0140-6736 (14) 60497-9
PubMed Аннотация | CrossRef Полный текст | Google Scholar
3. Лаун Дж. Э., Бленкоу Х., Оза С., Ю Д., Ли А. С., Вайсва П. и др. Каждый новорожденный: прогресс, приоритеты и потенциал за пределами выживания. Ланцет . (2014) 384: 189–205. DOI: 10.1016 / S0140-6736 (14) 60496-7
PubMed Аннотация | CrossRef Полный текст | Google Scholar
4. Бленкоу Х., Кузенс С., Джассир Ф. Б., Сэй Л., Чоу Д., Мазерс С. и др.Национальные, региональные и мировые оценки показателей мертворождаемости в 2015 году с тенденциями с 2000 года: систематический анализ. Lancet Global Health. (2016) 4: e98–108. DOI: 10.1016 / S2214-109X (15) 00275-2
PubMed Аннотация | CrossRef Полный текст | Google Scholar
5. Lawn JE, Blencowe H, Waiswa P, Amouzou A, Mathers C., Hogan D, et al. Мертворождения: частота, факторы риска и ускорение к 2030 году. Lancet . (2016) 387: 587–603. DOI: 10.1016 / S0140-6736 (15) 00837-5
PubMed Аннотация | CrossRef Полный текст | Google Scholar
6.Американский колледж акушеров и гинекологов. Оперативные вагинальные роды . Вашингтон: Колледж (1991).
Google Scholar
8. Голдабер К., Гилстрап III Л., Левено К., Дакс Дж., Макинтайр Д. Патологическая ацидемия плода. Obstet Gynecol. (1991) 78: 1103–7.
PubMed Аннотация | Google Scholar
9. Сехдев Х.М., Стамилио Д.М., Маконес Г.А., Грэм Э., Морган М.А. Факторы прогнозирования неонатальной заболеваемости у новорожденных с pH пуповины менее 7.00. Am J Obstet Gynecol. (1997) 177: 1030–4. DOI: 10.1016 / S0002-9378 (97) 70008-5
PubMed Аннотация | CrossRef Полный текст | Google Scholar
10. Кинг Т.А., Джексон Г.Л., Джози А.С., Ведро Д.А., Хокинс Х., Бертон К.М. и др. Эффект глубокой ацидемии пупочной артерии у доношенных новорожденных, поступивших в отделение для новорожденных. J Pediatr. (1998) 132: 624–9. DOI: 10.1016 / S0022-3476 (98) 70350-6
PubMed Аннотация | CrossRef Полный текст | Google Scholar
12.Goodwin TM, Belai I, Hernandez P, Durand M, Paul RH. Асфиксические осложнения у доношенных новорожденных с тяжелой пупочной ацидемией. Am J Obstet Gynecol . (1992) 167: 1506–12. DOI: 10.1016 / 0002-9378 (92) 91728-S
PubMed Аннотация | CrossRef Полный текст | Google Scholar
14. Рудольф AM, Heymann MA. Кровообращение плода внутриутробно. Методы изучения распределения кровотока, сердечного выброса и кровотока в органах. Circ Res. (1967) 21: 163–84. DOI: 10.1161 / 01.RES.21.2.163
PubMed Аннотация | CrossRef Полный текст | Google Scholar
16. Koehler RC, Jones M, Traystman RJ. Церебральная реакция кровообращения на угарный газ и гипоксическую гипоксию у ягненка. Am J Physiol Heart Circ Physiol. (1982) 243: h37–32. DOI: 10.1152 / ajpheart.1982.243.1.h37
PubMed Аннотация | CrossRef Полный текст | Google Scholar
17. Джонс М., Шелдон Р. Э., Петерс Л. Л., Маковски Е. Л., Мешия Г. Регулирование церебрального кровотока у плода овцы. Am J Physiol Heart Circ Physiol. (1978) 235: h262–6. DOI: 10.1152 / ajpheart.1978.235.2.h262
PubMed Аннотация | CrossRef Полный текст | Google Scholar
18. Ашвал С., Дейл П.С., Лонго Л.Д. Регионарный церебральный кровоток: исследования на плоде ягненка при гипоксии, гиперкапнии, аддозе и гипотонии. Pediatr Res. (1984) 18: 1309–16. DOI: 10.1203 / 00006450-198412000-00018
PubMed Аннотация | CrossRef Полный текст | Google Scholar
19.Dawes G, Jacobson H, Mott JC, Shelley HJ, Stafford A. Лечение асфиксированных зрелых плодов ягнят и макак-резусов внутривенным введением глюкозы и карбоната натрия. J. Physiol. (1963) 169: 167–84. DOI: 10.1113 / jphysiol.1963.sp007248
PubMed Аннотация | CrossRef Полный текст | Google Scholar
20. Линде Дж. Э., Шульц Дж., Перлман Дж. М., Оймар К., Фрэнсис Ф., Эйлевстьённ Дж. И др. Нормальная частота сердечных сокращений новорожденного в первые пять минут жизни оценивается с помощью электрокардиографии с сухим электродом. Неонатология . (2016) 110: 231–7. DOI: 10.1159 / 000445930
PubMed Аннотация | CrossRef Полный текст | Google Scholar
21. Мсемо Г., Массаве А., Ммбандо Д., Русибамайила Н., Манджи К., Киданто Х. Л. и др. Показатели смертности новорожденных и новорожденных в Танзании после тренинга «Помогаем младенцам дышать». Педиатрия . (2013) 131: e353–60. DOI: 10.1542 / peds.2012-1795
PubMed Аннотация | CrossRef Полный текст | Google Scholar
23. Эрсдал Х.Л., Мдума Э., Свенсен Э., Перлман Дж. М..Раннее начало основных реанимационных мероприятий, включая вентиляцию с помощью лицевой маски, может снизить смертность, связанную с асфиксией при рождении, в странах с низким уровнем дохода. Реанимация. (2012) 83: 869–73. DOI: 10.1016 / j.resuscitation.2011.12.011
PubMed Аннотация | CrossRef Полный текст | Google Scholar
24. Энгл В. Д., Лэпток А. Р., Перлман Дж. М.. Острые изменения в PaCO 2 , кислотно-основном статусе и ранних неврологических характеристиках у доношенных детей после перинатальной асфиксии. Реанимация . (1999) 42: 11–17. DOI: 10.1016 / S0300-9572 (99) 00081-7
CrossRef Полный текст | Google Scholar
25. Камала Б.А., Эрсдал Х.Л., Дален И., Абейд М.С., Нгарина М.М., Перлман Дж. М., Киданто Х.Л. Внедрение нового непрерывного фетального допплера (Moyo) улучшает качество мониторинга сердечного ритма плода во время родов в специализированной больнице с ограниченными ресурсами в Танзании: обсервационное исследование. PLoS ONE. (2018) 13: e020569. DOI: 10.1371 / journal.pone.0205698
PubMed Аннотация | CrossRef Полный текст | Google Scholar
26.Mdoe PF, Ersdal HL, Mduma E, Moshiro R, Dalen I., Perlman JM, Kidanto H. Рандомизированное контролируемое испытание непрерывного допплерографии по сравнению с периодическим мониторингом сердечного ритма плода с помощью фетоскопа в условиях ограниченных ресурсов. Int J Gynaecol Obstet. (2018) 143: 344–50. DOI: 10.1002 / ijgo.12648
PubMed Аннотация | CrossRef Полный текст | Google Scholar
27. Perlman JM, Risser R: Сердечно-легочная реанимация в родильном зале: связанные клинические события. Arch Pediatr Adolesc Med. (1995) 149: 20–5. DOI: 10.1001 / archpedi.1995.02170130022005
CrossRef Полный текст | Google Scholar
28. Литтл Дж., Кинан В., Сингхал Н., Нирмейер С. Помощь младенцам дышать: эволюция глобальной программы реанимации новорожденных для регионов с ограниченными ресурсами. Neoreviews . (2015) 15: e369–80. DOI: 10.1542 / neo.15-9-e369
CrossRef Полный текст | Google Scholar
29. Вайнер Г., Зайчкин Ю. редакторы. Учебник реанимации новорожденных (НРП) .7-е изд. Элк Гроув, Иллинойс: Американская академия педиатрии и Американская кардиологическая ассоциация (2017). п. 82.
Google Scholar
30. Моширо Р., Перлман Дж. М., Мдоэ Р., Киданто Х., Квалёй Дж. Т., Эрсдал Х.Л. Возможные причины ранней смерти новорожденных, поступивших в сельскую больницу Танзании. PLOS ONE . (2019) 14: e0222935. DOI: 10.1371 / journal.pone.0222935
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Наблюдение за развитием младенцев, испытывающих перинатальную асфиксию
С первыми активными вдохами после рождения новорожденный приводит в движение каскад событий, который заканчивается успешным переходом от внутриутробной жизни к внеутробной.Когда легкие надуваются, уровень кислорода в крови младенца повышается. Кровяное давление также повышается, что заставляет больше крови течь через теперь раздутые легкие, где происходит газообмен. Когда легкие надуваются и наполняются кровью, они заменяют плаценту в качестве органа дыхания. Легкие теперь несут ответственность за постоянное поступление кислорода в кровь и удаление углекислого газа.
У большинства новорожденных нет проблем с установлением первого эффективного дыхания, которое запускает эту последовательность изменений.Если младенец не может начать и поддерживать эффективное дыхание после рождения, или если плацента вышла из строя до рождения, кислород и углекислый газ не могут быть должным образом обменены, что приводит к опасному падению уровня кислорода в крови младенца, сопровождаемому повышением уровня углекислого газа и накопление кислоты. Эта комбинация событий называется перинатальной асфиксией (буквально означает удушье). Если быстро не исправить, сердце ослабнет, а частота сердечных сокращений опасно замедлится, не давая достаточному количеству крови достичь органов, особенно мозга.Органы, в первую очередь мозг, могут быть повреждены, иногда безвозвратно.
Перинатальная асфиксия встречается как у недоношенных, так и у доношенных детей. Как правило, если эпизод асфиксии протекает в легкой форме, у младенцев нет признаков стойкого повреждения мозга и долговременных проблем развития. Однако, если эпизод асфиксии тяжелый, младенец может умереть или выжить с пожизненными неврологическими нарушениями, включая церебральный паралич, умственную отсталость, нарушения зрения и слуха и неспособность к обучению.Такие проблемы не обязательно проявляются до тех пор, пока младенец не подрастет, что требует длительного наблюдения.
Любой младенец, переживший перинатальную асфиксию, должен пройти специальное наблюдение в течение первых нескольких лет жизни. Целью последующего наблюдения за младенцами, страдающими асфиксией, является выявление потенциальных неврологических проблем и проблем развития с направлением на соответствующие интервенционные методы лечения в самом раннем возрасте.
В течение раннего периода наблюдения младенец должен периодически проходить специальную оценку двигательного развития для выявления возможных проблем с мышечным тонусом (силой) и любых признаков церебрального паралича.Любые признаки проблем с мышцами требуют последующих обследований физической и / или профессиональной терапии с продолжающейся терапией при наличии показаний.
Орально-моторные и глотательные затруднения также могут возникать у младенцев в тяжелой форме асфиксии и мешать нормальному кормлению. У некоторых младенцев проблемы возникают только из-за того, что пища становится более текстурной. Первым признаком может быть неудовлетворительная прибавка в весе, поскольку младенец испытывает трудности с потреблением достаточного количества калорий. С трудностями при кормлении лучше всего обращаться к эрготерапевту и / или логопеду, имеющему специальную подготовку и опыт решения проблем с питанием у детей.Лечащий врач ребенка может также захотеть провести специальные рентгеновские исследования, чтобы оценить орально-моторный процесс и процесс глотания.
Регулярные осмотры глаз и слуха у младенцев, страдающих асфиксией, рекомендуются перед выпиской из больницы и снова в возрасте от 6 до 12 месяцев (с поправкой на недоношенность). Дополнительные обследования будут определяться в соответствии с типом выявленных проблем.
Тестирование развития и психологическое тестирование рекомендуется начиная с возраста 1 года (с поправкой на недоношенность).В этом возрасте начинают использоваться более высокие когнитивные области мозга, которые впоследствии могут быть оценены на предмет каких-либо признаков повреждения. Эти оценки включают оценку интеллектуальных и поведенческих навыков, а также конкретных академических способностей в более старшем возрасте. Ожидается, что эти оценки будут распространяться на весь школьный возраст, поскольку различные области мозга продолжают развиваться и с возрастом все чаще используются.
Родители должны проконсультироваться с лечащим врачом своего младенца для получения информации о том, где можно получить наблюдение за развитием в их районе.
Контактное лицо по электронной почте
Повреждение головного мозга в результате асфиксии около или около Асфиксия при рождении оказывает различное воздействие на мозг новорожденного в зависимости от гестационного возраста ребенка, а также тяжести и времени начала удушья, которое может произойти в любой момент в дородовой, интранатальный и послеродовой периоды жизни ребенка. Хотя гипоксически-ишемическая энцефалопатия (ГИЭ) является признаком тяжелой асфиксии, в таких случаях часто может наблюдаться мультисистемная недостаточность, включающая
Они хорошо описаны в стандартных учебниках и обзорных статьях (3-7). Повторное рассмотрение многих из этих «стандартных» протоколов выходит за рамки данной статьи. Вместо этого цель данной статьи состоит в том, чтобы осветить определенные аспекты медицинского лечения асфиксии при рождении и поделиться некоторым из нашего опыта с надеждой, что это приведет к дальнейшему обсуждению и оценке такой практики в отдельных подразделениях. Это также может послужить стимулом для Хотя некоторые младенцы (небольшая часть) рождаются неожиданно «плоскими», важно предвидеть, какие младенцы могут нуждаться в реанимации. В связи с этим в дородовой и во время родов Большинство доношенных детей, страдающих асфиксией, выздоравливают при соответствующей вентиляции, даже при комнатной температуре. Высокая концентрация дополнительного кислорода. (80–100%) обычно рекомендуются в большинстве учебников и руководств по реанимации новорожденных.Однако нет никаких научных оснований для такой рекомендации, и результаты недавнего крупного многоцентрового международного исследования даже предполагают, что реанимация с высокой концентрацией кислорода может иметь пагубные последствия для новорожденных (8). По нашему опыту, большинству таких младенцев дополнительный кислород не требуется. Только если реанимация воздухом в помещении не принесла успеха в течение 90 секунд, мы даем концентрацию кислорода 40-60% и корректируем ее в соответствии с клиническим ответом. При интубации эндотрахеальная трубка (ЭТТ) с максимальным внутренним диаметром Наличие густого раствора, окрашенного меконием, во время доставки представляет собой особую ситуацию (9). Изотонический раствор столь же эффективен, как 5% альбумин для лечения гипотонии или для замещения объема, и имеет дополнительное преимущество, заключающееся в меньшей задержке жидкости в первые 48 часов (10). Фактически, обзор современной литературы не поддерживает продолжение использования коллоидов для восполнения объема у пациентов в критическом состоянии (11). Лекарства обычно не используются для реанимации, но в случае стойкой брадикардии или неопределяемого выброса адреналин вводится через Дальнейшее управление Даже если младенец не нуждается в HIE Лечение судорог часто бывает трудным и может потребовать многократной противосудорожной терапии. Разногласия по поводу наиболее подходящей терапии остаются, но мы обычно используем следующие препараты (13): Фенобарбитон: Он используется в качестве противосудорожного средства первой линии для контроля неонатальных судорог, принимается как начальная ударная доза 20 мг / кг. IV для обеспечения оптимального терапевтического Фенитоин: Принимается в ударной дозе 20 мг / кг внутривенно в течение не менее 20 минут, если фенобарбитон не контролирует судороги. Клоназепам: Это также хорошее противосудорожное средство второй линии, которое все чаще используется в большинстве отделений. Ударная доза составляет 100 мкг / кг внутривенно в виде медленного болюса, а младенцам обычно требуется дополнительная инфузия 10-60 мкг / кг / ч с целью достижения концентрации в плазме 30-100 мкг / литр.Необходимо внимательно следить за стабильностью дыхательных путей, поскольку угнетение дыхания может потребовать искусственной вентиляции легких. Лигнокаин: Этот препарат недавно был рекомендован при тяжелых неонатальных судорогах. Он обладает меньшим седативным действием, чем другие препараты второго ряда, и полезен при резистентных судорогах. Ударная доза составляет 2 мг / кг внутривенно, затем 2 мг / кг / час путем непрерывной внутривенной инфузии до тех пор, пока судороги не купируются. Затем настой следует прекратить в течение 24-36 часов. В ситуациях, когда судорожная активность может быть замаскирована, как в случае нервно-мышечного паралича во время вентиляции, и при отсутствии средств для церебрального мониторинга, мы выборочно вводим ударную дозу фенобарбитона.Лечение отека головного мозга у новорожденных, страдающих асфиксией, остается предметом споров и предположений. Осмотические агенты, такие как маннит, обычно не рекомендуются. Использование стероидов при цитотоксическом отеке может быть привлекательным с теоретической точки зрения, но доказательств их эффективности нет, и их не следует использовать. Высокий уровень PC0 в крови 2 может вызвать вазодилатацию Сердечно-сосудистая Частым спутником асфиксии при рождении является ишемия миокарда, приводящая к сердечной дисфункции и системному пониженному напряжению. Это приводит к недостаточной перфузии периферических тканей и тканей). системы жизненно важных органов, то есть «шок», что вызывает дальнейшую недостаточную перфузию уже скомпрометированного мозга.Клинические признаки сердечной дисфункции и периферической системной недостаточности перфузии включают задержку наполнения капилляров, брадиаритмию и повышенный центрально-периферический температурный градиент.Гипотония — это поздний признак недостаточной перфузии. Причиной гипотонии редко бывает потеря крови, чаще всего из-за периферической вазодилатации или плохого сердечного выброса. Если возможно, эхокардиография дает полезную оценку сердечной функции. В нашей практике, даже если у ребенка нормальное давление, мы регулярно делаем рентген грудной клетки для проверки кардиомегалии. Вспомогательная вентиляция легких часто необходима младенцам с тяжелой асфиксией в качестве лечения дыхательной недостаточности и как часть лечения сопутствующих проблем, таких как судороги, проходимости дыхательных путей. Если используются миорелаксанты, судорожная активность может быть пропущена, если обнаружение зависит только от наблюдения. Если возможно, мониторинг церебральной функции (CFM), Почечный Острый канальцевый некроз является частым последствием асфиксии и распознается по повышению концентрации креатинина в плазме или олигурии, определяемой как почасовой поток мочи менее 0.5 мл / кг. Однако зарождающуюся и установленную почечную недостаточность можно дифференцировать по фракционной экскреции натрия (FENA% В большинстве случаев почечная недостаточность, возникшая в результате острого некроза канальцев, улучшается консервативными методами. β 2 Агонисты адренорецепторов (сальбутамол) уменьшают гиперкалиемию, но, в отличие от детей старшего возраста, их эффективность не подтверждена у новорожденных. Кардиотоксические эффекты гиперкалиемии могут быть уменьшены путем корректировки концентрации кальция и магния в плазме. Перитонеальный диализ, гемодиализ и гемофильтрация — это варианты, доступные при Диссеминированная внутрисосудистая коагуляция Это хорошо известное осложнение асфиксии при рождении, которое требует немедленного лечения тромбоцитами, свежезамороженной плазмой и криопреципитатом. Исследования Обязательным является выполнение определенных исследований у младенцев, страдающих от последствий асфиксии при рождении. Они делятся на две категории, помогающие диагностировать и планировать Ежедневные базовые исследования должны включать определение уровня электролитов в сыворотке крови, функциональные тесты печени и почек, исследования свертывания крови и определение газов артериальной крови. Из-за мультисистемы Неврологическая реабилитация Медико-правовые вопросы A. Значительная часть судебных разбирательств по акушерской и неонатальной халатности утверждает, что неонатальное повреждение головного мозга и последующая неврологическая инвалидность, i.е., церебральный паралич, эпилепсия и умственная отсталость возникают из-за халатности медицинских работников во время беременности, родов, родов и / или в ближайшем неонатальном периоде. Хотя нет сомнений в том, что некоторые плоды и младенцы действительно получают стойкое повреждение головного мозга в результате гипоксии и ишемии в течение этого периода времени, на самом деле они составляют очень небольшой процент (примерно 10%) от общего числа неврологических заболеваний. |
Ведение родовой асфиксии при родах на дому в сельских районах Гадчироли: влияние двух типов акушерок и реанимации с помощью ротовой полости, трубки-маски или мешка-маски
В данном исследовании неонатальная помощь в домашних условиях Вмешательства по уходу были введены в сельской местности Гадчироли, где> 90% родов происходят дома.Мероприятия включали обучение грамотной деревенской женщины, VHW, тому, как присутствовать при родах вместе с TBA, и заботиться о новорожденном при рождении, включая реанимацию, если это необходимо. Вмешательства подготовленных VHW снизили смертность, связанную с асфиксией, CF почти на 50% и ASMR на 65% по сравнению с лечением только TBA. Частота легкой асфиксии также снизилась на 60%, но о ее значении нельзя судить, поскольку легкая асфиксия не была связана с риском смерти.Частота тяжелой асфиксии не снизилась. Это было понятно, учитывая тот факт, что исследование не включало каких-либо серьезных акушерских вмешательств и почти полностью упор делался на немедленную диагностику и лечение асфиксии. Это также может быть связано с тем, что некоторые из предотвращенных новых мертворождений могут проявляться как тяжелая асфиксия.
Исследование не предназначалось для сравнения различных методов реанимации. Но сравнение за разные периоды времени показывает, что для такой домашней реанимации мешок и маска были более эффективными и приемлемыми для медицинского работника.Трубка и маска были одинаково эффективны в снижении ASMR, но мешок и маска были более эффективными в снижении CF и свежего SBR, и их было легче использовать для VHW. Реанимационные мероприятия «рот в рот» с применением ТВП были наименее эффективными. Для дальнейшего снижения заболеваемости и смертности из-за асфиксии может оказаться полезным улучшение акушерского ухода в указанных родах и предотвращение ненужного использования окситоцитов неквалифицированными врачами во время родов на дому.
На основании этой оценки мы пришли к выводу, что домашние вмешательства, проводимые обученным медперсоналом при рождении, в дополнение к TBA, были эффективными в снижении смертности от асфиксии.Сумка и маска представляются более эффективным оборудованием для реанимации.
У этой оценки есть несколько ограничений. Суммарный эффект асфиксии проявляется в виде муковисцидоза, свежих мертворождений и последствий для нервного развития. У нас есть полные данные о смертях (CF и ASMR), данные о свежих SBR только с 1996 г., нет данных о влиянии на развитие нервной системы. Следовательно, оценка в основном возможна только на CF и ASMR.
Это не было контролируемым испытанием лечения асфиксии, и, следовательно, большинство оценок проводится путем сравнения до и после.Было бы этически невозможно наблюдать асфиксию при рождении, но не вмешиваться в контрольную группу. Возможность наблюдения без вмешательства была доступна только в 1995–1996 годах в зоне вмешательства до того, как VHW были обучены лечению асфиксии при рождении, что предоставило уникальные данные по наблюдению естественной заболеваемости и смертности из-за асфиксии. Следовательно, результаты последующих вмешательств необходимо сравнивать с оценками в 1995–1996 годах. Так же, как и многие другие факторы, такие как созревание навыков по мере увеличения опыта или введение других вмешательств, также могут изменить показатели результатов, прежде чем –После сравнения — менее надежное свидетельство.
Тем не менее, доступно контролируемое сравнение ASMR на основе причины смерти, назначенной путем словесного вскрытия для исходного (1993–1995), периода наблюдения (1995–1996) и интервенции (1996–1999) (Таблица 6). Такое сравнение показывает чистую разницу в ASMR между областями вмешательства и контрольными участками в период с 1993 по 1995 год на 11,7%. Эта разница объясняется более ранним обучением ТАП реанимации «рот в рот» в области вмешательства. Было обнаружено снижение ASMR на 41,8% из-за обучения VHW и использования трубки и маски.Устное вскрытие было прекращено в 1999 году, и поэтому у нас нет результатов с 2000 по 2003 год, когда были введены сумка и маска.
Эффект реанимации «рот в рот», оцениваемый TBA, путем сравнения ASMR в интервенции и контрольной зоне в 1993–1995 годах (таблица 6), показывающий разницу в 11,7%, следует понимать с двумя квалификациями. Метод вербальной аутопсии никогда не применялся у новорожденных. Оперативные органы в контрольной зоне также прошли обучение по государственной программе.
Полевые исследования асфиксии при рождении в общинах страдают неточностью, поскольку диагностическое определение асфиксии и ее измерение сопряжены с огромными трудностями. 20 Присутствие обученного наблюдателя во время родов на дом, клиническая оценка новорожденного через 1 и 5 минут, точное измерение времени при наличии экстренной ситуации, невозможность последующей встречной проверки правильности записанных данных , отличия асфиксии от других причин нарушения дыхания при рождении, этическая невозможность иметь контрольную группу — все это делает такие полевые исследования очень сложными.Следовательно, относительно неточные измерения, оценки и оценки являются неотъемлемыми ограничениями.
Мы использовали простое клиническое определение, наблюдая за новорожденным через 1 и 5 минут. Это определение было подтверждено в условиях больницы. 7 Мы изменили время первого наблюдения с 1 минуты на 30 секунд, начиная с 1999 года. Это изменение, если оно вообще будет, должно привести к увеличению частоты легкой асфиксии при рождении. Следовательно, снижение заболеваемости асфиксией в годы вмешательства не может быть объяснено изменением определения.Однако более раннее начало реанимации может улучшить результат, такой как% CF при тяжелой асфиксии, наблюдаемой с мешком и маской.
CF и ASMR основаны на смерти — определенном, поддающемся проверке событии. Это исследование показывает большое и значительное снижение этих двух показателей. Снижение смертности может быть вызвано реанимацией при рождении и последующим поддерживающим уходом за такими новорожденными, как дети из группы высокого риска (вставка 1).
Можно ли объяснить наблюдаемый эффект снижения смертности другими изменениями? В течение периода вмешательства произошло небольшое увеличение доли родов в стационаре и кесарева сечения (таблица 2).Это произошло полностью после 1999 г. (годовые данные не представлены) из-за системы стимулирования, введенной правительством в 2000 г. для неизбирательного поощрения институциональных поставок. Но это не объясняет сокращения CF и ASMR (Таблица 4), которые были полностью основаны на домашних родах, наблюдаемых VHW, или сокращении ASMR, наблюдавшемся в период с 1996 по 1999 год (Таблицы 5 и 6). Более того, рост количества родов в больницах очень незначителен. Следовательно, наблюдаемое снижение смертности от асфиксии можно отнести на счет домашних вмешательств.
Есть несколько исследований, с которыми можно сравнить результаты. Мета-анализ оценки обучения ТАП оценил чистое снижение уровня перинатальной смертности на 8% и на 11% по шкале ASMR. 21 По нашим оценкам, сокращение ASMR из-за обучения ТАП сопоставимо, 11,7% (Таблица 6). Мы не можем использовать коэффициент перинатальной смертности для оценки эффекта вмешательств против асфиксии, потому что наш пакет вмешательств по уходу за новорожденными на дому включал множество других вмешательств, чтобы повлиять на неонатальную смертность в течение 1-7 дней, что способствует увеличению перинатальной смертности.
В ходе полевых испытаний подготовки трансгендеров в сельских районах Северной Индии эффект повышения квалификации, включая экипировку сумкой и маской, сравнивался с эффектом реанимации «рот в рот». CF был меньше на 20% в группе с сумкой и маской, а ASMR в двух группах составлял 6 на 1000 и 19 на 1000. 22, 23 Наши результаты по ASMR сопоставимы по величине, но по CF мы обнаружили гораздо большее сокращение: на 55%. По нашему опыту, грамотные VHW могут лучше наблюдать и записывать по сравнению с неграмотными TBA, которые не умеют считать или записывать.VHW можно лучше обучить следовать алгоритму (вставка 1). Более того, TBA + VHW помогает лучше управлять матерью и новорожденным в критический момент родов.
Основными ограничивающими факторами внедрения являются стоимость обучения и оборудования, а также редкость использования. Трубка и маска (10 долларов) были дешевле, чем сумка и маска (20 долларов). В среднем TBA в нашем регионе выполняет от 5 до 20 доставок, а VHW обслуживает от 20 до 25 доставок в год. При частоте легкой асфиксии менее 6% (таблица 3) необходимость использования реанимационного оборудования может возникнуть один или два раза в год.Следовательно, коэффициент использования относительно низкий.
В следующей статье, 24 мы подсчитали, что вмешательства на дому в испытании Гадчироли предотвратили 31 неонатальную смерть, связанную с асфиксией, в 39 деревнях в период с 1996 по 2003 год. (Если мешок и маска использовались с начала вмешательства, вероятно, можно было бы предотвратить больше смертей.) Кроме того, мешок и маска предотвратили шесть новых мертворождений на 1000 рождений (Таблица 5), следовательно, предотвратили бы дополнительно 30 мертворождений в период с 1996 по 2003 год.Предполагая, что одна сумка и маска на деревню (до сих пор не было необходимости в замене оборудования), стоимость сумки и маски оценивалась в 13 долларов на предотвращенную смерть (свежие мертворождения + неонатальные смерти, связанные с асфиксией). Стоимость обучения и вознаграждения VHW, а также результат, такой как предотвращение неврологических последствий, в расчет не принимаются.
Однако более трудным, но важным условием является обеспечение присутствия обученного работника во время доставки на дом.Несмотря на создание штатных оплачиваемых кадров, называемых «вспомогательной медсестрой-акушеркой», одной на 5000 человек населения, почти 15 лет назад во всей стране в рамках национальной программы в Индии сообщалось о присутствии этого работника только в 15% домашних хозяйств. поставки. 25 VHW, проживающая в той же деревне, с большей вероятностью будет посещать роды на дому. В исследовании Gadchiroli 84% домашних родов принимали участие VHW (Таблица 2). Выбор оборудования будет эффективным только в том случае, если работник присутствует при рождении.
Снижение почти на 60% случаев легкой асфиксии является результатом присутствия двух акушерок (TBA + VHW) вместо одной и, как следствие, немедленной сушки, тактильной стимуляции и очистки горла. Это снизило потребность в реанимации с использованием зонда или мешка почти до 6% (частота легкой асфиксии) за последние 5 лет вмешательств. Однако маловероятно, что это окажет какое-либо влияние на смертность, потому что сначала легкая асфиксия не была связана с повышенным риском смерти (таблица 1).
В сценарии после вмешательства все факторы риска, связанные с тяжелой асфиксией или свежим мертворождением (таблица 7), предположительно были связаны с акушерством. Излишняя практика применения окситоцитов была явно связана с трехкратным риском этих событий. Поскольку продолжительные роды не показали повышенного риска асфиксии при рождении в этой когорте, они не действовали как фактор, вызывающий ложную связь между применением окситоцитов и асфиксией при рождении. Эта вредная практика требует немедленного внимания.
Лечение ГИЭ | Терапия гипотермией (охлаждение мозга)
Существует одно признанное лечение, которое может минимизировать необратимое повреждение головного мозга от гипоксически-ишемической энцефалопатии (ГИЭ). Тем не менее, его необходимо вводить очень скоро после рождения / инцидента с кислородным голоданием, чтобы он был эффективным (в идеале, в течение шести часов). Это лечение известно как терапия гипотермией, но у него много других названий, таких как «терапевтическая гипотермия», «охлаждающая терапия» и «охлаждение новорожденных». Терапия гипотермией включает охлаждение ребенка до температуры ниже гомеостаза, чтобы позволить мозгу восстановиться после гипоксически-ишемического повреждения.Обычно целевая температура составляет около 33,5 градусов по Цельсию (92,3 градуса по Фаренгейту) (1). Существует два способа проведения терапии гипотермии: использование охлаждающего колпачка для «избирательного охлаждения мозга» или путем охлаждения всего тела ребенка («охлаждение всего тела»). Любой из этих вариантов может быть эффективным; выбор использования одного по сравнению с другим зависит от того, какие протоколы используются и какое оборудование имеет конкретное отделение интенсивной терапии (2).
Перейти к:
Уход при гипотермии
До, во время и после лечения гипотермией медицинские работники должны тщательно следить за здоровьем ребенка и при необходимости проводить вмешательства.Среди прочего, это может повлечь за собой:
- Проведение анализов газов крови и лечение ацидоза (избыток кислоты в крови)
- Поддержание нормального уровня глюкозы и электролитов
- Обеспечение респираторной и сердечно-сосудистой поддержки по мере необходимости
- Тестирование и лечение инфекций
- Поддержание седативного эффекта на соответствующем уровне
- Мониторинг ЭЭГ (признаки судорожной активности) и контроль приступов
Как работает терапия гипотермии?
Когда моему ребенку следует пройти терапию от гипотермии?
Если вашему ребенку был поставлен диагноз гипоксически-ишемическая энцефалопатия (ГИЭ), врачи должны начать терапию гипотермией вскоре после кислородного голодания.По данным Организации по безопасности пациентов Академического медицинского центра (AMC PSO), в идеале терапию гипотермией следует начинать в течение шести часов после рождения (при определенных обстоятельствах это может быть сделано в течение 12 часов) (2).
Чем раньше начнется терапия гипотермии, тем больше вероятность того, что потенциальная инвалидность ребенка будет сведена к минимуму. Есть определенные критерии, которым младенцы должны соответствовать, чтобы иметь право на терапию, и они могут незначительно отличаться в зависимости от больницы, в которой находится ваш ребенок.Согласно AMC PSO, младенцам, отвечающим следующим критериям, следует давать лечебную гипотермию:
Один или несколько из следующего:
- Произошло осложнение кислородного голодания / родовая травма
- Оценка ребенка по шкале Апгар (на 10-й минуте жизни) была пять или ниже
- Ребенок перенесен в длительную реанимацию
- У ребенка тяжелый ацидоз
- У ребенка ненормальный результат анализа газов крови пуповины или новорожденного
Дополнительно, один или оба из следующих:
- У ребенка были судороги
- У ребенка наблюдались клинические признаки поражения головного мозга
AMC PSO также описывает ситуации, в которых гипотермия может считаться .Пожалуйста, ознакомьтесь с их инструкциями (2) для получения дополнительной информации.
Неспособность предоставить терапию гипотермии ребенку, который в ней нуждается, является врачебной халатностью (важно отметить, что во многих случаях ГИЭ может быть вызвано злоупотреблением служебным положением; дополнительную информацию см. На нашей странице о родовых травмах).
Согревание ребенка после гипотермии
Хотя точные способы, которыми гипотермия защищает мозг, полностью не известны, одно из предполагаемых преимуществ состоит в том, что она снижает вероятность реперфузионного повреждения.Реперфузионное повреждение возникает, когда кровоток восстанавливается слишком быстро к поврежденным частям головного мозга; это может усугубить повреждение головного мозга (3).
После терапевтического переохлаждения ребенка необходимо медленно согревать, чтобы предотвратить реперфузионное повреждение. AMC PSO предлагает повысить температуру ребенка на 0,2-0,5 градуса по Цельсию, пока она не достигнет 36,5 градусов по Цельсию. Поскольку существует повышенный риск судорожной активности во время согревания, врачи также должны рассмотреть возможность мониторинга ЭЭГ (2).
Где младенцы получают терапию от гипотермии?
Не все больницы будут оборудованы для обеспечения терапевтического переохлаждения, потому что не все отделения интенсивной терапии одинаковы. Например, в общинных больницах может не быть оборудования для охлаждения мозга, но у них должна быть возможность перевести ребенка в более крупную или более специализированную больницу, которая может обеспечить охлаждение. При обследовании больниц рекомендуется узнать, какой вид ухода может предоставить отделение неонатальной помощи.
* Обновление исследования: период времени для проведения лечения от гипотермии может быть больше, чем предполагалось ранее
Традиционно считалось, что терапию гипотермией необходимо проводить в течение шести часов после рождения, чтобы она была эффективной.Однако недавнее исследование (4) показывает, что это может быть не так. Laptook et al. (2017) намеревались изучить, может ли терапия гипотермии, проводимая через 6–24 часа после рождения, принести пользу младенцам с ГИЭ. Они провели рандомизированное клиническое испытание на 168 младенцах с ГИЭ средней или тяжелой степени. Их результаты были неубедительными. Однако байесовский анализ показал, что терапия гипотермией могла немного снизить вероятность смерти или инвалидности. Авторы призывают к дальнейшим исследованиям временного окна, в течение которого терапия гипотермией может быть эффективной, подчеркивая, что если позднее назначение терапии гипотермией даже немного лучше, чем отсутствие терапии гипотермией, эти знания все равно будут чрезвычайно важны. Конечно, нейрозащитное действие охлаждающего лечения тем сильнее, чем раньше оно проводится, поэтому медицинские работники должны проводить его как можно быстрее.
О справочном центре HIE и юридических центрах ABC
Справочный центр HIE находится в ведении юридического центра ABC (Reiter & Walsh, P.C.), фирмы, занимающейся врачебной халатностью, занимающейся исключительно случаями, связанными с HIE и другими родовыми травмами. Наши юристы обладают более чем 100-летним опытом работы в этом виде права и защищают интересы детей с ВИЭ и связанными с ними нарушениями с момента основания фирмы в 1997 году.
Мы с энтузиазмом помогаем семьям получить компенсацию, необходимую для покрытия их значительных медицинских счетов, потери заработной платы (если один или оба родителя вынуждены пропускать работу, чтобы ухаживать за своим ребенком), вспомогательных технологий и других предметов первой необходимости.
Если вы подозреваете, что ГИЭ у вашего ребенка мог быть вызван халатностью врача, свяжитесь с нами сегодня, чтобы узнать больше о расследовании дела. Мы предоставляем бесплатные юридические консультации, в ходе которых мы проинформируем вас о ваших юридических вариантах и ответим на любые ваши вопросы.Более того, ничего не заплатит на протяжении всего судебного процесса , если мы не добьемся благоприятного урегулирования.
Вы можете связаться с нами по телефону 888-329-0122, нажав кнопку «чат» или заполнив контактную форму.
Источники
- Wu, Y. (нет данных). Клиника, диагностика и лечение энцефалопатии новорожденных. Получено 11 апреля 2019 г. с https://www.uptodate.com/contents/clinical-features-diagnosis-and-treatment-of-neonatal-encephalopathy
- Целевая группа по неонатальной энцефалопатии Организации по безопасности пациентов Медицинского центра Academica (AMC PSO).(2016). Терапевтическая гипотермия у новорожденных: рекомендации рабочей группы по неонатальной энцефалопатии [Брошюра].
- Винтермарк, П., Хансен, А., Грегас, М. К., Соул, Дж., Лабрек, М., Робертсон, Р. Л., и Варфилд, С. К. (2011). Перфузия головного мозга у новорожденных с асфиксией, получавших терапевтическую гипотермию. Американский журнал нейрорадиологии , 32 (11), 2023-2029.
- Лэпток, А. Р., Шанкаран, С., Тайсон, Дж. Э., Муньос, Б., Белл, Э. Ф., Голдберг, Р.
.

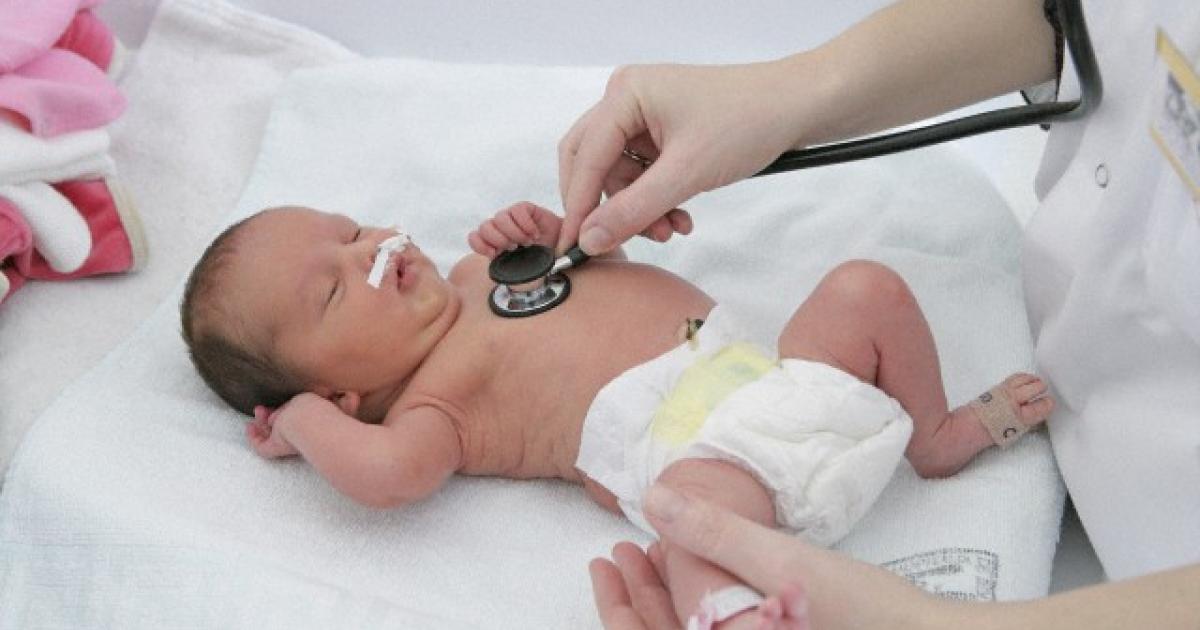 Это приводит к тому, что легкие младенца или не раскрыты полностью, или не раскрыты вообще.
Это приводит к тому, что легкие младенца или не раскрыты полностью, или не раскрыты вообще. Эта угрожающая жизни стадия может привести к нарушению функций головного мозга или к летальному исходу.
Эта угрожающая жизни стадия может привести к нарушению функций головного мозга или к летальному исходу.