Прививки Пентаксим
Вакцинация по схеме
Первичная вакцинация делается курсом, схема которого предполагает три введения вакцины плюс 1 ревакцинация. Иммунизация производится следующим образом: введение 1 дозы, через 45 дней введение 2 дозы, по прошествии еще 45 дней – введение 3 дозы, а через год после этого – обязательная ревакцинация.
Вакцинация показана детям, начиная с трех месяцев.
Схему вакцинации нарушать нежелательно, поскольку напряженность иммунитета ребенка к активным веществам вакцины может снизиться. Для детей от 1 года и старше введение вакцины Пентаксим с гемофильным компонентом выполняется однократно, Профилактика у ребенка от 1 года и старше полиомиелита, столбняка, коклюша и дифтерии в дальнейшем выполняется вакциной Пентаксим, но уже без применения гемофильной составляющей.
Плановая вакцинация
В России утвержден Национальный календарь профилактических прививок, согласно которому прививка Пентаксим детям ставится трижды – по 1 дозе в возрасте 3, 4, 5 и 6 месяцев, а в возрасте 18 месяцев выполняется ревакцинация. Приказом от 31 января 2011 года за № 51 в данный календарь также включена прививка против гемофильной инфекции.
Одновременное введение препарата. Пентаксим с другими вакцинами
Поставить прививку Пентаксим детям допускается одновременно с любыми другими вакцинами из российского календаря профилактических прививок – в один день, но в разные части тела. Исключение составляет прививка БЦЖ.
На способность выработки иммунитета (иммуногенность) применение прививки Пентаксим вместе с другими вакцинами влияния не оказывает. Не увеличивается число побочных реакций, не становится хуже переносимость прививок.
На иммунитет введение в 1 день нескольких вакцин избыточной нагрузки не оказывает.
Использовать прививку Пентаксим можно на любом этапе курса вакцинации (завершение, продолжение), даже если он был начат другими прививками от гемофильной инфекции, столбняка, коклюша, полиомиелита, дифтерии. Причем взаимозаменяемыми являются все вакцины для профилактических прививок, указанные в российском календаре.
Причем взаимозаменяемыми являются все вакцины для профилактических прививок, указанные в российском календаре.
Побочные реакции
Прививка Пентаксим может вызывать общие и местные реакции.
Общие реакции на прививку в большинстве случаев – это лихорадка, субфебрильная (до 10% детей) или фебрильная (очень редко – до 1% детей). Еще реже осложнения более тяжелые (менее 1%), проявляющиеся уплотнением в месте укола, головной болью, раздражительностью, зудом, нарушением сна, лимфоаденопатией.
Местные реакции бывают не часто (до 10% детей), из них чаще всего проявляются болезненность, отек, покраснение в месте укола.
Противопоказания
Собираясь поставить прививку Пентаксим детям, следует учитывать некоторые противопоказания:
- гиперчувствительность (подтвержденная системная реакция) к любому из составляющих прививки;
- обострение хронических болезней, острые инфекционные заболевания, увеличение температуры тела вследствие болезни – в любом из этих случаев прививка переносится до полного выздоровления;
- аллергическая реакция, появившаяся после предшествующей прививки против полиомиелита, коклюша, столбняка, дифтерии и инфекции, возбудителем которой является Haemophilus influenzae типа b.
Дополнительная информация
Прививка Пентаксим не дает иммунитет против пневмоний и менингитов другой этиологии, как и против инфекций, возбудителями которых являются Haemophilus influenzae других типов.
Делать вакцины препаратом Пентаксим можно только полностью здоровым детям, перед прививкой в обязательном порядке нужно пройти осмотр у педиатра, чтобы оценить состояние здоровья ребенка и исключить инфекционные заболевания . Нельзя использовать прививку Пентаксим, если у ребенка имеются подтвержденные неврологом противопоказания со стороны нервной системы.
Вакцина Пентаксим
Производитель: SANOFI PASTEUR, S.A., Франция
Пентаксим цена
| Услуга | Цена | Примечание |
|---|---|---|
Пентаксим, Франция (коклюш, дифтерия, столбняк, полиомиелит, гемофильная инф. ) ) | 3100 | с 3-х мес возраста |
Описание препарата
Вакцина Пентаксим — одна из самых современных комбинированных вакцин, которая позволяет единовременно защитить ребенка от пяти опасных инфекций. Пентаксим относится к новому поколению ацеллюлярных (бесклеточных) вакцин, пришедших на смену целлюлярным (клеточным) вакцинам. Ацеллюлярные вакцины менее реактогенны, т.к. лишены липополисахаридов бактериальной мембраны, вызывающих реакции после вакцинации. Пентаксим относится к высокоиммуногенным вакцинам, т.е. дающим высокий иммунный ответ организма после вакцинации.
Пентаксим является комбинированной вакциной, содержащей в своем составе адсорбированную ацеллюлярную коклюшно-дифтерийно-столбнячную вакцину, инактивированную полиомиелитную вакцину и вакцину для профилактики Haemophilus influenzae тип b. Это позволяет одним уколом иммунизировать ребенка против коклюша, дифтерии, столбняка, полиомиелита и заболеваний, вызываемых гемофильной палочкой (менингит, сепсис, пневмония, эпиглоттит и др.).
Наличие пяти компонентов в одной вакцине позволяет максимально сократить количество уколов, тем самым значительно уменьшаются болезненные ощущения у ребенка.
Показания к применению
Вакцина Пентаксим показана для первичной и бустерной иммунизации детей грудного возраста с целью профилактики дифтерии, столбняка, коклюша, полиомиелита и инфекций, вызываемых Haemophilus influenzae типа B.
Вакцина предназначена для детей в возрасте от 3 месяцев.
Способ применения и дозы
Первичная вакцинация проводится согласно календарю профилактических прививок РФ в 3, в 4,5 и 6 месяцев, ревакцинация в 18 месяцев. По рекомендации врача вакцинация и бустерная иммунизация (ревакцинация) может быть проведена по индивидуальному графику. Разовая доза вакцины составляет 0,5 мл.
В том случае, если ребенку не планируется в данный момент вакцинация от гемофильной инфекции, возможно использовать только вакцину в шприце для профилактики дифтерии, столбняка; коклюша и полиомиелита, не разводя её во флаконе с лиофилизатом, содержащим 1 дозу полисахарида Haemophilus influenzae B, конъюгированного со столбнячным анатоксином.
Совместимость с другими вакцинами
Вакцину Пентаксим можно вводить одновременно со всеми препаратами из национального календаря профилактических прививок в один день, в разные участки тела, за исключением вакцины БЦЖ. Применение вакцины Пентаксим совместно с другими прививками не влияет на их иммуногенность (способность выработки иммунитета). Переносимость вакцин не ухудшается, количество побочных реакций не возрастает. Пентаксим можно применять для продолжения и завершения курса вакцинации, начатого другими вакцинами против коклюша, дифтерии, столбняка, полиомиелита и гемофильной инфекции.
Введение нескольких вакцин в один день не является избыточной нагрузкой на иммунитет. Все вакцины национального календаря прививок России взаимозаменяемы.
Схема вакцинации
Курс первичной вакцинации состоит из 3 доз вакцины и ревакцинации. Схема иммунизации: первое введение, далее второе через 45 суток от первого, далее третье через 45 суток от второго и ревакцинация через год от законченной третьей. Применение вакцины не имеет четкой привязки к возрасту. Важно соблюдать сроки вакцинации. Если сроки удлинены, то вакцинация заново не возобновляется.
Нарушение схемы вакцинации может привести к снижению напряженности иммунитета к компонентам вакцины. Гемофильный компонент вакцины Пентаксим для детей старше года вводится однократно. Поэтому, как только ребенку старше года проводится инъекция вакцины Пентаксим с гемофильным компонентом, то она является последней для иммунизации от гемофильной инфекции. Дальнейшая профилактика дифтерии, коклюша, столбняка и полиомиелита вакциной Пентаксим у ребенка старше года проводится без использования гемофильного компонента.
Побочные действия
Препарат обычно переносится хорошо. Среди местных реакций могут встречаться покраснение, отек, болезненность в месте введения инъекции (у 10% привитых). Общие реакции в основном выражаются лихорадкой. Чаще всего субфебрильной (у 1-10% привитых), реже фебрильной (у 0,1-1% привитых). Возможно уплотнение в месте введения вакцины, которое сохраняется некоторое время, затем рассасывается.
Возможно уплотнение в месте введения вакцины, которое сохраняется некоторое время, затем рассасывается.
Как проходит вакцинация?
Вакцинация проводится в прививочном кабинете, с соблюдением всех требований санитарного режима. Все препараты сертифицированы. Сертификат на препарат предоставляется по первому требованию.
Без напоминаний, в обязательном порядке перед прививкой медицинский работник показывает препарат, срок годности вакцины.
Используется только стерильный и одноразовый инструментарий. Обязательно прививка проводится в одноразовых медицинских перчатках.
В день вакцинации ребенка осматривает врач-педиатр, измеряется температура. При отсутствии противопоказаний проводится прививка. Данные о проведенной прививке заносятся в карту, прививочный сертификат, а также даются подробные рекомендации по уходу за ребенком в поствакцинальном периоде.
Перед прививкой доктор ответит на все волнующие Вас вопросы. Обязательно возьмите на прием данные о предыдущих вакцинациях!
Пожалуйста, обратите внимание, что вакцинация ребенка, постановка реакции Манту, Диаскинтеста могут быть проведены только в присутствии родителей или законных представителей ребенка (опекунов), или при наличии у сопровождающего лица НОТАРИАЛЬНО заверенную доверенность на проведение манипуляции (с указанием препарата, планируемого к введению). В ином случае — в вакцинации будет отказано. Мы соблюдаем законы РФ.
Только у нас!
Мы осуществляем поствакцинальное сопровождение: если Вы связываете недомогание с проведенной у нас прививкой, Вы всегда можете нам позвонить или обратиться в клинику на прием к врачу-вакцинологу БЕСПЛАТНО!
Центр семейной иммунизации детской городской поликлиники № 1
Home » Новости » Центр семейной иммунизации детской городской поликлиники № 1
- ru/wp-content/uploads/thumbs_dir/IMG_20180911_100133-nw22fwkv7fsdhp8tb0olfzlwx8s9loujuv6p96v28w.jpg»>
Вакцинопрофилактика является важнейшей составляющей национальной системы здравоохранения, так как именно прививки помогают сохранить жизнь и здоровье, как отдельных людей, так и общества в целом.
В составе отделения платных услуг на базе ГБУЗ АО «Детская городская поликлиника № 1» осуществляет свою деятельность единственный в Астраханской области Центр семейной иммунизации, где прививку могут получить дети, и взрослые.
Ответить на самые популярные «прививочные» вопросы мы попросили заведующую отделением платных услуг врача аллерголога-иммунолога Ирину Лендову.
Как понять, нужны ли прививки, и какие?
— Моя позиция, как врача и как мамы однозначная – прививаться необходимо! Особенно детям. Вакцинация детей от рождения до 17 лет регламентируется Национальным календарем прививок. На сегодняшний день в него входят обязательные вакцины от одиннадцати тяжелых заболеваний, которые могут серьезно подорвать здоровье и даже привести к летальному исходу. Это и менингит, и полиомиелит, и гепатит, и дифтерия. В определенном возрасте к ним добавляются вакцины против ротавирусной инфекции, а также ветряной оспы. Есть прививки, которые ставят по индивидуальным показаниям.
Какова вероятность, что заболеет даже привитый ребенок?
— Да, такая возможность не исключается, но он перенесет болезнь намного легче и без осложнений по сравнению с малышом без прививки.
Когда нужно делать первые прививки малышу?
Самые первые прививки здоровому доношенному младенцу ставят в роддоме. Это БЦЖ (вакцина от туберкулеза) и вакцина против вирусного гепатита B. Гепатит прививают в течение первых суток после рождения, туберкулез, как правило, на третьи-четвертые сутки – перед выпиской из роддома.
Это БЦЖ (вакцина от туберкулеза) и вакцина против вирусного гепатита B. Гепатит прививают в течение первых суток после рождения, туберкулез, как правило, на третьи-четвертые сутки – перед выпиской из роддома.
Имеет ли право родитель отказаться от вакцинации в роддоме?
— Да, имеет. В этом случае еще до родов подписывается официальный отказ. Пометку об отказе фиксируют в детской выписке, а сделанные прививки запишут в прививочный сертификат. Хотя педиатры обычно рекомендуют сделать хотя бы прививку против туберкулеза, к сожалению, в нашем регионе это достаточно распространенное заболевание.
Какие прививки надо делать взрослым?
— С возрастом иммунная система уже не способна обеспечить организму адекватную защиту, даже если человек был в детстве привит. Поэтому ревакцинация от коклюша и столбняка, например, необходима раз в 10 лет. А от гриппа следует прививаться ежегодно.
Осуществить свое право на защиту от болезней может каждый гражданин, достигший совершеннолетия. Если до 18 лет у человека по каким-то причинам нет прививок, это нужно сделать обязательно. Наши специалисты подходят индивидуально к каждому пациенту и при необходимости составляют индивидуальный план прививок, согласно которому будет проведена вакцинация. Известно, что ветрянка в 30 лет переносится намного тяжелее, чем в детстве. А краснуха – страшный враг беременных женщин, у которых в организме нет антител к этой болезни.
В нашем Центре семейной иммунизации на платной основе мы предлагаем привиться против следующих заболеваний: ветряной оспы, пневмококковой инфекции, гриппа, вируса папилломы человека, вирусных гепатитов А и В, дифтерии, коклюша, столбняка, гемофильной (хиб) инфекции, клещевого энцефалита, кори, краснухи, паротита, ротавирусной инфекции, желтой лихорадки и брюшного тифа.
Отечественная или импортная вакцина. Какую выбрать?
— Выбор всегда остается за пациентом. Большой разницы между этими вакцинами нет, они все соответствуют международным стандартам, но по наблюдениям мамочек, импортные вакцины детки переносят легче.
Большой разницы между этими вакцинами нет, они все соответствуют международным стандартам, но по наблюдениям мамочек, импортные вакцины детки переносят легче.
Если хотите обязательно заграничный препарат, а его на данный момент нет в наличии или нужно поставить прививку от болезни, для которой нет отечественных вакцин – для повышения качества обслуживания граждан мы открыли предварительную электронную запись на сайте нашей поликлиники, где сам пациент выбирает удобное для него время или заказывает нужную вакцину. Когда необходимый препарат появляется в наличии, пациенту сообщают об этом сотрудники центра. Это очень удобно и для медперсонала и для самих посетителей, т.к. поток пациентов регулируется по времени, не возникает очередей и большого скопления народа, что позволяет минимизировать стрессовые ситуации и авральный режим работы в дни, когда проводится вакцинация.
Сколько это стоит? Можно ли принести свою вакцину, купленную в аптеке?
Цена будет зависеть от вакцины и стоимости непосредственно услуг центра. Как правило, в вакцинацию входит обязательный предварительный осмотр врачом. Прейскурант цен также можно найти на нашем сайте в разделе «Центр семейной иммунизации».
Поликлиника имеет право отказаться сделать прививку импортной вакциной, которую вы сами купили в аптеке. Есть строгие правила хранения и перевозки любой вакцины – соблюдение «холодовой цепи», а дать гарантию врачу, что она соблюдена, вы не можете.
Вопрос, который часто задают родители: возьмут ли без прививок в садик/школу?
Прививки – вещь, настоятельно рекомендуемая педиатрами и Минздравом, но не обязательная! Не допустить не привитого ребенка до занятий в садике или школе – грубейшее нарушение федерального закона «Об иммунопрофилактике инфекционных болезней».
Исключение – реакция Манту. Это даже не прививка, а проба. Раз в год ее обязательно нужно делать, чтобы подтвердить, что у ребенка нет туберкулеза. Но если в садике или в школе возникает эпидемия какого-то заболевания, по закону об иммунопрофилактике, в котором прописан временный отказ в приеме граждан в образовательные организации в случае возникновения массовых инфекционных заболеваний или при угрозе возникновения эпидемий, непривитого ребенка могут временно отстранить от посещений.
Но если в садике или в школе возникает эпидемия какого-то заболевания, по закону об иммунопрофилактике, в котором прописан временный отказ в приеме граждан в образовательные организации в случае возникновения массовых инфекционных заболеваний или при угрозе возникновения эпидемий, непривитого ребенка могут временно отстранить от посещений.
Имеют ли право сделать прививку без разрешения родителей?
Во всем мире законодательно закреплено, что прививки детям делают только с согласия родителей – иное считается грубым нарушением. В дошкольных и общеобразовательных учреждениях проводится плановая вакцинация, но родители должны быть заранее уведомлены и либо согласиться на прививку, либо отказаться. Все оформляется документально. Если вы принципиально против прививок в учебном учреждении, попросите отметить это в медкарте ребенка и ваш малыш должен знать, что любые уколы ему могут делать только с согласия и в присутствии родителей.
Что является основанием для противопоказания к вакцинации?
Острые инфекционные и неинфекционные заболевания, обострение хронических заболеваний – это временные противопоказания для проведения прививок. Плановые прививки проводятся через две — четыре недели после выздоровления или в период ремиссии. При нетяжелых ОРВИ, острых кишечных заболеваниях и.т.п. прививки проводятся сразу после нормализации температуры.
Среди постоянных противопоказаний ко всем прививкам сильная реакция или осложнение на предыдущую вакцинацию. Далее в зависимости от вакцины: маленький вес ребенка при рождении, прогрессирующие заболевания нервной системы, аллергия на яичный белок или пекарские дрожжи. Подробно все противопоказания расписаны в Методических указаниях МУ 3.3.1.1095-02 «Медицинские противопоказания к проведению профилактических прививок препаратами национального календаря прививок».
Вакцинопрофилактика помогает сохранить жизнь и здоровье людей и поэтому очень важно в этом вопросе довериться специалисту, его профессиональным навыкам, знаниям и опыту.
— В центре принимают только высококвалифицированные специалисты, прошедшие специальную подготовку. Имеются все необходимые лицензии и соответствующее материально-техническое оснащение.
Средний медперсонал также имеет специальную подготовку и владеет правилами организации и техникой проведения прививок.
Перед вакцинацией проводится обязательный врачебный осмотр детей и взрослых. Пациентам рассказывают о действии вакцин и о возможных реакциях. После прививки во избежание аллергических реакций за пациентом осуществляется наблюдение в течение определенного времени, с последующим осмотром врачом.
Сотрудники центра руководствуются российскими нормативными документами, регламентирующими вакцинальную деятельность.
Используются лучшие отечественные и импортные вакцины, качество которых подтверждено сертификатами.
Вся подробная информация о Центре, графике работы, стоимости услуг и о прививках, включенных в Национальный календарь профилактических прививок России можно прочесть на сайте поликлиники http://kirova47.ru в разделе «Центр семейной иммунизации».
Мы находимся по адресу: г. Астрахань, ул. Кирова, 47, обращаться в кабинет № 224 с понедельника по пятницу с 08.00 до 16.45 ч.
Телефон: (8512) 48-16-41
НА ЗАМЕТКУ
От чего убережет прививка из Национального календаря
Дифтерия
Чем опасна: Инфекция может спровоцировать тяжелую ангину, поразить гортань, сердце, почки, нервную систему. Болеют ей в любом возрасте. Осложнения разные, вплоть до параличей.
В каком возрасте прививать: 3 месяца, 4,5 месяца, 6 месяцев, 1,5 года, 6-7 лет, 14 лет
Чем прививать: АД-М, АДС, АДС-М, АКДС, Инфанрикс, Пентаксим
Столбняк
Чем опасен: Инфекция проникает в организм через раны и поражает нервную систему. Распространена повсеместно. После заболевания у человека не формируется иммунитет. Часто приводит к смерти.
Часто приводит к смерти.
В каком возрасте прививать: 3 месяца, 4,5 месяца, 6 месяцев, 1,5 года,6-7 лет, 14 лет
Чем прививать: АД-М, АДС, АДС-М, АКДС, Инфанрикс, Пентаксим
Коклюш
Чем опасен: тяжелые приступы кашля, мучающие детей. Сложней всего болезнь протекает у новорожденных. Высок риск воспаления легких. Но если уж ребенок переболел, у него формируется практически пожизненный иммунитет.
В каком возрасте прививать: 3 месяца, 4,5 месяца, 6 месяцев, 1,5 года, 14 лет
Чем прививать: АКДС, Инфанрикс, Пентаксим
Гемофильная инфекция тип b
Чем опасна: вакцину ввели календарь после роста числа заболеваний, вызванных гемофильной палочкой. Среди них пневмония, гнойный менингит, отит и сепсис. Заболевания протекают тяжело, потому что организм ребенка до пяти лет не может самостоятельно противостоять этой инфекции.
В каком возрасте прививать: 3 месяца, 4,5 месяца, 6 месяцев, 1,5 года
Чем прививать: Акт-Хиб, Хиберикс, Пентаксим
Полиомелит
Чем опасен: Инфекция, которая почти наверняка приведет к параличу или парезу рук и ног. Полностью выздоравливают не больше тридцати процентов от общего числа заболевших.
В каком возрасте прививать: 3 месяца, 4,5 месяца, 6 месяцев, 1,5 года, 20 месяцев, 14 лет
Чем прививать: Имовакс Полио, Инфанрикс Гекса, Пентаксим, Полиорикс
Гепатит B
Чем опасен: вызывает массивное поражение печени с развитием цирроза. Высока вероятность перехода в онкологию. У переболевших детей часто переходит в хроническую форму.
В каком возрасте прививать: первые сутки жизни, 1 месяц, 6 месяцев,
Чем прививать: Комбиотех, Регевак, Энжерикс В
Корь
Чем опасна: детская болезнь чревата тяжелыми осложнениями: воспалением легких, головного мозга, судорогами. При этом инфекция приводит к образованию стойкого пожизненного иммунитета. Все чаще болеют взрослые
В каком возрасте прививать: 12 месяцев, 6 лет
Чем прививать: паротитно-коревая (или коревая) вакцина, Приорикс
Эпидемический паротит (свинка)
Чем опасен: инфекция поражает слюнные железы, может добраться до поджелудочной и головного мозга.![]() Считается особо опасной для мальчиков, у которых может развиться воспаление яичек.
Считается особо опасной для мальчиков, у которых может развиться воспаление яичек.
В каком возрасте прививать: 12 месяцев, 6 лет
Чем прививать: паротитно-коревая (или паротитная) вакцина, Приорикс
Краснуха
Чем опасна: у детей обычно протекает легко, но чрезвычайно опасна для беременных женщин, точней их малышей. Поэтому прививать от нее надо, особенно девочек.
В каком возрасте прививать: 12 месяцев, 6 лет
Чем прививать: Краснуха, Приорикс
Туберкулез
Чем опасен: инфекция чаще всего поражает легкие. Сейчас она успешно, но очень долго лечится, и если не распознать болезнь на ранней стадии, может привести к смерти.
В каком возрасте прививать: 3-5 день жизни, 7 либо 14 лет. В промежутках ежегодно делать пробу Манту.
Чем прививать: БЦЖ, БЦЖ-М, для Манту — Туберкулин
Пневмококковая инфекция
Чем опасна: поражает дыхательные пути, может давать осложнения на уши, головной мозг. У детей возникают рецидивирующие отиты, бронхиты, пневмонии. Не редко может вызвать менингит.
В каком возрасте прививать: в зависимости от типа вакцины возможно, применение с двухмесячного возраста
Чем прививать: Пневмо-23, Превенар.
По желанию
Ветряная оспа
Чем опасна: У малышей до семи лет в общем-то ничем серьезным она не заканчивается, хуже, когда заразились школьники и взрослые. Они переносят инфекцию достаточно тяжело. Если решитесь прививать, то лучше сделать это перед школой.
В каком возрасте прививать: начиная с 12 месяцев
Чем прививать: Варилрикс
Гепатит А
Чем опасен: Поражает печень. Сопровождается желтухой и интоксикацией организма.
В каком возрасте прививать: можно с 12 месяцев
Чем прививать: Хаврикс 720, Хаврикс 1440, Аваксим, Вакта
Менингококковая инфекция
Чем опасна: одна из самых тяжелых бактериальных инфекций.![]() Менингит – самая распространенная ее форма. Особенно подвержены заболеванию дети.
Менингит – самая распространенная ее форма. Особенно подвержены заболеванию дети.
В каком возрасте прививать: начиная с полутора лет
Чем прививать: Менинго А+С, Менцевакс ACWY, Менактра.
Вопрос — ответ | ДГП 91
Результаты независимой оценки качества
Формирование кадрового резерва
Здоровый образ жизни
Вакцинация
Защита персональных данных
МГФОМС
ЕМИАС
Услуги и сервисы на сайте Мэра Москвы
Правительство Москвы
Департамент здравоохранения
Дирекция ДЗМ
Роспотребнадзор
Росздравнадзор
Департамент труда и социальной защиты
Министерство Здравоохранения
Скорая помощь
Краудсорсинг проекты
Мульти-тренинг Мама в деле
Союз педиатров России
Здоровая Россия
Союз педиатров России, советы родителям (видео)
Про прививки
Уважаемые родители! Мы рады сообщить Вам, что у нас в клинике проводится вакцинопрофилактика!
В связи с этим, по многочисленным просьбам родителей я отвечу на вопросы, которые наиболее часто возникают на приеме у педиатра.
Сразу же хочу сказать, что я 100-% сторонник вакцинации. Нередко в интернете и других СМИ мы сталкиваемся с потоком негативной информации о профилактических прививках. И даже у меня, врача, эта информация порой вызывала некоторые сомнения в пользе вакцинации.
Дело в том, что у нас в стране по непонятным для меня причинам активно работает целая команда антивакцинаторов, тогда как во всем цивилизованном мире вопрос о профилактике инфекционных заболеваний является основой экономической, биологической, экологической, социальной безопасности страны. Это обязательный аспект жизни, за нарушение которого следует наказание. У нас же в стране антивакцинаторы, среди которых практически нет врачей, а в лучшем случае люди с биологическим образованием ( вирусологи, химики, биологи ), своей деятельностью безнаказанно перечеркивают все достижения великих ученых, создававших вакцины и спасавших жизни миллионов людей.
Человеку всегда кажется, что если и произойдет что-то плохое, то с кем-то другим, а его самого это не коснется. Неужели эти антивакцинаторы, пропагандирующие жизнь без прививок, могут дать гарантию, что ребенок не встретится с источником какого-либо инфекционного заболевания, и, даже если это и произойдет, на его пути окажется хороший врач-профессионал? Почему в таком хрупком вопросе, как человеческая жизнь, надо полагаться на русское « авось»? Почему люди, не занимающиеся медицинской деятельностью, позволяют себе говорить о каких-то тяжелых поствакцинальных реакциях, которые они никоим образом не могут наблюдать в своей профессиональной сфере? И почему им верят и не запрещают их деятельность на государственном уровне?
В России, как и в любой другой стране, существует свой Национальный Календарь профилактических прививок. У нас, согласно этому Календарю, обязательна вакцинация против туберкулеза, гепатита В, дифтерии, коклюша, столбняка, гемофильной инфекции, кори, краснухи, паротита, пневмококка и гриппа. В других странах Национальные Календари помимо этого включают в себя и профилактику против ветряной оспы, ротовирусной и папилломавирусной инфекций. Врач, назначающий ребенку прививку, всегда должен ориентироваться на Календарь. Чтобы провести иммунизацию согласно Национальному Календарю, очень важно выбрать период, наиболее благоприятный для ребенка. Иными словами, ребенок к назначенному сроку вакцинации должен быть абсолютно здоров, у него должны быть в норме анализы и он не должен находиться в контакте с инфекционными больными в семье и детских учреждениях. Врач-педиатр-вакцинолог обязан быть непреклонен в соблюдении этих правил в день вакцинации. В обязанности же прививочной медсестры входит строгое соблюдение все принципов асептики и антисептики в специальном кабинете, контроль за температурой в холодильнике, где хранятся вакцины, контроль за их сроком годности, правильное разведение вакцины, грамотный выбор места для инъекции, обеспечение хорошей психологической доброжелательной обстановки и, конечно, наблюдение за пациентом после введения вакцины. Именно совокупность всех этих факторов и позволяет минимизировать поствакцинальные реакции.
Врач, назначающий ребенку прививку, всегда должен ориентироваться на Календарь. Чтобы провести иммунизацию согласно Национальному Календарю, очень важно выбрать период, наиболее благоприятный для ребенка. Иными словами, ребенок к назначенному сроку вакцинации должен быть абсолютно здоров, у него должны быть в норме анализы и он не должен находиться в контакте с инфекционными больными в семье и детских учреждениях. Врач-педиатр-вакцинолог обязан быть непреклонен в соблюдении этих правил в день вакцинации. В обязанности же прививочной медсестры входит строгое соблюдение все принципов асептики и антисептики в специальном кабинете, контроль за температурой в холодильнике, где хранятся вакцины, контроль за их сроком годности, правильное разведение вакцины, грамотный выбор места для инъекции, обеспечение хорошей психологической доброжелательной обстановки и, конечно, наблюдение за пациентом после введения вакцины. Именно совокупность всех этих факторов и позволяет минимизировать поствакцинальные реакции.
Не скрою, в своей профессиональной деятельности я иногда сталкиваюсь с поствакцинальными реакциями. К ним относятся гипертермия, отек и покраснение в месте инъекции, плохое самочувствие, аллергическая симптоматика. Такие реакции могут возникнуть на любую вакцину, т.к. в состав вакцины, кроме иммуногенного компонента, входят дополнительные вещества, использующиеся при ее производстве. Это и адъюванты, т.е. вещества, сохраняющие в месте инъекции вакцинальные антигены, и антибиотики, применяющиеся для уничтожения микробной клетки, и консерванты, позволяющие продлить срок годности вакцины. Например, такой адъювант, как гидроксид алюминия, присутствующий в вакцинах АКДС, «Пентаксим», «Инфанрикс», Пневмококковых вакцинах, вакцинах против гепатита В, некоторых антигемофильных вакцинах, обуславливает вышеуказанные поствакцинальные реакции. Заявления антивакцинаторов о нейротоксичности гидроксида алюминия не имеют под собой оснований, поскольку это вещество практически не растворимо и в кровоток попадает не более 0,0001% . Не содержат гидроксид алюминия вакцины против кори, паротита. краснухи, гриппа. Убрать балластные и другие неиммуногенные вещества технологически невозможно. Единственный способ – это ввести вместе с большим количеством иммуногенных компонентов меньшее количество дополнительных. Для этого и создаются поливалентные вакцины, содержащие в одной ампуле несколько иммуногенных веществ и немного балласта. Примером таких новых вакцин является «Пентаксим», содержащий анатоксины дифтерии, коклюша, столбняка, полисахарид гемофильной палочки и инактивированный вирус полиомиелита 1-3 типов, а также и дополнительные вещества — гидроксид алюминия, формальдегид, некоторые другие компоненты. АКДС-вакцина и «Инфанринкс» состоят из убитых коклюшных микробов и дифтерийно-столбнячного анатоксинов, а также гидроксида алюминия, формальдегида, консерванта.
Не содержат гидроксид алюминия вакцины против кори, паротита. краснухи, гриппа. Убрать балластные и другие неиммуногенные вещества технологически невозможно. Единственный способ – это ввести вместе с большим количеством иммуногенных компонентов меньшее количество дополнительных. Для этого и создаются поливалентные вакцины, содержащие в одной ампуле несколько иммуногенных веществ и немного балласта. Примером таких новых вакцин является «Пентаксим», содержащий анатоксины дифтерии, коклюша, столбняка, полисахарид гемофильной палочки и инактивированный вирус полиомиелита 1-3 типов, а также и дополнительные вещества — гидроксид алюминия, формальдегид, некоторые другие компоненты. АКДС-вакцина и «Инфанринкс» состоят из убитых коклюшных микробов и дифтерийно-столбнячного анатоксинов, а также гидроксида алюминия, формальдегида, консерванта.
Сейчас очень много споров как в медицинском мире, так и среди пациентов о том, какая же вакцина лучше – «инактивированная» или «бесклеточная».
Хочу немного рассказать о разнице между вакциной «Инфанрикс» производства Бельгия и российской АКДС — вакциной. Она заключается в том, что российская вакцина содержит убитые коклюшные тела, «Инфанрикс», как и «Пентаксим», содержит анатоксин коклюшный. Возможно, что переносится легче «Инфанрикс». Однако, иммунный ответ формируется лучше на введение не анатоксина, а клеточных субстратов, содержащихся в АКДС-вакцине. Практика показывает, что сейчас в странах ЕС имеет место настоящая эпидемия коклюша. Министерства здравоохранения европейских стран решают вопрос о дополнительной вакцинации детского населения вакциной «Инфанрикс» или «Пентаксим». Такая ситуация, вероятно, стала возможной в связи с тем, что выросло целое поколение детей, которых иммунизировали бесклеточным коклюшным компонентом, входящим в состав «Пентаксим», «Инфанрикс», «Инфанрикс гекса», что и способствовало формированию недостаточно крепкого противококлюшного иммунитета. Подобная ситуация стала возможна и у нас, т.к., во-первых, последние лет десять у нас в приоритете «Пентаксим» и «Инфанрикс», а не отечественная АКДС-вакцина; во-вторых, не соблюдаются сроки иммунизации (часто из-за элементарного отсутствия вакцин в России), что так же приводит к снижению напряженности иммунитета у детского населения; в-третьих, так же как люди в разных странах говорят на своих языках, так и микробы имеют в разных регионах свои антигенные отличия, которые защищают их от чужестранных вакцин и лекарственных препаратов. В своей практике я столкнулась с несколькими случаями коклюша, подтвержденного иммунологически. Ранее это были редкие, единичные случаи. Этой же зимой была совершенно нестандартная, тяжелая ситуация с заболеваемостью гриппом h2N1. Если раньше грипп редко осложнялся пневмонией, то прошедшей зимой на фоне гриппа пневмония развивалась на 1-2 день от начала заболевания. Вакцинологи обьяснили такую агрессию вируса способностью мутировать в организме человека и «увиливать» от иммунокомпетентных клеток, которые накоплены в течение жизни человека. Единственным спасением является иммунизация против гриппа. Вакцинологи, изучая «поведение» вируса гриппа и прогнозируя каждый год возможный штамм, создают новые вакцины, которые формируют хороший противогриппозный иммунитет. К сожалению, что касается гриппа, не все противовирусные препараты и индукторы интерферона действовали в этом году. Так, например, совершенно не эффективен в отношении h2N1 в эту эпидемию был старый проверенный годами Ремантадин.
В своей практике я столкнулась с несколькими случаями коклюша, подтвержденного иммунологически. Ранее это были редкие, единичные случаи. Этой же зимой была совершенно нестандартная, тяжелая ситуация с заболеваемостью гриппом h2N1. Если раньше грипп редко осложнялся пневмонией, то прошедшей зимой на фоне гриппа пневмония развивалась на 1-2 день от начала заболевания. Вакцинологи обьяснили такую агрессию вируса способностью мутировать в организме человека и «увиливать» от иммунокомпетентных клеток, которые накоплены в течение жизни человека. Единственным спасением является иммунизация против гриппа. Вакцинологи, изучая «поведение» вируса гриппа и прогнозируя каждый год возможный штамм, создают новые вакцины, которые формируют хороший противогриппозный иммунитет. К сожалению, что касается гриппа, не все противовирусные препараты и индукторы интерферона действовали в этом году. Так, например, совершенно не эффективен в отношении h2N1 в эту эпидемию был старый проверенный годами Ремантадин.
Согласно нашему демократичному законодательству, родители вправе отказаться от вакцинации своего ребенка. Конечно, всю ответственность за жизнь своего ребенка несут они сами. Но родители должны быть очень хорошо информированы и знать, на что идут и чем рискуют. Прежде всего, родителям необходимо обсудить все риски с лечащим доктором их ребенка и совместно принять решение о возможности вакцинации.
Меня окончательно убедил в пользу вакцинации один случай из жизни. Я гостила у приятелей в США. И во время моего пребывания там заболела дочь моей подруги. Заболевание сопровождалось высокой гипетермией, менингеальными знаками, сильнейшей головной болью и рвотой. Без рецепта врача, как известно, в США не купишь никакие лекарства, кроме жаропонижающих, поэтому обратиться к врачу было необходимо. Несмотря на такое тяжелое состояние ребенка, удалось записаться на прием только через два дня. До этого было рекомендовано по телефону только снижать температуру и не волноваться. На момент визита к врачу состояние девочки стало гораздо лучше, врач осмотрел и рекомендовал попить жаропонижающие препараты еще 2 дня. Я не могла не задать вопрос американской коллеге: «Как Вам не страшно? По всем критериям тут был риск менингококковай инфекции, а Вы осмотрели только через 2 дня ребенка». На что получила ответ, который окончательно развеял все мои сомнения против прививок. «А чего мне бояться?- спросила доктор. – Я посмотрела прививочный анамнез ребенка, она привита и от менингококка, и от гемофильной инфекции. А это значит, что идет банальная вирусная инфекция с такой симптоматикой. Вот и был назначен жаропонижающий препарат».
Я не могла не задать вопрос американской коллеге: «Как Вам не страшно? По всем критериям тут был риск менингококковай инфекции, а Вы осмотрели только через 2 дня ребенка». На что получила ответ, который окончательно развеял все мои сомнения против прививок. «А чего мне бояться?- спросила доктор. – Я посмотрела прививочный анамнез ребенка, она привита и от менингококка, и от гемофильной инфекции. А это значит, что идет банальная вирусная инфекция с такой симптоматикой. Вот и был назначен жаропонижающий препарат».
В заключение хочу еще раз сказать, что вакцинация в наше время нужна. Особенно с той туристической активностью, которая наблюдается последние годы в нашей стране.
Врач должен принимать решение об иммунизации ребенка, выбрав для него наиболее благоприятный период и учитывать Национальный Календарь профилактических прививок. И тогда, если через несколько лет все-таки возникнет ситуация, подобная ситуации с дочерью моей подруги, то можно будет не волноваться, не искать знакомых врачей, не думать ни о чем страшном, а просто лечить своего любимого малыша и быть уверенным в его будущем!
С уважением,
ваша Татьяна Николаевна Домостроева
ВАКЦИНАЦИЯ | Медицинский центр ГРААЛЬ
♦
NEW Ультрикс Квадри —Вакцина гриппозная четырехвалентная инактивированная расщепленная для профилактики гриппа!!! Только у нас в Истре (Медицинский центр «ГРААЛЬ»)
Самая новая вакцина от гриппа на фармакологическом рынке.
В состав входит : Антиген вируса гриппа типа A (H1N1) Антиген вируса гриппа типа A (H3N2) Антиген гриппа типа В (линия Yamagata) Антиген вируса гриппа типа В (линия Victoria)
Разрешена взрослым с 18 лет. Для детишек у нас есть другая вакцина от гриппа, а именно
♦
Гриппол плюс в Истре ( Медицинский центр «ГРААЛЬ»). Вакцина гриппозная трехвалентная инактивированная для профилактики гриппа у детей!!!
Вакцина гриппозная трехвалентная инактивированная для профилактики гриппа у детей!!!
В состав входит: Полиоксидоний, Антиген вируса гриппа типа A (H1N1)* с содержанием гемагглютинина, Антиген вируса гриппа типа A (H3N2)* с содержанием гемагглютинина, Антиген вируса гриппа типа В* с содержанием гемагглютинина.
♦
Вакцина Пентаксим в Истре ( Медицинский центр «ГРААЛЬ»).
Пентаксим – это поливалентная вакцина, которая защищает от пяти опасных инфекционно-вирусных болезней: дифтерии, столбняка, полиомиелита, коклюша и патологий, провоцируемых гемофильной инфекцией (менингита, септицемии, пневмонии).
Производителем является французская фармацевтическая компания Sanofi Pasteur.
♦
Вакцина ММR в Истре ( Медицинский центр «ГРААЛЬ»)
ММR— это комбинированная ослабленная живая вакцина от инфекций: свинки (эпидемический паротит), краснухи, кори.
В случае естественного заражения этими инфекциями антитела не допустят развитие болезней. Иммунитет против кори , краснухи и паротита после плановой вакцинации сохраняется в течение 11 лет или больше.
Иммунизация MMR вакциной делается при плановой и экстренной вакцинации
Схема иммунизации вакциной ММR:
- Иммунизация детей проводится первый раз в 12-15 месяцев
- Ревакцинация (вторая прививка MMR) в 4-6 лет, но если ее ставят раньше, то не менее чем через месяц после первой вакцинации
- Следующая прививка в 15 или 17 лет
- Возрастной группе от 22 до 29 лет
- Возрастным группам от 32 до 49 лет, а потом каждые 10 лет
Производителем вакцины является американская компания MERCKSHARP & DOHME.
♦
Вакцина Акт-ХИБ в Истре ( Медицинский центр «ГРААЛЬ»)
Вакцина Акт ХИБ — это прививка против гемофильной инфекции.
Прививка Акт-ХИБ предназначена для профилактики ХИБ-инфекций. В их число входит:
- менингит может привести к органическим поражениям головного мозга или даже к летальному исходу,
- сепсис может стать осложнением любого заболевания
- эпиглоттит опасен возникновение асфиксии (удушья)
- пневмония отличается тяжестью течения и большим количеством смертельных случаев. Гемофильная пневмония находится на втором месте по частоте среди детского населения.
- отит
- бронхит
- артрит
- и многие другие заболевания, которые вызывает палочка Haemophilus influenzae тип b.
Лечение гемофильной инфекции довольно затруднительно из-за высокой устойчивости штаммов палочки-ХИБ к антибиотикам. Именно поэтому так остро стоит вопрос о предотвращении самого факта заражения путем вакцинации.
Если пациент уже успел заразиться, проводить вакцинацию нет смысла. Препарат не останавливает активность инфекционного агента, а лишь вырабатывает правильную иммунную реакцию.
Производителем является французская фармацевтическая компания Sanofi Pasteur
♦
Вакцина Варилрикс в Истре ( Медицинский центр «ГРААЛЬ»)
Вакцина Варилрикс от ветряной оспы.
Варилрикс- это живая ослабленная вакцина вируса ветряной оспы.
Ветряная оспа-это острое вирусное заболевание. Ветрянка считается детской болезнью, но заразиться ее могут и взрослые. Возбудителем заболевания считается разновидность вируса герпеса- Varicella Zoster virus (герпес вирус 3-его типа). Заражение происходит при контакте с больным во время разговора, чихании, кашле. Во время беременности инфекция передается плоду. Заражение ветрянкой может произойти не только при контакте с больным не только ветряной оспой, но и заболевшим опаясывающим лишаем, т. к. у этих инфекций идентичный возбудитель.
к. у этих инфекций идентичный возбудитель.
Вакцинация «Варилрикс» проводится по следующей схеме:
- прививка делается детям возрастной группы от 12 месяцев и до 13 лет однократно
- детям старше 13 лет прививка делается дважды с интервалом 6-10 недель
- экстренная вакцинация «Варилрикс» делается однократно в течение 4-х суток после контакта с заболевшим ветрянкой.
На сколько лет «Варилрикс» обеспечивает иммунитет от ветрянки? Согласно инструкции минимум на 7 лет. Однако исследования крови выявляют антитела к вирусу через 10 и даже через 20 лет после прививки.
Прививка показана также пациентам из группы высокого риска:
- пациенты, получающие иммунодепресанты и кортикостероиды
- пациенты, проходящие курс лучевой терапии
- пациенты готовящиеся к трансплантации
- пациенты, страдающие хроническим нефритом и гепатитом
- больные лейкозом
Особенности вакцинации пациентов из группы высокого риска:
- вакцинация проводится в состоянии ремиссии
- пациенты, проходящую лучевую терапию, прививку делают между ее курсами
- при подготовке пациентов к трансплантации органов прививкой от ветрянки вакциной «Варилрикс» должна быть сделана за месяц до пересадки
- больным с лейкозом и пациентов принимающих антидепрессанты делается анализ крови на лимфоциты. Их количество не должно быть меньше 1200 в одном мм3 крови
После перенесенного заболевания ветряной оспы иммунитет может быть пожизненный.
Производителем вакцины «Варилрикс» является британская фармацевтическая компания GlaxoSmithKline
ВАКЦИНОПРОФИЛАКТИКА в Истре
Вакцинация в нашей клинике проводится под контролем квалифицированного специалиста в соответствии с Национальным календарем прививок. Кроме того, осуществляется вакцинация против некоторых инфекций, не входящих в список обязательных прививок, в том числе от гриппа.
В клинике используются только качественные отечественные и импортные вакцины.
Мы пристально следим за тенденциями фармацевтического рынка и оперативно приобретаем в арсенал клиники вакцины нового поколения, то есть более эффективные и безопасные.
Побочные явления вакцинации
После прививки ребенок может проявлять некоторое беспокойство, у него может отмечаться небольшое повышение температуры или такие побочные явления, как болезненность, покраснение и опухание. Эти явления обычно держатся очень непродолжительное время, и врач, как правило, посоветует вам дать ребенку жидкий нурофен, чтобы снять болезненные ощущения и снизить температуру. Если ребенок плачет некоторое время после прививки, то это, вероятно, связано с болью или испугом; если, однако, он плачет пронзительно или долго, это, вероятно, связано с реакцией. В этом случае, а также, если у ребенка наблюдается высокая температура или признаки плохого самочувствия после прививки, обратитесь к врачу.
Мифы и правда о прививках
Благодаря прививкам навсегда исчезли чума и холера, истребляющие государства и континенты.
Вакцинация стёрла с лица земли чёрную (натуральную) оспу, смертность от которой достигала 40%, а у выживших людей навсегда оставляла обезображивающие рубцы на лице и теле. Окончательное исчезновение оспы в мире было объявлено на Ассамблее ВОЗ в 1980 году. С того же времени была прекращена сама вакцинация от оспы. В наше время благодаря прививкам удалось остановить распространение полиомиелита в большинстве стран.
Без прививок сейчас в мире бушевали бы эпидемии опасных инфекций, распространяясь по всему миру гораздо быстрее, чем два века назад.
Какие мифы о прививках наиболее распространены
Вся правда о прививках — волнующая тема для родителей и животрепещущая — для СМИ. Рассмотрим, как опровергают врачи некоторые мифы о прививках.
Миф № 1 — о вакцинах, содержащих ртуть
«Вакцины содержат ртуть в качестве консерванта и провоцируют развитие аутизма у детей»
Правда такова — в составе некоторых вакцин действительно в качестве консерванта содержится этил ртути (мертиолят или тимеросал). Этил ртути используется для защиты вакцины от попадания в неё микробов. Однако незначительное количество тимеросала в 1 дозе 6 мкг не может навредить здоровью. По нормативам ВОЗ, грудной ребёнок, может, без опасения для здоровья получать в неделю 5 мкг ртути. К тому же мертиолят выводится из организма меньше чем за неделю, в то время как метил ртути может находиться до 40 дней. В действительности, содержание ртути в продуктах питания, которые мы употребляем, намного выше, чем в 1 дозе вакцины. К примеру, в креветках содержится ртути 27 мкг на 1 кг. В тунце, который мы употребляем, ртути содержится до 165 на 1 кг, а в жареном палтусе 70 мкг на 1 кг.
Этил ртути используется для защиты вакцины от попадания в неё микробов. Однако незначительное количество тимеросала в 1 дозе 6 мкг не может навредить здоровью. По нормативам ВОЗ, грудной ребёнок, может, без опасения для здоровья получать в неделю 5 мкг ртути. К тому же мертиолят выводится из организма меньше чем за неделю, в то время как метил ртути может находиться до 40 дней. В действительности, содержание ртути в продуктах питания, которые мы употребляем, намного выше, чем в 1 дозе вакцины. К примеру, в креветках содержится ртути 27 мкг на 1 кг. В тунце, который мы употребляем, ртути содержится до 165 на 1 кг, а в жареном палтусе 70 мкг на 1 кг.
Тем не менее под давлением общественности производители стали создавать вакцины без добавления тимеросала. В настоящее время в РФ имеются в продаже тимеросал содержащие и без него вакцины. Россия выпускает вакцину от гепатита B «Комбиотех» без содержания мертиолята (тимеросал). Отказ от прививок вакцинами, которые содержат мертиолят, однако, не смог остановить нарастание аутизма во всех странах, потому что природа аутизма генетически обусловлена и не связана с прививками.
Миф № 2 — о заработке государства на прививках
«Государство и врачи зарабатывают деньги на вакцинации, а дети страдают от прививок»
Правда — в обязанности врачей входит обеспечение прививками населения, но они не получают за это премию либо другой вид денежного вознаграждения. Что касается прибыли государства от прививок, то, напротив, оно берёт на себя охрану населения от инфекций и обеспечивает бесплатную вакцинацию по календарю. Кроме того, дорогостоящий процесс создания вакцин также финансируется государственным бюджетом.
Миф № 3 — прививки хуже инфекций
«Прививки более страшны, чем сама инфекция»
Правда о прививке — каждый лекарственный препарат, в том числе вакцины, имеют допустимые побочные действия. Осложнения после прививки развиваются в отдельных случаях, а вот после перенесённой болезни — гораздо чаще и тяжелее. По информации ВОЗ такое осложнение, как вакциноассоциированный паралитический полиомиелит наблюдается в 1 случае из 1500000 прививок. Такое осложнение, к тому же чаще развивается после применения живой оральной вакцины. В России сейчас стоит вопрос о прекращении использования живой и замены её на инактивированную вакцину. В случае же заражения полиомиелитом параличи по статистике развиваются в каждом десятом случае. При прошедшей эпидемии полиомиелита в Африке почти в каждом классе школ имелся искалеченный параличом ученик.
По информации ВОЗ такое осложнение, как вакциноассоциированный паралитический полиомиелит наблюдается в 1 случае из 1500000 прививок. Такое осложнение, к тому же чаще развивается после применения живой оральной вакцины. В России сейчас стоит вопрос о прекращении использования живой и замены её на инактивированную вакцину. В случае же заражения полиомиелитом параличи по статистике развиваются в каждом десятом случае. При прошедшей эпидемии полиомиелита в Африке почти в каждом классе школ имелся искалеченный параличом ученик.
По другим инфекциям статистика осложнений также печальна. Заболевание дифтерией заканчивается летальным исходом в 1 случае из 20. При эпидемии кори осложнение в виде пневмонии развивается в 6 случаях из 100. Энцефалит как осложнение кори выявляется в 1 случае из 1000. Прививка же от кори в большинстве случаев протекает в форме лёгкой реакции на месте инъекции.
Миф № 4 — о прививке вакциной АКДС
«Прививка АКДС даёт слишком много реакций, и вакцину нужно отменить»
Правда действительно совпадает с нареканиями. Однако нужно учесть, что тяжёлые побочные реакции от прививки вакциной АКДС даёт только её коклюшный компонент. В 70-х годах в Японии прививка АКДС была отменена. Три последующих года без вакцинации повлекли за собой подъем заболеваемости коклюшем, приведший к 41 смертельному исходу на 13 000 заболевших. Инфекцию удалось погасить возобновлением прививок с применением другой, более лёгкой вакцины. Во многих странах, в том числе в России, для поддержания иммунитета от коклюша при ревакцинации стала применяться бесклеточная вакцина «Инфанрикс». Она настолько же эффективна, как цельноклеточная АКДС, но даёт намного меньше реакций.
Миф № 5 — о вине прививок в смерти детей
«Вакцинация повинна во внезапной младенческой смерти»
Правда — в мифах о прививках циркулирует неподтвержденная научно идея о связи вакцинации с внезапной смертью детей раннего детского возраста. Так называемый синдром внезапной младенческой или детской смерти (СВМС или СВДС).
Внезапная смерть взрослого человека или младенца известна не только врачам во всём мире. Из общего числа внезапных летальных исходов детская смертность составляет не более 9%. Чаще всего синдром регистрируется в США, Новой Зеландии, Англии, России. Большинство случаев младенческой смертности в возрасте 2–4 месяцев регистрируется как раз во время проведения прививок. В связи с этим исследования, проведённые в институте США, не смогли доказать причастность прививок к синдрому детской смертности.
Миф № 6 — о вреде прививок для детей до года
«Нужно подождать с прививками до года, когда ребёнок окрепнет, и тогда уже прививать»
Правда в том, что у ребёнка до шестимесячного возраста имеются в организме защитные материнские антитела. По истечении 6 месяцев он ещё может получать антитела против инфекций с молоком матери. При искусственном вскармливании иммунная система ребёнка после 6 месяце очень уязвима против инфекций. В этом возрасте ребёнок начинает активную жизнь и контактирует с родственниками и соседями, подвергаясь риску инфицирования.
К 6 месяцам ребёнок по календарю прививок успевает получить защиту против туберкулёза, гепатита B, дифтерии, коклюша, столбняка и полиомиелита. Таким образом, прививки гарантируют малышу безопасное знакомство с окружающим миром.
Миф № 7 — о вреде прививки против гепатита
«Гепатитная вакцина разрушает печень»
Правда такова, что прививка от гепатита B не может оказать отрицательного воздействия на печень, так как вакцина не метаболизируется в ней. Сложные химические процессы расщепления и трансформации вакцины происходят в плазме крови, а не в печёночных клетках. Антиген вакцины захватывается кровяными клетками, после чего в ответ иммунные клетки индуцируют антитела против вируса гепатита.
Миф № 8 — о замалчивании вреда от прививок
«Государство замалчивает действительное число случаев побочного действия прививок»
Правда состоит в том, что согласно закону «Об иммунопрофилактике инфекционных заболеваний» все случаи побочного действия вакцин входят в государственную статистику. Случаи осложнений после прививок врачи докладывают в Федеральную службу по защите прав населения — Роспотребнадзор. Система регистрации и расследования осложнений после прививок в России на самом деле действует.
Случаи осложнений после прививок врачи докладывают в Федеральную службу по защите прав населения — Роспотребнадзор. Система регистрации и расследования осложнений после прививок в России на самом деле действует.
Миф № 9 — лучше переболеть, чем сделать прививку
«Прививка не обеспечивает 100% защиту от инфекции, тогда уж лучше переболеть»
Правда в том, что целью прививки является не только предупреждение от заражения, но также избавление от тяжёлых форм инфекций со смертельным исходом. Даже если прививка даст защиту не на 100%, а меньше, то в случае заражения человек переболеет более лёгкой формой инфекционного заболевания. В таком случае у заражённого пациента не будет тяжёлых осложнений, которые могут привести к инвалидности на всю жизнь.
Миф № 10 — о вреде комбинированных прививок
«Если уж прививать ребёнка, то не одновременно от нескольких инфекций, а раздельно, через интервал, чтобы не перегружать его иммунную систему»
Правда в том, что даже детский организм в состоянии воспринять одновременно 10 тысяч антигенов и выработать иммунитет. В комбинированной вакцине АКДС — 3002 антигена. А в комбинированной пятивалентной вакцине «Пентаксим» — всего 45 антигенов. Иммунная система при этом не напрягается, а тренируется. Комбинированные вакцины при совместном применении содержат меньше добавок, чем сумма тех же вакцин раздельно. Это значит, что риск аллергических реакций от комбинированных прививок в итоге уменьшается.
Кроме того, с вакциной человек получает меньше антигенов, чем с пищей, воздухом и водой. Ведь только в воздухе содержится неисчислимое количество различных антигенов микробов. А питьевая вода всегда содержит антигены в виде палочек и бактерий, которые мы не видим невооружённым глазом. И к такой армии антигенов организм адаптируется и вырабатывает антитела. Вы замечали, что, когда мы приезжаем в другую местность, где меняется питьевая вода, первое время случается расстройство пищеварительного тракта. Это происходит, потому что иммунная система ещё не выработала антитела к бактериальному составу местной воды.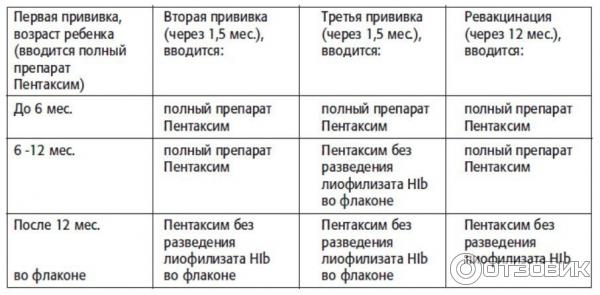 Но вот проходит 2–3 дня, и наша иммунная система выработала антитела, которые автоматически продолжают успешно бороться с бактериями местной воды.
Но вот проходит 2–3 дня, и наша иммунная система выработала антитела, которые автоматически продолжают успешно бороться с бактериями местной воды.
В заключение подчеркнём, что большинство мифов о вакцинации рождаются от медицинской неосведомлённости и страха перед неизвестным. Надеемся, что наши ответы внесли ясность и позволят изменить отношение людей к вакцинации.
В России производство вакцин осуществляется в государственных НИИ. Наблюдение за качеством выпускаемых вакцин ведёт НИИ стандартизации и контроля медицинских биологических препаратов им. Л. А. Тарасевича. Все вакцины проходят лабораторные и клинические испытания на безопасность применения. Случаи реакций на прививку врачи сообщают в Роспотребнадзор. Закупка импортных вакцин и их регистрация в России проводятся под контролем Министерства Здравоохранения.
обзор 16-летнего клинического опыта
Expert Rev. Vaccines 10 (7), (2011)
1002
Vaccine Profile Plotkin, Liese, Madhi & Ortiz
12 Decker M, Bogaerts H, Edwards K.
Комбинированные вакцины. В кн .: Вакцины. 5-е издание
. Плоткин С.А., Оренштейн В., Оффит ПА
(Ред.). Saunders Co., PA, USA 1069–1101
(2008).
• Обзор комбинированных вакцин.
13 Вт JP, Wolfson LJ, O’Brien KL et al.
Бремя болезней, вызываемых Haemophilus
гриппом типа b у детей младше
5 лет: глобальные оценки. Ланцет 374 (9693),
903–911 (2009).
14 Всемирная организация здравоохранения. Дифтерия
позиционный документ. Wkly Epidemiol. Рек. 81 (3),
24–32 (2006).
15 Всемирная организация здравоохранения. Позиционный документ по столбняку
. Wkly Epidemiol. Рек. 81 (20),
198–208 (2010).
16 Всемирная организация здравоохранения.Инактивированная вакцина против полиовируса
после прекращения применения вакцины против перорального полиовируса
. Wkly Epidemiol. Рек.
81 (15), 137–144 (2006).
17 центров по контролю и профилактике заболеваний.
Рекомендуемая иммунизация детей
График
— США, 2001 г. MMWR
50 (1), 1–3 (2001).
18 центров по контролю и профилактике заболеваний.
Обновленная информация о полиовирусах вакцинного происхождения —
во всем мире, январь 2006 г. — август 2007 г.
MMWR 56 (38), 996–1001 (2007).
19 Heymann DL, Sutter RW, Aylward RB. Глобальный вызов
на новые вакцины против полиомиелита. Nature
434 (7034), 699–700 (2005).
20 Кью О.М., Саттер Р.В., де Гурвилль Е.М.,
Даудл В.Р., Палланш М.А. Вакцина-
Полиовирусы, полученные из
, и стратегия endga me
для глобальной ликвидации полиомиелита. Анну.
Ред. Microbiol. 59, 587–635 (2005).
21 Всемирная организация здравоохранения.Внедрение
инактивированной полиовакцины в страны, использующие пероральные
вакцины против полиовируса. Wkly
Epidemiol. Рек. 78 (28), 241–252 (2003).
22 Всемирная организация здравоохранения. Вакцина
производных от
полиовирусов — обновленная информация. Wkly
Epidemiol. Рек. 81 (42), 398–404 (2006).
23 Вашишта В.М., Калра А., Джон Т.Дж.,
Такер Н., Агарвал Р.К.
Рекомендации 2-го Национального консультативного совещания
Индийской академии
педиатрии по искоренению полиомиелита
и улучшению рутинная
иммунизация.Indian Pediatr. 45 (5),
367–378 (2008).
24 центра по контролю заболеваний и
профилактики. Профилактика полиомиелита в США
. Обновленные рекомендации
Консультативного комитета по практике иммунизации
. MMW R 49, 1–22
(2000).
25 Bonnet MC, Dutta A. Мировой опыт
с инактивированной вакциной против полиовируса
. Vaccine 26 (39), 4978–4983
(2008).
26 Decker MD, Edwards KM, Steinhoff MC
et al. Сравнение 13 бесклеточных коклюшных вакцин
: побочные реакции. Педиатрия 96 (3
Педиатрия 96 (3
Pt 2), 557–566 (1995).
27 Pichichero ME, Deloria MA, Rennels MB
et al. Безопасность и иммуногенность
Сравнение 12 бесклеточных коклюшных вакцин
и одной цельноклеточной коклюшной вакцины
, введенных четвертой дозой детям в возрасте от 15 до
в возрасте 20 месяцев.Педиатрия 100 (5),
772–788 (1997).
28 Beutels P, Bonanni P, Tormans G,
Canale F, Crovari PC. Экономическая оценка
всеобщей вакцинации против коклюша
в Италии. Vaccine 17 (19),
2400–2409 (1999).
29 Ekwueme DU, Strebel PM, Hadler SC,
Meltzer MI, Allen JW, Livengood JR.
Экономическая оценка использования вакцины против дифтерии,
столбняка и бесклеточного коклюша или
вакцины против дифтерии, столбняка и цельноклеточной
коклюшной вакцины в США,
1997.Arch. Педиатр. Adolesc. Med. 154 (8),
797–803 (2000).
30 Tormans G, Van Doorslaer E, Van
Damme P, Clara R, Schmitt HJ. Экономическая
оценка профилактики коклюша с помощью
цельноклеточной и бесклеточной вакцины в
Германии. Евро. J. Pediatr. 157 (5), 395–401
(1998).
31 Thisyakorn U, Montellano M, Ortiz E,
Lane A. Обзор схем введения вакцины против гепатита B
младенцам.
Представлено на 5-м Азиатском педиатрическом конгрессе
Инфекционные болезни. Тайбэй, Тайвань, 23–26
сентября 2010 г.
32 Capeding MR, Cadorna-Carlos J,
Book-Montellano M, Ortiz E.
Иммуногенность и безопасность DTaP–
IPV // PRP ~ Комбинированная вакцина T
с вакциной против гепатита B: рандомизированное открытое испытание
. Бык. Всемирный орган здравоохранения.
86 (6), 443–451 (2008).
•• Первичная серияиммуногенностьиsafet y
Испытание
на Филиппинах, после
Pentaxim ™ вна6, 10,
14 «Недельный» график.
33 Dutta AK, Verghese VP, Pemde HK,
Mathew LG, Ortiz E. Иммуногенность и
безопасность пятивалентной дифтерии, столбняка,
бесклеточного коклюша, комбинации инактивированного полиовируса,
ue вакцина (Пентаксим) с вакциной против гепатита
. Indian Pediatr. 46 (11),
975–982 (2009).
•• Первичная серияиммуногенностьиsafet y
Испытание
в Индии, после Penta xim
Администрация
на6, 10, 14 неделя
расписание.
34 Мадхи С.А., Катленд С., Джонс С., Ортис Э.
Антитела после первичной вакцинации
Устойчивость и иммуногенность / безопасность бустерной вакцины
DTaP – IPV // PRP ~ T у
младенцев из Южной Африки 18-19
мес. Программы и тезисы 26-го конгресса
Международной педиатрической ассоциации
педиатрии. Йоханнесбург, Южная Африка
(2010).
35 Мадхи С.А., Катленд С., Джонс С., Ортис Э.
Иммуногенность и безопасность бесклеточного
коклюш, дифтерия, столбняк, инактивированный
полиовирус, комбинированный Hib-конъюгат
вакцина (Pentaxim ™) и моновалентная
вакцина против гепатита B
на сроке 6, 6 месяцев возраст младенцев в Южной Африке. S. Afr.
Мед. J. 101, 126–131 (2011).
36 Канра Г., Силиер Т., Юрдакок К. и др.
Исследование иммуногенности комбинированной вакцины
против дифтерии, столбняка, бесклеточного коклюша,
инактивированной вакцины против полиомиелита, используемой для
восстановления лиофилизированной вакцины Haemophilus
в вакцине fluenzae типа B –
– 9V DTaP // одновременно с
вакциной против гепатита В через два, три и четыре
месяцев жизни.Vaccine 18 (9–10), 947–954
(1999).
37 Li RC, Li FX, Li YP и др. Иммуногенность
и безопасность пятивалентной бесклеточной
комбинированной коклюшной вакцины, включая
дифтерии, столбняка, инактивированного полиовируса
и конъюгированного Haemophilus в uenzae
2 0003 или полисахарида типа b
,
, полисахарид типа b
,
для первичной вакцины 5 месяцев возраста
у младенцев в Китае. Vaccine 29 (10),
Vaccine 29 (10),
1913–1920 (2011).
38 La ngue J, David T., Roussel F, Pines E,
Hoffenbach A. Безопасность и иммуногенность
вакцин DTaP – IPV и Act-Hib
, вводимых в комбинации или отдельно
младенцам в возрасте 2 лет. 3-х и 4-х месячный возраст.
Программы и тезисы 15-го ежегодного
собрания Европейского общества
детских инфекционных болезней. Париж, Франция
(1997).
39 Mallet E, Hoffenbach A, Salomon H,
Blondeau C, Fritzell B.Первичная
иммунизация комбинированной бесклеточной вакциной
DTaP – IPV – Act-HIB, вводимая в возрасте
2–3–4 или 2–4–6 месяцев. Программы
и Рефераты 14-го Европейского общества
по детским инфекционным заболеваниям. Элиснор,
Дания (1996) (Реферат 19).
40 Reinert P, Boucher J, Pines E, Leroux MC,
Hoffenbach A, Salomon H. Первичная или
бустерная иммунизация
вакциной DTaP – IPV
Экспертный обзор вакцин, загруженный с сайта informahealthcare.com от 41.234.15.214 от 20.05.14
Только для личного пользования.
Санофи Пастер запускает в Китае комбинированную вакцину 5-в-1
12 мая 2011 г.
Новая вакцина Пентаксим сокращает количество детских инъекций с 12 до четырех
Компания по производству вакцин Sanofi Pasteur представила Пентаксим, первую в Китае комбинированную вакцину 5-в-1 для иммунизации против дифтерии, столбняка, коклюша, полиомиелита и Haemophilus influenzae типа b.
Вакцина
Пентаксим (DTaP-IPV-Hib) впервые поступила в продажу в 1997 году. На сегодняшний день более 100 миллионов доз пентаксима были распределены в более чем 100 странах, и вакцина была включена в национальные программы иммунизации в 23 странах.
Вакцина Пентаксим — первая бесклеточная пентавалентная вакцина от коклюша в Китае против пяти смертельных детских болезней. Это сокращает количество прививок с двенадцати до четырех и обеспечивает тот же уровень защиты, что и иммунизация вакцинами с одним антигеном.
Выпуск вакцины Пентаксим состоится всего через 18 месяцев после того, как Санофи Пастер представила в Китае первую и единственную инактивированную вакцину от полиомиелита (ИПВ). Он также дополняет длинный список инновационных вакцин, которые Санофи Пастер привезла в страну, включая первую вакцину против бешенства, первую вакцину от гриппа и первую вакцину против Hib.
«Мы искренне рады и гордимся тем, что доставили в Китай первую комбинированную вакцину 5-в-1, и мы очень воодушевлены доверием и поддержкой китайских экспертов по иммунизации», — сказал генеральный директор Sanofi Кристофер А.Viehbacher.
«Спустя столетие после того, как Луи Пастер изобрел первую в мире вакцину против бешенства, Санофи Пастер по-прежнему придерживается своего видения — мира, в котором никто не страдает и не умирает от болезни, которую можно предотвратить с помощью вакцин».
Помимо меньшего количества инъекций для младенцев и большего комфорта для родителей, комбинированная вакцина 5-в-1 (DTaP-IPV-Hib) обеспечивает лучшее соблюдение графика вакцинации. Меньшее количество прививок также означает экономию времени для родителей и большую эффективность на пунктах вакцинации.
«Выпуск первой комбинированной вакцины 5-в-1 поддерживает общую приверженность китайского правительства и научного сообщества улучшению профилактического здравоохранения», — сказал профессор Шэнь Сючжуан из Пекинской детской больницы. «Комбинированные вакцины, несомненно, являются будущей тенденцией в разработке вакцин благодаря большему удобству, комфорту и безопасности».
Иммуногенность и безопасность комбинированной вакцины DTaP – IPV // PRP ~ T, вводимой с вакциной против гепатита B: рандомизированное открытое исследование
Maria Rosario Capeding
a , Josefina Cadorna-Carlos b , May Book-Montellano c , Esteban Ortiz d
Введение
Первоначальной целью Расширенной программы иммунизации ВОЗ (РПИ) была защита детей от шести детских болезней: туберкулеза, дифтерии, столбняка новорожденных, коклюша, полиомиелита и кори. Впоследствии были добавлены другие, в том числе гепатит В и Haemophilus influenzae тип b. Комбинированные вакцины, включающие несколько валентностей, помогают обеспечить высокий охват вакцинацией.
Впоследствии были добавлены другие, в том числе гепатит В и Haemophilus influenzae тип b. Комбинированные вакцины, включающие несколько валентностей, помогают обеспечить высокий охват вакцинацией.
Обеспокоенность по поводу безопасности и реактогенности цельноклеточных коклюшных вакцин (wP) привела к разработке «бесклеточных» коклюшных (AP) вакцин, содержащих очищенные антигены Bordetella pertussis , которые лучше переносятся, чем цельноклеточные вакцины, и имеют аналогичную иммуногенность. . 1 — 3 Защитная эффективность противораковых вакцин была подтверждена в контролируемых испытаниях. 4 — 6 Сегодня они используются в национальных программах иммунизации в Канаде, Соединенных Штатах Америки (США) и различных странах Европы и Азии (например, Австралии, Японии и Республике Корея). 7 В недавнем документе с изложением позиции ВОЗ в отношении коклюшных вакцин 8 говорится, что: «Лучшие вакцины против антибиотика показали такую же защитную эффективность, как и лучшие вакцины против против коклюша» и что «все лицензированные вакцины оказались высокоэффективными в борьбе с коклюшем у младенцы и дети младшего возраста ».
Санофи пастер разработала вакцину АР, содержащую коклюшный токсоид (PT) и нитчатый гемагглютинин (FHA), который используется в педиатрических комбинациях не только с белками дифтерии (D) и столбняка (T), но и с вакциной на основе инактивированного полиовируса (IPV) и вакциной . Haemophilus influenzae капсульный полирибозил-рибитол-фосфат типа b, конъюгированный со столбнячным анатоксином (PRP ~ T). Как антиген PRP ~ T, так и вакцина IPV являются вакцинами, преквалифицированными ВОЗ. 9 Вакцина DTaP – IPV // PRP ~ T (известная как Pentaxim ™ или Pentavac ™), используемая в этом исследовании, проходила клиническую оценку в различных исследованиях. 10 — 14 Вакцина была впервые лицензирована в европейских странах в 1997 году, а сейчас она лицензирована примерно в 67 странах мира.
Имеется мало данных об иммуногенности, реактогенности и безопасности комбинированных вакцин против АР во многих странах, которые следуют графикам иммунизации РПИ. В результате настоящее исследование было проведено для оценки этих характеристик, когда вакцина DTaP – IPV // PRP ~ T вводилась младенцам в возрасте 6, 10 и 14 недель вместе с сопутствующей вакцинацией против вируса гепатита B, вводимой на любом из на Филиппинах соблюдались два рекомендованных ВОЗ расписания вакцинации.Результаты сравнивали с результатами, полученными ранее у европейских младенцев, которым вводили ту же вакцину DTaP – IPV // PRP ~ T в возрасте 2, 3 и 4 месяцев.
Методы
Дизайн исследования
В этом рандомизированном контролируемом открытом исследовании участвовали младенцы из трех медицинских центров в Маниле, Филиппины: Научно-исследовательского института тропической медицины (RITM), Мемориального медицинского центра Университета Восточного Рамона Магсайсай и больницы Мэри Чилс. Комиссия по этике в каждом центре одобрила протокол.Письменное информированное согласие было получено от родителей или законных представителей младенцев до зачисления. Кроме того, матери потенциальных субъектов исследования также дали согласие на клиническую оценку и забор крови в течение третьего триместра беременности для тестирования на поверхностный антиген гепатита B (HBsAg). У тех, кто был серопозитивным по HBsAg, также измеряли уровень е-антигена гепатита В (HBeAg).
Субъекты
В исследовании участвовали здоровые доношенные новорожденные со сроком беременности ≥ 37 недель и весом ≥ 2.5 кг и чья мать была анти-HBsAg серонегативна. Все младенцы получали вакцину DTaP – IPV // PRP – T в возрасте 6, 10 и 14 недель. Кроме того, они были рандомизированы в течение 24 часов после рождения с использованием списка случайных чисел для получения рекомбинантной вакцины против гепатита В либо в возрасте 0, 6 и 14 недель (Группа A), либо в возрасте 6, 10 и 14 недель (Группа B). Младенцы, чья мать была HBsAg-серопозитивной, не включались в исследование, но получали иммуноглобулины против гепатита В и первую дозу вакцины против гепатита В в течение 24 часов после рождения.Родители или опекуны были проинформированы о серологическом статусе их ребенка, а частные врачи обеспечили последующее наблюдение.
Младенцы, чья мать была HBsAg-серопозитивной, не включались в исследование, но получали иммуноглобулины против гепатита В и первую дозу вакцины против гепатита В в течение 24 часов после рождения.Родители или опекуны были проинформированы о серологическом статусе их ребенка, а частные врачи обеспечили последующее наблюдение.
Младенцы были исключены из исследования, если у них было заболевание иммунной системы, включая ВИЧ-инфекцию, серьезные врожденные пороки или состояния, серьезное заболевание или злокачественное новообразование, неврологические расстройства или судороги в анамнезе, мать с заболеванием печени или аллергией на компонент вакцины, или если они получали иммуносупрессивную терапию (кроме ингаляционных и местных стероидов), иммуноглобулины или другие продукты крови, предыдущую иммунизацию против АКДС, H.influenzae типа b, полиомиелита или вакцины, отличной от бациллы Кальметта-Герена (БЦЖ), которая включена в национальный календарь вакцинации Филиппин.
Вакцины
Комбинированная вакцина DTaP – IPV // PRP ~ T (Pentaxim ™, партия W1538) была произведена и поставлена санофи пастер, Лион, Франция. Каждая доза 0,5 мл содержала ≥ 30 МЕ [предел флокуляции (Lf) дифтерийного анатоксина 25], ≥ 40 МЕ (10 Lf) столбнячного анатоксина, 25 мкг PT, 25 мкг FHA, 40 единиц антигена D (DU) ИПВ типа 1 (штамм Махони), 8 ЕД ИПВ типа 2 (штамм MEF-1), 32 ЕД ИПВ типа 3 (штамм Саукетта) и 10 мкг PRP ~ T.Лиофилизированный компонент PRP ~ T восстанавливали жидкой вакциной DTaP-IPV непосредственно перед инъекцией. Антигенный состав исследуемой вакцины был идентичен составу исторической контрольной вакцины. Рекомбинантная вакцина против гепатита В (Recomvax B / Euvax B, партия UVA3002, LG Life Sciences, Сеул, Республика Корея) содержала 10 мкг рекомбинантного HBsAg. Он лицензирован и коммерчески доступен на Филиппинах. Вакцины DTaP – IPV // PRP ~ T и гепатита B вводились внутримышечно в правую и левую переднюю часть бедра, соответственно.
Серология
Образцы крови были взяты для определения антител, когда младенцы были в возрасте 6 недель, непосредственно перед первой инъекцией комбинированной вакцины, и примерно в возрасте 18 недель, через месяц после третьей вакцинации. Серологические анализы были выполнены, как описано ранее 12 в центральной лаборатории Sanofi pasteur в Пенсильвании, США. Уровни антител к HBsAg, PT, FHA и антитоксину столбняка определяли с помощью иммуноферментного анализа (ELISA).Антитела против PRP измеряли с помощью радиоиммуноанализа типа Фарра. 12 Антитоксин против дифтерии и антитела против полиовируса типа 1, -2 и -3 измеряли серонейтрализацией. Предварительно определенные уровни антител для серопротекции были: анти-PRP ≥ 0,15 мкг / мл и ≥ 1,0 мкг / мл, против полиовируса ≥ 8 обратных разведений (1 / разведение), против дифтерии ≥ 0,01 МЕ / мл, против столбняка ≥ 0,01. МЕ / мл и анти-HBsAg ≥ 0,01 мМЕ / мл. Поскольку не существует общепринятых коррелятов серопротекции против коклюшных антител, ответ вакцины на противококлюшные антигены был определен как ≥ четырехкратное или ≥ двукратное увеличение концентрации антител после первичной вакцинации.
Реактогенность и безопасность
Младенцы наблюдались в течение 30 минут после каждой инъекции на предмет немедленных местных или системных реакций. Родители или законные опекуны ежедневно регистрировали вызываемые местные реакции (например, покраснение в месте инъекции, отек, боль или болезненность) и запрашиваемые системные события (например, ректальная температура ≥ 38 ° C, сонливость, необычная суетливость, необычный плач, потеря аппетита, рвота и диарея). в течение 8 дней после вакцинации. Боль или болезненность оценивались как сильные, если младенец плакал при движении конечности или если боль мешала нормальной активности.Чтобы быть серьезным, плач или раздражительность должны продолжаться более 3 часов. Лихорадка считалась тяжелой, если ректальная температура была ≥ 40 ° C. Дата начала, интенсивность и разрешение любых нежелательных явлений записывались в течение 30 дней после каждой вакцинации.
Статистический анализ
Для каждого вакцинного антигена рассчитывались средняя степень серопротекции или вакцины и средний геометрический титр антител (GMT), а также 95% доверительный интервал (ДИ) для каждой исследуемой группы и для объединенных данных из двух исследуемых групп.Кривые обратного кумулятивного распределения (RCDC) для титров антител также были построены для иллюстрации иммунных ответов.
Основная цель исследования состояла в том, чтобы показать, что уровни серопротекции дифтерии, столбняка, различных типов полиовирусов и PRP, а также частота ответа вакцины на коклюшные антигены, полученные с помощью комбинированной вакцины, не уступают таковым, наблюдаемым во французском историческом контрольном исследовании, в котором та же вакцина DTaP – IPV // PRP ~ T вводилась в возрасте 2, 3 и 4 месяцев.Это контрольное исследование было выбрано из-за отсутствия данных об использовании исследуемой вакцины в возрасте 6, 10 и 14 недель.
Вакцина считалась неэффективной, если 95% доверительный интервал серопротекции или скорости реакции вакцины полностью превышал историческое референсное значение за вычетом заранее определенной клинически приемлемой разницы в 10%. Учитывая ожидаемые уровни серопротекции и сероконверсии, полученные из исторического контрольного исследования, предварительно определенную клинически значимую разницу в 10% и мощность 90%, было обнаружено, что размер выборки 180 субъектов на группу был необходим, чтобы показать не меньшую эффективность.Кроме того, исходя из предположения, что 15% испытуемых будут потеряны для оценки, планировалось включить 212 в каждую группу. Статистический анализ проводили с использованием программного обеспечения SAS (SAS Institute, Кэри, Северная Каролина, США). Все субъекты, получившие хотя бы одну дозу комбинированной вакцины, были включены в оценку безопасности.
Результаты
Исследуемая популяция
В исследование были включены 424 младенца: 264 в RITM, 75 в Мемориальном медицинском центре Университета Восточного Рамона Магсайсай и 85 в больнице Мэри Чайлс.Из них 213 были рандомизированы в группу A, а 211 — в группу B. Младенцев мужского пола было больше, чем девочек (57% против 43%). Их средний возраст (± стандартное отклонение) при зачислении составлял 1,0 (± 0,6) дня. Их средний возраст приема первой дозы комбинированной вакцины составлял 6,4 (± 0,5) недели. Из 424 зарегистрированных младенцев 397 (204 в группе A и 193 в группе B) получили по крайней мере одну дозу комбинированной вакцины (т.е. полный набор для анализа), а 387 (200 в группе A и 187 в группе B) получили три дозы. (т.е. набор для каждого протокола).Рис. 1. Двадцать семь субъектов (6,7%, девять в группе A и 18 в группе B) прекратили исследование или были исключены из полного набора анализов до получения первой дозы комбинированной вакцины. Из тех, кто получил первую дозу, 10 не завершили исследование: четыре в группе A и шесть в группе B. Все зарегистрированные нарушения протокола, кроме одного (рис. 1), связаны с получением АКДС и пероральной вакцины против полиомиелита. Одному субъекту перед введением первой дозы комбинированной вакцины было проведено переливание крови. Два пациента выбыли из исследования из-за серьезных побочных эффектов: у одного был сепсис новорожденных, а у другого — остановка сердца и легких вследствие дефекта межжелудочковой перегородки.Ни то, ни другое не было связано с вакцинацией.
Рис. 1. Блок-схема исследования, показывающая количество младенцев, включенных в исследование, их случайное распределение и количество, которые выполнили или не выполнили схемы вакцинации
DTaP – IPV // PRP ~ T, дифтерия – столбняк – бесклеточный коклюш – инактивированный полиовирус — конъюгат Haemophilus influenzae типа b.
Иммуногенность
Наблюдаемые уровни серопротекции и ответа вакцины через 1 месяц после третьей комбинированной дозы вакцины DTaP – IPV // PRP ~ T были высокими для каждого вакцинного антигена, сходными в обеих исследуемых группах и сходными с соответствующими показателями, наблюдаемыми в историческом контрольном исследовании (Таблица 1).В обеих исследуемых группах и для каждого антигена, включенного в комбинированную вакцину, 95% доверительный интервал серопротекции или скорости ответа вакцины полностью превышал показатель исторического контрольного исследования за вычетом предварительно определенного 10% -го предела не меньшей эффективности. Объединенные данные из двух групп показали, что 98,7% имели уровень анти-PRP ≥ 0,15 мкг / мл и 67,2% имели уровень ≥ 1,0 мкг / мл. Уровень серопротекции составлял 100% для столбняка и полиовируса типа 1, -2 и -3 и 97,1% для дифтерии. Частота вакцинного ответа для анти-PT и анти-FHA, определяемая как по крайней мере четырехкратное увеличение титра антител, составляла 95.1% и 88,8% соответственно. Соответствующие показатели двукратного увеличения составили 98,8% и 95,5% соответственно. Титр антител против PT ≥ 25 эквивалентов международных единиц (ЕС) / мл наблюдался в 99,5% и 99,0% в группах A и B соответственно, а титр антител против FHA ≥ 25 EU / мл наблюдался в 98,5% и 99,4% случаев. % соответственно.
Не было значительных различий в GMT антител для любого вакцинного антигена между группами A и B, что позволило объединить данные (таблица 2).GMTs антител значительно увеличились от до и после первичной вакцинации для каждого вакцинного антигена. Объединенное значение GMT против PRP увеличилось с 0,2 до 2,0 мкг / мл. GMT антиполиовируса типа 1 увеличился с 9,3 до 569 л / разл, GMT типа 2 увеличился с 16,5 до 769 л / разл, а GMT типа 3 — с 10,3 до 1788 л / разл. GMT анти-PT и анти-FHA увеличились с 3,14 до 142 EU / мл и с 5,23 до 115 EU / мл, соответственно. Кривые обратного кумулятивного распределения (RCDC) на фиг. 2 и 3 показывают титры антител против PT и антител против FHA, соответственно, у субъектов из Группы A, Группы B, из обеих групп, объединенных вместе, и из исторического контрольного исследования. .Иммунные ответы на PT и FHA были сходными в двух исследуемых группах. RCDC для антител против PT показывают, что ответы в группах A и B были сильнее, чем в исторической контрольной группе. Серопротекторный титр анти-HBsAg ≥ 10 мМЕ / мл наблюдался как минимум у 97,8% всех младенцев (таблица 1), но GMT был выше в группе A, чем в группе B, и составлял 601 мМЕ / мл против 207 мМЕ / мл, соответственно. (Таблица 2). RCDC на фиг. 4 показывают ответы против HBsAg в группах A и B в сыворотках, полученных в возрасте 6 и 18 недель.
Рис. 2. RCDC для титров антител против коклюшного анатоксина после третьей комбинированной дозы вакцины DTaP – IPV // PRP ~ T
DTaP – IPV // PRP ~ T, дифтерия – столбняк – бесклеточный коклюш – инактивированный полиовирус — Конъюгат Haemophilus influenzae типа b; RCDC, обратная кумулятивная кривая распределения. a Историческая контрольная группа получала комбинированную вакцину DTaP – IPV // PRP ~ T в возрасте 2, 3 и 4 месяцев. b Группа A получала комбинированную вакцину DTaP – IPV // PRP ~ T в возрасте 6, 10, 14 недель и рекомбинантную вакцину против гепатита B в возрасте 0, 6 и 14 недель. c Группа B получала вакцину DTaP-IPV // PRP ~ T и рекомбинантную вакцину против гепатита B в возрасте 6, 10 и 14 недель.
Рис. 3. RCDC для титров противококлюшного нитчатого гемагглютинина после третьей комбинированной дозы вакцины DTaP – IPV // PRP ~ T
DTaP – IPV // PRP ~ T, дифтерия – столбняк – бесклеточный коклюш – инактивированный полиовирус — Конъюгат Haemophilus influenzae типа b; RCDC, обратная кумулятивная кривая распределения. a Историческая контрольная группа получала комбинированную вакцину DTaP – IPV // PRP ~ T в возрасте 2, 3 и 4 месяцев. b Группа A получала комбинированную вакцину DTaP – IPV // PRP ~ T в возрасте 6, 10, 14 недель и рекомбинантную вакцину против гепатита B в возрасте 0, 6 и 14 недель. c Группа B получала вакцину DTaP-IPV // PRP ~ T и рекомбинантную вакцину против гепатита B в возрасте 6, 10 и 14 недель.
Рис. 4. RCDC для титров поверхностных антигенов гепатита B в сыворотках, полученных в возрасте 6 и 18 недель от младенцев в группах A и B
DTaP – IPV // PRP ~ T, дифтерия – столбняк – бесклеточный коклюш – инактивированный полиовирус — Конъюгат Haemophilus influenzae типа b; RCDC, обратная кумулятивная кривая распределения. a Группа A получала комбинированную вакцину DTaP – IPV // PRP ~ T в возрасте 6, 10, 14 недель и рекомбинантную вакцину против гепатита B в возрасте 0, 6 и 14 недель. b Группа B получала вакцину DTaP-IPV // PRP ~ T и рекомбинантную вакцину против гепатита B в возрасте 6, 10 и 14 недель.
Реактогенность
Боль в месте инъекции была наиболее часто регистрируемой местной реакцией. Это наблюдалось после 12,0% и 21,2% комбинированных доз вакцины DTaP – IPV // PRP ~ T в группах A и B, соответственно, и после 13 лет.7% и 18,9% доз вакцины против гепатита В в двух группах соответственно. Сильная боль наблюдалась не более чем у 0,7% (таблица 3). Сообщалось о покраснении, отеке и уплотнении после приема не более 3% любой дозы.
Лихорадка и раздражительность были наиболее частыми нежелательными системными явлениями, при этом лихорадка наблюдалась после 12,2% и 11,0% доз в группах A и B, соответственно, и раздражительность после 11,6% до 16,6% соответственно. Сильная лихорадка или раздражительность наблюдались после 0,2% до 0.5%. Сонливость или потеря аппетита отмечались у 5,4–6,5% пациентов без серьезных случаев.
Из 397 субъектов, получивших одну дозу или более комбинированной вакцины, 213 (53,7%) сообщили по крайней мере об одном нежелательном нежелательном явлении в течение 30 дней. Только два из этих событий, оба из которых были связаны с лихорадкой после третьей дозы у младенцев в группе B, были интерпретированы исследователем как связанные с вакцинацией. Наиболее частыми нежелательными системными нежелательными явлениями в группе А были инфекция верхних дыхательных путей (42 ребенка), назофарингит (31), гипертермия (30) и кашель (26).В группе B это были инфекция верхних дыхательных путей (40 младенцев), ринофарингит (34), гипертермия (26) и кашель (20). Никакие серьезные побочные эффекты не рассматривались как связанные с вакцинацией.
Обсуждение
В этом исследовании оценивали иммуногенность и безопасность комбинированной вакцины DTaP – IPV // PRP ~ T, вводимой младенцам в качестве первичной серии в возрасте 6, 10 и 14 недель. Результаты сравнивали с исторической контрольной группой, получавшей ту же вакцину в возрасте 2, 3 и 4 месяцев в клинических испытаниях, проведенных во Франции, где вакцина применялась в повседневной практике.Младенцы были рандомизированы при рождении перед введением комбинированной вакцины для получения коммерчески доступной рекомбинантной вакцины против гепатита В либо в возрасте 0, 6 и 14 недель, либо в возрасте 6, 10 и 14 недель. Исследование предоставило важные данные о комбинированной вакцине АР, которую вводят на 6, 10 и 14 неделе во многих схемах РПИ. Насколько нам известно, это также первый клинический отчет о комбинированной вакцине против АП, вводимой вместе с моновалентной вакциной против гепатита В по графику, начиная с рождения или в возрасте 6 недель.
Иммуногенность комбинированной вакцины была высокой для всех антигенов, была сходной в двух настоящих исследуемых группах и аналогична таковой в исторической контрольной группе. Уровни серопротекции и GMTs антител, связанные с вакциной IPV, представляли особый интерес из-за используемого графика. Действительно, серозащита против всех трех полиовирусов присутствовала у всех младенцев после вакцинации. Значительное увеличение GMTs антиполиомиелитных нейтрализующих антител произошло: с 9.От 2 до 569 л / раз для полиовируса типа 1, от 16,5 до 769 л / раз для типа 2 и от 10,3 до 1788 1 / раз для типа 3. Ответ на вакцинные антигены ИПВ, представленный здесь, предоставляет дополнительные данные об иммуногенности вакцина ИПВ в тропических странах, таких как Филиппины, и согласуется с результатами предыдущих клинических исследований в странах с умеренным климатом. 10 — 17
После введения третьей дозы комбинированной вакцины титр антител против PRP был ≥ 0.15 мкг / мл у 98,7% младенцев, а анти-PRP GMT увеличился с 0,2 до 2,0 мкг / мл. Этот результат, полученный в нашем исследовании с вакцинацией, сделанной в возрасте 6, 10 и 14 недель, согласуется с результатами предыдущих исследований, в которых использовался тот же график, и с результатами исследований, в которых использовался тот же антиген PRP ~ T, но вводимые дозы в 2 года. , 3 и 4 месяца или 2, 4 и 6 месяцев. 11 , 12 , 14 , 15
Поскольку не существует признанных серологических коррелятов для защиты от коклюша, четырехкратное увеличение титра антител от до вакцинации до после вакцинации было использовано в качестве критерия ответа вакцины на коклюшные антигены.Четырехкратное увеличение титров антител против PT и против FHA было получено у 95,1% и 88,8% младенцев, соответственно, и двукратное увеличение было получено у 98,8% и 95,5% соответственно. GMTs анти-PT и анти-FHA антитела были сходными в двух исследуемых группах до вакцинации: 3,1 EU / мл для PT и 5,2 EU / мл для FHA. После вакцинации более 99% младенцев имели титр антител против PT или FHA ≥ 25 EU / мл. Распределения, наблюдаемые на RCDC, показали, что ответы FHA, индуцированные у младенцев в группах A и B, были подобны и сопоставимы с таковыми, наблюдаемыми в исторической контрольной группе (рис.2). Обе группы в этом исследовании также имели схожее распределение антител против PT, но RCDC был смещен вправо по сравнению с исторической контрольной группой, что указывает на несколько более сильный иммунный ответ в настоящем исследовании. Иммуногенность, наблюдаемая для PT и FHA, измеренная по ответу на вакцину и GMT, также согласуется с наблюдаемой в исследованиях в Европе. 11 , 12 , 14 Предыдущие исследования показали, что вакцина против АП, использованная в этом исследовании, эффективна. 4 , 6 Дополнительные доказательства были также получены в результате эпиднадзора в Швеции после нескольких лет рутинного использования в национальной программе вакцинации. 18 , 19
Доза вакцины против гепатита B, вводимая при рождении, обеспечивает защиту групп населения, где гепатит B является эндемическим и риск перинатальной передачи повышен. Вакцинация при рождении является важной мерой общественного здравоохранения для младенцев, рожденных от HBsAg-серопозитивных матерей или чей статус гепатита B неизвестен, и когда возникают ошибки скрининга. 20 , 21 Результаты этого исследования подтверждают, что используемая комбинированная вакцина совместима с графиками вакцинации против гепатита B, рекомендованными РПИ ВОЗ. После введения третьей дозы вакцины против гепатита B GMT анти-HBsAg был выше в группе A, чем в группе B. Известно, что величина анти-HBsAg-ответа зависит от графика. Это исследование также подтверждает наблюдение, сделанное в предыдущих исследованиях, о том, что увеличение интервала между двумя последними дозами увеличивает конечный титр анти-HBsAg. 20 — 22 Однако, несмотря на наблюдаемую здесь разницу в титрах анти-HBsAg антител, не было никакой разницы в степени серопротекции между группами.
В этой исследуемой популяции вакцинация была связана с низкой частотой запрошенных местных и системных побочных реакций. Сильная боль регистрировалась только после приема 0,2–0,7% доз, и о других тяжелых местных реакциях не сообщалось. Аналогичная картина наблюдалась для сильной лихорадки и раздражительности, которые возникли не более чем через 0.5% доз.
Таким образом, это исследование продемонстрировало, что комбинированная вакцина DTaP – IPV // PRP ~ T обладает высокой иммуногенностью по отношению ко всем антигенам, хорошо переносится и безопасна при введении младенцам в возрасте 6, 10 и 14 недель — схема, часто используемая в ВОЗ. EPI. Более того, ее можно вводить одновременно с моновалентной вакциной против гепатита В в возрасте 0, 6 и 14 недель или 6, 10 и 14 недель. Однако величина иммунного ответа на гепатит В была выше, когда первая доза была введена при рождении.Иммуногенность и безопасность комбинированной вакцины DTaP – IPV // PRP ~ T у здоровых детей на Филиппинах были аналогичны тем, которые наблюдались в европейском историческом контрольном исследовании, в котором та же вакцина вводилась в возрасте 2, 3 и 4 месяцев. ■
Благодарности
Мы благодарим Agnès Garinga и Pascale Chavand за мониторинг исследования, Christèle Deroche и Valèrie Bosch-Castells за анализ данных исследования и Clement Weinberger за помощь в подготовке рукописи.Вышеуказанные лица являются сотрудниками санофи пастер на Филиппинах или во Франции.
Финансирование: Это исследование (http://www.clinicaltrials.gov/ct/show/NCT00254917?order=3) было проведено при поддержке санофи пастер, Лион, Франция.
Конкурирующие интересы: Эстебан Ортис и Валери Бош работают в компании Санофи Пастер, Лион, Франция. Мария Росарио Капединг получала гонорары от Санофи Пастер за выступление на медицинских конгрессах.
Список литературы
- Pines E, Barrand P, Fabre P, Salomon H, Blondeau C, Wood SC, et al., и другие. Новые бесклеточные коклюшные педиатрические комбинированные вакцины. Vaccine 1999; 17: 1650-6 DOI: 10.1016 / S0264-410X (98) 00422-8 pmid: 10194818.
- Decker MD, Edwards KM, Steinhoff MC, Rennels MB, Pichichero ME, Englund JA, et al., Et al. Сравнение 13 бесклеточных коклюшных вакцин: побочные реакции. Педиатрия 1995; 96: 557-66 pmid: 7659476.
- Эдвардс К.М., Мид Б.Д., Деккер М.Д., Рид Г.Ф., Реннельс М.Б., Штейнхофф М.С. и др. И др. Сравнение 13 бесклеточных коклюшных вакцин: обзор и серологический ответ. Педиатрия 1995; 96: 548-57 pmid: 7659475.
- Вишня JD. Сравнительная эффективность бесклеточных коклюшных вакцин: анализ последних испытаний. Pediatr Infect Dis J 1997; 16: S90-6 DOI: 10.1097 / 00006454-199704001-00004 pmid: 9109163.
- Эдвардс К.М., Декер М. Коклюшные вакцины. В: Плоткин С.А., Оренштейн В.А., ред. Вакцины . 4-е изд. Филадельфия, Пенсильвания: Saunders Co .; 2004. 21: 471-528.
- Simondon F, Preziosi MP, Yam A, Kane CT, Chabirand L, Iteman I, et al., и другие. Рандомизированное двойное слепое испытание, сравнивающее двухкомпонентную бесклеточную и цельноклеточную коклюшную вакцины в Сенегале. Vaccine 1997; 15: 1606-12 DOI: 10.1016 / S0264-410X (97) 00100-X pmid: 9364690.
- Therre H, Baron S. Иммунизация против коклюша в Европе — ситуация в конце 1999 г. Euro Surveill 2000; 5: 18-10 вечера, id: 12631876.
- Вакцины против коклюша. Wkly Epidemiol Rec 2005; 80: 29-40 pmid: 15715139.
- Вакцины, преквалифицированные Организацией Объединенных Наций (список вакцин ВОЗ для закупок агентствами ООН по состоянию на апрель 2008 г.).Доступно по адресу: http://www.who.int/immunization_standards/vaccine_quality/pq_suppliers/en/index.html [по состоянию на 5 мая 2008 г.].
- Lagos R, Kotloff KL, Hoffenbach A, San Martin O, Abrego P, Ureta AM, et al., Et al. Клиническая приемлемость и иммуногенность пятивалентной парентеральной комбинированной вакцины, содержащей дифтерию, столбняк, бесклеточный коклюш, инактивированный полиомиелит и конъюгированные антигены Haemophilus influenzae типа b, у двух-, четырех- и шестимесячных чилийских младенцев. Pediatr Infect Dis J 1998; 17: 294-304 DOI: 10.1097 / 00006454-199809001-00010 pmid: 9576383.
- Карлссон Р.М., Клаессон Б.А., Селстам У., Фагерлунд Э., Гранстром М., Блондо С. и др. И др. Безопасность и иммуногенность комбинированной вакцины против полиомиелита, инактивированной дифтерией, столбняком, бесклеточным коклюшем и вакцины против Haemophilus influenzae типа b, вводимой в возрасте 2–4–6–13 или 3–5–12 месяцев. Pediatr Infect Dis J 1998; 17: 1026-33 DOI: 10.1097 / 00006454-199811000-00013 pmid: 9849987.
- Mallet E, Fabre P, Pines E, Salomon H, Staub T., Schödel F, et al., и другие. Иммуногенность и безопасность новой жидкой шестивалентной комбинированной вакцины по сравнению с раздельным введением референсных лицензионных вакцин младенцам. Pediatr Infect Dis J 2000; 19: 1119-27 DOI: 10.1097 / 00006454-200012000-00001 pmid: 11144370.
- Carlsson RM, Claesson BA, Fagerlund UE, Knutsson N, Laudin C. Персистенция антител у пятилетних детей, получивших пятивалентную комбинированную вакцину в младенчестве. Pediatr Infect Dis J 2002; 21: 535-41 DOI: 10.1097 / 00006454-200206000-00011 pmid: 12182378.
- Канра Г., Селиер Т., Юрдакок К., Явуз Т., Баскан С., Улукол Б. и др., И др. Исследование иммуногенности комбинированной вакцины против дифтерии, столбняка, бесклеточного коклюша и инактивированного полиомиелита, используемой для восстановления лиофилизированной вакцины Haemophilus influenzae типа b (DTacP-IPV // PRP-T), вводимой одновременно с вакциной против гепатита В через два, три часа. и четыре месяца жизни. Vaccine 1999; 18: 947-54 DOI: 10.1016 / S0264-410X (99) 00331-X pmid: 10580209.
- Gylca R, Gylca V, Benes O, Melnic A, Chicu V, Weisbecker C, et al., Et al. Новая вакцина DTPa-HBV-IPV, вводимая совместно с Hib, по сравнению с коммерчески доступной вакциной DTPw-IPV / Hib, вводимой совместно с HBV, через 6, 10 и 14 недель после рождения HBV. Vaccine 2000; 19: 825-33 DOI: 10.1016 / S0264-410X (00) 00231-0 pmid: 11115705.
- Кришнан Р., Джадхав М., Джон Т.Дж. Эффективность вакцины против инактивированного полиовируса в Индии. Bull World Health Organ 1983; 61: 689-92 pmid: 6605215.
- Плоткин С.А., Видор Э. Полиовирусная вакцина — инактивированная. В: Плоткин С.А., Оренштейн В.А., ред. Вакцины . 4-е изд. Филадельфия, Пенсильвания: Сондерс, 2004. стр. 625–49.
- Эпиднадзор за коклюшем в Швеции с усиленным наблюдением за когортами, иммунизированными бесклеточными коклюшными вакцинами . [Приложение 2 SP-MSD]. Шведский институт по контролю за инфекционными заболеваниями; 2006 г. Доступно по адресу: http://www.smittskyddsinstitutet.se/upload/PDF-filer/seven-year-report-app-2-SP-MSD.pdf [доступ 5 мая 2008 г.].
- Олин П., Густафссон Л., Баррето Л., Хессель Л., Маст TC, Ри А.В. и др. И др. Снижение заболеваемости коклюшем в Швеции после внедрения бесклеточной коклюшной вакцины. Vaccine 2003; 21: 2015-21 doi: 10.1016 / S0264-410X (02) 00777-6 pmid: 12706691.
- Вакцины против гепатита В. Wkly Epidemiol Rec 2004; 79: 255-64 pmid: 15344666.
- Goldstein ST, Zhou F, Hadler SC, Bell BP, Mast EE, Margolis HA. Математическая модель для оценки глобального бремени гепатита B и воздействия вакцинации. Int J Epidemiol 2005; 34: 1329-39 DOI: 10.1093 / ije / dyi206 pmid: 16249217.
- Гринберг Д.П., Вонг В.К., Партридж С., Хоу Б.Дж., Уорд Д.И. Безопасность и иммуногенность комбинированной вакцины против дифтерии, столбняка, бесклеточного коклюша и гепатита В, вводимой в возрасте двух, четырех и шести месяцев, по сравнению с моновалентной вакциной против гепатита В, вводимой при рождении, в возрасте одного месяца и шести месяцев. Pediatr Infect Dis J 2002; 21: 769-76 DOI: 10.1097 / 00006454-200208000-00014 pmid: 12192167.
Принадлежности
- Научно-исследовательский институт тропической медицины (RITM), Манила, Филиппины.
- Мемориальный госпиталь Университета Восточного Рамона Магсайсай, Кесон-Сити, Филиппины.
- Госпиталь Мэри Чайлс, Манила, Филиппины.
- Санофи пастер, Лион, Франция.
Вакцина 5-в-1 или 6-в-1 | Уход за детьми
Вы можете защитить своих детей от 5 болезней, сделав им 1 легкую вакцину.Вакцина 5-в-1 защищает от:
- Дифтерия
- Столбняк
- Коклюш (коклюш)
- Полиомиелит
- Hib-инфекция
В некоторых провинциях вакцина против гепатита B также включена, что делает ее вакциной 6-в-1.
В Канаде большинство детей получают вакцину 5-в-1 в возрасте 2, 4, 6 и 18 месяцев. Вакцина 6-в-1 может заменить вакцину 5-в-1 через 2, 4 и 6 месяцев или через 2, 4 и 18 месяцев. Требуется всего три дозы вакцины против гепатита В.
Ваш ребенок получит ревакцинацию вакцины 4-в-1 в возрасте от 4 до 6 лет. Вакцина 4-в-1 защищает от:
- Дифтерия
- Столбняк
- коклюш
- Полиомиелит
Ревакцинация вакцины против Hib не требуется, если ваш ребенок уже получил все 4 дозы вакцины 5-в-1.
Для полной защиты ваш ребенок должен получить все вакцины в нужное время. Попросите у врача или медсестры записную книжку, которая поможет вам вести учет прививок вашего ребенка.
Что такое дифтерия?
- Дифтерия — это заболевание, вызываемое бактериями (микробами). Он производит яд (токсин), который убивает клетки слизистой оболочки горла и вызывает серьезные проблемы с дыханием. Он также может поражать сердце, нервы и почки.
- Примерно 1 из 10 больных дифтерией умрет от этой болезни. Младенцы, получившие это заболевание, с большей вероятностью умрут.
- Дифтерию необходимо лечить с помощью антитоксина (сыворотки, которая борется с ядом). Антибиотики не влияют на болезнь, но используются для предотвращения распространения бактерий среди других.
- Люди, заболевшие дифтерией, не всегда становятся невосприимчивыми. Все должны пройти вакцинацию.
Что такое столбняк?
- Столбняк, также называемый тризмом, вызывается микробами (бактериями), которые обнаруживаются в грязи и пыли в виде спор (семяподобных клеток). Эти бактерии обитают в кишечнике людей и животных и могут быть обнаружены в стуле.
- Столбняк не заразен: он не передается от человека к человеку.
- Если возбудитель столбняка попадет в открытый порез, например, укол, укус или серьезный ожог, яд (токсин) от микроба может распространиться на ваши нервы, а затем на мышцы.Мышцы могут заблокироваться в одном месте или спазмировать (стать очень напряженными). Это очень больно.
- Мышцы челюсти часто поражаются первыми. Возможно, вы не сможете глотать или открывать рот. Если яд попадет в мышцы, которые помогают дышать, вы можете быстро умереть.
- Основное лечение столбняка — антитоксин (сыворотка, которая борется с ядом).
- Также назначают антибиотики для уничтожения микробов. Другие препараты используются для контроля мышечных спазмов. Для облегчения дыхания может потребоваться машина.
- От столбняка умрут от 1 до 8 человек из 10.
- У людей, переживших столбняк, могут быть длительные проблемы с речью, памятью и мышлением.
- Выжившие могут снова заболеть столбняком. Инфекция не дает иммунитета. Вакцина нужна каждому.
Что такое коклюш?
- Коклюш, также называемый коклюшем, вызывается микробами, которые попадают в горло и легкие и затрудняют удаление слизи из дыхательных путей.
- Дети могут кашлять так долго и так сильно, что они не могут дышать. Младенцы младшего возраста могут быть не в состоянии кашлять и могут перестать дышать.
- У младенцев с коклюшем могут быть припадки (припадки), а в серьезных случаях они могут впадать в кому.
- Примерно 1 из 400 младенцев, больных коклюшем, умирает из-за пневмонии или повреждения головного мозга.
- Дети старшего возраста, подростки и взрослые, заболевшие коклюшем, будут кашлять более 3 недель, а кашель может длиться до 12 недель.
- Кашель нарушает сон и может быть достаточно сильным, чтобы вызвать перелом ребер, грыжу или потерю контроля над мочеиспусканием.
Что такое полиомиелит?
- Полиомиелит — это инфекция, вызываемая вирусом полиовируса.
- Некоторые люди, больные полиомиелитом, совсем не чувствуют себя больными.
- Симптомы могут включать жар, боль в горле, головную боль, мышечные боли и боли, сонливость, потерю аппетита, тошноту, рвоту, боль в желудке и запор. Это также может вызвать менингит (головная боль и скованность в шее и спине).
- Примерно 1 из 100 человек, инфицированных вирусом, заболеет тяжелой формой болезни, которая вызывает паралич (неспособность двигать руками или ногами).Если грудные мышцы парализованы, человек не может дышать, и ему понадобится аппарат, чтобы дышать.
- Некоторые люди умирают от полиомиелита. Большинство выживших парализованы на всю оставшуюся жизнь.
Что такое Hib-инфекция?
- Hib означает Haemophilus Influenzae type b. Несмотря на название, это не имеет ничего общего с гриппом.
- Hib — это бактерия (микроб), которая зарождается в носу или горле и может заразить практически любую другую часть тела, например мозг, легкие, сердце, суставы, кости и кожу.
- Он может вызвать очень серьезное заболевание, называемое менингитом, когда поражает жидкость и покровы головного и спинного мозга.
- Без лечения все дети с менингитом, вызванным Hib, умирают. Даже после лечения примерно 1 из 20 детей с менингитом, вызванным Hib, умрет.
- Примерно у 1 из 3 выживших детей будет необратимое повреждение головного мозга.
Что такое инфекция гепатита В?
Гепатит B — это заболевание, вызываемое вирусом, поражающим печень. Для получения дополнительной информации посетите страницу о гепатите B.
Насколько безопасны снимки 5-в-1 и 6-в-1?
- Они очень безопасны.
- Дети, у которых была серьезная аллергическая реакция на предыдущую дозу вакцины (отек лица или губ, затрудненное дыхание или падение артериального давления), не должны получать вакцину повторно, если не будут осмотрены специалистом и вакцинированы в специальной клинике. может контролировать тяжелые реакции.
Есть ли у вакцины побочные эффекты?
- При использовании любой вакцины может появиться покраснение, припухлость, болезненность или боль в месте, где игла вошла в руку или ногу.
- Лихорадка — обычное дело.
Как уменьшить боль?
Иглы могут повредить. Чтобы уменьшить боль, вы можете:
- Нанесите местный анестетик (крем, вызывающий временное онемение) за час до введения иглы. Возможно, вам придется спросить своего врача или медсестру, куда будет делаться укол (например, в руку или ногу). Ваш фармацевт может помочь вам найти крем.
- Кормите ребенка грудью, пока он получает иглу, или дайте ему воду с сахаром (чайной ложкой или соской) непосредственно перед уколом.
- Для детей старшего возраста используйте отвлекающие факторы (надувайте мыльные пузыри, читайте книгу), предлагайте глубокое дыхание, сохраняйте спокойствие и физически утешайте ребенка (обнимайте, держитесь за руки) во время иглы.
Родители и опекуны НЕ должны давать своим детям ибупрофен или парацетамол до или вскоре после вакцинации , поскольку это может повлиять на эффективность вакцины. Подождите не менее 6 часов после вакцинации, чтобы облегчить боль или жар.
Дополнительная информация из CPS
Проверено следующими комитетами CPS
- Комитет по инфекционным болезням и иммунизации
Дифтерия, коклюш, полиомиелит, столбняк, Haemophilus Influenzae, тип B Вакцина — обзор
DTaP5
В дополнение к ранее обсуждавшимся DTaP5 / IPV (Quadracel), другие комбинированные вакцины на основе канадской пятикомпонентной вакцины АП5, такие как HTaP5 (Actacel), DTaP5 / IPV // Hib (Pentacel) и DTaP5 / IPV / Hib (Pediacel) оценивались в различных регионах.В сравнительном испытании комбинации DTaP5 // Hib в сравнении с отдельными компонентами на Тайване 95% реципиентов комбинации достигли уровня как минимум 1 мкг / мл антител к PRP. Средние геометрические уровни антител к коклюшу и Hib не различались при комбинированном и раздельном введении (таблица 40-8). 162 В другом сравнительном исследовании изучалась вакцинация в возрасте 2, 4, 6 и 18 месяцев с использованием (1) DTaP5 / IPV для восстановления лиофилизированного PRP-T (Pentacel), (2) полностью жидкого DTaP5 / IPV / PRP-T (Pediacel) или (3) DTaP5 / IPV и PRP-T назначаются отдельно. 164, 165, 206 Все три группы хорошо ответили после первичной и бустерной иммунизации (таблица 40-8). Жидкие и лиофилизированные комбинации выполнялись аналогично 164 ; ответы антител на жидкую комбинацию существенно не отличались от ответов отдельных вакцин для любого антигена. 164, 165, 206
Noriega et al 213 сравнили Pentacel с отдельными Daptacel, IPV (IPOL) и PRP-T (ActHIB) в качестве четвертых доз среди детей в США и не обнаружили существенных различий в иммуногенности. ; 98% и 96%, соответственно, достигли уровня антител PRP, равного 1.0 мкг / мл или выше. Гальперин и др. 214 сравнили DTaP3 / IPV // Hib и DTaP5 / IPV // Hib в качестве четвертых доз среди канадских детей и обнаружили значительно более высокие уровни антител к PRP (29 против 19 мкг / мл) у детей, получавших пентацел.
Guerra et al. 215 сообщили о сравнении Pentacel с отдельными Daptacel, IPOL и ActHIB, вводимыми в возрасте 2, 4 и 6 месяцев; в 15 месяцев дети получали Пентацел или Даптасел плюс АктХИБ. Частота побочных реакций после введения Pentacel была аналогична или ниже, чем после введения отдельных вакцин.Ответы антител существенно не различались между двумя группами. Chatterjee et al. 216 сообщили о результатах сравнения Pentacel, Quadracel + ActHIB и Daptacel + IPOL + ActHIB, назначенных в возрасте 2, 4 и 6 месяцев. Ответы антител существенно не различались между тремя группами, за исключением того, что Quadracel стимулировал более высокие ответы антител PRP, чем Pentacel или отдельные вакцины (которые давали почти идентичные ответы Hib). Частота побочных реакций была несколько ниже при использовании комбинации, чем при использовании отдельных вакцин.
Lin et al 209 сравнили Pediacel с Quadracel + PRP-T и обнаружили, что оба режима обладают высокой иммуногенностью. Уровни антител PRP 1,0 мкг / мл или выше были достигнуты в 97% и 99%, соответственно; GMT были очень высокими — 11,4 и 21,7 мкг / мл соответственно. Ответы на другие содержащиеся или сопутствующие антигены были отличными и сходными между двумя группами, а частота нежелательных реакций существенно не различалась. Год спустя у 93% реципиентов Pediacel уровень антител к PRP был равен 0.15 мкг / мл или выше. 210 После бустерной дозы Pediacel количество GMC выросло до 60 и 62 мкг / мл в комбинированной и отдельной группах вакцины, соответственно.
Grimprel et al. 211 сообщили о сравнении Pediacel с Infanrix-IPV-Hib, вводимой в возрасте 2, 3, 4 и от 12 до 18 месяцев вместе с 7vPnC. Большинство результатов были одинаковыми между двумя группами. Как и следовало ожидать от их составов, ответы FIM (фимбриальный) были выше в группе Pediacel, а ответы PRN (пертактин) были выше в группе Infanrix-IPV-Hib.Ответы на Hib были значительно выше в группе Pediacel после третьей дозы (1,38 против 0,59 мкг / мл) и четвертой дозы (32,4 против 19,3 мкг / мл).
Уже давно предполагалось, что менее выраженная интерференция Hib, наблюдаемая с комбинациями на основе DTaP5, может быть связана с тем фактом, что они однозначно используют фосфат алюминия в качестве адъюванта (комбинации на основе DTaP2 и DTaP3 используют гидроксид алюминия). Теперь появились доказательства, подтверждающие эту точку зрения. Mawas и его коллеги, 220 , используя свою модель на крысах для изучения гуморального и клеточного иммунитета, обнаружили, что ответы антител против Hib были снижены с DTaP3 / PRP-T по сравнению с одним PRP-T, но не были уменьшены с DTaP5 / IPV // PRP- Т.Затем исследователи оценили прием неадъювантного Hib; Hib адсорбируется на Al (OH) 3 или AlPO4; DTaP3; PRP-T в сочетании с DTaP3; и PRP-T в сочетании с отдельными неадъювантными компонентами DTaP3. Добавление PRP-T к DTaP не влияло на ответы DTaP. Комбинированное введение токсоида коклюша и PRP-T усиливало ответы Hib по сравнению с их совместным введением, тогда как сочетание PRP-T со столбнячным токсоидом или FHA подавляло ответы Hib. Наконец, они обнаружили, что адсорбция PRP-T на фосфате алюминия снижает отклики вдвое, тогда как адсорбция на гидроксиде алюминия снижает отклики в 5-11 раз. 221
Было высказано предположение, что вакцина PnC7 (Prevnar) может изменять иммуногенность совместно вводимых вакцин DTaP. Возможность такого взаимодействия с Pentacel оценивалась в нескольких исследованиях, ни одно из которых не продемонстрировало каких-либо существенных различий между группами, которые получали Prevnar одновременно с каждой дозой Pentacel или в течение 1 месяца отдельно от нее. 222–225 Частота реакций, как правило, была выше в группах, получавших одновременно Prevnar, особенно при лихорадке. 225
Halperin et al. 214 сравнили DTaP / IPV / PRP-T брендов Pentacel и Infanrix-IPV-Hib при использовании в качестве бустера четвертой дозы среди малышей, получавших три дозы Pentacel. Местные реакции чаще наблюдались при приеме Пентацел, тогда как системные реакции в целом были сходными для двух групп. Не было различий в соотношениях серорезависимых или серопротективных. Как и следовало ожидать, учитывая их соответствующие препараты, средние титры Hib были выше; Титры PT, FHA и PRN ниже; и титры FIM предположительно намного выше в группе Pentacel.Канадский национальный консультативный комитет по иммунизации пришел к выводу, что эти две комбинированные вакцины, а также Pediacel, могут использоваться взаимозаменяемо в четвертой (для малышей) и пятой (дошкольной) дозах для стимулирования должным образом подготовленных детей. 226
Безопасность комбинированной вакцины DTacP-IPV // PRP ~ T (PENTAXIM), вводимой в виде трехдозовой первичной вакцинации младенцам в возрасте 2, 3 и 4 месяцев в Китае
Нам нужна от вас некоторая информация, прежде чем вы начнете использовать платформу.Эта информация позволит нам лучше понять, как используется AdisInsight.
Он не требует или не заменяет отдельные учетные записи для входа, которые многие из вас используют для сохранения результатов поиска и создания предупреждений по электронной почте.
Защита вашей личной информации важна.
Вот почему AdisInsight собирает минимальный объем информации, необходимой для включения функциональности, отчетов об использовании и связи с вами с информацией об AdisInsight.
Для получения дополнительной информации о том, как мы защищаем и обрабатываем вашу личную информацию, пожалуйста, обратитесь к нашему
политика конфиденциальности.
Пожалуйста, введите ваш официальный адрес электронной почты
Адрес электронной почты
Страна
Выберите CountryAfghanistanAlbaniaAlgeriaAmerican SamoaAndorraAngolaAnguillaAntarcticaAntigua и BarbudaArgentinaArmeniaArubaAustraliaAustriaAzerbaijanBahamasBahrainBangladeshBarbadosBelarusBelgiumBelizeBeninBermudaBhutanBoliviaBonaire, Синт-Эстатиус и SabaBosnia и HerzegovinaBotswanaBouvet IslandBrazilBritish Индийский океан TerritoryBrunei DarussalamBulgariaBurkina FasoBurundiCambodiaCameroonCanadaCape VerdeCayman IslandsCentral африканских RepublicChadChileChinaChristmas IslandCocos (Килинг) IslandsColombiaComorosCongoCongo, Демократическая Республика theCook IslandsCosta RicaCote D’IvoireCroatiaCubaCuraçaoCyprusCzech RepublicDenmarkDjiboutiDominicaDominican RepublicEcuadorEgyptEl SalvadorEquatorial GuineaEritreaEstoniaEthiopiaFalkland (Мальвинские) острова Фарерские IslandsFijiFinlandFranceFrench GuianaFrench PolynesiaFrench Южные территорииГабонГамбияГрузияГерманияГанаГибралтарГрецияГренландияГренадаГваделупаГуамГватемалаГернсиГвинеяГвинея-БисауГайанаГайтиHeard Island and Mcdonald I slandsHoly Престол (Ватикан) HondurasHong KongHungaryIcelandIndiaIndonesiaIran, Исламская Республика ofIraqIrelandIsle из ManIsraelItalyJamaicaJapanJerseyJordanKazakhstanKenyaKiribatiKorea, Корейская Народно-Демократическая Республика ofKorea, Республика ofKosovoKuwaitKyrgyzstanLao Народная Демократическая RepublicLatviaLebanonLesothoLiberiaLibyan Арабская JamahiriyaLiechtensteinLithuaniaLuxembourgMacaoMacedonia, бывшая югославская Республика ofMadagascarMalawiMalaysiaMaldivesMaliMaltaMarshall IslandsMartiniqueMauritaniaMauritiusMayotteMexicoMicronesia, Федеративные Штаты ofMoldova, Республика ofMonacoMongoliaMontenegroMontserratMoroccoMozambiqueMyanmarNamibiaNauruNepalNetherlandsNew CaledoniaNew ZealandNicaraguaNigerNigeriaNiueNorfolk IslandNorthern Mariana IslandsNorwayOmanPakistanPalauPalestinian край, OccupiedPanamaPapua Новая ГвинеяПарагвайПеруФилиппиныПиткэрнПольшаПортугалияПуэрто-РикоКатарВоссоединениеРумынияРоссийская ФедерацияРуандаСент-БартелемиСент-ХеленаСент-Китс и НевисСент-ЛюсияСент-Мартен (Френк) ч часть) Сен-Пьер и MiquelonSaint Винсент и GrenadinesSamoaSan MarinoSao Томе и PrincipeSaudi ArabiaSenegalSerbiaSeychellesSierra LeoneSingaporeSint Маартен (Голландская часть) SlovakiaSloveniaSolomon IslandsSomaliaSouth AfricaSouth Джорджия и Южные Сандвичевы IslandsSouth SudanSpainSri LankaSudanSurinameSvalbard и Ян MayenSwazilandSwedenSwitzerlandSyrian Arab RepublicTaiwanTajikistanTanzania, Объединенная Республика ofThailandTimor-LesteTogoTokelauTongaTrinidad и TobagoTunisiaTurkeyTurkmenistanTurks и Кайкос IslandsTuvaluUgandaUkraineUnited Араб ЭмиратыВеликобританияМалые отдаленные острова СШАСоединенные Штаты АмерикиУругвайУзбекистанВануатуВенесуэлаВьетнамВиргинские острова, Британские Виргинские острова, СШАСан-Уоллис и Футуна, Западная Сахара, Йемен, Замбия, Зимбабве, Аландские острова.
Промышленность
Выберите отрасльБиотехнологииКонсалтингГосударствоИнженерия / ПроизводствоФинансы / ИнвестицииГосударственный институт или агентствоHMO / КлиникаБольница (общественная) Больница (другое) Больница (университетская или преподавательская) Юридические СМИ / Издательское делоМедицинская школаНеправительственная организацияДом для престарелых / Помощь в проживанииФармацевтика / Частный институт врача Кабинет врача (индивидуальная группа)
Название работы
Выберите должность доцент / лекторБизнес-консультантРазвитие бизнеса, лицензирование или передача технологийБизнес / финансовый аналитик или конкурентная разведкаКлинические вопросы / операции по клиническим испытаниямИнженерГлава академического отдела / факультетаДиректор лаборатории / руководитель библиотеки / специалист по информационным технологиям Библиотекарь / Библиотекарь метаданных / Библиотекарь по открытым наукам / Библиотека данных по исследованиям Директор / руководитель библиотекиПрофессиональный врач / врачДругиеФармацевтический надзор, нормативные вопросы или качествоPhD СтудентПрезидент / генеральный директор / владелец компанииОсновной исследовательМенеджер по закупкамПрофессор Управление НИОКР, научный сотрудникПродажи и маркетингСтарший научный сотрудник, научный сотрудник, научный сотрудник, стажер, преподаватель, научный сотрудник
ПРАЙМ PubMed | Иммуногенность и безопасность бустерной вакцины DTaP-IPV // PRP-T (Pentaxim) на втором году жизни у тайских детей, получавших бесклеточную комбинированную вакцину против коклюша
Citation
Thisyakorn, Usa, et al.«Иммуногенность и безопасность бустера вакцины DTaP-IPV // PRP-T (пентаксим) в течение второго года жизни у тайских детей, получавших комбинированную бесклеточную коклюшную вакцину». Журнал тропической медицины и общественного здравоохранения Юго-Восточной Азии, vol. 40, нет. 2, 2009, с. 282-94.
Thisyakorn U, Pancharoen C, Chuenkitmongkol S, et al. Иммуногенность и безопасность бустерной вакцины DTaP-IPV // PRP-T (Pentaxim) на втором году жизни у тайских детей, примированных бесклеточной комбинированной вакциной против коклюша. J Trop Med Public Health Юго-Восточной Азии . 2009; 40 (2): 282-94.
Thisyakorn, U., Pancharoen, C., Chuenkitmongkol, S., & Ortiz, E. (2009). Иммуногенность и безопасность бустерной вакцины DTaP-IPV // PRP-T (Pentaxim) на втором году жизни у тайских детей, примированных бесклеточной комбинированной вакциной против коклюша. Журнал тропической медицины и общественного здравоохранения Юго-Восточной Азии , 40 (2), 282-94.
Thisyakorn U, et al. Иммуногенность и безопасность бустера вакцины DTaP-IPV // PRP-T (пентаксим) на втором году жизни тайских детей, получавших комбинированную бесклеточную коклюшную вакцину. J Trop Med Public Health в Юго-Восточной Азии. 2009; 40 (2): 282-94. PubMed PMID: 19323013.
TY — JOUR
T1 — Иммуногенность и безопасность бустерной вакцины DTaP-IPV // PRP-T (Pentaxim) на втором году жизни у тайских детей, получавших бесклеточную комбинированную вакцину против коклюша.
AU — Thisyakorn, США,
AU — Панчароэн, Читсану,
AU — Chuenkitmongkol, Sunate,
AU — Ортис, Эстебан,
PY — 2009/3/28 / entrez
PY — 2009/3/28 / pubmed
PY — 2009/6/24 / medline
СП — 282
EP — 94
JF — Журнал тропической медицины и общественного здравоохранения Юго-Восточной Азии
JO — Юго-Восточная Азия J Trop Med Public Health
ВЛ — 40
ИС — 2
N2 — В этом исследовании оценивался бустерный иммунный ответ на пятивалентную комбинированную вакцину, содержащую дифтерию, столбняк, бесклеточный коклюш, инактивированный полиовирус и полисахаридные антигены конъюгированного Hib (DTaP-IPV // PRP-T, Pentaxim, вакцина семейства AcXim) при 18-24 месяцев.Субъекты исследования получили трехдозовую первичную вакцинацию через 2, 4 и 6 месяцев шестивалентной вакциной, содержащей те же антигены плюс рекомбинантный поверхностный антиген гепатита B. Концентрации антител измеряли непосредственно перед вакцинацией и через месяц после нее.
