Вакцина БЦЖ — «Наш опыт вакцинации от туберкулеза. Почему прививку мы ставили в год, а не при рождении? Как ухаживать за местом введения вакцины? Фото прививки спустя 3 месяца »
Ещё до рождения своих дочерей мы с мужем детально обсудили вопрос их вакцинации. В принципе, н какой полемики не было, мы оба были «за» прививание.
Но в нашем случае проблемы начались практически с рождения. К счастью, проблемы заключались не в детях, они были здоровы. Уже позже я узнала, что деткам с дефицитом веса прививку БЦЖ не делают. Точнее, ее переносят на более поздний срок. И хотя я долгое время переживала, что дочки родились крошечными (по 2,5 килограмма), они вписывались в нормы веса даже для одного ребенка, не говоря уже о двойне.
Проблема заключалась в отсутствии вакцин. Да, на момент моих родов детям смогли сделать лишь прививку от гепатита В.
Такой необходимой малышам прививки БЦЖ против туберкулеза в роддоме не было. Хотя моя подружка, которая родила двумя месяцами ранее там же, утверждала, что ее дочке БЦЖ сделали на третьи сутки жизни ребенка, как раз на кануне выписки.
Что самое удивительное, в моем городе не было вакцины даже ы платных клиниках, как говорилось в одном фильме
Даже за большие гроши
Ехать в другой город за 300 — 500 километров мы не решились, поэтому дети так и остались не привитые аж на целый год. Приходилось лишь надеяться, что эта беда нас минует.
Когда младшая дочь попала в больницу с подозрением на ротавирус, первое, о чем нас спросили в приемном покое — это есть ли у нее БЦЖ. После моего отрицательного ответа, на нас посмотрели, как на прокаженных, но в стационар все же положили.
Но, к счастью, вакцины все же государством были закуплены, одновременно с этим они появились и в частных клиниках.
БЦЖ мы делали бесплатно в поликлинике по месту прописки. В пятницу, накануне прививки детям сделали Манту. Если бы мы вакцинировались до 2 месяцев, можно было бы обойтись без нее. В других городах, говорят, детям до 7-9 месяцев делали БЦЖ без Манту, но у нас возрастная планка была 2 месяца. Дочкам в тот момент было 11,5.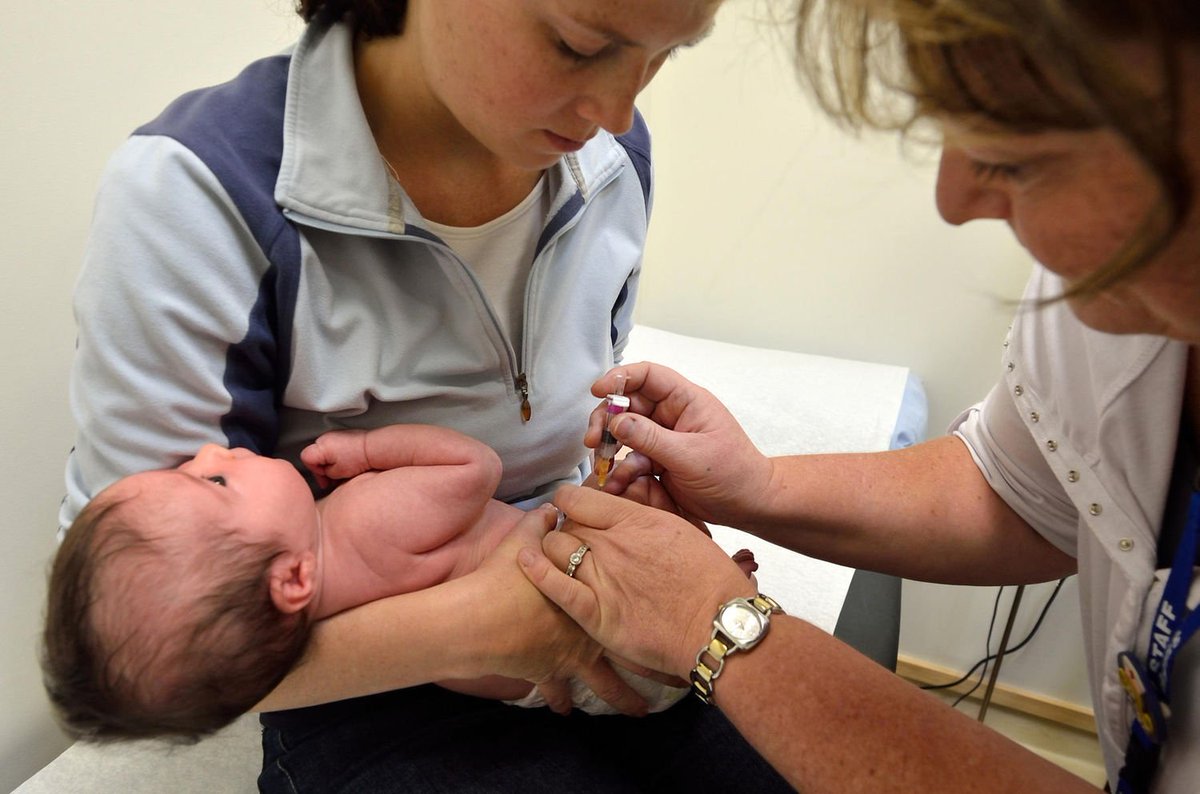
В понедельник, 19 сентября мы пришли в поликлинику всем своим большим семейством. В предвкушении жутких очередей моя мама занимала очередь с 7 утра. Но, к счастью, желающих прививаться было не много. Кстати, через неделю и в последующие разы народу, говорят, была тьма. И это с учетом того, что прививку БЦЖ в нашей поликлинике можно сделать лишь 2 раза в месяц: в первый и третий понедельник месяца с 10 до 12 часов дня.
В общем, педиатр сделала замеры, отметила, что Манту в норме, не увеличена, осмотрела детей, записала анамнез и направила на прививку.
А вот заведующий поликлиникой, с которым мы столкнулись на выходе из кабинета, не разрешил нам делать прививку, сказав, что дети в возрасте год должны будут прививаться в последнюю очередь, а в тот день прививали лишь детей до года. Но учитывая, что это решение было принято им в день вакцинации, мы с ним «мило пообщались» и он «разрешил» мне вакцинировать детей в тот день.
В общем, со всеми перипетиями мы все же добрались до прививочного кабинета. Там детей еще раз осмотрели, сказали оголить левое предплечье, куда и был сделан укол. Младшая дочь вообще на этот никак не прореагировала, тогда как старшая немного плакала.
Там детей еще раз осмотрели, сказали оголить левое предплечье, куда и был сделан укол. Младшая дочь вообще на этот никак не прореагировала, тогда как старшая немного плакала.
Далее нам были даны рекомендации по поводу ухода за местом укола и поведением в ближайшие дни.
В день вакцинации были запрещены прогулки и купание.
В последующие дни все это разрешалось, при условии нормального самочувствия детей.
За местом укола особого ухода не требовалось, даже наоборот: на нем не нужно было акцентировать внимание, его не нужно было чем-то обрабатывать, отдельно было сказано, что нагноение — это нормально, его не нужно выдавливать или промывать.
Мои дети, к счастью, довольно легко перенесли вакцинацию от туберкулеза. Не было ни температуры, ни плаксивости, ни других негативных симптомов. День мы просидели дома, а дальше вели обычный образ жизни.
К примеру, прививку АКДС мои дети перенесли намного тяжелее.
На сегодняшний день, через три месяца после вакцинации место, куда ставили прививку у детей выглядит следующим образом:
Старшая дочь.
Меня больше тревожит то, что у нее под прививкой. Это уплотнение появилось где-то да месяц до прививки и хирургом было диагностировано, как невскрывшийся жировик. Ребенка оно не тревожит, а вот меняч сильно. Причина его названа не была, в размерах он постепенно увеличивается и чего от него ждать — не известно. Врач сказал, что удалить его можно лишь хирургическим путем под общим наркозом. Будем ждать лета, а потом принимать какое-то решение.
Младшая дочь
У нее место введения вакцины пока что выглядит не самым приятным образом, но скоро, я надеюсь, этот этап будет пройдет и все начнет заживать.
Отдельно хочу написать несколько слов, почему так важна вакцинация от туберкулеза. Не буду говорить о других странах, но в Украине ситуация с этим заболеванием просто катастрофическая. Нет, я не буду приводить статистику цифр, я просто скажу, что моя мама работает в кабинете, где делают флюорографию. И к ним за день приходят по несколько человек, у которых в итоге обследования выявляют туберкулез. Самый вопиющий случай произошел где-то месяц назад, когда рожала женщина, больная туберкулезом. Весь город стоял на ушах: ребенка обследовали, к счастью, он был здоров, но его мама от лечения отказалась. Чем закончится эта история мне не известно.
Самый вопиющий случай произошел где-то месяц назад, когда рожала женщина, больная туберкулезом. Весь город стоял на ушах: ребенка обследовали, к счастью, он был здоров, но его мама от лечения отказалась. Чем закончится эта история мне не известно.
С тех пор флюорография рожениц стала обязательной, тогда как раньше от нее можно было написать отказ.
В общем , подводя итог всему вышесказанному, я хочу отметить, что вакцинацию против туберкулеза я рекомендую. Да, она не дает 100-% гарантии, что человек не заболеет, но обезопасить себя хоть в какой-то мере можно. Особенно, если речь идет о детях.
Я не буду никого ни о чем агитировать, каждый родитель сам принимает решение в этом вопросе, основываясь на своем опыте, но лично я чувствую себя спокойнее, зная, что мои крохи вакцинированы, в том числе и от туберкулеза.
Здоровья Вам и Вашим деткам!!!
Вакцина БЦЖ — «Прививка от туберкулеза — побочки, связь БЦЖ и манту.
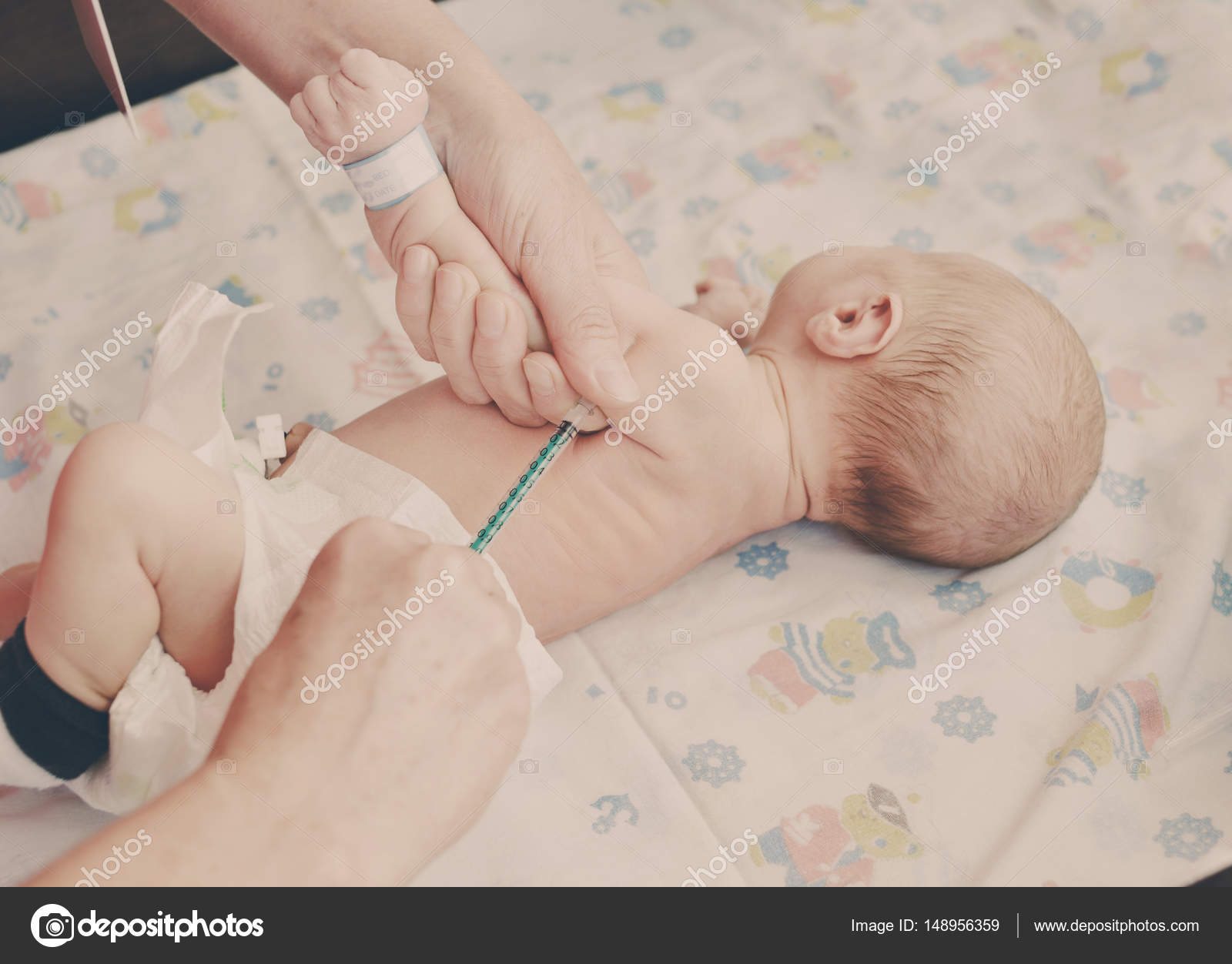 Ревакцинация в 6 лет. Когда пропадет шишка и появится рубец?»
Ревакцинация в 6 лет. Когда пропадет шишка и появится рубец?»
Всем доброго времени суток!
Сегодня мне захотелось поговорить о БЦЖ — прививке от туберкулеза.
Для начала просто немного статистики по России.
Туберкулёз — одна из острых медико-социальных проблем России.
На конец 2018 года в России насчитывалось более 149 тысяч человек, состоящих на учёте в противотуберкулёзных диспансерах; за 2018 год у 65 тысяч человек впервые был диагностировано заболевание.
Россия входит в число 22 стран мира с наименее благоприятной ситуацией по заболеваемости туберкулёзом (44,4 случая на 100 тысяч населения) и в тройку стран с наибольшим распространением устойчивых форм заболевания.
До 2014 года смертность от данного заболевания в стране составляла более 50% случаев смерти от всех известных инфекционных заболеваний. В последние годы смертность в стране сократилась, но по-прежнему остается высокой: почти 30% случаев смертей от инфекционных заболеваний.
И не надо думать, что туберкулез — болезнь только сидевших, бомжей и прочих ассоциалов. С ней может столкнуться каждый, если особенно он ездит в общественном транспорте или ходит по магазинам. Я знаю реальный случай, как в моем детстве мальчик из соседнего двора, которого я знала лично, умер от туберкулеза, хотя вроде бы совсем недавно он бегал живой и здоровый, никаким ассоциалом не являлся, но где-то все же нашел болезнь.
Никого не принуждаю ставить прививки, но сама поставила на всякий случай прививку от туберкулеза своим детям, хотя она все равно не дает гарантии полной защищенности от этой страшной болезни.
Как расшифровывается БЦЖ?
— Бацилла Кальмета-Жерена. И вакцина, между прочим, живая!
БЦЖ, это буквальная копия аббревиатуры BCG, которой названа противотуберкулезная вакцина, созданная в начале прошлого века французскими учеными – микробиологом Альбертом Кальметтом и ветеринарным врачом Шарлем Гереном, и названная в их честь.
В оригинале звучит, как Bacillus Calmette-Gurin (Бацилла Кальметта-Герена).
Она приготовленная из штамма ослабленной живой бычьей туберкулёзной палочки, которая практически утратила вирулентность для человека, будучи специально выращенной в искусственной среде.
Прививка БЦЖ у нас в России бесплатная, так как входит в национальный календарь профилактических прививок. А ставится в поликлиниках и роддомах либо вакцина БЦЖ, либо БЦЖ-М. Обе отечественного производства. Разница у них в том, что БЦЖ М — это облегченная разновидность вакцины БЦЖ.
Как правило, первую БЦЖ ставят в роддоме на 3-7 день жизни малыша, а ревакцинацию прививки проводят в 6-7 лет ребенка.
Я считаю, что не стоит бояться делать БЦЖ ребенку в роддоме, если малыш хорошо себя чувствует, у него нет противопоказаний, развивается он по возрасту, и врачи рекомендуют сделать эту прививку.
Своим двум детям я ставила БЦЖ в роддоме, но перенесли они прививку БЦЖ от туберкулеза по-разному.
Противопоказания к вакцинации БЦЖ
У моих детей противопоказаний для вакцинации не было, но ради интереса приведу перечень существующих.
Противопоказания к вакцинации БЦЖ по позиции ВОЗ 2008 года:
- лицам с нарушениями иммунитета: с установленным или подозреваемым врожденным иммунодефицитом, раком, ВИЧ-инфицированным с клиническими проявлениями;
- пациентам, проходящим терапию препаратами, подавляющими иммунитет;
- беременным.
Противопоказание против проведения вакцинации БЦЖ беременных — условное: нет исследований, обосновывающих отвод от вакцинации для беременных. Это общая позиция ВОЗ — не прививать беременных живыми вакцинами.
У отечественных вакцин к вакцине БЦЖ имеются следующие противопоказания:
- для вакцинации:
- Недоношенность новорождённого — масса тела при рождении менее 2500 г.
- Внутриутробная гипотрофия III—IV степени.
- Острые заболевания. Вакцинация откладывается до окончания острых проявлений заболевания.
- Обострения хронических заболеваний. Вакцинация откладывается до окончания обострения.
- ВИЧ-инфекция у матери новорождённого, следует воздержаться от введения ему БЦЖ до возраста 18 месяцев, когда будет уточнён ВИЧ-статус младенца.
- Первичное иммунодфицитное состояние, злокачественные новообразования.
- При назначении иммунодепрессантов и лучевой терапии прививку проводят не ранее, чем через 6 месяцев после окончания лечения.
- Генерализованная инфекция БЦЖ, выявленная у других детей в семье.
- для ревакцинации:
- Острые инфекционные и неинфекционные заболевания, обострения хронических и аллергических заболеваний. Прививка проводится через месяц после выздоровления или ремиссии.
- иммунодефицитное состояния, злокачественные заболевания крови и новообразования.
Противопоказания к вакцине БЦЖ-М:
- Недоношенность новорождённого — масса тела при рождении менее 2000 г.
- Острые заболевания. Вакцинация откладывается до окончания острых проявлений заболевания и обострения хронических заболеваний.
- Первичное иммунодефицитное состояние, злокачественные новообразования. При назначении иммунодепрессантов и лучевой терапии прививку проводят не ранее, чем через 6 месяцев после окончания лечения.
- Генерализованная инфекция БЦЖ, выявленная у других детей в семье.
- ВИЧ-инфекция у ребёнка с клиническими проявлениями вторичных заболеваний.
- ВИЧ-инфекция у матери новорождённого, не получавшей во время беременности антиретровирусную терапию.
Вопреки распространённому мнению, вакцинация от гепатита В не является противопоказанием для одновременного (в тот же день) введения вакцины БЦЖ
А еще самое важное, на мой взгляд, это побочные реакции, которые могут быть.
Побочное действие вакцины наблюдается очень редко.
У ребенка могут отмечаться следующие нежелательные изменения:
- повышенная температура тела;
- раздражительность;
- увеличение в размерах лимфатических узлов;
- понос;
- насморк;
- аллергия;
- общее ухудшение самочувствия;
- плаксивость;
- потеря аппетита;
- кашель;
- нарушения сна (чрезмерная сонливость, инсомния).

Как правило, подобная симптоматика в лечении не нуждается. Побочные эффекты самостоятельно исчезают спустя 2-3 суток после иммунизации.
Ничего из перечня выше у моих детей замечено не было после постановки прививки БЦЖ.
Осложнения после прививки
- Лимфаденит. Воспаление лимфоузлов отмечается с левой стороны в подмышечной области. Возникает воспалительный процесс при проникновении возбудителей болезни в региональные лимфатические узлы. Лимфаденит у малыша протекает в умеренной степени и сопровождается симптомами интоксикации. Не исключен гнойный процесс в лимфоузлах. Также возможно образование свищей. Необходимо хирургическое вмешательство. Пораженные лимфатические узлы иссекаются.
- Кожные реакции. Нагноение сильное, разливается за место введения вакцины. Папула наполнена гноем, может самостоятельно раскрыться, образуя мокнущую область большого размера. Отмечаются такие изменения, если младенец поражен первичным иммунодефицитом.
- Холодный абсцесс. Отличается от нормального инфильтрата. Появляется спустя месяц после БЦЖ. Его возникновение обусловлено несоблюдением правил вакцинации. Пораженная область не болит. Как правило, общее состояние не ухудшается. Негативные изменения возможны при самопроизвольном вскрытии холодного абсцесса и вытекании его содержимого.
- БЦЖ-остеомиелит. Считается самым опасным осложнением. Поражена оказывается костная система. Патологический процесс развивается постепенно, медленно. Первые симптомы наблюдаются спустя три месяца после вакцинации. Причиной развития болезни может быть некачественная вакцина. Также остеомиелит развивается при иммунодефиците.
- Келоидный рубец. Появляется при внутрикожном введении препарата. Окончательное формирование грубых рубцов наблюдается спустя год после вакцинации. При отсутствии должной терапии рубец увеличивается в размерах, провоцирует появление болевых ощущений, зуда. Применяются консервативные методы терапии.
Ребенок находится под наблюдением фтизиатра, хирурга, педиатра.
- Изъязвления, превышающие в диаметре десять миллиметров. Указывают на повышенную чувствительность к компонентам введенного препарата. Опасность язв заключается в риске проникновения инфекции. Кроме того, компоненты БЦЖ могут не оказать должного эффекта.
- Генерализованная БЦЖ-инфекция. Отмечается очень редко. Защитные функции организма при этом отсутствуют полностью. Причина развития осложнения – иммунодефицитное состояние.
Как перенесли прививки в роддоме мои дети?
Я в роддоме подписала согласие на прививку и помню, как старшую дочку на 3 день жизни у меня унесли из палаты. Я была в это время за дверью в процедурном кабинете, внутрь не пустили, только слышала, как она очень сильно плакала, и у меня сердце кровью обливалось. В итоге принесли с поставленным уколом в плечо. Никаких побочек и осложнений в итоге замечено не было. Температура не поднималась, ребенок чувствовал себя хорошо, место укола сильно не опухало.
Температура не поднималась, ребенок чувствовал себя хорошо, место укола сильно не опухало.
И зажило место укола уж очень быстро, даже никакого заметного рубца толком не осталось, как будто ничего и не делали.
Теперь я считаю, что прививка в роддоме у дочки просто не привилась. Так как рубчика толком и не образовалось. Такая прививка значится как сомнительная.
Ко всему этому, когда в 1 год и 4 мес дочке стали ставить манту, у неё сразу уже было отрицательное значение папулы. Это был просто маленький синячок, никакой пуговки даже не образовывалось. Повторные манту нам иногда рисовали размером 2 или 3 мм в поликлинике, но по факту это были одни и те же синячки.
Теперь про сына и реакцию БЦЖ.
Рожала я его в другом городе, в другом роддоме, из-за этого видимо по другим правилам и проходила вакцинация. Я присутствовала в процедурном кабинете, когда сыну ставили БЦЖ в плечо.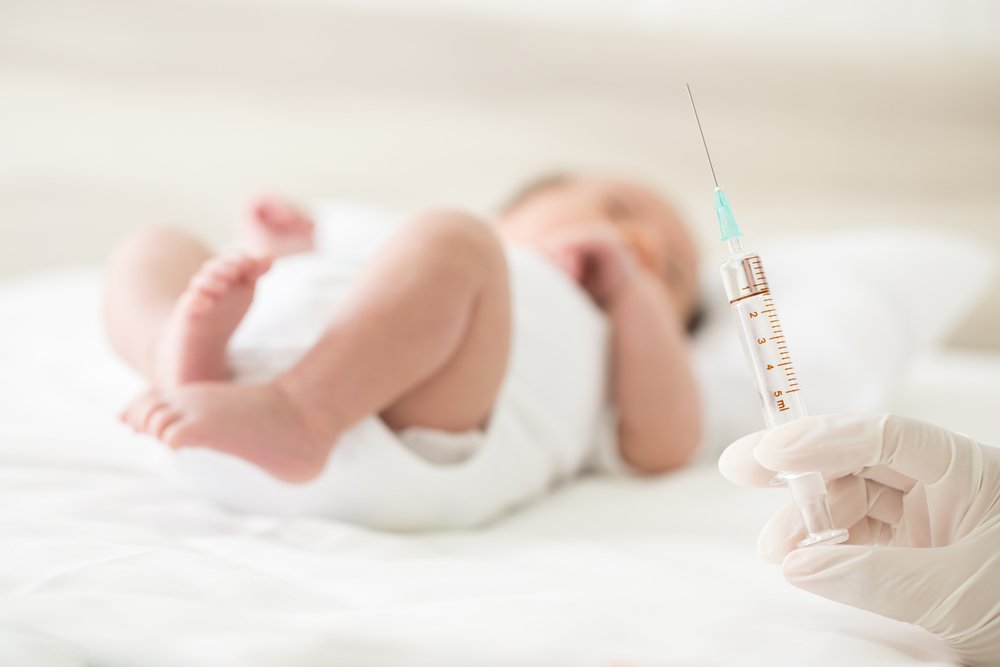 Конечно сказали в это день сына не купать, место укола не мочить, не тереть, не чесать, фенистилом не смазывать. Место укола может гноиться долгое время, но это по их словам было нормой.
Конечно сказали в это день сына не купать, место укола не мочить, не тереть, не чесать, фенистилом не смазывать. Место укола может гноиться долгое время, но это по их словам было нормой.
В итоге никаких страшных побочек после этого не было, не считая того, что у сына место укола гноилось целый год! Когда приходила врач на осмотр, то говорила, что это нормальная реакция организма. Только когда сыну исполнился один годик, все заросло и наконец образовался видимый рубец.
На фото внизу Показываю, как сейчас выглядит рубец после БЦЖ у сына в 1 год 9 месяцев.
Рубец после БЦЖ у сына в 1 год и 9 мес
Связь БЦЖ и Манту
Думаю, не все знают о том, что прививка БЦЖ и проба Манту неразрывно связаны друг с другом. Я лично не знала до поры до времени, например, в роддоме мне про это никто не рассказывал.
Проба Манту помогает определить, среагировал ли организм ребенка на БЦЖ, и можно ли надеяться на выработку иммунитета от туберкулеза.
После постановки БЦЖ нельзя ставить манту целый год!
В первый год жизни размер папулы Манту смотрят опираясь на размера рубчика от прививки БЦЖ.
На втором-седьмом году жизни ребенка размер рубчика уже не имеет такого значения.
Первую пробу манту сыну сделали в 1 год и 1 месяц. И в первый день пробы пуговка расплылась на всю руку, а в день замера на 4 день намеряли папулу 11, сказали, что это норма, учитывая его большой рубчик. Что будет дальше, поживем увидим.
Мой рубец после БЦЖ намного больше, чем у сына. Мне 33 года. И у меня всю жизнь проба манту зашкаливала по показателям, была примерно 12-18 мм. Мне тут чуть ли не приписывали туберкулез.
И из-за этого меня даже отправляли в санаторий по профилактике туберкулеза во время учебы в школе, только толку от этого санатория я не увидела.
А я просто расчесывала манту ночью не самопроизвольно, когда спала. Этот зуд после манту мне не давал покоя. Почему-то в то время врачи не хотели думать, что может у меня просто аллергия на манту, а ведь и такое возможно.
Почему-то в то время врачи не хотели думать, что может у меня просто аллергия на манту, а ведь и такое возможно.
Если проба Манту чешется, то это признак повышенной чувствительности кожи, иногда возбудимости нервной системы. Зуд возникает при склонности к аллергическим и кожным заболеваниям.
Сейчас я уже давно не ставила манту и туберкулезом не болею, живу себе счастливо и никого не трогаю.
Рубец после БЦЖ в 33 года
Ревакцинация БЦЖ
Как известно, прививка БЦЖ не дает защищенности от туберкулеза на всю жизнь, поэтому при необходимости её ставят повторно в 6-7 лет.
Из-за отрицательных показателей, нам в дочкины 6 лет настоятельно рекомендовали повторную вакцинацию БЦЖ в поликлинике.
Проводится ревакцинация БЦЖ ребенка обязательно после 3 дней и не более 2 недель после постановки манту.
Если не успел в этот срок, то надо получается через какое-то время манту повторить и успевать вновь сделать прививку БЦЖ за эти 2 недели.
Делается БЦЖ после замера манту, чтобы знать результаты, хотя у нас они и так уже были предсказуемы. Значение папулы отрицательное.
Дочь у меня аллергик и после постановки пробы манту, я уже неоднократно заметила, что у неё начинают течь сопли. То есть в первую неделю после постановки манту сделать ревакцинацию БЦЖ мы не смогли, а к концу второй недели, как раз успели поправить здоровье и поставили БЦЖ в последний возможный день срока.
Нормой в первый день постановки прививки считается шишечка до 10 мм, а вот если больше, то это уже возможно абсцесс. У дочки на плече место укола не сразу опухло, только к вечеру образовалась красная шишка и небольшая опухоль.
На следующий день после того, как дочке поставили прививку, шишка в месте укола еще увеличилась.
В этот же день утром дочь проснулась с заложенным носом, хотя вчера чувствовала себя отлично. То есть тоже связываю это с аллергическими проявлениями и уже реакцией на БЦЖ.
Утро 2 день — ревакцинация БЦЖ в 6 лет
К вечеру место укола еще больше опухло, появилась видимая болючая шишка. И эта шишка начала жутко чесаться. Но так как мазать ничем эту шишку от БЦЖ нельзя, чесать тоже нельзя, пришлось просто дуть,чтобы хоть как-то дочке стало полегче.
И эта шишка начала жутко чесаться. Но так как мазать ничем эту шишку от БЦЖ нельзя, чесать тоже нельзя, пришлось просто дуть,чтобы хоть как-то дочке стало полегче.
2 день вечером — ревакцинация БЦЖ в 6 лет
Первые 4 дня шишка была побольше, потом постепенно опухоль стала уменьшаться.
3 день — ревакцинация БЦЖ в 6 лет
Сильно чесалось место укола около 5 дней подряд, но дочь не расчесывала. Я ей сказала, что трогать эту шишку ни в коем случае нельзя.
5 день — ревакцинация БЦЖ в 6 лет
А еще спустя 7 дней после прививки дочка заболела. У неё поднялась температура 38,8, сопли потекли рекой, появился сильный кашель. Пришлось давать противовирусные, лечить по полной программе. Связываю болезнь с ослаблением иммунитета после прививки, так как до постановки БЦЖ и взятия пробы Манту дочь давно ничем не болела, наверное на 3 месяца мы точно забыли при лекарства и вот опять их достали.
Прошло 10 дней после ревакцинации БЖЦ, прививка пока не заживает. Шишка не гниет, как было у сына, и больше не чешется. Во время мытья место укола мы не трогаем, мылом этот участок не намыливаю, ничем не мажу.
10 день — ревакцинация БЦЖ в 6 лет
Спустя 3 недели место укола от прививки так и не заживает, чувствую, что заживаление будет долгим.
3 недели — ревакцинация БЦЖ
Жду, когда же уже все наконец пройдёт. Но если вакцина прививлась, возможно заживление до года.
Добавляю еще фото прививки спустя 2.5 месяца. Так ничего и не зажило. Всё время прививка гноится, при купании лопается и вытекает жидкость. В бассейне всё это выглядит не очень эстетично, но приотивопоказаний к его посещению нет. А в школе у нас бассейн — обязательный урок.
Фото БЦЖ спустя 7 месяцев постановки. Рубец так и не образовался.
Рубец так и не образовался.
Спустя 9 месяцев образовался рубец. И почему-то внутри прививки оказался маленький гнойный прыщик. Думаю, что он так и останется навсегда, не лопнет.
Повторная проба манту у дочки через год. Время покажет, что в это раз у нас вышло, будет ли отрицательный результат.
ИТОГИ в отношении вакцины БЦЖ
Достоинства:
1) Для России актуальная прививка, так как очень много людей у нас болеет туберкулезом и умирает от этой болезни;
2) Делается бесплатно в поликлинике.
Недостатки:
1) У сына целый год гноилось место укола;
2) Прививка подрывает иммунитет. Дочь после ревакцинации БЦЖ легко поймала очередной вирус, сопровождавшийся высокой температурой тела, соплями и сильным кашлем;
3) Сильный зуд в месте укола;
4) БЦЖ не дает гарантии, что ребенок не заболеет туберкулезом. То есть это только ощущение защиты, которой по факту нет;
То есть это только ощущение защиты, которой по факту нет;
5) Прививка может совсем не привиться и показывать отрицательные результаты во время проведения пробы Манту.
ВЫВОД. Ставить или не ставить БЦЖ — это дело каждого. Но если поставили, то будьте готовы к возможному долгому заживлению места укола, сильному зуду и ослаблению иммунитета.
Всем крепкого здоровья! И надо помнить, что всё конечно индивидуально.
Вакцина БЦЖ — «Что делать если прививку не поставили в роддоме? Реакция ребёнка с заболеванием печени на вакцину БЦЖ.»
Здравствуйте!
Наверное, еще весной каждый слышал о том что короновирус легче переносят люди которые привиты от туберкулёза. Честно признаюсь не знаю правда это или нет, но я очень переживала что мой сын не привит. Поэтому не могла дождаться когда нам дадут разрешение поставить прививку от туберкулёза. Этот день настал, расскажу как это было.
В КАКОМ ВОЗРАСТЕ СТАВЯТ ПРИВИВКУ БЦЖ.
Все родители знают что первую прививку БЦЖ ребёнок получает еще в роддоме. У нас получилось иначе. Сын родился с кистой в печени, врачи написали медицинский отвод. Поэтому прививку от гепатита и БЦЖ ему не поставили.
После регулярных наблюдений у специалистов нам дали разрешение начинать ставить прививки в 7,5 месяцев. Первой из них была БЦЖ.
Так что как видите, в идеале первая прививка ставится в роддоме на 3-4 день жизни малыша. Но бывают и исключения.
Вторая прививка — ревакцинация, ставится в 7 лет. Нам до нее еще далеко, поэтому речь пойдет только о первой прививке.
ПОЧЕМУ РЕБЁНКУ НУЖНО ДЕЛАТЬ ПРИВИВКУ СРАЗУ ПОСЛЕ РОЖДЕНИЯ.
Выделяют легочный и внелегочный туберкулез. Кроме легких, микобактерия поражает суставы, кости, головной мозг, почки. Для новорожденных инфекция особо опасна, поскольку у них нет специфического иммунитета, а собственная иммунная система не может справится с бактерией.
У малышей часто развивается туберкулезный менингит.
Думаю, что теперь вы понимаете почему я переживала что мой сын не привит. Конечно в наше время многие считают что детей не нужно прививать и что от прививок только ухудшается здоровье ребёнка. Я к таким мамам не отношусь. В моей семье все привиты и я даже не хочу задумываться о том что бы не прививать своего ребёнка.
ПРОТИВОПОКАЗАНИЯ.
Вакцина БЦЖ имеет противопоказания.
— глубокая недоношенность;
— вес младенца менее 2,5 кг;
— рождение ребенка от ВИЧ-инфицированной матери;
— тяжелые врожденные пороки развития;
— генетические заболевания;
— гемолитическая болезнь, возникающая в результате резус-конфликта;
— контакт с бактерией туберкулеза в первые сутки после рождения.
У моего сына совсем другое заболевание, но тем не менее врачи в роддоме побоялись брать на себя ответственность и ставить прививку.
ПОБОЧНЫЕ РЕАКЦИИ.
Наверное, все родители боятся побочных реакций. Но поверьте, они не так страшны как та болезнь которой может заболеть непривитый ребёнок в будущем.
Вот самые частые побочные реакции которые возникают у детей.
- повышение температуры до 37,5 градусов;
- покраснение и припухлость места инъекции;
- вялость, отсутствие аппетита;
- повышенная сонливость малыша.
КАК ПЕРЕНЕС ПЕРВУЮ ПРИВИВКУ МОЙ СЫН.
Так как прививку в роддоме сыну не поставили, и сын уже вовсю контактировал с окружающим миром, нам сначала назначили пробу Манту.
Вакцина БЦЖ
Пробу Манту сыну сделали 22 июня, на тот момент ему было 7,5 месяцев. Тонкую иглу вводят под кожу на запястье, процедура занимает несколько секунд. Сын даже не плакал. Было впечатление что он даже не понял что произошло. Медсестра прививочного кабинета умилялась и хвалила за смелость, а я радовалась что сыну не больно и что он не испугался.
После манту ребенка нельзя купать и вообще место укола нельзя мочить. Мы мочили место укола, в эти дни стояла ужасная жара и не мыть ребёнка было невозможно. Тем не менее укол не распухал и вообще никак не беспокоил сына. Это была просто точка, которую даже сфоткать не получилось.
26 июня мы пришли проверить Манту. Ее уже даже не видно было — реакция отрицательная. Нам сразу поставили БЦЖ.
Прививку БЦЖ ставят в плечо. Сын опять не плакал. Мужчина однако растёт! В первый день место укола было красное. Купать ребёнка нельзя, в этот раз мы не стали нарушать рекомендации. Боялись что поднимется температура, но никаких негативных последствий не было. И первые, и вторые, и третьи сутки прошли как обычно.
Так же врач сказала что три дня нужно ограничивать общение ребёнка с посторонними, не ходить в людные места. Эти рекомендации мы тоже соблюдали. Гулять ходили, но сами и по немноголюдным улицам.
Врач предупредила что прививку нельзя обрабатывать какими-либо средствами и что она может гноиться. У сына не гноилась, к счастью.
У сына не гноилась, к счастью.
Спустя 1 месяц прививка выглядела так.
Вакцина БЦЖ
Сейчас прошло уже 4 месяца. Место укола выглядит следующим образом.
Вакцина БЦЖ
Я считаю что сын прививку перенес хорошо. И после прививки я спокойна за его здоровье.
Кстати, после прививки уже дважды делали УЗИ печени и сдавали кровь на анализ. БЦЖ никак не повлияла на заболевание сына.
ИТОГ.
Плюсы:
— прививка бесплатная;
— ставят сразу в роддоме или в поликлинике по месту жительства;
— быстро зажила;
— не было побочных реакций;
— считаю что она необходима.
Минусов в нашем случае не было.
Я однозначно рекомендую не отказываться от прививки БЦЖ, если ребёнок здоров и не имеет противопоказаний. А решать конечно Вам. Здоровье Вашего ребёнка в Ваших руках.
Р.S. Если вам понравился мой отзыв, приглашаю вас посетить Мой профиль.
Новорожденному сделали прививку без разрешения — мать в грусти и ярости
Роддом подал в суд на женщину и, выиграв, провел вакцинацию.
Телеведущая, блогер и мама двоих сыновей Ирена Понарошку разместила в своем Instagram пост, в котором рассказала историю женщины из Хабаровска и ее новорожденной дочери. Если коротко: малышка родилась абсолютно здоровой, и мама отказалась прививать ее в роддоме. Сотрудники роддома подали на женщину в суд, выиграли его и самостоятельно провели вакцинацию без разрешения матери.
А вот вся история целиком:
«Ни разу за 7 лет на моей странице не было антипрививочной агитации. Не будет ее и сегодня! Да, я не прививаю своих детей. Но я никогда не призывала принимать решение о вакцинации, основываясь на моем примере! Я уважаю право родителей на выбор: только семья может решать, прививать или нет ребенка, если прививать — то когда, после каких обследований и какими вакцинами!
Вчера в роддоме №4 города Хабаровска произошел дикий, вопиющий случай нарушения прав матери и ребенка! Нарушения закона! Мама здоровой новорожденной девочки отказалась от вакцинации, в результате чего столкнулась с агрессией со стороны медицинского персонала, обвинениями и угрозами, главврач роддома @kgbuzrodilnyidom4 тут же подал в суд иск о защите интересов несовершеннолетнего лица и требовании проведения медицинских вмешательств «Для спасения жизни»! Подчеркиваю, ребенок родился здоровым, и «спасать» его вакцинами от туберкулеза и гепатита B в первые дни жизни не было никакой необходимости!
Суд в тот же день иск удовлетворил, решение суда тут же вступило в силу (вот бы суды всегда так оперативно работали!) и ребенка насильно вакцинировали! Хотя в Федеральном законе «Об иммунопрофилактике инфекционных болезней» прямо указывается право граждан на отказ от профилактических прививок! Но суд почему-то не увидел разницы между «спасением жизни» и «профилактической вакцинацией»!
Я связалась с мамой, она в слезах, раздавлена этой чудовищной несправедливостью, цитирую: «…когда еще сутки не прошли после родов, и я держу малышку на руках, и полная палата народу, сил нет вспоминать, слезы бегут…обидно, вместо того чтобы наслаждаться таким событием, плачу только…»
Роддом, тем временем, вчера опубликовал гордый пост о том, как они «спасли» ребенка от необразованной матери, и даже выложил решение суда. Однако потом публикация исчезла из аккаунта @kgbuzrodilnyidom4, а комментарии к постам были закрыты. Хотя в их же профиле есть пост от 4 июня, где черным по белому написано, что согласно приказу Минздрава №109 от 21 марта 2003 года вакцинация проводится только «при наличии информированного добровольного согласия законного представителя»!
Однако потом публикация исчезла из аккаунта @kgbuzrodilnyidom4, а комментарии к постам были закрыты. Хотя в их же профиле есть пост от 4 июня, где черным по белому написано, что согласно приказу Минздрава №109 от 21 марта 2003 года вакцинация проводится только «при наличии информированного добровольного согласия законного представителя»!
Мама собирается подавать в суд на роддом и оспаривать решение суда. Хотя уже ходят слухи, что ей угрожают и запугивают, и я не исключаю, что она передумает. И это тоже ее право! Все, что я могу сделать, это предложить ей юридическую, финансовую, и информационную помощь, потому что не хочу, чтобы это повторялось в других роддомах страны!
В СМИ об этой ситуации вы не найдете ни слова! Уважаемые коллеги — журналисты, не молчите! Речь не идет от том, хорошо прививки или плохо! Мама могла принять решение о вакцинации позже, проведя полное обследование ребенка, так делают тысячи мам, это их право! Это наше право! До тех пор, пока мы будем молчать, наши права будут нарушать, и это может коснуться каждого!»
После вакцинации от туберкулеза поступили жалобы на осложнения
Жительница Бишкека Камила Судольская рассказала, что примерно через месяц после прививки против туберкулеза (БЦЖ) осложнение проявилось у ее малыша в виде лимфаденита в подмышечной области:
— Родила в роддоме №5 города Бишкека. Ребенка привили на следующий день. Как такового письменного соглашения не было. Всех массово повели на прививку. Уже после укола я подписала бумажку. Они дали расписаться. Единственным объяснением было, что прививка делается от туберкулеза. Никто не проверил, есть аллергия или нет. После вакцинации температура у ребенка поднялась, не значительно — до 38 градусов. Но никто не обратил внимание, даже не спросили.
Ребенка привили на следующий день. Как такового письменного соглашения не было. Всех массово повели на прививку. Уже после укола я подписала бумажку. Они дали расписаться. Единственным объяснением было, что прививка делается от туберкулеза. Никто не проверил, есть аллергия или нет. После вакцинации температура у ребенка поднялась, не значительно — до 38 градусов. Но никто не обратил внимание, даже не спросили.
После появления осложнений мама малыша обратилась сначала к врачам, а потом в туберкулезный диспансер. Там прописали лечение сильнодействующими противотуберкулезными препаратами, которые влекут за собой побочные действия в виде дисбактериоза и так далее, рассказала Камила Судольская.
Жительница города Токмака Татьяна Новикова в июле 2018 года в Национальном центре охраны материнства и детства посредством кесарева сечения родила тройню. По ее словам, пока она отходила от наркоза врачи без ее разрешения сделали прививки всем троим младенцам:
— Оба моих старших детей привиты. Поэтому моя мама без задних мыслей дала согласие на прививку. Ей не объяснили, чем это может быть чревато, что по республике есть случаи осложнений. Третья девочка находилась в реанимации, у нее был слабый иммунитет. У меня возникает вопрос, если они знали, что ребенок слабый, все трое рождены с малым весом, недоношенные, потому что я родила на 34-й неделе, то почему они торопились моих двоих детей привить? Ведь они могли дать время и объяснить, что дети маленькие, давайте подождем, дадим им прийти в себя. Нет, они взяли и обоих привили. В итоге теперь у моей второй девочки из тройни осложнение в виде лимфоузла под левой подмышкой. Мальчика пронесло, слава богу. Он не пострадал.
Поэтому моя мама без задних мыслей дала согласие на прививку. Ей не объяснили, чем это может быть чревато, что по республике есть случаи осложнений. Третья девочка находилась в реанимации, у нее был слабый иммунитет. У меня возникает вопрос, если они знали, что ребенок слабый, все трое рождены с малым весом, недоношенные, потому что я родила на 34-й неделе, то почему они торопились моих двоих детей привить? Ведь они могли дать время и объяснить, что дети маленькие, давайте подождем, дадим им прийти в себя. Нет, они взяли и обоих привили. В итоге теперь у моей второй девочки из тройни осложнение в виде лимфоузла под левой подмышкой. Мальчика пронесло, слава богу. Он не пострадал.
Официально зарегистрировано 33 младенца
Врач Республиканского центра иммунопрофилактики Гульбара Ишенапысова сообщила, что в 2018 года официально зарегистрированы 33 младенца, у которых после прививки появился лимфаденит:
Гүлбара Ишенапысова.
— Вообще вакцину против туберкулеза или по-другому БЦЖ делают сразу после рождения. Новорожденные часто сталкиваются с туберкулезным менингитом. Для его предотвращения вакцину нужно вводить сразу. Говорят, что вакцина БЦЖ из Турции, поэтому появляется реакция. Но все наши вакцины из Японии. Конечно, могут быть негативные последствия. Мы об этом постоянно предупреждаем родителей. На месте укола появляются пузырьки, в течение пяти-девяти месяцев они уплотняются и уходят. Иногда может проявиться воспаление подмышечных лимфоузлов. В 2018 году было зарегистрировано 33 случая лимфаденита после прививки БЦЖ.
Новорожденные часто сталкиваются с туберкулезным менингитом. Для его предотвращения вакцину нужно вводить сразу. Говорят, что вакцина БЦЖ из Турции, поэтому появляется реакция. Но все наши вакцины из Японии. Конечно, могут быть негативные последствия. Мы об этом постоянно предупреждаем родителей. На месте укола появляются пузырьки, в течение пяти-девяти месяцев они уплотняются и уходят. Иногда может проявиться воспаление подмышечных лимфоузлов. В 2018 году было зарегистрировано 33 случая лимфаденита после прививки БЦЖ.
Во время написания материала мы узнали о других родителях, которые жаловались на осложнения после БЦЖ. Одна из них — Элеонора — лечила ребенка несколько месяцев:
— В три месяца у ребенка появились пузырьки в области подмышки. Мы сразу поехали в больницу. Там провели УЗИ и выявили, что это осложнение после прививки от туберкулеза. Сказали, что после прививки появляется такая реакция, и отправили в Национальный центр фтизиатрии. Там мы встали на учет и взяли курс лечения. Принимали лекарства от туберкулеза. Прописали специальную мазь. До пяти месяцев мы принимали лекарства, а шишка увеличилась. Ее убрали во время операции. В общем, мы лечились шесть месяцев.
Там мы встали на учет и взяли курс лечения. Принимали лекарства от туберкулеза. Прописали специальную мазь. До пяти месяцев мы принимали лекарства, а шишка увеличилась. Ее убрали во время операции. В общем, мы лечились шесть месяцев.
«Туберкулез встречается часто»
Главный неанатолог Национального центра охраны материнства и детства Сагынбу Абдувалиева отметила, что в развитых странах не отказываются от прививки БЦЖ, а в Кыргызстане это необходимо делать сразу после рождения:
— После БЦЖ невозможны осложнения, только у 0,1 процента привитых детей встречается такая реакция. У ребенка может воспалиться лимфоузел. В таких случаях нужно обращаться к врачам, которые лечат туберкулез. Нельзя отказаться от БЦЖ. Ведь с каждым днем у нас больше больных туберкулезом. После вакцинации у ребенка появится устойчивость к этой болезни.
В соответствии с национальным календарем прививок, вакцинация БЦЖ проводится на следующий день после рождения.
В Кыргызстане в 2018 году было зарегистрировано свыше 150 тысяч новорожденных. До этого были случаи отказа от вакцинации по религиозным причинам. В последние годы из-за увеличения заболеваемости корью, даже те, кто отказывался, начали прививать детей.
JsO
Перевод с кыргызского. Оригинал материала здесь.
Вакцинация детей | КДЦ «Ультрамед»
Вакцинация – самое эффективное средство предотвращения инфекционных заболеваний у детей, возможность избежать ряда серьезных заболеваний и их последствий. Например, как при заболевании паротитом у мальчиков может быть осложнение в виде бесплодия. Избежать этого можно с помощью своевременной вакцинации.
Делать ли прививки новорожденному ребенку в роддоме при условии, что у него еще не сформировался иммунитет – делать! Ведь иммунитет ребенка подразделяется на неспецифический и специфический.
Иммунная система борется со всеми агентами, несущими в себе чужеродную генетическую информацию, как правило, это грибы, вирусы, бактерии. При ослабленных защитных силах организма, любая болезнь перетекает в серьёзное заболевание.
При ослабленных защитных силах организма, любая болезнь перетекает в серьёзное заболевание.
-
Специфический иммунитет ещё называют приобретённым, хотя существует и врождённая его разновидность. Он появляется тогда, когда возникают специфические факторы – выработка антител под воздействием антигена. Специфический иммунитет образуется после того, как человек переболел или был вакцинирован. Специфический иммунитет у новорожденных представлен слабо, все необходимые иммуноглобулины (защитные антитела) он получает с грудным молоком от матери. Вакцинация детей приводит к тому, что у них возникает специфический иммунитет к опасным заболеваниям, таким как полиомиелит, дифтерия, корь и др.
-
Неспецифический (врожденный) иммунитет – это те защитные силы организма, которые начинают формироваться у ребенка еще внутри утробы из материнских антител и продолжают развиваться на протяжении всей его жизни и является врожденной невосприимчивостью человека противостоять негативному влиянию внешних агентов бактерий, вирусов и др.
 )
)
ВАЖНО! Доверяйте ВАШЕМУ педиатру, его мнение и возможность следить за развитием вашего ребенка, помогут грамотно спланировать индивидуальный прививочный календарь (при необходимости)
Выбирать прививать или нет будете вы сами, главное, чтобы принятое решение было наилучшим выбором для роста и развития вашего ребенка и семьи!
Прививки детям
В детском отделении «Ультрамед» Вы можете получить прививку от:
- коклюша, дифтерии, столбняка, полиомиелита, гемофильной инфекции вакциной «Пентаксим» (производитель Франция)
- пневмококковой инфекции вакциной «Превенар» (производитель США)
- коклюша, дифтерии, столбняка, полиомиелита, гемофильной инфекции, гепатита В вакциной «Инфанрикс Гекса» (производитель Бельгия, Франция)
- кори, паротита (паротитно-коревая, краснушная культуральная живая) – (производитель Россия)
- дифтерии, столбняка и коклюша вакциной «АДАСЕЛЬ» (ревакцинация с 4 лет) (производитель Канада)
- кори, паротита и краснухи вакциной «М-М-Р II» живая (производитель США)
- клещевого энцефалита вакциной «Клещ-Э-Вак» (производитель Россия)
- гепатита В «Регевак» (производитель Россия)
Вакцинация в Детском отделении «Ультрамед» это:
- индивидуальный подход к Вашему ребенку
- консультация педиатра
- сбор аллергоанамнеза
- осмотр пациента
- термометрия
- манипуляция по введению вакцины
- наблюдение за ребенком в течении 30 минут в клинике, после введения вакцины
- выдача документа о проведенной вакцинации.

Будьте внимательны, не нервничайте и помните – любовь родителей и забота врачей победят любые недуги!
В детском отделении «Ультрамед» проводится вакцинация против ветряной оспы и менингококка
Подробнее
Стоимость услуг
| Вакцинация против кори, паротита | 350 ₽ |
| Вакцинация против дифтерии, столбняка и коклюша вакциной «АДАСЕЛЬ» | 2600 ₽ |
| Вакцинация против кори, паротита и краснухи вакциной «М-М-Р II» | 1100 ₽ |
| Вакцинация против ветряной оспы вакциной «Варилрикс» | 3500 ₽ |
| Вакцинация против коклюша, дифтерии, столбняка «Инфанрикс» | 1500 ₽ |
| Внутрикожная проба с туберкулезным аллергеном (туберкулиновая проба Манту) | 600 ₽ |
| Диаскинтест | 520 ₽ |
| Вакцинация против гриппа вакциной «Гриппол» с выездом на предприятие | 650 ₽ |
| Вакцинация против полиомиелита вакциной «Полиорикс» | 520 ₽ |
| Вакцинация против клещевого энцефалита вакциной «ФСМЕ-ИММУН | 1200 ₽ |
| Вакцинация против клещевого энцефалита вакциной «ФСМЕ-ИММУН Джуниор» | 1200 ₽ |
| Вакцинация против клещевого энцефалита вакциной «Энцевир» | 900 ₽ |
| Вакцинация против клещевого энцефалита вакциной «Энцевир» с выездом на предприятие | 1100 ₽ |
| Вакцинация против клещевого энцефалита вакциной «Энцепур» | 1050 ₽ |
| Вакцинация против коклюша, дифтерии, столбняка, полиомиелита, гемофильной инфекции вакциной «Пентаксим» | 2100 ₽ |
| Вакцинация против гепатита В вакциной «Энджерикс» | 600 ₽ |
| Вакцинация против пневмококковой инфекции вакциной «Превенар» | 4000 ₽ |
| Вакцинация против клещевого энцефалита вакциной «Клещ-Э-Вак» | 950 ₽ |
| Вакцинация против гриппа вакциной «Гриппол» | 530 ₽ |
| Вакцинация против коклюша, дифтерии, столбняка, полиомиелита, гемофильной инфекции, гепатита В вакциной «Инфанрикс Гекса» | 2900 ₽ |
| Вакцинация против гриппа вакциной «Ультрикс» | 550 ₽ |
| Вакцинация против гриппа вакциной «Ультрикс» с выездом на предприятие | 730 ₽ |
Вакцинация против менингококковой инфекции.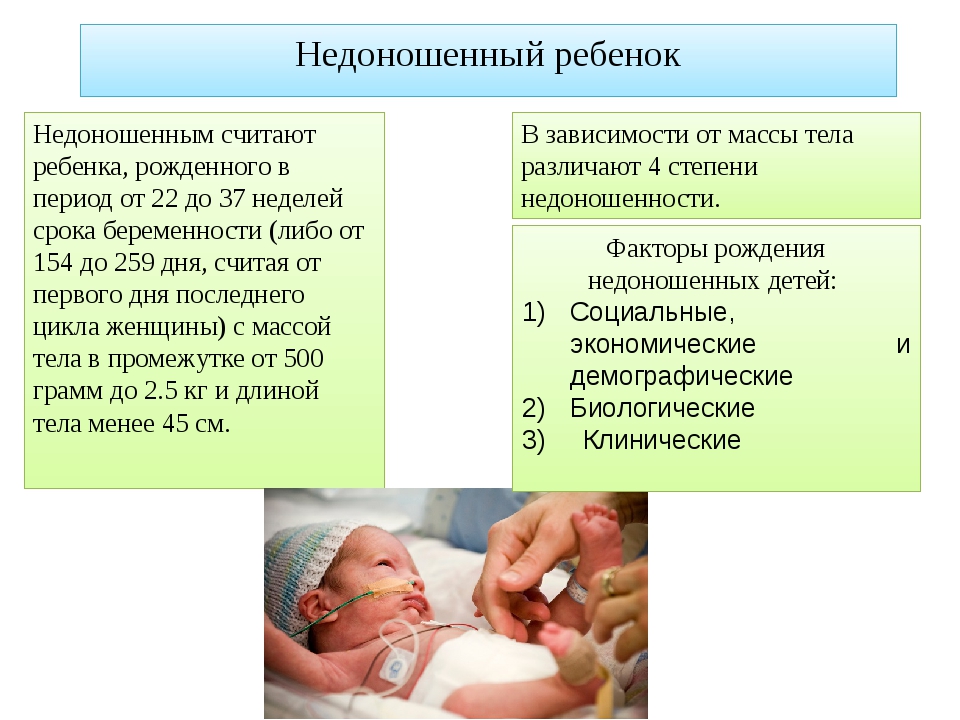 Менактра (США), вакцина Менактра (США), вакцина | 4800 ₽ |
| Вакцинация против гриппа вакциной «Совигрипп» с выездом на предприятие | 550 ₽ |
| Вакцинация против гриппа вакциной «Совигрипп» | 500 ₽ |
| Вакцинация против гриппа вакциной «Флю М» (предварительная оплата) | 600 ₽ |
| Вакцинация против грипп вакциной «Флю М» с выездом на предприятие (предварительная оплата) | 700 ₽ |
| Профилактический прием (осмотр, консультация) врача-педиатра перед вакцинацией | 400 ₽ |
ВГВ | Прививки.уз — Предупредить. Защитить. Привить.
Вы спрашивали
Следующий вопрос
Вирусный гепатит B
Ребенок ранее привит против ВГВ (в роддоме получал прививку ВГВ, в 2 ,3 и 4 месяц – пентавалентную вакцину). Недавно у отца ребенка выявлен хронический ВГВ. Нужны ли ребенку дополнительные прививки?
Недавно у отца ребенка выявлен хронический ВГВ. Нужны ли ребенку дополнительные прививки?
Вирусный гепатит B
Кому не рекомендуется введение вакцины против ВГВ?
Вакцина против ВГВ противопоказана только тем, у кого ранее наблюдались тяжелые аллергические реакции
Подробнее
Вирусный гепатит B
В три месяца ребенку прививку против ВГВ делать не стали, так как был низкий гемоглобин. Когда лучше сделать третью прививку? Врач сказала – только при наличии нормального анализа крови.
Анемия, выявленная при обследовании, никак не может являться медицинским отводом к вакцинации.
Подробнее
Вирусный гепатит B
Взаимозаменяемость рекомбинантных вакцин
Первую прививку против ВГВ ребенку сделали в роддоме вакциной одной вакциной.
Подробнее
Вирусный гепатит B
Когда можно привить против ВГВ ребенка с хроническим заболеванием?
Вакцинация временно откладывается до купирования обострения.
Подробнее
Вирусный гепатит B
Ребенок родился в 37 недель, маловесный, последствия гипоксии еще присутствуют, понижен мышечный тонус, снижен уровень гемоглобина. Можно ли на таком фоне прививать против гепатита В?
Иммунизация против ВГВ недоношенных детей проводится по всему миру
Подробнее
Вирусный гепатит B
Можно ли заразиться от вакцины вирусом гепатита В? Заразен ли привитой?
Вирусный гепатит B
Можно ли прививать против ВГВ на фоне приема различных лекарств?
В инструкциях по применению рекомбинантных вакцин против ВГВ не указано никаких лекарственных веществ
Подробнее
Вирусный гепатит B
В какую часть тела лучше получать прививку против ВГВ? Можно ли делать эту прививку в ягодицу?
Вакцины должны вводиться только тем способом, который указан в инструкции по их применению.
Подробнее
Вирусный гепатит B
Прививали ребенка от ВГВ перед детским садом. Успели сделать 2 прививки, между 2 и 3 прививкой получается интервал 2 года. Нам рекомендуют начинать прививаться снова. Правильно ли это?
При увеличении интервалов между прививками против ВГВ никаких дополнительных прививок не требуется
Подробнее
Вирусный гепатит B
Каков график вакцинации против ВГВ в Узбекистане?
По национальному календарю Республики Узбекистан первая вакцинация против ВГВ
Подробнее
Вирусный гепатит B
Можно ли вводить вакцину против ВГВ одновременно с другими вакцинами?
Допускается введение вакцин (кроме вакцин для профилактики туберкулеза), применяемых в рамках Календаря профилактических прививок, в один день разными шприцами в разные участки тела.
Подробнее
Вирусный гепатит B
Как долго защищает вакцинация против ВГВ? Нужна ли ревакцинация?
Вакцинация (введение трех доз вакцины), проведенная в течение раннего детства, создает долговременную защиту от носительства вируса.
Подробнее
Вирусный гепатит B
Безопасна ли вакцина против ВГВ?
Да, безопасна. Вакцина против ВГВ безопасна при введении новорожденным, младенцам, детям, подросткам и взрослым
Подробнее
Вирусный гепатит B
Можно ли прививать против ВГВ новорожденных с желтухой?
Желтуха встречается у большинства (приблизительно от 40 до 70%) совершенно здоровых доношенных новорожденных и обычно является результатом естественных процессов, происходящих в его организме
Подробнее
Вирусный гепатит B
Не является ли грудное вскармливание противопоказанием для прививки ребенка против ВГВ?
Кормление грудью не является противопоказанием к вакцинации против ВГВ
Подробнее
Вирусный гепатит B
Ребенку 4 месяца. В поликлинике делают 4 прививки сразу в один день (Пентавалентная вакцина -3, включающая в свой состав и ВГВ), ОПВ-3 и ИПВ . Можно ли их делать сразу? Стоит ли сделать все три прививки, или лучше отказаться временно от ОПВ и ИПВ?
В поликлинике делают 4 прививки сразу в один день (Пентавалентная вакцина -3, включающая в свой состав и ВГВ), ОПВ-3 и ИПВ . Можно ли их делать сразу? Стоит ли сделать все три прививки, или лучше отказаться временно от ОПВ и ИПВ?
Одновременное введение вакцин – международный стандарт, применяющийся для обеспечения безопасности ребенка.
Подробнее
Вирусный гепатит B
Как производятся рекомбинантные вакцины против ВГВ?
Рекомбинантные вакцины, зарегистрированные в Республике Узбекистан, производятся с применением культуры пекарских дрожжевых грибков
Подробнее
Вирусный гепатит B
Если у ребенка с момента первой прививки против ВГВ в роддоме прошло более 3 месяцев, по какой схеме его прививать далее?
Если первичный курс прерван после первой дозы
Подробнее
Вирусный гепатит B
У нас в семье нет носителей вируса ВГВ, зачем прививать ребенка в роддоме?
Ребенок в первые же месяцы жизни подвергается множеству медицинских манипуляций при осмотрах и обследованиях.
Подробнее
Вирусный гепатит B
Если ребенку вакцинация против ВГВ в роддоме не проведена, по какой схеме его прививать?
Если новорожденный не был привит против ВГВ в родильном доме
Подробнее
Вирусный гепатит B
Почему надо обязательно начинать делать прививки сразу после рождения ребёнка? Можно ли подождать хотя бы год?
Вакцинацию против ВГВ проводят сразу после рождения ребенка, так как он уязвим и не имеет защитного иммунитета, вирус легко передается при медицинских манипуляциях и в быту.
Подробнее
Вирусный гепатит B
Слышала, что между прививками против гепатита лучше не делать других прививок, правда ли это?
Информация о том, что между прививками против гепатита нежелательно делать другие прививки
Подробнее
Вирусный гепатит B
Мой ребенок не был привит в родильном доме из-за болезни (сепсис новорожденного). Когда можно привить против ВГВ?
Когда можно привить против ВГВ?
Вакцина против ВГВ не содержит цельного вируса ни в живом, ни в инактивированном виде, только фрагмент его оболочки.
Подробнее
Вирусный гепатит B
Вакцинация детей с частыми ОРВИ
Нужно ли дожидаться окончания катаральных явлений после снижения температуры?
Подробнее
Вирусный гепатит B
Можно ли бесплатно получить прививку против ВГВ и кому?
В медицинских учреждениях по месту жительства бесплатно (за счет государственного финансирования) можно привиться против ВГВ детям в сроки
Подробнее
Вирусный гепатит B
Когда можно привить против ВГВ ребенка с острым заболеванием?
Как и в случае вакцинации против других инфекций
Подробнее
Все вопросы
Безопасность и эффективность вакцинации новорожденных
Abstract
Новорожденные имеют незрелую иммунную систему, которая подвергает их высокому риску инфицирования, одновременно снижая реакцию на большинство вакцин, что создает проблемы для защиты этой уязвимой группы населения. Тем не менее, некоторые вакцины, такие как Bacillus Calmette Guérin (BCG) и вакцина против гепатита B (HBV), действительно демонстрируют безопасность и некоторую эффективность при рождении, обеспечивая принципиальное доказательство того, что определенные комбинации антиген-адъювант способны вызывать защитные реакции новорожденных.Более того, рождение ребенка является важным направлением медицинского обслуживания во всем мире, а это означает, что эффективные вакцины для новорожденных достигают высокого уровня распространения среди населения. Учитывая потенциально значительную пользу вакцинации при рождении, доступность более широкого спектра более эффективных неонатальных вакцин является неудовлетворенной медицинской потребностью и приоритетом общественного здравоохранения. Этот обзор посвящен безопасности и эффективности вакцинации новорожденных людей, а также недавним исследованиям, в которых используются новые подходы к повышению эффективности вакцинации новорожденных.
Тем не менее, некоторые вакцины, такие как Bacillus Calmette Guérin (BCG) и вакцина против гепатита B (HBV), действительно демонстрируют безопасность и некоторую эффективность при рождении, обеспечивая принципиальное доказательство того, что определенные комбинации антиген-адъювант способны вызывать защитные реакции новорожденных.Более того, рождение ребенка является важным направлением медицинского обслуживания во всем мире, а это означает, что эффективные вакцины для новорожденных достигают высокого уровня распространения среди населения. Учитывая потенциально значительную пользу вакцинации при рождении, доступность более широкого спектра более эффективных неонатальных вакцин является неудовлетворенной медицинской потребностью и приоритетом общественного здравоохранения. Этот обзор посвящен безопасности и эффективности вакцинации новорожденных людей, а также недавним исследованиям, в которых используются новые подходы к повышению эффективности вакцинации новорожденных.
Ключевые слова: адъювант, иммунизация, новорожденный, новорожденный, Toll-подобный рецептор
Введение
Новорожденные и младенцы страдают высокой частотой и серьезностью микробной инфекции, приводящей к миллионам смертей во всем мире [1]. Те же иммунодефицитные состояния, которые делают новорожденных восприимчивыми к инфекции, также снижают их реакцию памяти на большинство антигенов, тем самым потенциально сводя на нет усилия по защите этой группы высокого риска. Поскольку роды являются наиболее надежным пунктом обращения за медицинской помощью во всем мире [1], а эффективная вакцинация при рождении обеспечит раннюю защиту новорожденных и младенцев, расширение и совершенствование доступных средств неонатальной вакцинации является глобальным приоритетом здравоохранения.
Те же иммунодефицитные состояния, которые делают новорожденных восприимчивыми к инфекции, также снижают их реакцию памяти на большинство антигенов, тем самым потенциально сводя на нет усилия по защите этой группы высокого риска. Поскольку роды являются наиболее надежным пунктом обращения за медицинской помощью во всем мире [1], а эффективная вакцинация при рождении обеспечит раннюю защиту новорожденных и младенцев, расширение и совершенствование доступных средств неонатальной вакцинации является глобальным приоритетом здравоохранения.
У новорожденных нарушены иммунные ответы из-за ряда недостатков как адаптивного иммунитета [2], так и врожденного иммунитета [3], а также потенциально подавляющих эффектов материнских антител (MatAb) [4, 5]. Новорожденные проявляют повышенную активность супрессивных Т-регуляторных клеток [6, 7] в сочетании с нарушениями функциональной активности антигенпрезентирующих клеток (APC) [8, 9]. Таким образом, исследование вакцинации новорожденных — это отчасти поиск комбинаций антиген (Ag) / адъювант (Aj), которые будут эффективны при рождении. Кроме того, новорожденные и младенцы имеют ограниченный репертуар Ab и могут продуцировать субоптимальные Ab в ответ на некоторое количество Ag [10, 11].
Кроме того, новорожденные и младенцы имеют ограниченный репертуар Ab и могут продуцировать субоптимальные Ab в ответ на некоторое количество Ag [10, 11].
В этом обзоре обобщены клинические данные о безопасности и эффективности вакцинации новорожденных людей, а также трансляционные исследования, направленные на разработку новых подходов к эффективной вакцинации новорожденных. На всем протяжении нашего внимания мы будем уделять внимание безопасности и эффективности подходов к вакцинации новорожденных, имея в виду, что основные аспекты неонатального иммунитета (с особым акцентом на клетки дендритных клеток) рассматриваются в сопроводительной статье Willems et al [12].
Возможные препятствия для иммунизации новорожденных
Проблемы безопасности
Проблемы, которые были высказаны в отношении вакцинации новорожденных и младенцев, включают: i) сомнения в эффективности, учитывая ограниченную способность новорожденных реагировать на многие виды антигена; и ii) потенциальные эффекты на поляризацию иммунной системы, включая возможность запуска аутоиммунитета через мимикрию эпитопа или эффект Aj [13, 14]. С теоретической точки зрения эти опасения частично смягчаются: i) документально подтвержденной способностью новорожденных реагировать на несколько вакцин, включая Bacillus Calmette Guérin (BCG) и вакцину против гепатита B (как описано ниже), что служит доказательством концепции, что неонатальный вакцинация может быть безопасной и эффективной; ii) наличие обширных иммунологических механизмов центральной и периферической толерантности, которые устраняют самореактивные Т- и В-клетки у новорожденных в сочетании с; iii) доказательства того, что несколько педиатрических вакцин, включая БЦЖ, не связаны с аллергией или аутоиммунитетом [15].Тем не менее, несмотря на эти концептуальные заверения, новые вакцины, как и любые новые лекарства, действительно обладают потенциалом вызывать побочные эффекты и, безусловно, должны проходить тщательный и постоянный анализ безопасности, в том числе проводимый в США Системой отчетности о побочных эффектах вакцин ( VAERS), программа Управления по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) и Центров по контролю за заболеваниями (CDC).
С теоретической точки зрения эти опасения частично смягчаются: i) документально подтвержденной способностью новорожденных реагировать на несколько вакцин, включая Bacillus Calmette Guérin (BCG) и вакцину против гепатита B (как описано ниже), что служит доказательством концепции, что неонатальный вакцинация может быть безопасной и эффективной; ii) наличие обширных иммунологических механизмов центральной и периферической толерантности, которые устраняют самореактивные Т- и В-клетки у новорожденных в сочетании с; iii) доказательства того, что несколько педиатрических вакцин, включая БЦЖ, не связаны с аллергией или аутоиммунитетом [15].Тем не менее, несмотря на эти концептуальные заверения, новые вакцины, как и любые новые лекарства, действительно обладают потенциалом вызывать побочные эффекты и, безусловно, должны проходить тщательный и постоянный анализ безопасности, в том числе проводимый в США Системой отчетности о побочных эффектах вакцин ( VAERS), программа Управления по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) и Центров по контролю за заболеваниями (CDC). Действительно, опасения по поводу безопасности вызвали отмену и / или изменение некоторых педиатрических вакцин, и два примера обсуждаются ниже.
Действительно, опасения по поводу безопасности вызвали отмену и / или изменение некоторых педиатрических вакцин, и два примера обсуждаются ниже.
В 1998 г. вакцина против кори, паротита и краснухи (MMR) вызвала споры в Великобритании, когда Andrew Wakefield et al. [16] сообщил о двенадцати детях, у которых развились симптомы расстройства аутистического спектра вскоре после того, как они получили вакцину MMR. Раздел интерпретации этого исследования был позже отозван в 2004 году десятью соавторами Уэйкфилда, и последующие крупные исследования пришли к выводу, что нет никаких доказательств связи между MMR и аутизмом [17]. Было высказано предположение, что раннее воздействие тиомерсала связано с нейропсихологическим дефицитом у детей, хотя эта связь не была подтверждена в исследовании 1047 детей в возрасте от 7 до 10 лет [18].Тем не менее, в 1999 году Американская академия педиатрии и Центры по контролю и профилактике заболеваний потребовали удалить тиомерсал из всех детских вакцин, и этот консервант, содержащий этилртуть, больше не использовался в обычных детских вакцинах в США с 2001 года. связь была опровергнута, сохраняется необходимость строгого мониторинга безопасности при разработке всех вакцин, особенно тех, которые можно вводить новорожденным.
связь была опровергнута, сохраняется необходимость строгого мониторинга безопасности при разработке всех вакцин, особенно тех, которые можно вводить новорожденным.
Живая аттенуированная ротавирусная вакцина RotaShield (Wyeth-Ayerst) содержала три реассортанта ротавируса с различными генами, кодирующими специфические серотипы (VP4 или VP7), вызывающие вирусспецифические Ab, наряду с генами ротавируса, пассированного макаками резуса, которые ослабляли вирулентность [19] .После одобрения в систему наблюдения VAERS поступили сообщения о 76 случаях инвагинации кишечника, при которых один сегмент кишечника заворачивается в другой сегмент, вызывая непроходимость. 70% случаев инвагинации произошли после первой дозы вакцины. В связи с этим наблюдением CDC рекомендовал приостановить введение ротавирусной вакцины до проведения дальнейших исследований. Одно исследование выявило один случай на каждые 5000–9500 вакцинированных младенцев, с самым высоким риском после первой дозы. Из-за возможной связи с инвагинацией, Rotashield был снят с продажи в 1999 году.
Неадекватная иммуногенность большинства вакцин при рождении
Иммунизация в раннем возрасте является важнейшей задачей общественного здравоохранения, но остается сложной областью. Иммунологическая среда новорожденных, смещенная в сторону иммунитета Th3 для предотвращения распознавания развивающегося плода как аллотрансплантата материнской иммунной системой [20], представляет собой важное препятствие, которое вакцинация в неонатальный период должна преодолеть. В дополнение к проблеме, связанной с незрелостью лейкоцитов новорожденных, эффективные вакцины для новорожденных должны также преодолевать потенциальный ингибирующий эффект MatAb [20].Считается, что ингибирование адаптивных иммунных ответов с помощью MatAb зависит от соотношения между титрами MatAb и дозой вакцинного антигена и связано с детерминантно-специфическим маскированием В-клеточных эпитопов [21]. Поглощение APC младенцами и ответы Т-клеток, по-видимому, в значительной степени не затрагиваются. Например, что касается вакцин, конъюгированных с Haemophilus influenzae типа b (Hib), MatAb к белку-носителю столбнячного анатоксина (TT) подавляет ответы младенцев на TT, но не подавляет ответы Ab на полисахаридную составляющую Hib [22] .Таким образом, MatAb приводит к специфическому маскированию ТТ, но не антигенных детерминант Hib для В-клеток младенца, сохраняя захват APC иммунных комплексов MatAb: Ag и обеспечивая ответ на полисахаридную составляющую Hib. В целом реакции новорожденных людей на вакцины непредсказуемы из исследований на младенцах старшего возраста или взрослых. Тем не менее, было показано, что некоторые вакцины вызывают клинически значимый иммуногенный ответ при рождении, как описано ниже.
Следует отметить, что при оценке потенциальной эффективности вакцин для новорожденных, хотя профилактика инфекции является конечной целью и наиболее важной конечной точкой, необходимо тщательно учитывать корреляты иммунитета, вызванного вакциной, как это недавно было рассмотрено Плоткиным [23].Как количественные, так и качественные (, т.е. , функциональная активность) Ab могут служить «коррелятами» и суррогатными маркерами защиты и преимущественно используются в исследованиях вакцин. Тем не менее, клеточный иммунитет имеет решающее значение для защиты от внутриклеточных инфекций и, благодаря функции клеток CD4 + , необходим для усиления развития В-клеток, как показано ниже в случае БЦЖ.
Ранние исследования цельноклеточной коклюшной вакцины, вводимой отдельно или в комбинации с вакцинами против дифтерии и столбняка в течение первых 24 часов жизни, продемонстрировали безопасность без каких-либо признаков эритемы, инфильтрации, лихорадки, раздражительности, рвоты или анорексии [24].Однако иммунизация против коклюша при рождении привела к серологически неадекватным ответам и притуплению бустерных ответов на коклюш у 75% испытуемых до 5-месячного возраста, что свидетельствует об антиген-специфическом «иммунологическом параличе» или толерантности, вызванной иммунизацией. Считалось, что этот сбой не зависит от каких-либо эффектов MatAb, поскольку они были незначительными или необнаруживаемыми. Напротив, иммунизация в возрасте 3 недель приводила к адекватному серологическому ответу [24].
Очищенная полисахаридная вакцина (PRP), первая вакцина, лицензированная для предотвращения болезни Hib, не была ни иммуногенной для новорожденных, ни стабильно иммуногенной для детей старше 18 месяцев [25].Напротив, текущая конъюгированная вакцина против Hib, дифтерийный белковый конъюгат CRM 197 (HbOC), вводится серией из трех инъекций, начиная с двухмесячного возраста. Либерман и др. [25] попытался усилить ответ антител на HbOC путем введения вакцины против дифтерии и столбняка (DT) при рождении, но обнаружил, что в 7 месяцев у детей, подвергшихся воздействию DT при рождении, был более низкий ответ антител, чем у иммунизированных, начиная с 2 месяцев. возраста. Нарушение ответа Т-хелперных Т-лимфоцитов у новорожденных по сравнению со взрослыми может способствовать снижению неонатального ответа на некоторые вакцины.Например, после пероральной вакцинации против полиомиелита (ОПВ) у младенцев вырабатывается относительно слабый IFN-γ и клеточно-опосредованный ответ по сравнению со взрослыми, хотя они вырабатывают высокие титры нейтрализующих антител [26], которые, как считается, необходимы для защитного иммунитета против полиовируса. [27].
Как правило, у новорожденных наблюдаются нарушенные ответы на Т-независимые полисахаридные антигены, а их антительные ответы на Т-зависимые белковые антигены непродолжительны [5]. Соответственно, 23-валентная полисахаридная вакцина Streptococcus pneumoniae (PPV23) не является иммуногенной для детей младше 2 лет [28].Хотя пневмококковая конъюгированная протеин-полисахаридная вакцина безопасна и эффективна при введении младенцам серией из четырех доз (2, 4, 6 и ≥ 12 месяцев), ее эффективность при рождении неизвестна и в настоящее время исследуется [29].
Вакцины, вводимые в настоящее время при рождении
Хотя у новорожденных обычно более слабая реакция, чем у пожилых людей, на широкий спектр вакцин, некоторые вакцины действительно обладают определенной эффективностью при введении при рождении.
Bacillus Calmette-Guérin
Вакцина Bacillus Calmette-Guérin (БЦЖ) представляет собой живую аттенуированную вакцину Mycobacterium bovis , которую вводят в течение первых нескольких дней жизни в большинстве стран для предотвращения детского туберкулезного менингита и милиарной болезни.Ее получили более 3 миллиардов человек, и это наиболее широко используемая вакцина во всем мире [30]. Обычно его не рекомендуется использовать в США из-за относительно низкой распространенности туберкулеза и различной эффективности иммунизации против туберкулеза легких у взрослых.
В целом вакцина БЦЖ демонстрирует отличный профиль безопасности. Основными побочными эффектами вакцинации являются местные реакции, включая рубцевание (до 92% здоровых новорожденных), образование пустул и дренаж [31].Обычно они поддаются консервативному менеджменту. Подмышечная и шейная лимфаденопатия являются наиболее частыми региональными побочными эффектами и могут сохраняться в течение нескольких месяцев, иногда приводя к хирургическому дренированию [32]. Распространенная инфекция БЦЖ — редкое осложнение, встречающееся менее чем у одного человека на миллион. Об этом сообщалось у детей с врожденными иммунными нарушениями, такими как тяжелый комбинированный иммунодефицит, хроническая гранулематозная болезнь и синдром приобретенного иммунодефицита.Около половины случаев диссеминированной инфекции БЦЖ у детей связаны с редкими иммунодефицитами путей IFN-γ и IL-12 [33], включая сообщение о смертельной инфекции БЦЖ у младенцев с дефицитом IFN-γ-рецепторов [34] . Относительно высокая заболеваемость оститом, остеомиелитом и диссеминированной инфекцией БЦЖ была отмечена при использовании датского штамма вакцины БЦЖ 1331, производимого Statens Serum Institut, с участием нескольких сотен детей в Финляндии в период с 2000 по 2006 год. хотя в пределах ожидаемой частоты нежелательных реакций, ожидаемых для продукта, они могут быть связаны с комбинацией факторов, включая повышенную осведомленность об использовании недавно доступной вакцины БЦЖ SSI после публикации, связанной с отменой ранее использованного продукта, относительно более высокой активности / реактогенность датского штамма 1331 и ошибки введения (неправильная доза или способ введения) [35, 36].Низкий и снижающийся уровень заболеваемости туберкулезом в Финляндии побудил изменить политику вакцинации в Финляндии от всеобщей к целевой группе риска [37].
Исследования эффективности вакцины БЦЖ дали самые разные результаты. Эффективность варьировала от 0 до 80% в исследованиях случай-контроль с использованием различных штаммов БЦЖ [32]. Эта вариабельность объясняется разным воздействием микобактерий окружающей среды среди исследуемых популяций, вариациями штаммов в препаратах БЦЖ, генетическими или пищевыми различиями и другими факторами окружающей среды, такими как воздействие солнечного света и плохое поддержание холодовой цепи [38].В метаанализе Rodrigues et al. , был отмечен защитный эффект от 75 до 86% против милиарного и менингеального туберкулеза [39]. При измерении эффективности вакцины с помощью относительного риска или отношения шансов для туберкулеза у вакцинированных детей по сравнению с невакцинированными младенцами, защитный эффект составил 0,74 по результатам четырех рандомизированных контролируемых испытаний и 0,52 по результатам девяти исследований случай-контроль [40]. В метаанализе влияния вакцинации БЦЖ на детский туберкулезный менингит и милиарный туберкулез во всем мире Bourdin Trunz et al.По оценке , введение 100,5 миллионов доз вакцины БЦЖ новорожденным в 2002 г. предотвратило ~ 30 000 случаев туберкулезного менингита и ~ 11 500 случаев милиарной болезни в течение первых пяти лет жизни [41]. Наибольшая полезная иммунизация БЦЖ была отмечена в регионах, где как риск туберкулеза, так и уровень охвата вакцинацией были самыми высокими, включая Юго-Восточную Азию, Африку к югу от Сахары и западную часть Тихого океана. Следует отметить, что эффективность введения БЦЖ новорожденным была связана с ее способностью эффективно индуцировать Th2-поляризованный иммунный ответ новорожденных [42].Следует отметить, что БЦЖ также влияет на иммунный ответ на неродственный Ag в раннем возрасте, усиливая ответы как Th2-, так и Th3-типа на другие Ag (, например, HBV и пероральные вакцины против полиомиелита), вероятно, за счет своего влияния на созревание DC [43]. При нынешних расходах в 2–3 доллара США за дозу глобальная стоимость вакцинации БЦЖ составляет примерно 206 долларов США за год здоровой жизни.
Исследования, направленные на разработку еще более эффективных вакцин против туберкулеза, продолжаются с использованием двух стратегий вакцинации.Одна из стратегий включает предварительную вакцинацию БЦЖ при рождении и введение бустерной дозы для продления иммунитета и защиты взрослого населения. Гетерологичная бустерная вакцинация также возможна с использованием одной из новых, более эффективных противотуберкулезных вакцин вместо БЦЖ [44]. Новые противотуберкулезные вакцины включают живые рекомбинантные вакцины БЦЖ, такие как rBCG30, который экспрессирует большое количество главного секреторного белка M. tuberculosis [45], модифицированная вакцина против вируса осповакцины, экспрессирующая защитный AG 85A (MVA-85A), а также адъювантные субъединичные вакцины. , такие как h2 / IC31, вводимый парентерально, и h2 / LTK63, вводимый через слизистые оболочки [46].ДНК-вакцина, содержащая белок hsp65 (см. Ниже), является многообещающим кандидатом как в качестве замены БЦЖ, так и в качестве бустерной дозы.
Вакцина против гепатита B
В связи с тем, что более 2 миллиардов человек во всем мире имеют серологические доказательства инфекции гепатита B (HBV) и субоптимальное лечение, обеспечиваемое текущей противовирусной терапией, первичная профилактика посредством иммунизации остается наиболее эффективным способом контроля распространения HBV [47] .
Безопасные и эффективные вакцины против инфекции HBV доступны с 1982 года.Доступны три класса вакцин, производимых в плазме, дрожжах или клетках млекопитающих. Вакцина, полученная путем концентрирования и очистки плазмы от носителей поверхностного антигена гепатита B (HBsAg) для получения субвирусных частиц, хотя и является высокоэффективной и безопасной, больше не используется в большинстве развитых стран из-за опасений по поводу потенциальной передачи инфекций, передающихся через кровь. Дрожжевые рекомбинантные вакцины против HBV получают путем клонирования гена HBV S в дрожжевых клетках и содержат тиомерсал в качестве консерванта.Рекомбинантная вакцина, полученная из клеток млекопитающих, помимо S-антигена, содержит либо антигены из области pre-S2, либо как области pre-S1, так и области pre-S2, которые собираются в вирусоподобную частицу и вызывают усиленный иммунологический ответ [48 ]. В 1991 г. Консультативный комитет по практике иммунизации Центров США по контролю и профилактике заболеваний (CDC) рекомендовал вакцинацию против HBV всем младенцам, независимо от HBsAg-статуса матери [49]. Вакцина против ВГВ обычно вводится тремя внутримышечными дозами в течение 6 месяцев, причем первая доза вводится при рождении.Этот график вакцинации снизил бремя ВГВ в США, защитный эффект также отмечен во многих других странах. В 2005 г. это руководство было обновлено, чтобы рекомендовать проведение всеобщей вакцинации новорожденных перед выпиской из больницы [50].
Побочные эффекты вакцины против ВГВ легкие и чаще всего включают боль в месте инъекции (3–29%), легкую лихорадку> 37,7 ° C (1–6%), недомогание, головную боль, боль в суставах и миалгию. Об этих эффектах сообщалось не чаще среди детей, получавших вакцину против ВГВ и против дифтерии / столбняка / цельноклеточного коклюша (АКДС), чем среди детей, получавших только АКДС.В литературе описаны более серьезные побочные реакции [49], но сила этих ассоциаций остается неясной. По оценкам, частота анафилаксии после вакцинации против ВГВ среди детей и подростков составляет один случай на 1,1 миллиона доз вакцины [50]. Хотя ретроспективное исследование случай-контроль показало связь с рассеянным склерозом у взрослых, а плановая вакцинация в школах была приостановлена во Франции в 1998 году, о рассеянном склерозе после иммунизации вакциной против ВГВ среди детей не сообщалось [50].Аналогичным образом, возможная связь с синдромом Гийена-Барре, который предполагалась у взрослых реципиентов вакцины против HBV из плазмы, не была подтверждена [50].
Эффективность вакцины против HBV измеряется по ее способности индуцировать поверхностные антитела против гепатита B (Hbs Ab) с титром> 10 МЕ / л. У здоровых младенцев одна доза обеспечивает ~ 30–50% защиты, две дозы — 50–75%, а три дозы -> 90% защиты от инфекции HBV, тем самым устраняя необходимость в бустерных дозах [48]. Замечательная степень защиты была продемонстрирована в 1980-х годах, хотя этот эффект не был столь значительным, как эффект, полученный при использовании вакцины в сочетании с пассивной иммунизацией с множественными инъекциями иммуноглобулина против гепатита B.По оценкам, иммунизация снижает уровень носительства у новорожденных, рожденных от HBsAg-позитивных матерей-носителей, примерно на 90% [51, 52]. Чанг и др. показали, что всеобщая вакцинация на Тайване была связана со снижением заболеваемости гепатоцеллюлярной карциномой у детей более чем на 50% [53].
Оральная вакцина против полиомиелита
Halsey et al. изучали эффективность трехвалентной пероральной полиовакцины (TOPV) и АКДС, вводимых новорожденным людям [54]. Авторы отметили, что, хотя MatAb может изменять или блокировать сывороточный иммунный ответ в течение первых нескольких недель жизни, первая или предварительная доза АКДС может быть эффективно введена к 4-недельному возрасту.TOPV, вводимый младенцам в течение первой недели жизни, приводил к кишечным инфекциям и местным иммунным ответам у 50–100% младенцев и к индукции сывороточных антител у 30–70% младенцев. К 4–8 неделям введение TOPV вызывало такой же ответ сывороточных антител, как у младенцев старшего возраста. Хотя Программа иммунизации ВОЗ рекомендовала начинать схемы АКДС и ТОПВ в возрасте 6 недель, авторы предложили рассмотреть возможность введения первой дозы ТОПВ при рождении (или как можно ближе к рождению) для стран, где полиомиелит еще не контролируется. .
Противококлюшная вакцина
Тяжесть коклюша среди младенцев и иммуногенность бесклеточного коклюша у новорожденных мышей, в отличие от толерогенности цельноклеточной коклюшной вакцины у новорожденных людей [24], побудили исследовать АП у людей. новорожденные. Knuf и соавторы [55] сравнили бесклеточную коклюшную вакцину с алюминиевым адъювантом (АР; содержащую коклюшный токсоид, нитчатый гемагглютинин и пертактин) или HBV, вводимую внутримышечно в возрасте 2–5 дней с последующим введением DTaP-HBV-IPV / Hib в 2 года. , 4 и 6 месяцев.Они [55] продемонстрировали, что вакцинация против АП у новорожденных была безопасной (без значительных различий в реактогенности между группами), вызывала более высокие ответы антител на коклюшный антиген к 3 месяцам (, т. Е. не индуцировала иммунологическую толерантность) и приводила к более ранним ответам антител на DTaP, но подавлял ответ Ab на вакцины против Hib и HBV. Авторы предполагают, что ослабление ответов на Hib и HBV было связано с сильными вторичными Т-лимфоцит-специфичными реакциями коклюша после первой дозы DTaP-IPVHBV / Hib, потенциально влияющей на помощь Т-лимфоцитов CD4 + , явление, известное как «случайный наблюдатель». вмешательство ».Учитывая, что риск смерти из-за коклюшной инфекции снижается при введении первой младенческой дозы АР в стандартный в настоящее время 2-месячный возраст [56], авторы предполагают, что доза при рождении еще больше снизит риск коклюша. смертей, связанных с текущим ранним периодом уязвимости.
Вакцины, вводимые в младенческом возрасте
Вакцины, вводимые в раннем возрасте, в младенчестве, но после неонатальной фазы, включают ротавирус, дифтерийно-столбнячный бесклеточный коклюш (DTaP; в 2, 4, 6 и 15–18 месяцев), Hib ( 2, 4, 6, 12–15 месяцев), пневмококковая конъюгированная вакцина (PCV; 2, 4, 6, 12–15 месяцев), инактивированная вакцина против полиовируса (IPV; 2, 4, 6–18 месяцев), грипп (ежегодно с От 6 месяцев до 18 лет), вакцины MMR (12 месяцев), ветряной оспы (12 месяцев) и гепатита A (12–18 месяцев) [57].Хотя полное обсуждение безопасности и эффективности всех детских вакцин выходит за рамки данного обзора, ротавирусная вакцина будет обсуждаться в качестве иллюстрации исследований безопасности и эффективности вакцинации детей раннего возраста.
Ротавирусная вакцина является самым последним дополнением к панели иммунизации в раннем возрасте и недавно была рассмотрена Еженедельным эпидемиологическим отчетом Всемирной организации здравоохранения (ВОЗ) [58], а также Деннехи [19]. Защита от ротавирусной инфекции представляет большой клинический интерес, поскольку она является основной причиной тяжелой диареи у детей младше 5 лет во всем мире, с более чем 25 миллионами амбулаторных посещений и более 2 миллионами госпитализаций в год.Лицензированные в 2006 году две живые аттенуированные пероральные ротавирусные вакцины, моновалентная ротавирусная вакцина человека Rotarix® и пятивалентная вакцина коровьего-человека RotaTeq, заменили их аналог RotaShield® , , который был снят с рынка в 1999 году из-за возможной связи с инвагинацией. Две новые вакцины имеют схожий профиль безопасности и эффективности, но разный график иммунизации: Ротарикс вводят по схеме из 2 доз в период от 6 до 12 недель (с интервалом не менее 4 недель), а RotaTeq — в виде 3 доз через 2, 4 и 6 месяцев. (первая доза между 6–12 неделями и последующие дозы с интервалами 4–10 недель, причем первая доза вводится не позднее, чем через 12 недель, а третья доза назначается в возрасте до 32 недель).Первую дозу этих вакцин не следует вводить младенцам старше 12 недель, поскольку безопасность не установлена, и это создает потенциально более высокий риск инвагинации. Согласно Глобальному консультативному комитету по безопасности вакцин и его данным по постлицензионному надзору до июня 2007 г., использование этих вакцин не было связано с повышенным риском инвагинации или других серьезных побочных эффектов [58]. Редкие осложнения включали легкие и преходящие симптомы со стороны дыхательных путей или желудочно-кишечного тракта.Вакцины противопоказаны младенцам с инвагинацией в анамнезе или анатомическими пороками развития, которые могут предрасполагать к инвагинации. Следует отметить, что ни одна из этих вакцин не содержит тиомерсал.
Обе вакцины обеспечивают 74–85% защиту от ротавирусной диареи любой степени тяжести и ~ 90–100% защиту от тяжелой ротавирусной болезни, которая распространяется на второй год наблюдения. Считается, что и доза вакцины, и факторы хозяина (, например, . MatAb, мешающие бактериальные и вирусные агенты и недостаточность питания) определяют степень иммунного ответа.Хотя оптимальные суррогатные маркеры эффективности вакцины еще предстоит четко определить, специфический IgA к кишечному вирусу коррелировал с защитой, и сывороточные IgA-ответы на поверхностные структурные белки VP4 и VP7 использовались в качестве конечных точек, хотя считается, что клеточно-опосредованный иммунитет также вносят свой вклад в анти-ротавирусную защиту [59]. Поскольку клиническая эффективность до сих пор была продемонстрирована в основном в США, Европе и Латинской Америке, ВОЗ еще не рекомендовала глобальное включение ротавирусных вакцин в национальные программы иммунизации до тех пор, пока их потенциал не будет подтвержден во всех регионах мира.
Клинические исследования новых вакцин для раннего возраста
Малярия — это ведущая глобальная проблема здравоохранения, против которой эффективная вакцина еще не внедрена в клиническую практику. Кандидатская вакцина против малярии RTS, S / AS02D оказалась безопасной, хорошо переносимой и иммуногенной для детей в возрасте до 18 недель, проживающих в высокоэндемичных районах Мозамбика [60]. Это гибридный рекомбинантный белок, состоящий из тандемных повторов из белка Plasmodium falciparum и S-антигена HBV, созданный с адъювантной системой AS02 (смесь монофосфориллипида A агониста Toll-подобного рецептора (TLR) (активная часть липополисахарида / эндотоксина) и детергент сапонин QS21) [60, 61].Также разрабатываются вакцины-кандидаты от ВИЧ, способные вызывать устойчивые иммунологические реакции у грудных детей [62]. Другие новые вакцины для раннего возраста, которые в настоящее время изучаются, включают вакцины против Salmonella typhi , RSV, гриппа и парагриппа. Дополнительные исследования оценивают совместное введение вакцины против гепатита В при рождении в сочетании с вакциной против гепатита А или БЦЖ, что может изменить реакцию на другие вакцины [43].
Потребность в новых подходах к вакцинации новорожденных
Способность некоторых вакцин, таких как вакцина БЦЖ и ВГВ, проявлять некоторую эффективность при рождении, подтверждает концепцию того, что, несмотря на общее нарушение функции APC и ответов Th2, вакцинация новорожденных возможна.Медицинские преимущества, присущие неонатальным вакцинам, эффективным при рождении, включают: i) раннюю защиту, которая закроет окно уязвимости, присущее схемам вакцинации, которые начинаются в более позднем возрасте (, например, 2 месяца), ii) практичность рождения является глобальной точкой. контакта с системами здравоохранения, и ii) потенциальные преимущества новых вакцин, которые могут потребовать меньших доз для достижения эффективности. В этом контексте мы рассматриваем недавние подходы к разработке моделей неонатальных животных и недавнюю работу in vitro с человеческими неонатальными клетками.
Животные модели вакцинации новорожденных
Применимость моделей вакцинации новорожденных животных к людям
При оценке значимости исследований на животных для человека важно признать, что виды млекопитающих различаются по типу плаценты и относительному переносу плаценты и молозива. иммуноглобулины (Ig) плоду / новорожденному [63]. Например, у свиней, лошадей и жвачных животных имеется эпителиохориальная или синдесмохориальная плацентация и отсутствует плацентарный перенос Ig, что очень сильно зависит от переноса молозива [64].Напротив, у грызунов и приматов имеется гемендотелиальная и гемохориальная плацентация, соответственно, и оба в значительной степени зависят от плацентарного переноса с меньшим переносом молозива. В целом виды, которые допускают ранний (плацентарный) перенос материнского Ig (, например, мыши и люди), демонстрируют более медленную скорость иммунного созревания. Интересно, что для развития репертуара В-клеток и антител у кроликов необходимы лимфоидные ткани, ассоциированные с кишечником [65].
Еще один аспект, который следует учитывать при интерпретации моделей на животных, — это относительно высокая дивергенция врожденной иммунной системы.Например, врожденная иммунная система мышей особенно отличается от иммунной системы человека [66]. Таким образом, хотя мышиные модели абсолютно необходимы для иммунологических исследований и дают убедительные данные, результаты на мышах не всегда передаются напрямую людям.
Наконец, время введения вакцины также является важным и временами спорным аспектом моделей вакцинации новорожденных животных. В частности, многочисленные исследования были сосредоточены на мышах в возрасте 1 недели для моделирования неонатальных реакций [2].Однако, учитывая важность разработки вакцин, активных в первый день жизни, и растущие доказательства того, что особая перинатальная физиология при рождении, включая высокий уровень иммуносупрессивного аденозина при рождении [67], будет также важна для изучения вакцинации животных в первый день жизни.
Безопасность и эффективность вакцинации новорожденных на моделях животных
Многочисленные исследования документально подтвердили, что некоторые вакцины, очевидно, безопасны и эффективны при введении in utero или новорожденным животным.Хотя серьезные побочные эффекты, связанные с вакцинацией новорожденных животных, как правило, редки, пассивное наблюдение в Великобритании за вакцинацией собак продемонстрировало относительно высокую распространенность побочных эффектов, связанных с вакцинацией, у очень молодых животных [68]. Наиболее частыми побочными эффектами являются отек лица и зуд, которые, как полагают, связаны с реакцией гиперчувствительности немедленного типа (тип I), вызванной дегрануляцией тучных клеток, сенсибилизированных материнским IgE. Эти потенциальные побочные эффекты могут быть вторичными по отношению к высокому содержанию бычьего сывороточного альбумина в собачьих вакцинах и наиболее распространены у собак мелких пород, что позволяет предположить, что снижение дозы может быть целесообразным.Вакцины с квасцами или липидным адъювантом вызывают более сильное воспаление тканей, чем вакцины без адъюванта, после подкожного введения у котят в возрасте 14–16 недель [69].
Примеры эффективности вакцинации новорожденных на животных моделях включают исследования на птицах вакцины против живого вируса герпеса индеек (HVT), направленные на предотвращение неопластической болезни Марека у цыплят от α-герпесвируса, демонстрируют защиту даже при введении in ovo или в первый день [70]. Щенки бигля были вакцинированы подкожно модифицированным живым парвовирусом собак в возрасте 1 дня [63].И кинетика, и величина ответа Ab были аналогичны таковым у более старых щенков. В этой модели вакцинация после приема молозива или щенков выздоравливающих самок с высокими титрами против собачьего парвовируса оказалась безуспешной, что свидетельствует о потенциальной ингибирующей роли материнских антител. Однако при определенных обстоятельствах препятствие, связанное с материнским Ab, может быть преодолено. Щенки, рожденные от самок, бустированных во время беременности убитой адъювантной вакциной против бешенства и получившие колостральный иммунитет, тем не менее, проявили защитный ответ Ab после иммунизации вакциной RABISIN, состоящей из гликопротеинов вируса бешенства и адъюванта гидроксида алюминия [63].Авторы предполагают, что большее количество антигенов и / или свойства вектора могут позволить более эффективную презентацию Ag. Таким образом, при определенных условиях новорожденные мыши и люди могут вызывать эффективные адаптивные иммунные ответы . Хотя эти исследования не определяют механизмы, с помощью которых исследуемая вакцина преодолевает нарушения иммунитета новорожденных, они все же иллюстрируют возможность эффективной вакцинации при рождении.
Новые подходы к повышению эффективности неонатальных вакцин
В настоящее время исследуется множество новых подходов, направленных на преодоление недостатков неонатального иммунного ответа и, таким образом, на обеспечение эффективной вакцинации новорожденных [5].Ниже мы приводим примеры таких подходов, выбирая недавние примеры из опубликованной литературы.
Внутрицитоплазматическая доставка антигенов
Несколько исследований на мышах предполагают, что ключевым требованием для индукции эффективного неонатального адаптивного ответа является проникновение Ag в цитоплазму APC. Чен с соавторами изучали взрослых и новорожденных (в возрасте 1 недели) мышей BALB / c, иммунизированных внутрибрюшинно. вакциной против гриппа с инактивированным продуктом расщепления с последующей бустерной дозой через 3 недели или внутримышечной инъекцией и in vivo электропорацией плазмидной ДНК [71].Вакцинация новорожденных гемагглютинином или нейраминидазной ДНК защищала мышей от инфекции гриппа в присутствии MatAb. Авторы пришли к выводу, что для преодоления потенциального ингибирования адаптивных иммунных ответов с помощью MatAb матери и их потомство следует иммунизировать различными вакцинами против гриппа, нацеленными на разные Ag (, например, инактивированная вакцина против ДНК-вакцины; или использовать ДНК-вакцины, нацеленные на разные продукты от гриппа). Если использовать тот же самый Ag, исследование Pertmer предполагает, что материнские антитела не притупляют основанные на ДНК-вакцинах ответы на внутриклеточно экспрессируемый Ag [72].
Исследование неонатальных мышей C57BL / 6 и BALB / c, иммунизированных (внутрибрюшинно и подкожно) в течение 24 часов после рождения отключенным инфекционным вариантом HSV-1 с одним циклом, показывает, что один цикл репликации вируса резко усиливает защитные реакции [73]. CD4 + и CD8 + Т-клетки от неонатально вакцинированных мышей, переданных наивным реципиентам, обеспечивали защиту от летального вирусного заражения. УФ-инактивированные вирусные частицы в дозах, превышающих до 10 4 раз, не смогли достичь этого ответа, что позволяет предположить, что доставка Ag в цитоплазму может усиливать иммунные ответы новорожденных.
Коллман и его сотрудники продемонстрировали новый подход к вакцинации новорожденных, в котором используется ослабленный штамм внутриклеточной патогенной бактерии Listeria monocytogenes для доставки Ag в цитоплазму APC [74]. Важно отметить, что этот подход оказался безопасным для новорожденных мышей, поскольку они пережили заражение высокой дозой штамма ΔactA L. monocytogenes без каких-либо признаков заболевания или каких-либо восстанавливаемых бактерий в селезенке или печени через 7 дней после вакцинации.Новорожденных мышей однократно вакцинировали аттенуированным штаммом L. monocytogenes ΔactA, вызывающим сильные Т-клеточные ответы CD8 + и CD4 + , и они были защищены от последующего заражения L. monocytogenes дикого типа . Более того, ΔactA служил в качестве эффективного носителя для доставки гетерологичного Ag, что приводило к сильному ответу памяти типа CD8 и CD4 Th2, что позволяет предположить, что этот штамм может служить эффективным носителем вакцины для иммунизации новорожденных.Следует отметить, что рекомбинантные аттенуированные штаммы L. monocytogenes индуцируют специфический иммунитет даже при наличии ранее существовавшего иммунитета, потенциально преодолевая препятствие ранее существовавшего материнского иммунитета, которое может препятствовать ответам на вакцины новорожденных [75].
ДНК-вакцины
Пелизон и его сотрудники вакцинировали 5-дневных новорожденных мышей BALB / c внутримышечно плазмидой на основе интрона цитомегаловируса, содержащей встроенный фрагмент, кодирующий белок теплового шока 65 (hsp65) Mycobacterium leprae [76 ].pVAXhsp65 транскрибировался через 2-7 дней в мышечной ткани новорожденных мышей. Через 15 дней после последней дозы из 3 серий (в возрасте 5, 12 и 19 дней) повышенная ConA-индуцированная выработка селезенкой Th3-поляризующих цитокинов (IL-4 и IL-5) и несогласованное увеличение уровня анти-hsp65 IgG1 и уровни IgG2a в сыворотке были отмечены. pVAXhsp65 оказался безопасным, поскольку анализ саузерн-блоттинга не выявил доказательств интеграции в ряде органов, включая селезенку, печень, тимус и регионарные лимфатические узлы.Более того, как и БЦЖ, pVAXhsp65 при введении в виде однократной дозы был способен вызвать у мышей 5-дневного возраста смешанный иммунный ответ Th2 и Th3 на усиление pVAXhsp65 позже, во взрослом возрасте.
Вакцины на основе ДНК также показали себя многообещающими в усилиях по защите новорожденных от малярии. Новорожденных мышей BALB / c (7d) иммунизировали ДНК-вакциной Plasmodium yoelii циркумспорозоитного белка (PyCSP), смешанной с плазмидой, экспрессирующей фактор, стимулирующий макрофаги-колонии мышиных гранулоцитов, затем бустировали через 28 дней вирусом оспы, экспрессирующим PyCSP [77].Было отмечено, что иммунизированные новорожденные, в том числе рожденные от иммунных матерей, обладают CD8 + Т-клеточной защитой, как и взрослые.
ДНК-вакцина вируса кори (MV), состоящая из генов H, F и N кори, вводилась через внутрикожным путем с адъювантом IL-2 новорожденным макакам резус (4–5 дней), которые получали пассивную иммунизацию с помощью иммуноглобулин кори (для имитации присутствия MatAb) [78]. Всем макакам была проведена повторная вакцинация по той же схеме через 2 месяца после вакцинации.Несмотря на то, что она не усиливала MV-индуцированные ответы Ab, ДНК-вакцина MV вырабатывала MV-специфические Т-клеточные ответы, измеренные по индуцированной MV продукции IFN-γ с помощью PBMC. Более того, вакцина MV защищала новорожденных макак-резус от последующей сыпи, вызванной контрольным заражением MV, и иммуносупрессии. В целом иммунизация на основе ДНК представляет собой жизнеспособный вариант разработки новых неонатальных вакцин.
Интраназальное введение живых аттенуированных вакцин
Доставляемые через слизистые оболочки живые аттенуированные векторные вакцины Salmonella enterica были изучены в качестве платформы для доставки фрагмента C модельного антигена столбнячного токсина новорожденным мышам, иммунизированным интраназальным путем на 7 и 22 дни жизни [79].Живые векторы Salmonella колонизировались и сохранялись преимущественно в носовой ткани и индуцировали высокие (взрослые уровни) титры Frag C-специфических антител, слизистых и системных IgA- и IgG-секретирующих клеток, пролиферативные ответы Т-клеток и секрецию IFN-γ. Через неделю после бустера был установлен долговременный смешанный ответ Th2- и Th3-типа на Frag C. Такие эффекты были очевидны даже в присутствии высоких уровней материнских антител.
Mielcarek и его сотрудники разработали живой ослабленный штамм Bordetella pertussis , возбудителя коклюша [80].Штамм BPZE1, ослабленный делецией генов, кодирующих трахейный цитотоксин, токсин коклюша и дермонекротический токсин, вводили младенцам (3-недельного возраста) и взрослым мышам Balb / C в виде однократной интраназальной дозы. Эта ослабленная интраназальная вакцина вызвала более сильные неонатальные ответы против Bordetella IgG, чем бесклеточная коклюшная вакцина, демонстрируя стерилизующий иммунитет к последующей интраназальной провокации B. pertussis и B. parapertussis . BPZE1 индуцировал пониженный Th3-поляризованный ответ, что измерялось по соотношению анти-нитчатого гемагглютинина IgG1 / IgG21.Авторы предполагают, что BPZE1 может также представлять платформу для доставки гетерологичных антигенов. Это исследование было сосредоточено на модели мышей в возрасте 3 недель, и не было предоставлено никаких данных о потенциальной эффективности этого ослабленного штамма у новорожденных мышей. Однако другое исследование интраназального введения живых B. bronchispetica двухдневным новорожденным поросятам продемонстрировало эффективность против последующего заражения атрофическим ринитом [81], предполагая, что живые ослабленные штаммы Bordetella могут вызывать эффективный иммунитет у новорожденных при интраназальном введении.
Недавние исследования изучали интраназальное введение E. coli -экспрессируемого белка VP6 ротавируса и адъюванта E. coli лабильный токсин (LT-R192G) новорожденным (7 дней) и взрослым мышам, а также защиту от фекального ротавируса. выделение после заражения штаммом мышиного ротавируса EDIM [82]. В отличие от взрослых мышей, у которых развились как Т-клеточные ответы CD8 + (индуцируемые ротавирусом, сплееноциты, продуцирующие Th2-цитокины), так и антитела в течение 10 дней, новорожденные мыши не проявляли защиты до 28 дней, после чего они обладали ротавирусом памяти. специфические Т-клетки, но не продуцируют антитела против ротавируса.Эти исследования подчеркивают потенциал интраназальной иммунизации новорожденных живыми вакцинами.
Новые адъюванты
Нарушенная реакция неонатальных APC на многие стимулы является ключевым препятствием, которое необходимо преодолеть при разработке эффективных неонатальных вакцин [83]. Одним из подходов к преодолению дефицита APC у новорожденных является экзогенное введение костимулирующих сигналов, эндогенная продукция которых недостаточна, таких как неонатальное нарушение продукции IL-12 [84]. Совместное введение ИЛ-12 и субъединичной вакцины против гриппа в течение 24 часов после рождения повышает экспрессию в селезенке мРНК ИФН-γ, ИЛ-10 и ИЛ-15 и повышает защитную эффективность противовирусной вакцинации [85].Кроме того, совместное введение IL-12 также увеличивало уровни IFN-γ-, IL-2- и IL-4-секретирующих клеток и антител IgG2a, а также увеличивало выживаемость B-клеточно-зависимым образом после летального заражения взрослых инфекционным гриппом. вирус.
Открытие новых путей врожденного иммунитета и агонистов, которые их задействуют, открыло дверь для оценки новой вакцины Aj. Активация TLR, трансмембранных белков, которые опосредуют распознавание микробных продуктов, активирует APC, включая усиление созревания DC.Следовательно, агонисты TLR представляют собой потенциальную вакцину Aj, некоторые из которых (, например, липид A, который передает сигнал через TLR4) в настоящее время используются в клинической практике [86, 87]. Синтетическая дцРНК полирибоинозиновая: полирибоцитидиловая кислота является агонистом TLR3, который индуцирует продукцию IFN типа I / II и усиливает первичный иммунный ответ против столбнячного анатоксина (TT) у новорожденных мышей, увеличивая выработку анти-TT изотипов IgG1, IgG2a и IgG2b [88] . Усиление вторичного ответа анти-TT IgG было отмечено, когда полирибоинозиновая: полирибоцитидиловая кислота была объединена с ретиноевой кислотой / витамином А, комбинированным иммунологическим / нутритивным вмешательством, которое представляло собой эффективную вакцину Aj у новорожденных мышей.CpG-олигонуклеотиды, которые активируют TLR9, также, как было показано, усиливают неонатальные Th2-ответы на неонатальных мышиных моделях [89], хотя они, по-видимому, вызывают относительно слабые ответы в плазматических DC плазмацитоидов новорожденных пуповинной крови человека, испытанном in vitro [90].
Что касается in vitro исследований человеческих неонатальных APC, агонисты TLR8, включая некоторые синтетические имидазохинолины и одноцепочечную вирусную РНК, особенно эффективны при активации неонатального APC человека in vitro , что коррелирует с сильной активацией киназы p38 MAP. сигнальные пути NF-ΚB [91, 92].Агонисты TLR8 (и TLR7 / 8) были значительно более эффективны в индукции продукции TNF и IL-12 p40 / 70, а также в повышении регуляции костимулирующей молекулы CD40. В дополнение к их способности эффективно активировать APC, агонисты TLR8 также могут способствовать усилению неонатальных адаптивных иммунных ответов за счет своей способности обращать вспять ингибирующие эффекты регуляторных Т-клеток, которые подавляют адаптивные иммунные ответы [93], и которые особенно эффективны и многочисленны при рождение [6, 7]. Важно отметить, что агонист TLR7 / 8 R-848 является эффективной вакциной Aj, когда он ковалентно связан с белком Gag ВИЧ в модели макака-резус in vivo [94], что позволяет предположить, что эти многообещающие Aj заслуживают дальнейшего исследования, включая оценку на моделях неонатальных животных, где временное и селективное локальное усиление APC и Th2-функции, включая обращение функции Treg, может безопасно и эффективно усиливать местные адаптивные иммунные ответы новорожденных на вакцины без воздействия на общую центральную и периферическую толерантность [13], а также на системный перекос ответов против Th2 [2, 3].Таким образом, существуют теоретические основания, которые вкупе с появляющимися доказательствами очевидной безопасности этого подхода у взрослых нечеловеческих приматов (макак-резус) in vivo [94, 95] и эффективности этих агонистов в отношении неонатального APC человека in vitro. [91] предполагают, что такой подход может быть как безопасным, так и эффективным [92]. Тем не менее, как и при разработке всех новых лекарств, все новые вакцины для новорожденных должны пройти тщательную оценку безопасности, чтобы гарантировать, что дозы и пути введения избегают любых вредных побочных эффектов, включая потенциально чрезмерно чрезмерные воспалительные реакции / реактогенность [96] или риск аутоиммунитета [14].
Заключительные замечания
Во всем мире инфекционные заболевания вызывают смерть более 2 миллионов новорожденных и младенцев в возрасте до 6 месяцев. Значительное сокращение этого бремени потребует разработки вакцинации в раннем возрасте, включая вакцины, эффективные при рождении, которые являются наиболее надежной точкой глобального контакта в области здравоохранения. Основываясь на исследованиях на животных и людях, вакцинация новорожденных возможна, но требует сильных иммунных сигналов, таких как сигналы, обеспечиваемые in vivo репликацией ослабленных агентов и, возможно, некоторыми адъювантами.Достижения в управлении аттенуированными штаммами микробов и недавняя характеристика путей распознавания врожденного иммунитета предоставляют возможности для разработки новых систем доставки и / или адъювантов для решения этой важной задачи. Соображения безопасности будут иметь первостепенное значение, но большое бремя инфекций в раннем возрасте в сочетании с практичностью иммунизации при рождении дает сильную мотивацию для применения эффективных неонатальных вакцин.
Вакцина против COVID-19, безопасная для мамы и ребенка, новое исследование предлагает: прививки
Новое исследование показало, что вакцины COVID-19 производят эффективные уровни антител у беременных и кормящих женщин.Они могут принести пользу и младенцам.
Джейми Гриль / Getty Images
скрыть подпись
переключить подпись
Джейми Гриль / Getty Images
Новое исследование показало, что вакцины против COVID-19 производят эффективные уровни антител у беременных и кормящих женщин.Они могут принести пользу и младенцам.
Джейми Гриль / Getty Images
С начала пандемии беременные люди оказались перед трудным выбором: вакцинировать или не вакцинировать.
Риск тяжелого заболевания или даже смерти от COVID-19 — хотя и небольшой — во время беременности выше. В США зарегистрировано более 82000 случаев заражения коронавирусом среди беременных и 90 случаев материнской смерти от этого заболевания.С. по состоянию на последний месяц.
Но очень мало данных о том, являются ли вакцины COVID-19 безопасными и эффективными во время беременности, потому что люди, которые беременны или кормят грудью, не были включены в первоначальные клинические испытания. (Недавно компания Pfizer начала новое исследование с участием 4000 беременных женщин.)
Теперь исследователи начинают давать некоторые ответы. Исследование, опубликованное недавно в Американском журнале акушерства и гинекологии, показывает, что вакцины не только безопасны и эффективны для беременных и кормящих женщин, они также могут обеспечить некоторую защиту их младенцев.
«Это очень важное исследование», — говорит доктор Джудет Луи, акушер, до недавнего времени занимавшая пост президента Общества медицины материнского плода. «Люди пытались собрать как можно больше информации, и это исследование говорит:« Хорошо, есть выгода ».
Хотя и ограниченное — с размером выборки 131 — исследование является крупнейшим на сегодняшний день по данной теме. Ведущий автор доктор Кэтрин Грей, специалист по медицине материнского плода в Бригаме и женской больнице в Бостоне, говорит, что люди очень хотели принять участие.
«Люди просто добровольно предлагали нам любой образец, который они могли бы попытаться помочь сгенерировать данные», — говорит Грей.
131 участник был вакцинирован вакциной Pfizer или Moderna; 84 были беременны, 31 кормили грудью и 16 были небеременными женщинами в возрасте от 18 до 45 лет. В исследовании участвовали пациенты и исследователи из больницы Бригама и женщин, Массачусетской больницы общего профиля и Института Рагона.
Образцы крови были собраны во время первой и второй дозы вакцины и снова через шесть недель.
«Уровни антител, которые мы ищем в ответ на вакцинацию, были одинаковыми между группами», — говорит Грей.
И когда исследователи сравнили уровни антител с уровнями антител у женщин, которые были больны COVID-19 во время беременности, уровни антител в ответ на вакцину были выше.
Это открытие «предполагает, что даже если у вас была инфекция COVID, вакцинация приведет к более устойчивому ответу антител», — говорит Грей.
Побочные эффекты от вакцинации были легкими и аналогичными побочным эффектам небеременных людей, включая болезненность в месте инъекции после первой дозы и некоторые мышечные боли, головную боль, лихорадку и озноб после второй дозы, — говорит Грей.
Но, пожалуй, самое захватывающее открытие: антитела также были обнаружены в пуповинной крови и грудном молоке.
«Если эти антитела вырабатываются во время беременности и во время грудного вскармливания, ребенок явно получает их часть», — говорит д-р.Лаура Райли, акушер-гинеколог в Пресвитерианской больнице Нью-Йорка, заведующая отделением акушерства и гинекологии в Weill Cornell Medicine.
Райли сравнивает процесс с вакциной против гриппа: при введении во время беременности вырабатываются антитела, которые проникают через плаценту и «защищают ребенка в течение первых нескольких месяцев жизни», — говорит она.
Есть надежда, что вакцина COVID будет аналогичной, хотя Райли предупреждает, что пока не ясно, защитит ли она ребенка от болезни и как долго эта защита продлится.«Но, конечно, приятно видеть, что есть защита», — говорит она.
NewYork-Presbyterian также начала исследование эффективности вакцины во время беременности, говорит Райли, которая также является членом рабочей группы экспертов по COVID-19 Американского колледжа акушеров и гинекологов. Среди вопросов, которые у нее есть, — есть ли оптимальный триместр для вакцинации COVID, чтобы максимизировать ее преимущества.
По мере того, как вакцина Johnson & Johnson становится все более доступной, ее необходимо включить в будущие исследования.
Итак, хотя текущие результаты очень обнадеживают, Райли говорит, что необходимы дополнительные исследования.
Что касается людей, которые пытаются решить, делать ли им прививку прямо сейчас, доктор Джудет Луи советует своим пациентам взвесить преимущества и риски.
«Мы не видели никаких проблем с безопасностью вакцины, но мы определенно видим худшие результаты, если вы заразитесь COVID», — говорит Луис, который также является заведующим кафедрой акушерства и гинекологии в Университете Южной Флориды.
«Если вы беременны, у вас больше шансов попасть в отделение интенсивной терапии, у вас больше шансов попасть на искусственную вентиляцию легких.И немного больше похоже на смерть », — говорит Луи.
Сравните это с вакциной:« Это не просто защищает вас от серьезного заражения COVID и попадания в больницу. Кажется, он передает некоторые антитела вашему ребенку ».
Луи и другие акушеры поощряют своих беременных пациенток принять участие в программе CDC V-safe, которая пытается собрать как можно больше данных, чтобы помочь другим принимать осознанные решения. о вакцинации против COVID-19.
Своевременность вакцинации и связанные с ней факторы среди недоношенных детей в специализированной больнице в Уганде
Аннотация
Фон
Недоношенные дети подвержены повышенному риску инфекций, включая болезни, которые можно предотвратить с помощью вакцин.Поэтому своевременная вакцинация имеет решающее значение для обеспечения адекватной защиты от болезней. Информация о том, вакцинируются ли недоношенные дети в соответствии с рекомендациями по хронологическому возрасту, ограничена в странах с низким уровнем доходов.
Цели
Мы оценили своевременность вакцинации и сопутствующие факторы среди недоношенных детей в больнице Мулаго, Уганда.
Методы
Мы провели исследование с использованием смешанных методов в период с июля 2016 г. по апрель 2017 г. Сроки вакцинации недоношенных детей в возрасте 6–24 месяцев были получены из детских медицинских карт.Дополнительные данные были собраны с помощью анкеты. Было проведено пять интервью с ключевыми информаторами с медицинскими работниками и два обсуждения в фокус-группах с лицами, осуществляющими уход. Регрессионный анализ Кокса использовался для определения факторов, связанных со своевременностью вакцинации. Качественные данные были расшифрованы и проанализированы вручную с использованием тематического подхода.
Результаты
Мы включили 350 недоношенных детей со средним возрастом 8,4 месяца (IQR 6,8–10,8). Менее половины, 149/350 (42,6%) младенцев получили все вакцины в рекомендованный временной интервал.Своевременная вакцинация была наиболее высокой для БЦЖ (92%) и наименьшей — для ОПВ (45,4%). Несвоевременная вакцинация была наиболее высокой для вакцин, введенных через 6 недель (АКДС 1, ПКВ 1 и ОПВ 1), по сравнению с другими вакцинами из календаря РПИ. Роды из домашних или частных клиник и дефицит вакцин в значительной степени были связаны с несвоевременной вакцинацией БЦЖ и ОПВ 0. Низкий уровень образования матери и очень недоношенная беременность были связаны с несвоевременным получением АКДС 1 и АКДС 3. Поступление и длительное пребывание в неонатальном отделении были связаны с несвоевременным получением АКДС-1, в то время как крайне низкая масса тела при рождении была связана с несвоевременной вакцинацией АКДС-3.Рост паритета был связан с несвоевременной вакцинацией против кори. Качественные результаты показали, что отсутствие знаний и плохое отношение медицинских работников и лиц, обеспечивающих уход, пробелы в документации о вакцинационном статусе и неадекватное общение со стороны медицинских работников препятствовали своевременной вакцинации.
Заключение
Более половины недоношенных детей, обратившихся в специализированную клинику при Национальной специализированной больнице Мулаго в Уганде, не получили вакцины в рекомендованный период времени.Необходимы особые стратегии для улучшения своевременности вакцинации недоношенных детей, особенно среди детей с крайне низкой массой тела при рождении, очень недоношенных и детей с длительной госпитализацией.
Образец цитирования: Накатудде И., Ружумба Дж., Намиро Ф., Сэм А., Мугалу Дж., Мусоке П. (2019) Своевременность вакцинации и связанные с ней факторы среди недоношенных детей в специализированной больнице в Уганде. PLoS ONE 14 (9):
e0221902.
https://doi.org/10.1371/journal.pone.0221902
Редактор: Итало Франческо Анджелило, Университет Кампании, ИТАЛИЯ
Поступила: 30 апреля 2019 г .; Дата принятия: 16 августа 2019 г .; Опубликовано: 6 сентября 2019 г.
Авторские права: © 2019 Nakatudde et al.Это статья в открытом доступе, распространяемая в соответствии с условиями лицензии Creative Commons Attribution License, которая разрешает неограниченное использование, распространение и воспроизведение на любом носителе при условии указания автора и источника.
Доступность данных: Все соответствующие данные находятся в документе и его файлах с вспомогательной информацией.
Финансирование: Авторы не получали специального финансирования на эту работу.
Конкурирующие интересы: Авторы заявили, что никаких конкурирующих интересов не существует.
Введение
Вакцинация — одно из наиболее эффективных с точки зрения затрат мероприятий по обеспечению выживания детей во всем мире, позволяющее ежегодно предотвращать от двух до трех миллионов детских смертей от болезней, предупреждаемых с помощью вакцинации (УИ) [1]. Однако, несмотря на высокий глобальный охват вакцинацией, составляющий 85%, некоторые дети, особенно в развивающихся странах, по-прежнему сталкиваются с задержками в получении плановой вакцинации, что увеличивает их риск заражения УИ [2]. Своевременная вакцинация еще более важна для недоношенных детей из-за незрелой иммунной системы, которая увеличивает их восприимчивость к инфекциям.Ежегодно во всем мире преждевременно рождается около 13 миллионов детей со сроком беременности менее 37 полных недель. Примерно 60% преждевременных родов происходит в Юго-Восточной Азии и странах Африки к югу от Сахары [3, 4]. В Уганде ежегодно происходит примерно 200 000 преждевременных родов [3, 5]. Учитывая повышенный риск инфицирования недоношенных детей, они требуют ранней и адекватной защиты от болезней. Невозможно переоценить роль иммунизации матери во время беременности в снижении бремени таких болезней, как столбняк, грипп и коклюш, среди новорожденных [6–9].Однако только иммунизация матери может не обеспечить адекватной защиты от УИ у недоношенных детей, учитывая, что наибольшая доля материнских антител (IgG) передается в течение последнего триместра [8]. Таким образом, недоношенные дети, у которых уже есть незрелая иммунная система, могут испытывать УИ с повышенной частотой и тяжестью в младенчестве, если вакцины не вводятся вовремя [10, 11]. Например, зарегистрированные случаи пневмококковых заболеваний, госпитализации и осложнений, связанных с коклюшем и коклюшем, в развитых странах более распространены и тяжелы у детей с низкой массой тела при рождении и недоношенных детей [10, 12, 13].Более того, пассивно приобретенные материнские антитела ослабевают до неопределяемого уровня уже к 4 месяцам жизни [8]. Следовательно, для увеличения окна защиты от УИ, особенно в первый год жизни, требуется своевременное и полное вакцинация недоношенных детей. В настоящее время Всемирная организация здравоохранения (ВОЗ) рекомендует вакцинировать недоношенных детей в соответствии с хронологическим возрастом, как и других младенцев, без поправки на гестационный возраст или массу тела при рождении. Единственным исключением из этого правила является вакцинация против гепатита В младенцев с массой тела менее 2000 г из-за документально подтвержденного снижения иммунного ответа [14, 15].Несмотря на доказательства того, что вакцины безопасны и вызывают адекватный иммунный ответ у недоношенных детей [10, 11, 15], несколько исследований в развитых странах показали, что иммунизация недоношенных детей происходит со значительной задержкой, а иногда вакцинация может быть неполной, особенно для детей с низким уровнем вес при рождении (<2,500 г) [13, 16–19]. Задержка с вакцинацией недоношенных детей может быть отражением нерешительности в отношении вакцинации. По данным ВОЗ, нерешительность в отношении вакцинации, определяемая как «нежелание или отказ от вакцинации, несмотря на наличие вакцин», входит в десятку угроз глобальному здоровью в 2019 г. [20, 21].Причины, по которым люди предпочитают не вакцинировать своих детей, остаются сложными, но некоторые факторы были задокументированы как в развитых, так и в развивающихся странах [20, 22–25]. Систематический обзор нерешительности в отношении вакцинации в странах с низким и средним уровнем доходов документально подтвердил обеспокоенность по поводу страха перед вредными событиями после иммунизации и недоверия к программам вакцинации как наиболее распространенных факторов, влияющих на вакцинационное поведение [22]. Кроме того, исследования показали, что нерешительность в отношении вакцинации значительно увеличивает вероятность несвоевременной вакцинации [23, 24, 26].
Уганда внедрила Расширенную программу иммунизации (РПИ) в 1983 году, в задачу которой входит обеспечение полной вакцинации каждого ребенка высококачественными вакцинами против туберкулеза, полиомиелита, дифтерии, коклюша, столбняка и кори [27]. С тех пор другие вакцины, включая вакцину против гепатита B (2002), Haemophilus influenza type b (Hib) (2002), пневмококковая конъюгированная вакцина (PCV) (2013), инактивированная полиовакцина (IPV) (2016) и, совсем недавно, ротавирусная вакцина. (2018) также были представлены.Профилактические услуги по охране здоровья детей, такие как плановая иммунизация, доступны как в частном, так и в государственном секторе здравоохранения Уганды [28]. Большинство людей в стране получают доступ к этим услугам через сектор общественного здравоохранения [28]. Услуги общественного здравоохранения предоставляются посредством базового минимального национального пакета медицинских услуг (ЮНМХПН) на всех уровнях децентрализованной системы здравоохранения Уганды [28, 29]. Услуги иммунизации доступны бесплатно во всех медицинских центрах (HC) IIS, III, IV (подрайоны здравоохранения), больницах общего профиля, региональных больницах и национальных больницах, за исключением HC 1 (деревенские медицинские бригады) [28 ].Несмотря на неуклонное улучшение охвата вакцинацией Уганды с 64% (2006 г.) до 85% (2017 г.) [30], вспышки УИ, таких как корь, продолжают расти [31], что отчасти может быть отражением неполной и несвоевременной вакцинации. Текущий охват вакцинацией третьей дозой АКДС3 в Уганде оценивается в 85% [30]. Однако информация об охвате вакцинацией недоношенных детей недоступна, поскольку данные по иммунизации агрегированы как для доношенных, так и для недоношенных детей. Более того, хотя в развитых странах было проведено несколько исследований вакцинации недоношенных детей [16, 18, 32], исследования в развивающихся странах ограничены.Насколько нам известно, опубликованной информации о вакцинации недоношенных детей в Уганде нет. Таким образом, в этом исследовании оценивалась своевременность вакцинации и связанные с ней факторы среди недоношенных детей в больнице Мулаго, Уганда.
Методы
Рабочий кабинет
Исследование проводилось в клинике для преждевременных родов больницы Мулаго с июля 2016 года по апрель 2017 года. Госпиталь Мулаго является одной из двух национальных больниц направления в Уганде и учебной больницей Колледжа медицинских наук Университета Макерере.Больница обеспечивает специализированный последующий уход за недоношенными новорожденными после выписки из отделения для новорожденных (SCBU), неонатального отделения уровня III больницы, через амбулаторную клинику для недоношенных детей. В среднем 1500 младенцев, выписываемых из отделения неотложной помощи, ежегодно посещают клинику для недоношенных детей и около 30 младенцев посещают клинику ежедневно. Клиника проводится два раза в неделю, по понедельникам и четвергам, а младенцы осматриваются каждые 1-3 месяца до двухлетнего возраста. Клиникой руководят педиатр, медсестра и педиатр-резидент.Во время последующих посещений оценивается состояние питания, рост и развитие, прививочный статус и нервное развитие, а лица, осуществляющие уход, получают рекомендации по уходу за недоношенным ребенком. В течение периода исследования EPI предоставлял следующие вакцины; БЦЖ (Bacille de Calmette-Guérin), четыре дозы пероральной полиомиелитной вакцины (ОПВ), три дозы пентавалентной вакцины, защищающей от дифтерии, коклюша, столбняка, гепатита В и вакцины против Haemophilus influenzae типа b (Hib) и вакцины против кори.Иммунизация в больнице Мулаго проводится только в будние дни. Все недоношенные дети, поступившие в отделение SCBU, получают вакцины БЦЖ и ОПВ 0 при рождении, если они клинически стабильны. При выписке дата введения данной вакцины записывается в письме о выписке. Перед выпиской акушерка рекомендует опекунам отвезти недоношенного ребенка в медицинское учреждение рядом с домом для пропущенной и / или последующей вакцинации. При выписке недоношенным детям карты здоровья ребенка не выдаются; вместо этого лицам, осуществляющим уход, рекомендуется получать эти карточки в медицинских учреждениях, где они получат последующие вакцины.Лицам, осуществляющим уход, также назначается дата встречи, чтобы они вернулись для последующего наблюдения в клинике для новорожденных больницы.
Дизайн исследования
Это было перекрестное исследование с использованием как количественных, так и качественных методов сбора данных и последовательного пояснительного дизайна. Количественное исследование было проведено сначала с 11 июля 2016 г. по 23 9 42 марта 2017 г., а затем качественное исследование в апреле 2017 г.
Количественное исследование
Исследуемая популяция.
Недоношенные дети в возрасте 6–24 месяцев, посещающие клинику для новорожденных больницы Мулаго с карточкой здоровья ребенка (картой иммунизации) и чьи родители дали согласие.
Размер выборки.
Размер выборки был рассчитан с использованием формулы Киша Лесли для перекрестных исследований на основе доли младенцев с низкой массой тела при рождении, которым была отложена вакцинация в Лиме, Перу (65%) [17]. Расчетный размер выборки составил 350 с точностью 0,05, степенью 80% и доверительным интервалом 95%.
Процедура исследования и сбор данных.
Исследовательская группа состояла из главного исследователя и двух медсестер (младших научных сотрудников). Ассистенты-исследователи обращались ко всем родителям, посещавшим клинику для недоношенных детей со своими младенцами в дни клиники. Они предоставили информацию об исследовании родителям или опекунам. Затем помощники исследователей определили детей, подходящих для исследования, и получили письменное информированное согласие их родителей или опекунов. Недоношенные дети в возрасте от 6 до 24 месяцев соответствовали критериям включения в исследование.Доношенные и недоношенные дети, родители которых не пришли с картой иммунизации во время посещения клиники или не дали согласия на участие в исследовании, были исключены. Участников набирали последовательно, пока не был достигнут желаемый размер выборки.
Включены данные, полученные из медицинской карты ребенка и выписки из больницы; дата рождения, гестационный возраст при рождении, масса тела при рождении, место рождения и даты вакцинации для различных вакцинных антигенов.Во время личного интервью с родителем или опекуном научные сотрудники использовали предварительно протестированный структурированный вопросник для получения подробной информации о социальных, экономических, демографических и домашних характеристиках недоношенного ребенка. Они включали; возраст матери, посещаемость дородового наблюдения (ANC), уровень образования родителей, статус занятости родителей, религия, этническая принадлежность и продолжительность пребывания в SCBU. Все интервью проводились в день посещения клиники и длились около 20–30 минут.
Переменная результата.
Результат «своевременность» определялся как время до получения вакцины, рассчитанное в днях путем вычитания даты рождения из даты вакцинации младенца. Прививки были своевременными (вовремя), если они были сделаны в рекомендованные Всемирной организацией здравоохранения временные рамки (таблица 1) [33, 34].
Управление данными.
Заполненные формы данных ежедневно проверялись на полноту и точность главным исследователем и хранились в надежном шкафчике.Данные были дважды введены в Epidata v. 3.1 (Центры по контролю и профилактике заболеваний, Атланта, Джорджия) и проверены на предмет любых несоответствий. Все ошибки были исправлены, и очищенные данные были экспортированы в STATA 13 (STATA Corporation, College Station, Texas, USA) для анализа.
Анализ данных
Описательный анализ. Характеристики матерей, отцов и недоношенных детей были обобщены с использованием описательной статистики, такой как частота и пропорции для категориальных переменных.Непрерывные переменные были суммированы с использованием средних значений (стандартные отклонения) или медиан (межквартильный размах), в зависимости от распределения данных. Мы разделили результат на два уровня: младенцы , которые получили вакцины вовремя, (получили вакцину в пределах рекомендованных диапазонов) и те, которые не получили вакцины вовремя (получили вакцину так рано, поздно или пропустили), чтобы оценить доля младенцев, которые не получили вакцины в рекомендованные сроки.
Аналитический анализ. Для определения факторов, связанных со своевременностью вакцинации, «своевременность» результата была определена как время до получения каждой вакцины. Поэтому была использована модель регрессионного анализа Кокса. Допущения моделей пропорциональных рисков Кокса были проверены с использованием графиков невязки Scale Schoenfeld. Масштабированный тест невязки Шенфельда и расширенная модель с изменяющимися во времени ковариатами. Временной зависимости коэффициента опасности не было. Предположения были выполнены с использованием всех вышеперечисленных тестов.Мы использовали модель пропорциональных рисков Кокса при двумерном анализе. Следуя пошаговому подходу, все независимые переменные, которые имели значение p менее 0,2 при двумерном анализе, были рассмотрены для многомерного анализа. Переменные, о которых уже известно, что они связаны со своевременностью вакцинации, также учитывались для многопараметрического анализа независимо от p-значения, полученного при двумерном анализе. При многомерном анализе все переменные с p-значением ≤ 0,05 считались статистически значимыми.Никакого взаимодействия между переменными или смешения не наблюдалось. Окончательная модель была протестирована на предмет соответствия с использованием графика зависимости совокупной опасности Нельсона Алена от остатка Кокса-Снелла. Это показало экспоненциальную зависимость, указывающую на то, что модель хорошо подходит. Этот анализ был проведен для вакцины БЦЖ, ОПВ 0, АКДС 1, АКДС 3 и коревой вакцины.
Качественное исследование
Обсуждения в фокус-группах.
Восемнадцать специально отобранных лиц, осуществляющих уход за недоношенными новорожденными с отсроченной вакцинацией, приняли участие в двух обсуждениях в фокус-группах (ФГД) в больнице.Одна группа состояла из 8 участников в возрасте 15–24 лет, а другая — из 10 участников в возрасте ≥ 25 лет. Ассистент-исследователь, имеющий опыт качественных исследований, модерировал обсуждения, используя руководство для фокус-групп с подсказками, в то время как главный исследователь делал заметки. Обсуждения были сосредоточены на понимании участниками недоношенного ребенка, когда недоношенного ребенка следует иммунизировать, и причин, по которым некоторые недоношенные дети не были вакцинированы вовремя. Все ФГД были записаны на звук и длились примерно 60–90 минут.Обсуждения проводились на местном языке (луганда) и записывались на английский специалистом по качеству.
Интервью с ключевыми информаторами.
Было проведено пять интервью с ключевыми информантами (KII) с медицинскими работниками, ухаживающими за недоношенными детьми в течение более 6 месяцев в больнице. В их число входили один педиатр, две медсестры и два педиатрических врача-резидента. Руководство по собеседованию с датчиками было использовано для изучения предоставления услуг иммунизации в больнице Мулаго и выявленных препятствий на пути своевременной вакцинации недоношенных детей.Два научных сотрудника проводили интервью на английском языке; один модерировал обсуждение, а другой делал заметки. Все интервью были записаны на аудио и расшифрованы научным сотрудником, имеющим опыт проведения качественных исследований. Каждое интервью длилось 30–45 минут.
Управление данными и анализ.
Данные были проанализированы вручную с использованием тематического подхода [35] двумя опытными исследователями качества. Организационные темы и подтемы были получены на основе данных.Основными темами, связанными с отложенной вакцинацией, были: преждевременные роды, факторы, связанные с родителями и системой здравоохранения. Для представления результатов исследования использовались прямые цитаты участников.
Этические соображения.
Исследование было одобрено Комитетом по исследованиям и этике медицинского факультета Университета Макерере (SOMREC), REC REF 2016–064. Письменное информированное согласие было получено от всех родителей или опекунов недоношенных детей, а также от всех медицинских работников, которые участвовали в интервью с ключевыми информантами в этом исследовании.
Результаты
Количественные результаты
Социально-демографические характеристики недоношенных детей и их родителей.
Было обследовано пятьсот девяносто младенцев, посещающих клинику для недоношенных детей, и 384 ребенка соответствовали критериям включения в исследование. Мы зачислили 350 младенцев; процент ответов составил (91,1%) (рис. 1).
Средний возраст недоношенных детей составлял 8,4 месяца (IQR 6,8–10,8), и 183/350 (52,3%) составляли женщины. Около половины младенцев были очень недоношенными (28-32 недели) 178 (50.9%), 145 (41,4%) были поздними недоношенными (32–37 недель) и 27 (7,7%) были крайне недоношенными (<28 недель) (Таблица 2). Средний возраст матерей составлял 27 лет (IQR 23–32), из них 11 (3%) моложе 18 лет. Большинство матерей 341/350 (97,4%) посещали по крайней мере одно дородовое наблюдение и родили в больнице 307/350 (87,7%) (Таблица 2).
Своевременность вакцинации недоношенных детей.
Своевременность вакцинации, за исключением кори
В целом, менее половины 149/350 (42.6%) всех недоношенных новорожденных получили все вакцины в рекомендованные сроки. Доля недоношенных детей, своевременно вакцинированных, была разной для каждой вакцины (таблица 3). Что касается индивидуальных вакцин, БЦЖ была самой своевременной вакциной: 92% младенцев получили ее вовремя, в то время как ОПВ была наименее своевременной вакциной (45,4%). В целом, 201/350 (57,4%) недоношенных новорожденных были вакцинированы несвоевременно (не получили хотя бы одну вакцину в течение рекомендованного периода времени) (Таблица 3). Из них 176/350 (50.3%) получили хотя бы одну прививку поздно, а 87/350 (24,9%) пропустили хотя бы одну прививку. Один, 1/350 (0,3%) младенца получил вакцины на ранней стадии, включая АКДС 1, ПКВ 1, ОПВ 1, АКДС 3 и ПКВ 3 (таблица 4).
Доля недоношенных новорожденных с несвоевременной вакцинацией была самой высокой для вакцин, вводимых на сроке 6 недель; PCV 1 142/350 (40,6%), OPV 1 140/350 (40,0%) и DPT 1 129/350 (36,9%) по сравнению с другими вакцинами в календаре EPI (таблица 4). Среди несвоевременных прививок большинство было получено с опозданием по сравнению с вакцинами, которые не были получены (пропущены), и теми, которые были получены раньше (Таблица 4).Больше недоношенных детей опоздали на вакцины, введенные на 6-й неделе ОПВ 1139/350 (39,7%), ПКВ 1 137/350 (39,1%) и АКДС 1 128/350 (36,6%) по сравнению с вакцинами, введенными на 10-й и 14-й неделе. . С другой стороны, больше недоношенных новорожденных не получали (пропускали) вакцины, вводимые на 14 неделе ОПВ 3 (14%), ПКВ 3 (11,7%) и АКДС 3 (7,4%) по сравнению с вакцинами, введенными на 6 и 10 неделях ( Таблица 4).
Своевременность введения противокоревой вакцины.
Сто двадцать пять недоношенных детей соответствовали критериям вакцинации против кори.Из них 112 (89,6%) получили вакцину в рекомендованный период времени (таблицы 3 и 4). Тринадцать младенцев были несвоевременно вакцинированы против кори, из них 6 получили вакцину раньше, 4 не были вакцинированы и 3 получили вакцину поздно (таблица 4).
Факторы, связанные с несвоевременной вакцинацией недоношенных детей.
S1 В таблице показаны характеристики, которые были связаны с несвоевременной вакцинацией при двумерном анализе для отдельных вакцин.
При многомерном анализе роды из дома или в частной клинике и отсутствие запасов вакцины в значительной степени были связаны с несвоевременным получением БЦЖ и ОПВ 0.Очень преждевременные роды и низкий уровень образования матери были связаны с несвоевременной вакцинацией АКДС 1 и АКДС 3. Поступление и длительное пребывание в отделении SCBU были связаны с несвоевременным получением АКДС-1, в то время как крайне низкая масса тела при рождении была связана с несвоевременной вакцинацией АКДС-3. Повышение паритета было в значительной степени связано с несвоевременной вакцинацией против кори (Таблица 5).
Качественные результаты
Время вакцинации недоношенных детей.
Все участники ФГД и ключевые респонденты считали, что недоношенных детей следует вакцинировать, как и любого другого ребенка, утверждая, что их иммунизация должна быть приоритетной, учитывая их повышенную восприимчивость к инфекциям из-за недоношенности.
«… Нам необходимо вакцинировать недоношенных детей, потому что они рождаются раньше срока. , они легко заболевают заболеваниями, которые могут быть тяжелыми по сравнению с доношенными детьми из-за их слабости . ”(ОФГ для пожилых людей)
Однако информация о сроках вакцинации недоношенных новорожденных у лиц, осуществляющих первичный уход, была неточной. Большинство из них не знали, когда недоношенным детям следует вводить различные вакцины.
Причины отсрочки вакцинации недоношенных детей.
Три основные организационные темы, связанные с недоношенными детьми, системой здравоохранения и родительскими факторами, явились в результате обсуждений в качестве основных причин отсрочки вакцинации, как указано в (Таблица 6).
Факторы недоношенности.
Рост и вес недоношенного ребенка
Небольшой размер и малый вес недоношенных детей были упомянуты в качестве основных факторов, ответственных за отсрочку вакцинации. Некоторые воспитатели считали недоношенных детей слишком маленькими для вакцинации, в то время как другие опасались, что вакцины небезопасны, особенно для очень маленьких детей.
« Мне пришлось подождать, пока ребенок не наберет вес и не станет лучше выглядеть, прежде чем я смогу сделать его иммунизацию (опекуны FGD-Young)
Некоторые участники ФГД отметили, что страх вакцинировать недоношенных детей из-за того, что они маленькие, также преобладал среди медицинских работников, что приводило к отсрочке вакцинации.
« Хотя врач сказал мне сделать прививку ребенку , , медсестра посоветовала мне отложить, сказав , «… . ребенок весит всего 1 кг, и вы хотите сделать прививку ! ”(ОФГ — лица, осуществляющие уход за пожилыми людьми)
Болезнь недоношенного ребенка.
Болезнь недоношенного ребенка даже с незначительными симптомами, такими как лихорадка и простуда, привела к отсрочке или отсрочке вакцинации. Было отмечено, что как лица, осуществляющие уход, так и некоторые медицинские работники, особенно в периферийных медицинских учреждениях, откладывали вакцинацию недоношенных детей, когда они заболели.
« Мне сказал (медицинский работник) не брать ребенка для иммунизации, когда он болен . Я взяла малышку на иммунизацию только тогда, когда она полностью выздоровела. . ”(опекуны FGD-Young)
Продолжительность пребывания в отделении для новорожденных.
Продолжительное пребывание недоношенного ребенка в отделении SCBU также привело к задержке с получением последующих вакцин. Во время исследования отделение предоставляло только вакцины, введенные при рождении, БЦЖ и ОПВ 0. Независимо от продолжительности пребывания в SCBU, недоношенные дети получают последующие вакцины в детской поликлинике больницы Мулаго или другом медицинском учреждении поблизости. домой после выписки из СКБУ.
« Я провела два месяца в палате (SCBU) , ребенок получил первую прививку, но другие прививки не делались . При выписке , Мне сказали, что ребенок пропустил некоторые прививки, и посоветовали пойти в медицинское учреждение рядом с домом, чтобы получить их. . ”(опекуны FGD-Young)
Место доставки.
Кроме того, невыполнение родов из больницы было еще одним фактором, который способствовал отсутствию вакцинации или задержке вакцинации недоношенных детей.
« Матери, рожающие дома или в клиниках, не имеющих вакцины, пропускают БЦЖ и полиомиелит 0 . »(КИ-Медсестра)
Факторы системы здравоохранения.
Недостаточные знания медицинских работников
Недостаточные знания медицинских работников в отношении ухода за недоношенными детьми, включая их вакцинацию, были упомянуты в качестве основного фактора отсроченной вакцинации. Большинство участников исследования сообщили, что медицинские работники, особенно в периферийных медицинских центрах, редко сталкиваются с недоношенными детьми, поэтому не уверены, когда их иммунизировать.
« При выписке мы просим их (опекунов) продолжить иммунизацию из близлежащих учреждений , , к сожалению, когда они приносят нам младенцев , , мы получаем информацию , « медицинский работник отказался провести иммунизацию , Ребенок недоношенный . »(КИ-Педиатр)
Негативное отношение медицинских работников.
Некоторые лица, ухаживающие за больными, сообщили, что разочарованы возвращением для последующей иммунизации из-за того, как с ними обращаются медицинские работники.Утверждается, что некоторые медицинские работники жестоко обращаются с лицами, осуществляющими уход, и их детьми и предпочитают обращаться с доношенными детьми. Некоторые считали, что их младенцев даже не считали детьми, как рассказал один из воспитателей:
“ Медсестра спросила женщину с недоношенным ребенком в медицинском учреждении , , что это (имеется в виду недоношенный ребенок), который вы принесли сюда ? Убери ! Посоветовал отвезти ребенка в другую больницу . ”(ОФГ — лица, осуществляющие уход за пожилыми людьми)
Запас вакцин.
Участники исследования подчеркнули, что дефицит вакцин является основным препятствием для своевременной вакцинации их детей. Многие рассказывали, как они неоднократно посещали медицинские центры, чтобы вакцинировать своих детей.
« Я несколько раз безуспешно обращался в медицинское учреждение , Я получил вакцину от полиомиелита с третьей попытки, и только несколько человек получили вакцину в тот день , остальные пропустили . ”(ОФГ — лица, осуществляющие уход за пожилыми людьми)
Недостаточное общение медицинских работников.
Некоторые лица, осуществляющие уход, упомянули, что им не сообщили, были ли их дети вакцинированы во время пребывания в SCBU. Они не были уверены в прививочном статусе своих детей и в том, когда их следует проводить для дальнейшей вакцинации после выписки из больницы.
« Когда я выписывалась из больницы , , я заметила маленькую отметину на руке ребенка; Я думала, комар укусил ребенка . Позже мне сказали, что ребенку сделали прививки . ”(опекуны FGD-Young)
Ключевые респонденты подтвердили, что обычно недоношенным детям делали прививку, находясь в SCBU, без ведома их опекунов.
« Иногда в письме о выписке указывается, вакцинирован ли ребенок или нет. . Но матери могут не знать, что их ребенок был вакцинирован, даже если это было написано в письме о выписке, потому что они не были проинформированы. . »(КИ-Педиатр)
Недостаточная информация или отсутствие информации, предоставляемой лицам, осуществляющим уход, о вакцинации их недоношенных детей, не давало им уверенности в том, когда начинать или продолжать иммунизацию, что приводило к задержкам. Также было отмечено, что иногда медицинские работники забывают спросить о прививочном статусе недоношенного ребенка во время последующих посещений, в основном из-за загруженности клиник, в которых работает немного медицинских работников.
Пробелы в документации о вакцинационном статусе недоношенных детей.
Качественные результаты также показали, что вакцинированным недоношенным детям не выдаются карты иммунизации при выписке из SCBU. Информация о вакцинах, вводимых во время пребывания в яслях, записывается в письме о выписке, и опекуну рекомендуется получить карту при следующей иммунизации. Некоторые родители могут не знать прививочный статус младенца и не знать, когда делать прививку.
« При выписке , врач не сказал мне, что ребенку сделали прививки, пока я не спросила . Он сказал мне, что ребенку сделали первую прививку, не сообщая подробностей. . Когда я пошел в медицинское учреждение рядом с домом , , меня спросили, был ли ребенок привит , Я сказал им, что ребенок получил первую прививку, но они не поняли . У меня не было карты прививок из отделения особой помощи . ”(ОФГ — лица, осуществляющие уход за пожилыми людьми)
Родительские факторы.
Страх побочных эффектов
Воспитатели часто упоминали страх перед побочными эффектами как причину несвоевременной вакцинации недоношенных детей.
« Ребенок был недоношенным и весил менее 1 кг , , но мне сказали сделать прививку . Ребенку два месяца давали кислород ! Мои опасения были хуже, потому что это был мой первый ребенок . Мне сказали, что при вакцинации ребенка у него поднимается температура, и это может быть нежелательно , Я испугался . ”(опекуны FGD-Young)
Основные знания лиц, осуществляющих уход.
Некоторые матери не знали, когда следует делать вакцины, а некоторые предпочли не вакцинироваться.
Обсуждение
Наше исследование показало, что более половины (57%) недоношенных детей в возрасте от 6 до 24 месяцев, посещающих клинику последующего наблюдения в Национальной специализированной больнице Мулаго в Уганде, не получили хотя бы одной вакцины в рекомендованные сроки. Высокая доля недоношенных детей, прошедших несвоевременную вакцинацию, вызывает беспокойство, учитывая рост числа преждевременных родов в Уганде [3, 5] и тот факт, что эти дети очень восприимчивы к болезням, которые можно предотвратить с помощью вакцин.Оценки своевременной вакцинации в нашем исследовании, вероятно, будут выше, чем в медицинских учреждениях более низкого уровня, учитывая, что исследование проводилось в больнице третичного уровня, где младенцы регулярно наблюдаются. Несвоевременная вакцинация имеет далеко идущие последствия как для недоношенных детей, так и для других детей в обществе. Из-за отсроченной вакцинации недоношенные дети подвергаются повышенному риску заражения болезнями, которые можно предотвратить с помощью вакцинации, что влечет за собой смертность. Кроме того, дети с неполной вакцинацией предрасположены к вспышкам болезней, которые можно предотвратить с помощью вакцинации, в общинах.
Несвоевременное получение вакцин, влияющих на различные вакцинные антигены в нашем исследовании, также наблюдалось в других исследованиях, особенно в странах с высоким уровнем доходов [13, 16, 18].
БЦЖ была самой своевременной вакциной, и 92% младенцев получили ее вовремя. Эта оценка аналогична той, которая была получена среди детей в исследовании на уровне общины в Кампале (92,7%), хотя это не были недоношенные дети [34].
В нашем исследовании роды в больнице были в значительной степени связаны со своевременным получением БЦЖ и ОПВ 0, что аналогично результатам, полученным в других африканских странах [34, 36, 37].В Уганде введение БЦЖ и ОПВ 0 при рождении является обязательным требованием для всех зарегистрированных родильных домов, что может объяснить своевременное получение этих вакцин по сравнению с последующими вакцинами, указанными в календаре [37].
Несоответствие в сроках вакцинации БЦЖ и ОПВ 0, которые вводятся при рождении, было отмечено в этом исследовании, это открытие также наблюдалось в Кении, хотя это не относилось к недоношенным детям [37]. Это несоответствие можно объяснить дефицитом полиовакцины, о котором сообщили участники исследования и представитель больницы в РПИ.Нехватка вакцин препятствует своевременному получению вакцины среди детей. В этом случае дефицит вакцины против полиомиелита может подорвать усилия, направленные на ликвидацию полиомиелита в Уганде. Таким образом, Министерство здравоохранения (МЗ) должно обеспечить достаточное количество всех обычных вакцин во всех медицинских учреждениях по всей стране.
У большинства недоношенных детей была значительная задержка начала приема первой дозы АКДС 1, ПКВ 1 и ОПВ 1 на 6 неделе по сравнению со второй и третьей дозами на 10 и 14 неделе.Подобные результаты были получены среди недоношенных детей в Италии и Нидерландах [16, 18], что подчеркивает тот факт, что это может быть общей тенденцией и проблемой во всем мире. Отсроченное введение первой дозы обычно означает, что последующие дозы также могут быть отсрочены [18]. Поэтому крайне важно, чтобы первая вакцинация была сделана вовремя. Отсрочка вакцинации увеличивает риск заражения недоношенных новорожденных заболеваний, что может подорвать усилия по профилактике инвазивной пневмококковой инфекции, ликвидации полиомиелита и может привести к повторному возникновению других УИ, таких как коклюш в Уганде.Кроме того, количество недоношенных новорожденных, не получивших вакцины, увеличивалось на количество доз вакцины, вводимых на 6, 10 и 14 неделе. Это согласуется с данными других исследований об отсрочке вакцинации с увеличением возраста [38,39]. Это показывает, что младенцы, не получившие вакцины, не завершают рекомендованный график вакцинации, что в конечном итоге может снизить охват вакцинацией в стране. Поэтому крайне важно, чтобы вакцинация недоношенных детей была начата и завершена вовремя.
Несвоевременное получение АКДС 1 и АКДС 3 в нашем исследовании значимо ассоциировалось с гестационным возрастом, массой тела при рождении, продолжительностью пребывания в SCBU и уровнем образования матери. За исключением веса при рождении, эти результаты противоречат результатам итальянской когорты очень недоношенных детей. Tozzi и соавт. Обнаружили, что отсроченное начало АКДС 1 было связано с госпитализацией после выписки из отделения интенсивной терапии новорожденных, высоким числом детей и отцовской безработицей — факторами, которые в нашем исследовании были статистически незначимыми [16].Несвоевременное получение АКДС 1 в нашем исследовании можно объяснить тем фактом, что SCBU предоставляет вакцины только при рождении (БЦЖ и ОПВ 0), а не последующие вакцинации. Мы заметили, что с увеличением продолжительности пребывания в отделении SCBU младенцы реже получали АКДС 1 вовремя. Действительно, матери с младенцами, которые долго оставались в яслях, назвали это причиной поздней вакцинации своих младенцев. Наши результаты согласуются с данными из Швейцарии, где длительная госпитализация была связана с отсроченной вакцинацией АКДС-1 недоношенных новорожденных с массой тела <1500 г [40].Младенцы с очень низкой массой тела (<1000 г) получили несвоевременное получение АКДС 3, однако это было значимым для АКДС 1 только при двумерном анализе. Младенцы с очень низкой массой тела, вероятно, будут оставаться в больнице дольше после рождения из-за сопутствующих заболеваний, приводящих к задержке вакцинации, особенно в нестабильных случаях. Несмотря на то, что вакцинация начинается во время госпитализации недоношенного ребенка в SCBU больницы Мулаго, рекомендуется обеспечить последующие вакцины для младенцев, которые остаются на более длительный срок, чтобы свести к минимуму задержки.
Очень недоношенных детей вакцинировали со значительной задержкой как для АКДС-1, так и для АКДС-3. Подобные результаты были получены в других исследованиях [13, 16, 18, 32], несмотря на различия в графиках вакцинации в разных странах. Это подчеркивает сильную корреляцию между недоношенностью и отсроченной вакцинацией, как было ранее задокументировано [13, 18]. С другой стороны, крайняя недоношенность не была значимой для DPT 1 и DPT 3 в нашем исследовании. Это противоречит результатам других исследований [13, 18, 32], которые можно отнести к небольшому количеству крайне недоношенных детей в нашем исследовании.
В нашем исследовании низкий уровень материнского образования был связан с несвоевременной вакцинацией недоношенных детей как для АКДС 1, так и для АКДС 3. Это согласуется с выводами других исследований, которые показывают, что получение посленачального образования связано с более эффективным использованием медицинской помощи. услуги, включая иммунизацию [41–44]. Фактические данные показывают, что уровень знаний и использования услуг вакцинации выше у женщин, имеющих хотя бы некоторое среднее образование [42]. Хотя правительство Уганды обеспечивает всеобщее начальное образование, необходимы дальнейшие инвестиции и политическая воля для обеспечения того, чтобы большинство детей получали как минимум среднее образование, чтобы улучшить использование всех услуг первичной медико-санитарной помощи, включая иммунизацию.
Только 125/350 (35,7%) недоношенных детей в возрасте 9 месяцев и старше соответствовали критериям вакцинации против кори. В целом, большинство 112/125 (89,6%) этих младенцев получили вакцину против кори вовремя. Несвоевременное получение противокоревой вакцины было связано с увеличением паритета в нашем исследовании. Подобные результаты были задокументированы в других исследованиях и объясняются более высокими затратами и потребностями в ресурсах, вызванными многодетным рождением, что отрицательно сказывается на использовании медицинских услуг [34, 37].С увеличением числа братьев и сестер, вероятно, возрастут домашние и семейные обязанности матери или опекуна с ограниченным вниманием к младенцу, что может привести к тому, что о вакцинации забудут [44, 45]. Действительно, в предыдущих исследованиях причиной неполной вакцинации их младенцев была «очень занятая матери» [44–47]. Хотя эти исследования не проводились среди недоношенных детей, тем не менее, то же объяснение может быть правдоподобным. С другой стороны, 6 детей раннего возраста получили прививку от кори.Ранняя вакцинация имеет последствия для здоровья, затрат, административных и программных последствий [34]. Например, исследование, проведенное в Нидерландах, показало, что, хотя ранняя вакцинация против кори обеспечивает немедленную защиту, существуют опасения по поводу долгосрочной защиты [48]. Это стало результатом наблюдения, что у детей, получивших вакцину в возрасте менее 9 месяцев, уровень антител упал до уровня ниже порогового значения, необходимого для клинической защиты через 4 года [48]. Такое снижение защиты у детей, вакцинированных в раннем возрасте, может повысить риск будущих потенциальных вспышек болезни [48] и может потребовать введения бустерных доз против кори.Текущий график РПИ в Уганде предусматривает вакцинацию против кори один раз в 9 месяцев, поэтому дополнительные дозы будут иметь финансовые и программные последствия. Таким образом, своевременная вакцинация имеет первостепенное значение для предотвращения таких последствий и обеспечения успеха программы РПИ в стране.
Качественные результаты также показали, что пробелы в документировании статуса вакцинации, о чем свидетельствует невыдача карт иммунизации при выписке из SCBU, способствовали несвоевременной вакцинации. Этот результат согласуется с результатами предыдущего исследования в Уганде, которое показало, что отсутствие карты иммунизации снижает вероятность полной иммунизации ребенка [41].Наличие плана иммунизации в виде карты иммунизации с четко обозначенным графиком гарантирует, что матери могут легко следовать графику иммунизации. Это сводит к минимуму забвение и позволяет своевременно вакцинировать детей [41]. Поэтому важно, чтобы всем недоношенным детям были выданы карты вакцинации, в которых документирован прививочный статус при выписке из больницы.
Некоторым опекунам часто не сообщали, были ли их дети вакцинированы, где и когда сделать последующие вакцины, что приводило к несвоевременной вакцинации.Коммуникация играет важную роль в распространении информации о важных вопросах здоровья и доступных медицинских услугах [49]. Поэтому эффективная коммуникация и передача информации между медицинскими работниками и родителями важны для обеспечения того, чтобы они соблюдали график иммунизации, чтобы обеспечить своевременную вакцинацию.
Негативное отношение медицинских работников к воспитателям и их детям было названо еще одной причиной несвоевременной вакцинации недоношенных детей.Действительно, другие исследования документально подтвердили роль отношения и поведения медицинских работников по отношению к матерям как важную для определения использования услуг иммунизации [22,49–51]. Неприятность работников здравоохранения была выделена как главный барьер системы здравоохранения, влияющий на вакцинацию в странах с низким средним уровнем дохода [22]. Страх побочных эффектов после иммунизации и дезинформация, особенно об иммунизации больного ребенка, были названы в нашем исследовании причинами несвоевременной вакцинации недоношенных детей.Обеспокоенность по поводу вредных событий после иммунизации является основным фактором нерешительности в отношении вакцинации как в странах с высоким, так и с низким уровнем доходов [19, 22, 23, 25, 26, 49, 51]. По сути, это ключевое препятствие для своевременной вакцинации, отражающее необходимость усиления предоставления точной информации для повышения своевременности вакцинации.
Изучение сильных сторон и ограничений
Наше исследование было проведено с использованием смешанных методов, что повысило надежность наших результатов. Обсуждения с родителями или опекунами и интервью с медицинскими работниками позволили глубже понять факторы, способствующие отсроченной вакцинации недоношенных детей в больнице Мулаго.Насколько нам известно, это первое исследование по определению своевременности вакцинации и связанных с ней факторов среди недоношенных детей в Уганде.
В то время как количественное исследование не оценивало колебания вакцинации, качественное исследование пролило свет на него как на одно из основных препятствий на пути своевременной вакцинации недоношенных детей. Другие факторы, такие как наличие транспорта, расстояние до ближайшего медицинского учреждения, материнское заболевание и иммунизация матери во время дородовой помощи, которые могли повлиять на своевременность вакцинации недоношенных детей, также не оценивались.В тех случаях, когда даты вакцинации некоторыми антигенами не указывались в медицинской карте ребенка или письме о выписке из больницы, это фиксировалось как «не проводилось», даже когда лицо, осуществляющее уход, сообщало, что вакцина была сделана. Таким образом, в нашем исследовании фактическая своевременность могла быть недооценена. Однако таких случаев было очень мало, поэтому недооценка могла быть минимальной. В этом исследовании существует вероятность систематической ошибки вспоминания, поскольку родители не могли точно запомнить некоторую информацию. Это было исследование, проводимое в больнице; мнения лиц, ухаживающих за недоношенными новорожденными, с ограниченным взаимодействием с системой здравоохранения, могут быть недостаточно представлены.Однако смешанный характер нашего исследования позволил получить массу информации о препятствиях на пути своевременной вакцинации недоношенных детей, что важно для разработки стратегий усиления вакцинации этой очень уязвимой группы младенцев.
Заключение
Большинство недоношенных детей в больнице Мулаго не получили вовремя хотя бы одну вакцину, несмотря на плановое наблюдение врачей в специализированной клинике. Несвоевременная вакцинация повышает предрасположенность недоношенных детей к болезням, которые можно предотвратить с помощью вакцин.Мы рекомендуем объединить несколько действий, чтобы улучшить выполнение существующих рекомендаций. Сюда входит приоритетное внимание государства к вакцинации групп высокого риска, включая недоношенных детей. Выдача карт вакцинации с указанием прививочного статуса недоношенного ребенка при выписке из больницы. Медицинские работники должны продвигать вакцинацию недоношенных детей, регулярно проверяя их вакцинационный статус во время плановых последующих посещений. Другие меры по повышению своевременности вакцинации недоношенных детей в стране включают обучение медицинских работников и повышение осведомленности общественности с четкими сообщениями о вакцинации недоношенных детей, а также поддержание достаточного запаса всех обычных вакцин во всех медицинских учреждениях.Необходимы дальнейшие исследования, чтобы понять пробелы в знаниях, отношении и практике медицинских работников в отношении вакцинации недоношенных детей в Уганде.
Благодарности
Авторы хотели бы поблагодарить все семьи и медицинских работников, принявших участие в этом исследовании, а также научных сотрудников Эстер Бисасо, Роверенса Кабахагире и Ирен Лорну Акелло. Мы также благодарны Аллену Намагембе за ее вклад в разработку инструментов для сбора и ввода данных и Кристине Накабуго за перевод форм согласия и руководств по собеседованию.
Ссылки
- 1.
Всемирная организация здравоохранения. Охват иммунизацией. Женева: Всемирная организация здравоохранения; 2016 [доступ 29 января 2016 г.]. Доступно по адресу: http://www.who.int/mediacentre/factsheets/fs378/en/. - 2.
VanderEnde K, Gacic-Dobo M, Diallo MS, Conklin LM, Wallace AS. Глобальный охват плановой вакцинацией — 2017. MMWR Morb Mortal Wkly Rep. 2018 (67): 1261–4. - 3.
Марш десяти центов PMNCH, Спасите детей ВОЗ. Родился слишком рано: Глобальный доклад о действиях в отношении преждевременных родов.Хоусон С.П., Кинни М.В., Лон Дж. Э., редакторы. Женева: Всемирная организация здравоохранения; 2012. - 4.
Бек С., Войдыла Д., Сэй Л., Бетран А. П., Мериалди М., Рекехо Дж. Х. и др. Заболеваемость преждевременными родами во всем мире: систематический обзор материнской смертности и заболеваемости. Бюллетень Всемирной организации здравоохранения. 2010. 88 (1): 31–8. pmid: 20428351 - 5.
Министерство здравоохранения. Ситуационный анализ здоровья новорожденных в Уганде: текущее состояние и возможности для улучшения ухода и выживания.Кампала: Спасите детей, ЮНИСЕФ, ВОЗ, 2008. - 6.
Заман К., Рой Э., Арифин С.Е., Рахман М., Ракиб Р., Уилсон Э. и др. Эффективность иммунизации материнского гриппа у матерей и младенцев. Медицинский журнал Новой Англии. 2008. 359 (15): 1555–64. pmid: 18799552 - 7.
Муньос FM, Джеймисон DJ. Иммунизация матери. Obstet Gynecol. 2019; 133 (4): 739–53. pmid: 30913173 - 8.
Фуда Г.Г., Мартинес Д.Р., Свами Г.К., Пермар С.Р. Влияние трансплацентарной передачи IgG на иммунитет в раннем возрасте.ИммуноГоризонты. 2018; 2 (1): 14–25. pmid: 29457151 - 9.
Свами Г.К., Гейне Р.П. Прививки для беременных. Obstet Gynecol. 2015; 125 (1): 212–26. pmid: 25560127 - 10.
Бонхеффер Дж., Зигрист, Калифорния, Хит, PT. Иммунизация недоношенных детей. Архив болезней детства. 2006. 91 (11): 929–35. pmid: 17056868 - 11.
Хили CM. Стратегии иммунизации для защиты недоношенных детей. NeoReviews. 2010. 11 (8): 409–18. - 12.
Лангкамп Д.Л., Дэвис Дж. П.Повышенный риск зарегистрированного коклюша и госпитализации, связанной с коклюшем, у детей с низкой массой тела при рождении. Журнал педиатрии. 1996. 128 (5): 654–9. - 13.
Slack MH, Thwaites RJ. Сроки иммунизации недоношенных детей в неонатальном отделении и после выписки из сообщества. Commun Dis Public Health. 2000. 3 (4): 303–4. pmid: 11280267 - 14.
Всемирная организация здравоохранения. Резюме документов с изложением позиции ВОЗ — Рекомендации по плановой иммунизации.Женева: Всемирная организация здравоохранения; 2019 [доступ 20 марта 2019 г.]. Доступно по адресу: https://www.who.int/immunization/policy/Immunization_routine_table2.pdf?ua=1. - 15.
Эспозито С., Серра Д., Гуальтьери Л., Чезати Л., Принципи Н. Вакцины и недоношенные новорожденные: почему, когда и с чем? Раннее человеческое развитие. 2009. 85 (10): S43–5. - 16.
Tozzi AE, Piga S, Corchia C, Di Lallo D, Carnielli V, Chiandotto V и др. Своевременность плановой иммунизации итальянской популяции очень недоношенных новорожденных: результаты последующего проекта ACTION.Вакцина. 2014; 32 (7): 793–9. pmid: 24397902 - 17.
Очоа Т.Дж., Зеа-Вера А., Баутиста Р., Давила С., Салазар Дж. А., Базан С. и др. Соблюдение графика вакцинации младенцев с очень низкой массой тела при рождении в Лиме, Перу. Вакцина. 2015; 33 (2): 354–8. pmid: 25448091 - 18.
Woestenberg PJ, van Lier A, van der Maas NA, Drijfhout IH, Oomen PJ, de Melker HE. Отсроченное начало вакцинации против дифтерии, столбняка, бесклеточного коклюша и вакцинации против полиомиелита у недоношенных детей и новорожденных с низкой массой тела в Нидерландах.Pediatr Infect Dis J. 2014; 33 (2): 190–8. pmid: 24168985 - 19.
Hofstetter AM, Jacobson EN, deHart MP, Englund JA. Статус вакцинации недоношенных детей в раннем детстве. Педиатрия. 2019: e20183520. pmid: 313 - 20.
Макдональд NE. Неуверенность в отношении вакцины: определение, объем и детерминанты. Вакцина. 2015; 33 (34): 4161–4. pmid: 25896383 - 21.
Всемирная организация здравоохранения. Десять угроз глобальному здоровью в 2019 г. Женева: Всемирная организация здравоохранения; 2019 [доступ 17 июня 2019 г.].Доступно по адресу: https://www.who.int/emergencies/ten-threats-to-global-health-in-2019. - 22.
Кобос Муньос Д., Монсон Лламас Л., Бош-Капбланч X. Выявление опасений по поводу вакцинации в странах с низким и средним уровнем доходов: систематический обзор. Международный журнал общественного здравоохранения. 2015; 60 (7): 767–80. pmid: 26298444 - 23.
Наполитано Ф, Д’Алессандро А, Анжелилло ИФ. Изучение нерешительности итальянских родителей относительно вакцины: перекрестное исследование. Hum Vaccin Immunother.2018; 14 (7): 1558–65. pmid: 29641945 - 24.
Гилки М.Б., Макри А.Л., Магнус Б.Е., Рейтер П.Л., Демпси А.Ф., Брюэр Н.Т. Доверие к вакцинации и отказ родителей / отсрочка вакцинации детей младшего возраста. ПлоС один. 2016; 11 (7): e0159087. pmid: 273 - 25.
Фаччола А., Визалли Дж., Орландо А., Бертуччо М. П., Спатаро П., Скуери Р. и др. Неуверенность в вакцинации: обзор мнения родителей о вакцинации и возможных причинах отказа от вакцинации. J Public Health Res. 2019; 8 (1): 1436.pmid: 30997357 - 26.
Мастерс Н., Тефера Ю., Вагнер А., Бултон М. Неустойчивость к вакцинам среди лиц, осуществляющих уход, и ассоциация своевременности вакцинации детей в Аддис-Абебе, Эфиопия. Человеческие вакцины и иммунотерапевтические средства. 2018; 0 (0): 1–8. - 27.
Национальная академия наук Уганды. Консультативный комитет по вакцинам и иммунизации: улучшение охвата вакцинами и иммунизацией в Уганде. Первая аналитическая записка. Кампала: УНАС, 2013. - 28.
Республика Уганда.Отчет о народонаселении Уганды за 2016 год. Качественное здравоохранение: ключ к устойчивому развитию. Кампала: 2016. - 29.
Мукаса Н. Профиль системы здравоохранения Уганды: история вопроса, организация, политика и проблемы. Журнал устойчивых региональных систем здравоохранения. 2012; 1 (1): 2–10. - 30.
Всемирная организация здравоохранения. Уганда: оценки ВОЗ и ЮНИСЕФ по охвату иммунизацией: 2017 г., версия 2018 г. [27 мая 2019 г.]. Доступно по адресу: https://www.who.int/immunization/monitoring_surveillance/data/uga.pdf. - 31.
Маланде О.О., Мунубе Д., Афайо Р.Н., Аннет К., Бодо Б., Бакаинага А. и др. Препятствия на пути к эффективному внедрению и обеспечению иммунизацией в сельских районах Уганды. ПлоС один. 2019; 14 (2): e0212270. pmid: 30763355 - 32.
Уилсон К., Хокен С., Холдт Хеннингсен К., Квонг Дж. К., Дикс С.Л., Кроукрофт Н.С. и др. Охват своевременной вакцинацией недоношенных детей в Онтарио, 2002–2009 гг. Канадский журнал общественного здравоохранения = Revue canadienne de sante publique. 2012; 103 (5): e359–62.pmid: 23617988 - 33.
Кларк А., Сандерсон С. Сроки вакцинации детей в 45 странах с низким и средним доходом: анализ данных опроса. Ланцет. 2009. 373 (9674): 1543–9. - 34.
Бабирье Дж. Н., Энгебретсен И. М., Макумби Ф., Фаднес Л. Т., Вамани Х., Тиллескар Т. и др. Своевременность детских прививок в Кампале Уганда: кросс-секционное исследование на уровне общины. ПлоС один. 2012; 7 (4): e35432. pmid: 22539972 - 35.
Graneheim UH, Lundman B.Качественный контент-анализ в медсестринских исследованиях: концепции, процедуры и меры для достижения надежности Nurse Educ Today. 2004. 24 (2): 105–12. pmid: 14769454 - 36.
Olusanya BO. Характер и детерминанты задержек иммунизации БЦЖ в африканском сообществе к югу от Сахары. Политика и системы медицинских исследований. 2010; 8 (1): 1. - 37.
Mutua MK, Kimani-Murage E, Ettarh RR. Вакцинация детей в неформальных городских поселениях Найроби, Кения: кому делают прививки? BMC общественное здравоохранение.2011; 11 (1): 6. pmid: 21205306 - 38.
Фаднес Л.Т., Джексон Д., Энгебретсен IMS, Зембе В., Сандерс Д., Зоммерфельт Н. и др. Охват вакцинацией и своевременность в трех регионах Южной Африки: проспективное исследование. BMC общественное здравоохранение. 2011; 11 (1): 404. - 39.
Laryea DO, Abbeyquaye Parbie E, Frimpong E. Своевременность вакцинации детей, посещающих клинику иммунизации на базе учреждения третичного медицинского обслуживания в Гане. BMC общественное здравоохранение. 2014; 14 (1): 90. - 40.
Tillmann BU, Tillmann HC, Nars PW, Weber P. Уровень вакцинации и возраст недоношенных детей с массой тела <1500 г: пилотное исследование на северо-западе Швейцарии. Acta paediatrica. 2001. 90 (12): 1421–6. pmid: 11853341 - 41.
Ббаале Э. Факторы, влияющие на иммунизацию детей в Уганде. Журнал здоровья населения и питания. 2013. 31 (1): 118–29. - 42.
Нанкабирва В., Тиллескер Т., Тамвин Дж. К., Зоммерфельт Х., Исследовательская группа Promise-ebf.Материнское образование связано с вакцинационным статусом младенцев в возрасте до 6 месяцев в Восточной Уганде: когортное исследование. BMC Pediatr. 2010; 10: 92. pmid: 21159193 - 43.
О’Лири М., Томас С., Хёрт Л., Флойд С., Шеннон С., Ньютон С. и др. Сроки вакцинации детей с низкой массой тела при рождении в сельских районах Ганы: популяционное проспективное когортное исследование. Bull World Health Organ. 2016; 94: 442–51. pmid: 27274596 - 44.
Упадхьяй Р.П., Чоудхури Р., Мазумдер С., Танежа С., Синха Б., Мартинес Дж. И др.Практика иммунизации младенцев с низкой массой тела при рождении из сельской Харьяны, Индия: результаты вторичного анализа данных. Журнал глобального здоровья. 2017; 7 (2): 020415. pmid: 29423177 - 45.
Odutola A, Afolabi MO, Ogundare EO, Lowe-Jallow YN, Worwui A, Okebe J, et al. Факторы риска задержки вакцинации детей Гамбии в соответствии с возрастом. BMC Health Services Research. 2015; 15 (1): 346. - 46.
Руссо Дж., Миглиетта А., Пеццотти П., Бигуайо Р. М., Бутинг Маяка Дж., Собзе М. С. и др.Охват вакцинацией и детерминанты неполной вакцинации детей в возрасте 12–23 месяцев в Дшанге, Западный регион, Камерун: перекрестное обследование во время вспышки полиомиелита. BMC общественное здравоохранение. 2015; 15 (1): 630. - 47.
Калхун Л.М., ван Эйк А.М., Линдблейд К.А., Одхиамбо Ф.О., Уилсон М.Л., Винтербауэр Э. и др. Детерминанты и охват вакцинацией детей в западной Кении по данным поперечного исследования 2003 года. Американский журнал тропической медицины и гигиены. 2014; 90 (2): 234–41.pmid: 24343886 - 48.
Brinkman ID, de Wit J, Smits GP, ten Hulscher HI, Jongerius MC, Abreu TC, et al. Ранняя вакцинация против кори во время вспышки в Нидерландах: краткосрочное и долгосрочное снижение антител у детей, вакцинированных до 12 месяцев. Журнал инфекционных болезней. 2019; 220 (4): 594–602. - 49.
Фавин М., Штейнгласс Р., Филдс Р., Банерджи К., Сони М. Почему детям не делают прививки: обзор серой литературы.Международное здоровье. 2012. 4 (4): 229–38. pmid: 24029668 - 50.
Тадесс Т., Гетачью К., Ассефа Т., Абабу Ю., Симирета Т., Бирхану З. и др. Факторы и неправильные представления о распространении услуг плановой иммунизации детей в Эфиопии: результаты общенационального качественного исследования. Панафриканский медицинский журнал. 2017; 28 (1): 290. - 51.
Топузоглу А., Ай П, Хидироглу С., Гурбуз Ю. Препятствия на пути иммунизации детей: качественное исследование среди социально-экономически неблагополучных матерей.Европейский журнал общественного здравоохранения. 2007. 17 (4): 348–52. pmid: 170
прививок: чего ожидать в день и как к нему подготовиться
Как я узнаю, что моему ребенку должны быть сделаны прививки?
Когда вы берете ребенка к своему семейному врачу, педиатру или медсестре в первый раз, обычно через два или три дня после его рождения, вы получите информацию о прививках. Они начнут составлять карту для вашего ребенка и дадут вам буклет, содержащий график иммунизации в вашей провинции или территории.Вы можете получить ту же карту в больнице при выписке после родов, или от медсестры или акушерки.
Графики вакцинации немного отличаются в зависимости от провинции или территории, в которой вы живете. Как правило, ваш ребенок будет получать прививки в следующем возрасте:
- от рождения до двух месяцев
- в четыре месяца
- от 12 до 18 месяцев
- от четырех до шести лет
(Правительство Канады 2018a)
Попросите врача или медсестру заполнять карту вакцинации вашего ребенка каждый раз, когда ему делают прививки.Важно обновлять эту запись, особенно если вы переезжаете в другую провинцию или территорию с другим графиком вакцинации.
Вы также можете использовать бесплатное приложение для смартфонов от CANImmunize. Он хранит записи о вакцинации вашего ребенка и помогает вам вовремя вакцинировать его (Caring For Kids 2016a).
Что будет до прививок?
Перед первой вакцинацией вашего ребенка врач обычно проводит его краткое обследование и задает несколько вопросов о любых аллергиях или проблемах со здоровьем.Прививки вашего ребенка могут быть отложены на несколько дней, если у него высокая температура или он очень плохо себя чувствует (Правительство Канады, 2018a). Когда ему станет лучше, ему сделают укол.
Прочтите нашу статью о том, что делать, если ваш ребенок заболел во время запланированной иммунизации.
Кто будет делать прививки?
Прививки обычно делает ваш семейный врач, педиатр или медсестра общественного здравоохранения. Она, вероятно, попросит вас сесть, держа ребенка у вас на коленях, пока она делает ему инъекцию.
Некоторых родителей это немного расстраивает, но все быстро заканчивается. Если вы не хотите находиться в комнате, пока вашему ребенку делают инъекцию, вы можете вместо этого попросить своего партнера или другого родственника.
Как делаются прививки?
Большинство прививок вашему ребенку делается путем инъекции в верхнюю часть бедра. Если ему больше 12 месяцев, вероятно, ему сделают инъекцию в руку. Некоторые прививки делаются перорально или распыляются в нос (Правительство Канады, 2018a).
Некоторые вакцины, такие как менингококковая и пневмококковая вакцины, вводятся в виде однократной инъекции. Другие вводятся в виде инъекций, содержащих более одной вакцины (Правительство Канады, 2018a).
Так, например, в некоторых частях Канады дифтерия, коклюш, столбняк, полиомиелит и Hib вводятся одной инъекцией (часто называемой вакциной 5-в-1), а не пятью отдельными инъекциями. В других частях страны вакцина 6-в-1 также содержит вакцину против гепатита B (Caring for Kids 2016a).
Как я могу уменьшить боль от вакцинации для моего ребенка?
Вот несколько советов, которые помогут уменьшить боль:
- Если вы кормите грудью, кормите ребенка грудью непосредственно до, во время и после инъекции. В противном случае вы можете дать ребенку соску или воду с сахаром (с помощью пипетки) прямо перед инъекцией (Caring for Kids nd, CANImmunize 2019).
- Хотя исследований, показывающих, что сахарная вода уменьшает боль от инъекций, не так много (Kassab et al 2012, Taddio et al 2017), некоторые родители и врачи придерживаются этого мнения (Caring for Kids nd, CANImmunize 2019) .Чтобы приготовить сахарную воду, смешайте 5 мл (одну чайную ложку) белого сахара с 10 мл (двумя чайными ложками) дистиллированной или кипяченой воды. Если вашему ребенку больше шести месяцев, вы можете использовать водопроводную воду, если она безопасна для питья (CANImmunize 2019).
- Держите или обнимайте ребенка на коленях во время инъекции. Будьте осторожны, не обнимайте его слишком крепко, так как это может усугубить его страдания. Мягкое покачивание после инъекции тоже может успокаивать (CANImmunize 2019).
- Отвлеките ребенка игрушкой, погремушкой, книгой или песней (CANImmunize 2019, Caring for Kids nd).
- Постарайтесь сохранять спокойствие, сохранять позитивный настрой и говорить своим обычным голосом. Если вы беспокоитесь, сделайте несколько медленных глубоких вдохов, чтобы расслабиться (CANImmunize 2019).
- Нанесите анестезирующий крем, гель или пластырь на кожу ребенка перед инъекцией (обычно от 30 минут до часа). Эти продукты обезболивают кожу в месте введения иглы, но вам нужно заранее узнать у врача, куда их вводить. Анестезирующие кремы можно купить без рецепта в местной аптеке, они безопасны для новорожденных и младенцев.
(Taddio et al 2015, Caring for Kids nd, Правительство Канады 2018b, CANImmunize 2019) Спросите своего поставщика медицинских услуг, куда наносить крем, или просмотрите это руководство от HealthLinkBC.
Канадская педиатрическая ассоциация рекомендует не давать ребенку никаких обезболивающих, парацетамола или ибупрофена непосредственно перед вакцинацией. Это потому, что это может повлиять на эффективность вакцины (Caring for Kids 2016a).
Что произойдет после вакцинации моего ребенка?
Вас попросят остаться в клинике или кабинете врача в течение 15–20 минут после иммунизации.Это потому, что, как и у любого лекарства, вероятность аллергической реакции на инъекцию очень мала.
Ваш ребенок может немного расстроиться и в этот вечер стать раздражительным. Некоторые родители обнаруживают, что их младенцы после иммунизации нуждаются в более успокаивающем воздействии на ночь. Так что, возможно, стоит очистить свой график после приема ребенка, чтобы вы могли немного пообнимать его и уделить ему больше внимания.
Каковы побочные эффекты иммунизации?
Общие побочные эффекты включают легкую боль, покраснение и припухлость в месте, где игла входит в кожу.Об этих побочных эффектах обычно не стоит беспокоиться, и они исчезнут в течение дня или двух (Правительство Канады, 2018b).
У некоторых детей впоследствии поднимается небольшая температура. Если дать ребенку парацетамол или ибупрофен от температуры, он может чувствовать себя более комфортно (Уход за детьми, 2016a).
Хотя фебрильные судороги случаются редко, у маленьких детей после иммунизации иногда возникают. Лихорадочные судороги могут быть спровоцированы высокой температурой. На них может быть страшно смотреть, но они редко бывают вредными.Однако позвоните в службу 911, если припадок длится более трех минут или если вашему ребенку меньше шести месяцев (Уход за детьми, 2018).
Если судорожный припадок у вашего ребенка длится менее трех минут или если ваш ребенок старше шести месяцев, обратитесь к врачу, чтобы исключить другие возможные причины приступа.
Лихорадка вместе с сыпью может возникнуть после вакцинации MMR (корь, эпидемический паротит, краснуха) или ветряной оспы (ветряная оспа). Это означает, что у вашего ребенка небольшая реакция на вакцину, поскольку его организм вырабатывает иммунитет к этой болезни (Caring for Kids 2016b, NHS 2018).
Могу ли я дать ребенку обезболивающее после иммунизации?
Не сразу, так как это может повлиять на эффективность вакцины. Лучше подождать шесть часов после иммунизации, прежде чем давать ребенку парацетамол или ибупрофен от боли или температуры (Уход за детьми, 2016a).
Сначала поговорите со своим врачом, если вашему ребенку меньше трех месяцев, если он принимает парацетамол, и менее шести месяцев, если он дает ибупрофен (Правительство Канады, 2016 г., HealthLink BC 2019). Следуйте инструкциям по дозировке на флаконе.Доза зависит от веса вашего ребенка, а не от его возраста. Вы можете спросить своего фармацевта или врача, если не знаете, сколько давать ребенку.
Никогда не давайте ребенку аспирин, так как это может вызвать серьезное, иногда опасное для жизни состояние, называемое синдромом Рейе (Caring for Kids 2015).
Когда мне следует беспокоиться о симптомах моего ребенка после вакцинации?
Серьезные реакции на вакцины очень редки. Позвоните своему врачу, если у вашего ребенка появятся какие-либо из этих симптомов после вакцинации:
- ректальная лихорадка выше 38 градусов Цельсия, если вашему ребенку меньше шести месяцев, или выше 40 градусов Цельсия у ребенка старшего возраста
- плачет или суетится более 24 часов
- усиление опухоли в месте, куда вошла игла
- необычная сонливость (Правительство Канады 2018b)
Узнайте больше о том, что делать, если ваш ребенок заболел, когда назначена вакцинация, и ознакомьтесь с советами родителей о том, как облегчить посещение врача и прививки вашему ребенку.
Последние отзывы:
июль 2019 г.
Список литературы
CANImmunize. 2019. Обезболивание при вакцинации детей. https://immunize.ca [по состоянию на июнь 2019 г.]
Уход за детьми. 2016a. Вакцинация и ваш ребенок. Канадское педиатрическое общество. www.caringforkids.cps.ca [По состоянию на июнь 2019 г.]
Уход за детьми. 2016b. Вакцины: общие проблемы. Канадское педиатрическое общество. www.caringforkids.cps.ca [По состоянию на июнь 2019 г.]
Уход за детьми.2018. Фебрильные припадки. Канадское педиатрическое общество. www.caringforkids.cps.ca [Доступ в июле 2019 г.]
Уход за детьми. nd. Уменьшите боль вакцинации у младенцев: руководство для родителей. www.caringforkids.cps.ca [По состоянию на июнь 2019 г.]
Govt of Canada. 2016. Ацетаминофен и дети. www.canada.ca [По состоянию на июнь 2019 г.]
Govt of Canada 2018a. Вакцины для детей: когда вакцинировать ребенка. www.canada.ca [По состоянию на июнь 2019 г.]
Govt of Canada 2018b. Руководство для родителей по вакцинации. www.canada.ca [Доступ в июне 2019 г.]
HealthLink BC. 2019. Применение ибупрофена у детей раннего возраста. www.healthlinkbc.ca [По состоянию на июнь 2019 г.]
Kassab M, Foster P, Foureur M, et al. 2012. Сладкие на вкус решения от процедурной боли, связанной с иглой, у младенцев в возрасте от одного месяца до одного года. Кокрановская база данных систематических обзоров. (12): CD008411. www.cochranelibrary.com [по состоянию на март 2019 г.]
NHS. 2018. Побочные эффекты вакцины MMR . NHS, Здоровье от А до Я, Прививки. www.nhs.uk [по состоянию на июнь 2019 г.]
Taddio A, McMurty M, Shah V, et al. 2015. Уменьшение боли во время инъекций вакцины: руководство по клинической практике. CMAJ 187 (13): 975-982. www.ncbi.nlm.nih.gov [по состоянию на июнь 2019 г.]
Taddio A, Riddell RP, Ipp M, et al. 2017. Относительная эффективность дополнительных обезболивающих при вакцинации младенцев. CMAJ 189 (6): E227 – E234. www.ncbi.nlm.nih.gov [по состоянию на июль 2019 г.]
У кормящих новорожденных нет реакции на вакцину COVID
Как новая технология РНК используется для создания вакцин COVID-19
В вакцине COVID-19 используется новая технология, которая никогда раньше не использовалась в традиционных вакцинах. Вот как работает мРНК-вакцина.
Только ответы на часто задаваемые вопросы, США СЕГОДНЯ
Утверждение: новорожденные, кормящие грудью, реагируют на вакцинацию матерей
Стремясь подавить пандемию коронавируса и вернуть страну к нормальной жизни, президент Джо Байден объявил в марте о своем плане расширения соответствие вакцины всем U.S. Взрослые к 1 мая. Эти сроки были перенесены на две недели, объявил президент 6 апреля.
Открытие права на вакцинацию — хорошая новость: за последние несколько месяцев число новых случаев коронавируса снизилось, хотя в последнее время оно остановилось. , а число зарегистрированных ежедневных смертей упало до самого низкого уровня за более чем год 4 апреля. Есть надежда, что с увеличением количества вакцин, достигаемых всеми, существует большая вероятность того, что эти тенденции сохранятся.
Но в социальных сетях опасения по поводу вакцинации и нерешительность продолжаются: в одном заявлении утверждается, что кормящие грудью дети испытывают побочные реакции из-за вакцинированных матерей.
Опубликован в Facebook 30 марта, текст над изображением неопознанного ребенка, покрытого сыпью, спрашивает, «слышал ли кто-нибудь что-нибудь о младенцах, у которых проявляются реакции на вакцину против коронавируса их кормящим мамам?»
Комментарий Facebook под изображением дает объяснение.
«Линси получила вторую дозу в прошлую среду. В четверг ее ребенок, вскармливаемый грудью, был покрыт сыпью с головы до ног. К той ночи он был безутешен, и его состояние ухудшалось, поэтому они обратились в скорую», — пишет Кейтлин RN в своем профиле в Facebook. она дипломированная медсестра.
Кейтлин Р.Н. утверждает, что однажды в больнице у ребенка была диагностирована тромботическая тромбоцитопеническая пурпура, или ТТП, редкое и невероятно редкое заболевание крови, при котором в мелких кровеносных сосудах по всему телу образуются тромбы, а также повышается уровень ферментов печени. Несмотря на «различные методы лечения», ребенок умер 16 марта.
Комментарии под изображением выражают соболезнования плакату, который отрицает какие-либо связи с изображенным на фото ребенком, а также опасения по поводу безопасности вакцины для кормящих женщин.
«Я думал, что кормящим матерям нельзя делать прививку», — говорит один из пользователей Facebook.
«И я не получаю вакцину … Пробирками могут быть все остальные, а не я, друг», — написано на оригинальном плакате.
Проверка фактов: Данные CDC о побочных эффектах вакцины не могут определить причину
USA TODAY обратились к пользователю Facebook и Кейтлин Р.Н. для дальнейших комментариев.
Изображение не тот ребенок, смерть не подтверждена
Комментарий Кейтлин RN в Facebook, включенный в фотографию, взят из публикации 17 марта, в которой она упоминает смерть 5-месячного сына друга, используя его для предупреждения беременных женщин и кормящих грудью матерям «держаться подальше от этих экспериментальных вакцин.
В сообщении от 31 марта она поясняет, что покрытый сыпью ребенок, изображенный на изображении, и ребенок, упомянутый в сообщении от 17 марта, — не одно и то же.
«Ребенок, о котором я сообщила, скончался после того, как мама получила Вторая вакцина Pfizer — это НЕ ребенок, изображенный на Дискуссионном форуме по перевоспитанию вакцины. Я указал это в своем исходном сообщении, но, похоже, это упускается из виду. Изображенный на фото младенец явно чувствует себя намного лучше по состоянию на неделю назад, когда я последний раз видела обновление », — пишет она.
USA TODAY не смог проверить, действительно ли произошла младенческая смерть, о которой говорилось в исходном посте. В своем сообщении от 31 марта Кейтлин RN не предоставила никаких дополнительных подробностей, когда пользователи Facebook попросили подтвердить ее заявление, но в сообщении от 17 марта она сказала, что о смерти будет сообщено в Систему сообщений о побочных эффектах вакцин правительства США. USA TODAY не смогли найти никаких сообщений о связанных с ТТП смертях среди младенцев из-за вакцинации матери или других случаев, связанных с аналогичными состояниями, такими как иммунная тромбоцитопеническая пурпура (которая, как известно, поражает нескольких реципиентов вакцины Pfizer).
Грудное вскармливание и вакцинация против COVID-19
Есть ли риск для ребенка в случае вакцинации кормящей матери? Эксперты в области здравоохранения говорят, что это маловероятно.
«Во время лактации маловероятно, что липид вакцины попадет в кровоток и достигнет ткани груди. Если это произойдет, еще менее вероятно, что интактная наночастица или мРНК переместятся в молоко. присутствует в молоке, ожидается, что он будет усвоен ребенком и вряд ли будет иметь какие-либо биологические эффекты », — говорится в декабрьском заявлении Академии медицины грудного вскармливания.
Международный чрезвычайный детский фонд Организации Объединенных Наций признал, что, хотя данных о безопасности вакцины COVID-19 для кормящих женщин и кормящих детей мало, «поскольку вакцина не является вакциной против живого вируса, и мРНК не входит в ядро вакцины. клетка и быстро разлагается, биологически и клинически маловероятно, что она представляет опасность для грудного ребенка ».
Появляются новые данные о безопасности вакцины для кормящих женщин, и они показывают, что вакцинация от COVID-19 защищает не только мать, но и ребенка.
Недавнее исследование Медицинской школы Вашингтонского университета в Сент-Луисе показало, что вакцинированные кормящие матери могут передавать своим детям защитные антитела против коронавируса через грудное молоко в течение как минимум 80 дней после вакцинации.
Уровни антител в грудном молоке пяти кормящих матерей — детей в возрасте от 1 месяца до 2 — измеряли до вакцинации и еженедельно до 80 дней после их начальной дозы.
«Наше исследование показало огромный рост антител против вируса COVID-19 в грудном молоке, начиная с двух недель после первой прививки, и этот ответ сохранялся на протяжении всего нашего исследования, которое длилось почти три месяца», — сказал доктор .Джинни Келли, доцент кафедры акушерства и гинекологии и первый автор исследования, в заявлении Вашингтонского университета. «К концу нашего исследования уровни антител все еще были высокими, поэтому защита, вероятно, продлится еще дольше».
Келли сказала, что результаты ее группы добавляют к растущему количеству доказательств, подтверждающих вакцинацию COVID-19 у беременных и кормящих женщин.
«Этой информации у нас не было несколько месяцев назад, и она действительно помогает нам лучше консультировать наших пациентов, которые рассматривают возможность вакцинации.Я говорю своим беременным и кормящим мамам, что настоятельно рекомендую им пройти вакцинацию как можно скорее », — сказала она.
Наше решение: Отсутствует контекст
Мы оцениваем это утверждение как ОТСУТСТВУЮЩИЙ КОНТЕКСТ, потому что без дополнительного контекста оно может вводить в заблуждение. Изображение ребенка, покрытого сыпью, — это не тот ребенок, который упоминается в комментарии в Facebook, где утверждается, что ребенок умер после того, как его мать получила вакцину от COVID-19. Неясно, действительно ли произошла смерть; в правительственной публикации «Вакцина» такого отчета нет. Система сообщений о нежелательных явлениях.Согласно новым исследованиям, несколько медицинских агентств и организаций заявили, что вакцина COVID-19 вряд ли нанесет вред кормящемуся ребенку и что вакцинация матери может обеспечить защитный иммунитет против вируса.
Наши источники проверки фактов:
- США СЕГОДНЯ, 11 марта, «Выводы из речи Байдена: небольшие собрания до 4 июля, осуждение расистских атак и контраст Трампа»
- США СЕГОДНЯ, 6 апреля, «Байден в ход крайний срок, чтобы все взрослые имели право на вакцину против COVID-19 к 19 апреля «
- The New York Times, 6 апреля» По мере распространения вариантов, прогресс в борьбе с вирусом в США «.С. остановил «
- Холм, 5 апреля». Ежедневные сообщения о смертности от COVID-19 упали до самого низкого уровня за год в воскресенье «
- Национальные институты здравоохранения — Национальный институт сердца, легких и крови, по состоянию на 9 апреля», Тромботическая тромбоцитопеническая пурпура »
- StatPearls, 10 июля 2020 г.,« Оценка и лечение тромботической тромбоцитопенической пурпуры »
- Caitlyn RN, 17 марта, сообщение в Facebook.
- Caitlyn RN, 31 марта, сообщение в Facebook.
- Medscape, 2 апреля, «Человеческое молоко и лактация»
- Академия медицины грудного вскармливания, 14 декабря 2020 г., «Заявление ABM. Лактация »
- ЮНИСЕФ, доступ 9 апреля,« Что вам нужно знать о вакцине COVID-19 »
- Школа медицины Вашингтонского университета в Сент-Луисе, 6 апреля,« Для кормящих мам вакцинация COVID-19 может также защитить младенцы »
907 Февраль8, «У нескольких реципиентов вакцины против Covid развилось редкое заболевание крови»
Спасибо за поддержку нашей журналистики.Вы можете подписаться на нашу печатную версию, приложение без рекламы или копию электронной газеты здесь.
Наша работа по проверке фактов частично поддерживается грантом Facebook.
Обзоры здоровья и развития вашего ребенка
Что происходит при осмотре вашего малыша
Во время осмотра вашего ребенка патронажная сестра обсудит его здоровье и развитие и спросит, есть ли у вас какие-либо проблемы.
Если ваш ребенок набирает вес, и вы и ваш патронажный врач не беспокоитесь, его следует взвешивать не чаще:
- один раз в месяц до 6 месяцев
- один раз в два месяца с 6 до 12 месяцев возраст
- один раз в 3 месяца в возрасте старше 12 месяцев
Это дает четкое представление о прибавке веса вашего ребенка за определенный период времени.
Посмотрите, как контролируется вес вашего ребенка.
Если ваш ребенок родился преждевременно, его возраст развития будет рассчитываться от вашей первоначальной даты родов, а не от фактической даты его рождения, до тех пор, пока ему не исполнится 2 года.
Анкета по возрасту и этапам (ASQ-3)
Ваша медицинская бригада отправит вам анкету, известную как «Анкета по возрасту и этапам» или ASQ-3, которую необходимо заполнить до того, как ребенку исполнится 9–12 лет. ежемесячные и двухлетние обзоры разработки.
Это позволяет вам опробовать некоторые из заданий, описанных в анкете, с вашим ребенком дома, где ему будет комфортно и в знакомой обстановке.
Когда у вашего ребенка будут отзывы
У вашего ребенка обычно будут отзывы в том возрасте, о котором мы говорим на этой странице. Если у вас возникнут какие-либо проблемы в другое время, вы можете обратиться к патронажной сестре или терапевту или обратиться в местную детскую клинику.
Вскоре после рождения
Ваш ребенок будет взвешиваться при рождении и еще раз в течение первой недели.Они также пройдут тщательный медицинский осмотр в течение 72 часов после рождения. Медицинский работник обычно проверяет глаза, сердце, бедра и — у маленьких мальчиков — яички вашего ребенка.
Подробнее о медицинском осмотре новорожденных.
В возрасте 5 и 8 дней вашему ребенку будет проведен анализ пятен крови (укол в пятку), позволяющий выявить несколько редких заболеваний, включая муковисцидоз и серповидно-клеточную анемию. Обычно это делает акушерка.
Узнайте больше о тесте на пятку новорожденного.
Вскоре после рождения вашему ребенку будет проведена проверка слуха. Если ваш ребенок находится в больнице, это может произойти до вашего отъезда. В противном случае это будет сделано в течение первых нескольких недель у вас дома, в поликлинике или в вашем местном поликлинике.
Узнайте больше о тесте слуха новорожденных.
Акушерка и патронажная сестра также поддержат вас в кормлении грудью, уходе за новорожденным и приспособлении к жизни в качестве нового родителя.
1-2 недели
Патронажный врач проведет осмотр новорожденного в течение 10-14 дней после рождения.
Они дадут вам совет по телефону:
от 6 до 8 недель
Ваш ребенок будет приглашен на тщательный медицинский осмотр. Обычно это делает терапевт.
У вашего ребенка будут проверяться глаза, сердце, бедра и — для мальчиков — яички. У них также будут измерены их вес, длина и окружность головы.
Врач общей практики или патронажный врач обсудит с вами вакцинацию вашего ребенка. Они предлагаются в возрасте 8 недель, 12 недель, 16 недель и 12 месяцев, но до того, как ваш ребенок пойдет в школу.
Они также спросят, как вы себя чувствуете эмоционально и физически с момента рождения ребенка.
От 9 до 12 месяцев
В течение этого времени вашему ребенку следует предложить еще один обзор, посвященный, среди прочего, языку и обучению, безопасности, диете и поведению.
Обычно это делает член вашей медицинской бригады. Это возможность обсудить любые проблемы, которые могут у вас возникнуть.
Ваша медицинская бригада отправит вам анкету ASQ-3, которую необходимо заполнить перед рассмотрением.Это поможет вам и вашему лечащему врачу понять, как развивается ваш ребенок.
Не беспокойтесь, если вы не можете заполнить анкету целиком — патронажная сестра поможет вам заполнить ее.
От 2 до 2 с половиной лет
В 2–2 с половиной года вашему ребенку предстоит еще одна проверка здоровья и развития. Лучше всего, если вы и ваш партнер оба будете рядом.
Обычно это делает медсестра или патронажная сестра, и может происходить у вас дома, в детской поликлинике или детском центре.
Если ваш ребенок начал ходить в детский сад, игровую группу или няню, проверка может быть проведена там. Вы, патронажный работник, ключевой работник или няня — все будете делать обзор вместе.
Вам будет отправлена анкета ASQ-3 о развитии вашего ребенка, которую нужно заполнить перед проверкой. В этом вам могут помочь патронажный работник, ключевой работник или няня.
Этот обзор будет охватывать:
От новорожденных до подростков, практические медицинские и естественные способы защиты вашего ребенка: Лорен Федер: 9781578262519: Amazon.com: Книги
ВВЕДЕНИЕ
Противоречие о вакцинации
Когда я рос, посещение врача для прививки было освященной веками традицией, которую мы все принимали — нравится нам это или нет! Даже во время моего обучения в качестве ординатора в больнице я покорно ходил на ежегодные медицинские осмотры, которые включали обновление базовых прививок для взрослых. Как и мои родители, я никогда не ставил под сомнение прививки и не считал их чем-то другим, кроме обычной меры профилактики болезней.Только когда меня успешно вылечили от заболевания щитовидной железы с помощью холистической медицины, я заинтересовался дополнительным медицинским подходом, заключающимся в максимальном использовании естественной защиты организма от болезней. С этой точки зрения вакцинация может нарушить естественный иммунитет организма и сама по себе может вызвать заболевание.
Прививки, которые на протяжении десятилетий считались одним из главных достижений общественного здравоохранения, больше не защищены от споров. Во времена наших бабушек и дедушек почти все дети болели корью, паротитом и краснухой.Нередко можно услышать рассказы о вечеринках с ветряной оспой во времена наших родителей, которые процветали при первых признаках сыпи, когда все матери сгоняли своих детей в дом зараженного ребенка. С момента появления вакцин в двадцатом веке эти распространенные детские болезни больше не являются общими . Вроде бы хорошие новости. Но в последние годы профессиональные журналы и газеты все чаще сообщают о травмах от вакцины, токсичности ртути и возможных связях между вакцинацией и хроническими заболеваниями, такими как аутизм.
Одним из первых важных решений, которые должны принять в отношении здоровья новые родители, является вопрос о вакцинации или отказе от вакцинации. Многие родители даже не осознают, что есть выбор, поскольку существует предположение, что вакцинация является обязательной, а не добровольной при поступлении в школу. Наша система здравоохранения рекомендует делать прививки каждому ребенку. Однако, как и любые лекарства, вакцинация может вызвать побочные эффекты и не всегда на 100% безопасна. Иногда у ребенка может возникнуть реакция после укола — возникновение дискомфорта, аллергических реакций и даже сообщений о смерти.В средствах массовой информации широко распространены рассказы о связи аутизма с прививками от кори, паротита и краснухи. В результате все больше родителей начинают сомневаться в безопасности и эффективности вакцин. В настоящее время, когда имеется обилие доступной информации, родители больше осведомлены о пользе и риске вакцинации для здоровья, задают больше вопросов своим врачам и заинтересованы в том, чтобы взять на себя определенную ответственность за здоровье и благополучие своих детей. Некоторые из моих пациентов вакцинируются полностью по расписанию, некоторые — нет, а другие вакцинируются выборочно.
Текущее состояние здоровья наших детей
Медицинские достижения 1900-х годов были впечатляющими по своим достижениям: мы лечим болезни с помощью более сложных методов, лечим болезни с помощью сложных лекарств и обширных терапевтических режимов. Мы понимаем механику тела лучше, чем когда-либо в истории. Но даже несмотря на то, что нам говорят, что мы более здоровы и живем дольше, все больше детей с каждым годом получают ежедневные лекарства от хронических заболеваний. В последние годы я стал свидетелем резкого увеличения числа таких состояний — у детей, которые страдают от повторных ушных инфекций, тяжелой астмы, аллергии или экземы, или даже с поведенческими проблемами, такими как синдром дефицита внимания с гиперактивностью (СДВГ).Объяснения увеличения хронических детских болезней сложны и часто противоречивы; Однако последствия для детей и семей глубоки и очевидны. В результате с каждым годом все больше родителей сталкиваются с ограничениями традиционной медицины в лечении и устранении причин подобных хронических заболеваний.
К сожалению, здравоохранению в Соединенных Штатах предстоит пройти долгий путь, прежде чем оно станет удовлетворительным. Согласно статье в журнале Американской медицинской ассоциации (Барбара Старфилд, М.Д., «Действительно ли здравоохранение в США лучшее в мире?» ДЖАМА. 2000; 284: 483–485) Соединенные Штаты заняли 12-е место из группы из 13 стран по таким показателям здоровья, как низкий вес при рождении, младенческая смертность и ожидаемая продолжительность жизни. Наши дети, которые представляют будущее поколение, могут подвергаться большему риску, чем мы. Многие из наших детей, например, потребляют больше, чем безопасное количество фтора из местных источников воды, что повреждает зубную эмаль, связки, мышцы и кожу и связано с более низким уровнем IQ, артритом и раком.Известно, что ртуть, используемая в пломбах из амальгамы, токсична и может привести к повреждению мозга, почек и иммунной системы. Чрезмерное употребление антибиотиков вызвало резистентность к антибиотикам, разрастание дрожжей и ослабление иммунной системы.
В настоящее время, по данным Американской ассоциации ожирения, 15 процентов детей в Соединенных Штатах страдают ожирением, что более чем на 50 процентов среди детей в возрасте от 6 до 11 лет с 1960-х годов. Большинство подростков с избыточным весом вырастают и становятся взрослыми с ожирением. Этот тревожный рост ожирения объясняется рядом социальных причин, включая наш более сидячий образ жизни, высокий уровень просмотра телевидения (до 30 часов в неделю) и преобладание фаст-фуда и нездоровой пищи в школах.Во многих начальных и средних школах нередко можно найти торговые автоматы по продаже конфет и безалкогольных напитков. С финансовыми ограничениями и сокращениями, которые стали реальностью во многих школах, эти машины стали источником дохода для школ. Проблема ожирения усугубляется тем, что программы физического воспитания сокращаются в первую очередь во время школьных финансовых кризисов, и по всей стране дети все чаще лишаются возможности заниматься физическими упражнениями в школьные часы. Ожирение влечет за собой множество проблем со здоровьем: диабет, болезни сердца, высокий уровень крови. давление и более высокая заболеваемость некоторыми видами рака.
Также в последние годы значительно увеличилось количество детей, у которых диагностированы нарушения обучения и поведения, такие как СДВГ, дислексия, нарушение обработки слуха, нарушение зрения, синдром Аспергера и аутизм. По данным Scripps Howard News Service, нарушения обучаемости поражают 30 процентов детей в Соединенных Штатах. Большинство исследований не дали окончательных результатов относительно причин. Такие факторы, как загрязнение окружающей среды, плохое питание, чрезмерное употребление антибиотиков и изменения в семейной жизни, попали под подозрение как возможные причины.Тем не менее, многие семьи в моей офисной практике стали свидетелями побочных эффектов вакцинации и стали обвинять вакцины в том, что они вызывают или способствуют возникновению этих расстройств. Учитывая статистику здоровья наших детей практически во всех аспектах их жизни, многие родители и практикующие врачи заинтересованы в принятии активных мер, чтобы противостоять разногласиям. Врачи, даже практикующие традиционную медицину, применяют более целостный и профилактический подход к здравоохранению.Большинство согласны с тем, что поддержание и укрепление здоровья требует большего, чем просто прописывание лекарств. Благополучие распространяется на разум и дух, а также на тело и включает в себя полноценное питание, упражнения, здоровый образ жизни и гармонию в отношениях. Во время болезни многие родители обращаются к естественным лекарствам в качестве первой линии защиты и используют обычные лекарства только при необходимости. Теперь многие понимают, что такое отношение должно быть применимо и к вакцинации.
Что правильно для моего ребенка?
Каким бы ни было ваше решение относительно вакцинации, цель всегда одна: вырастить счастливых и здоровых детей, способных расцвести и реализовать свой жизненный потенциал.Как врач для многих семей, наиболее частый вопрос, который я слышу от обеспокоенных родителей, — это: «Что мне делать с прививками?» Я отвечаю, что это зависит от общего состояния здоровья вашего ребенка и рисков конкретных заболеваний или побочных эффектов, а также от ваших личных ценностей. Как врач, обученный как стандартной, так и холистической медицине, я могу думать о здоровье двумя способами. Как доктор медицины, я хорошо знаю, что стандарт лечения — вакцинация; Как целостный практик я понимаю, что вакцинация может представлять краткосрочный, а иногда и долгосрочный риск как для детей, так и для взрослых.Хотя цели традиционной и холистической медицины совпадают, подходы могут сильно отличаться, а предлагаемые варианты могут сбивать с толку и даже расстраивать родителей.
После тщательного рассмотрения вариантов мы с мужем решили не вакцинировать наших детей. Однако в своей офисной практике и на лекциях я стараюсь подчеркивать, что наше решение не вакцинироваться было личным семейным решением, и, как опекун многих семей, я не навязываю этот образ действий своим пациентам.Я понимаю, что вакцинация предотвращает многие тяжелые и опасные для жизни заболевания, и было бы наивно полагать, что здоровый образ жизни и естественные подходы к воспитанию всегда будут обеспечивать нам адекватные решения. Хотя гомеопаты успешно лечат инфекционные заболевания в течение нескольких столетий, я без колебаний полагаюсь на медицину и технические достижения двадцать первого века, когда это необходимо. Моя книга Natural Baby and Childcare дает больше информации о естественных и медицинских методах лечения многих из этих болезней.
Решение о вакцинации может быть запутанным и трудным для некоторых семей, поскольку все мы хотим делать то, что правильно для наших детей. Некоторые родители основывают свое решение на статистических данных, приведенных в книгах и в Интернете. Данные могут варьироваться от Центров по контролю и профилактике заболеваний (CDC) до Национального информационного центра по вакцинам (NVIC), который был начат родителями, чьи дети получили травмы в результате вакцинации. Некоторые люди основывают свое решение на личном опыте; они знают кого-то, кто болен полиомиелитом или страдает побочным эффектом от вакцины.
Какими бы ни были ваши решения, я решительно поддерживаю позицию «информированного выбора», которая побуждает вас принимать осознанные и информированные решения относительно вакцинации и всех других аспектов воспитания детей.


 В оригинале звучит, как Bacillus Calmette-Gurin (Бацилла Кальметта-Герена).
В оригинале звучит, как Bacillus Calmette-Gurin (Бацилла Кальметта-Герена).


 Ребенок находится под наблюдением фтизиатра, хирурга, педиатра.
Ребенок находится под наблюдением фтизиатра, хирурга, педиатра. У малышей часто развивается туберкулезный менингит.
У малышей часто развивается туберкулезный менингит.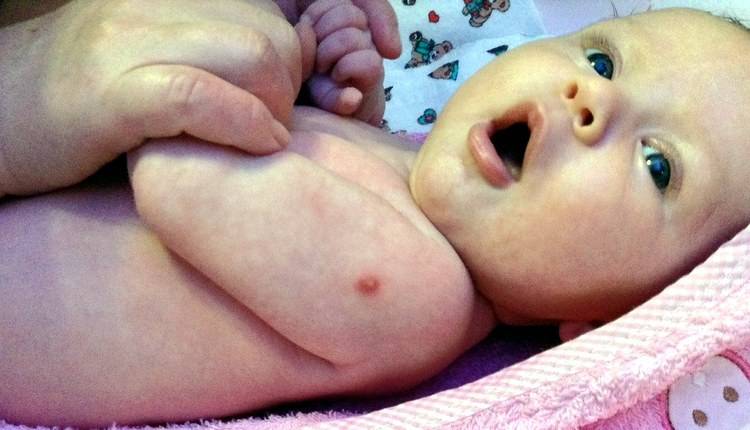 )
)